Nomenclatura: Alcoli, Eteri, AMmine


Università degli Studi della Campania "Luigi Vanvitelli"



Ancora esercizi su nomenclatura di alcani e cicloalcani

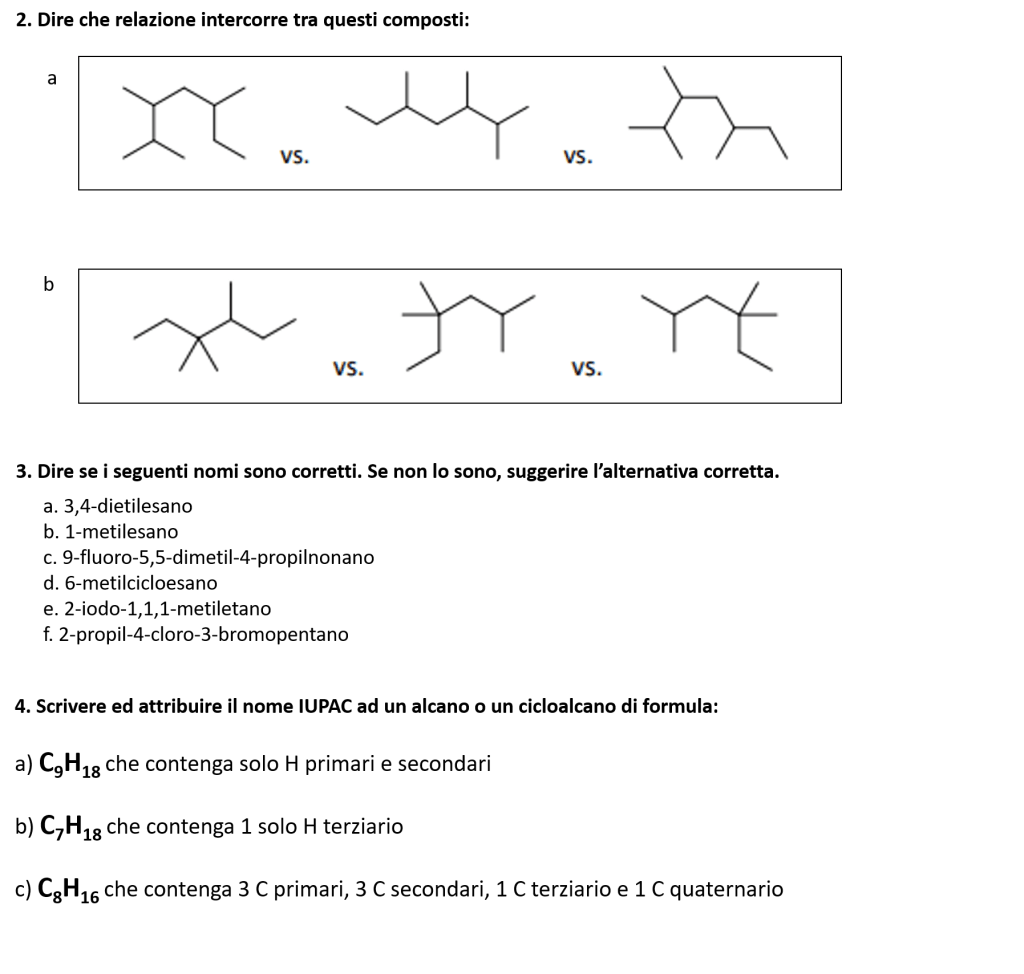
È inoltre possibile anche divertirsi con questi esercizi interattivi: 
ATTENZIONE: Esercizio 4 b) la formula bruta non è C7H18, ma C7H16!

Esercizio AN1
Assegna un nome ai seguenti composti:
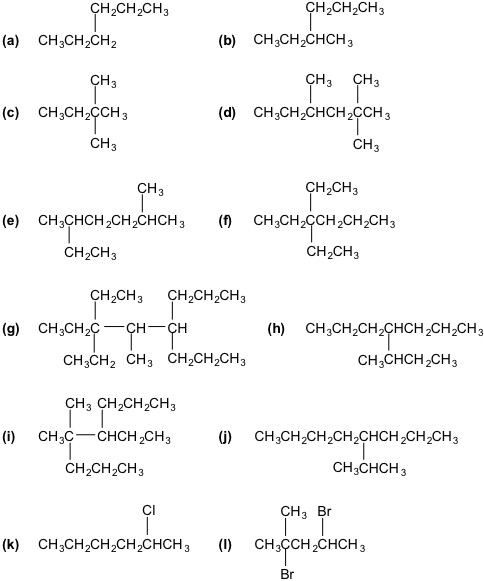

Esercizio AN2
Scrivi le formule di struttura dei seguenti composti:
| (a) 2,3-dimetilesano (b) 4,4-dietildecano (c) 4-isopropil-2,4,5-trimetileptano (d) 2,2-dimetil-4-propilottano (e) 4-isobutil-2,5-dimetilottano (f) neopentil bromuro (g) 4,5-diisopropilnonano (h) 4-terz-butileptano | (i) 5,5-dibromo-2-metilottano (j) 3,4-dimetilottano (k) 2,2,4-trimetilesano (l) 5-butil-2,2-dimetilnonano (m) 3,3-dimetilpentano (n) 1,1,1-tricloroetano (o) 3-etil-2,4,5-trimetilottano (p) 3-etil-5-iodoeptano |
Esercizio AN3
Spiega perché ognuno dei seguenti nomi non è un corretto nome IUPAC. Scrivi il nome IUPAC corretto.
| (a) 1,3-dimetilbutano (b) 4-metilpentano (c) 2,2-dietilbutano (d) 2-etil-metilpentano (e) 4,4-dimetilesano (f) 2-propilpentano | (g) 2,2-dietileptano (h) 5-butilottano (i) 2,2-dimetilciclopropano (j) 2-sec-butilottano (k) 4-isopentileptano (l) 1,3-dimetil-6-etilcicloesano |

Esercizio AB1
Scrivi gli acidi coniugati delle seguenti basi:
(a) NH3 (b) Cl– (c) OH– (d) H2O (e) CH3OH
Esercizio AB2
Scrivi le basi coniugate dei seguenti acidi:
(a) NH3 (b) HBr (c) HNO3 (d) H2O (e) CH3OH
Esercizio AB3
Nell’acido acetico il protone del gruppo OH è più acido dei protoni del gruppo metilico [CH3]. Mostra come il concetto di elettronegatività può essere usato per spiegare questa differenza di acidità.
Esercizio AB4
Usando i concetti di risonanza e di elettronegatività, se è il caso, fornisci una spiegazione per le seguenti osservazioni:
(a) l’H3O+ è un acido più forte dell’ NH4+;
(b) l’acido acetico è un acido più forte dell’etanolo;
(c) l’etanolo e l’acqua hanno approssimativamente la stessa acidità;
(d) l’acido cianidrico è un acido più forte dell’etino;
(e) i protoni dei metili [CH3] dell’acetone [CH3COCH3] sono più acidi di quelli dell’etano.
Esercizio AB5
Scrivi i prodotti delle seguenti reazioni acido-base e indica la direzione dell’equilibrio

Esercizio AB6
In ogni coppia, seleziona l’acido più forte:
(a) acido acetico (pKa 2,49) o acido lattico (pKa 3,85);
(b) acido citrico (pKa 3,08) o acido fosforico (pKa 2,10) ;
(c) acido nicotinico (Ka 1,4·10-5) o acido acetilsalicilico (Ka 3,3·10-4);(d) fenolo (Ka 1,12·10-10) o acido borico (Ka 7,24·10-10).
Esercizio AB7
i) Elenca i seguenti acidi carbossilici in ordine crescente di acidità:

ii) Perché la presenza di un atomo elettronegativo, come il cloro, influenza l’acidità dell’acido carbossilico?
iii) Perché la posizione del sostituente influenza l’acidità del composto?
Esercizio AB8
In ognuna delle seguenti coppie, individua la base più forte:
(a) CH3COO- o HCOO- [pKa CH3COOH = 4,8; pKa HCOOH = 3,8]
(b) OH– o NH2– [pKa H2O = 15,7; pKa NH3 = 36]
(c) H2O o CH3OH [pKa H3O+ = -1,7; pKa CH3OH2+ = -2,2]

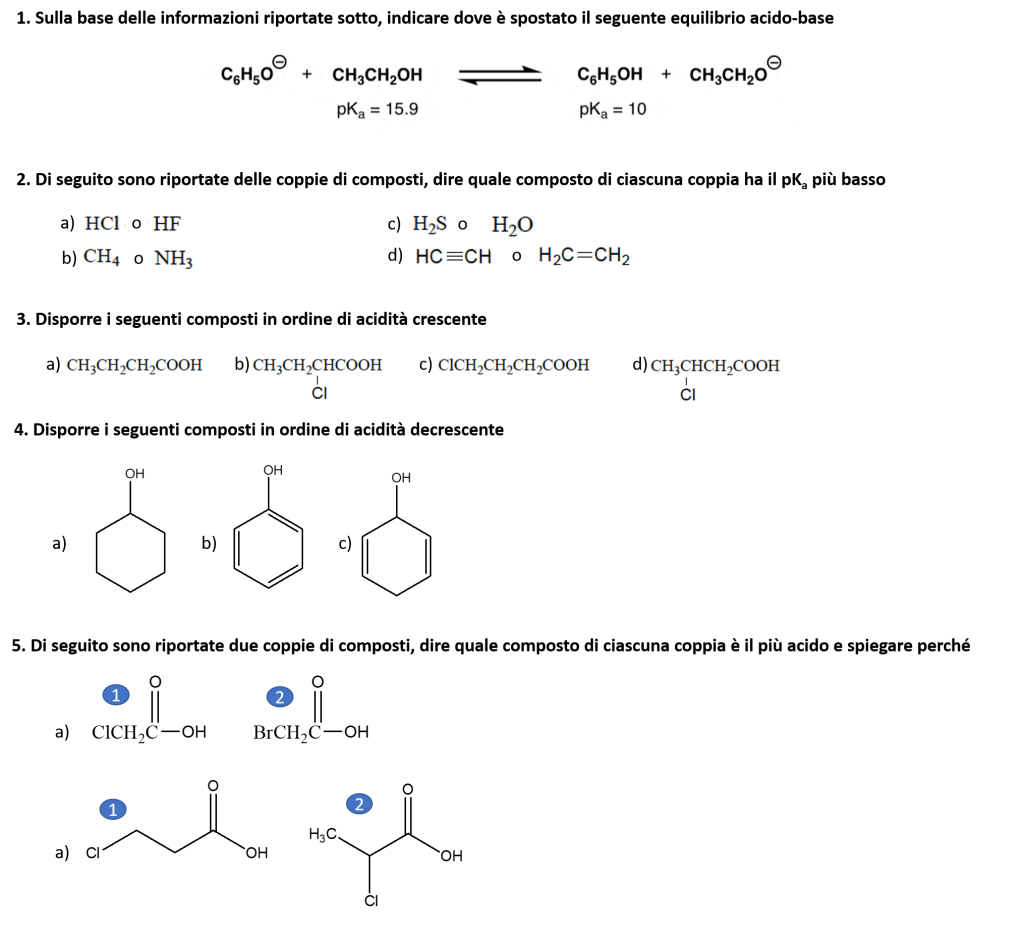
È il momento di esercitarsi su acidi e basi in chimica organica.
Riuscite a risolvere i seguenti quesiti?
NB: È possibile usare la sezione commenti per rispondere, porre domande e discutere!






1. Seguendo la regola che ogni atomo di carbonio, di azoto, di ossigeno e di alogeno reagisce in modo da completare il guscio più esterno con otto elettroni di valenza, aggiungi doppietti di elettroni non condivisi fino al completamento dei gusci di valenza nelle seguenti molecole o ioni. Assegna le cariche formali se è il caso.

2. Scrivi le strutture di Kekulé per ciascuno dei seguenti composti:
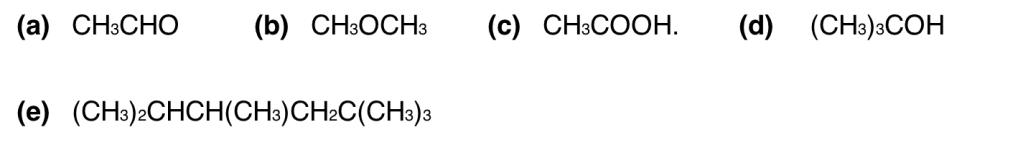

Esercizio n.1
Calcolare la carica formale per tutti gli atomi (tranne idrogeno) delle seguenti specie.

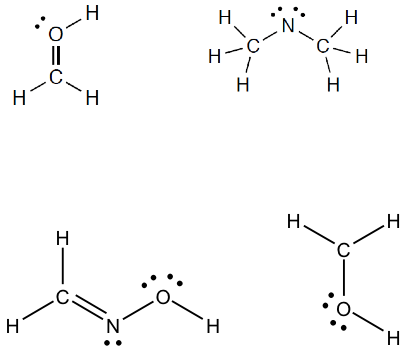
Esercizio n. 2
Scrivere la struttura di Lewis dell’anione nitrato
Esercizio n. 3
Rappresentare la struttura di Lewis dello ione idrogenosolfato. Calcolare le cariche formali e scrivere almeno due strutture di risonanza.
Esercizio n. 4
Rappresentare la struttura di Lewis, comprendendo i tipici contributi alla struttura di risonanza (ove appropriato) in relazione a: (a) cloruro di ammonio; (b) ipoclorito di calcio.
Esercizio n. 5
Scrivere tre strutture di risonanza a differente energia dello ione periodato. Determinare la carica formale di ciascun atomo ed identificare la struttura di energia minima
Esercizio n. 6
Rappresentare la struttura di Lewis dello:
(a) ione solfato
(b) ione solfito
Calcolare le cariche formali e scrivere almeno due strutture di risonanza per ogni specie
Esercizio n. 7
Per ciascuna coppia individuare il composto i cui legami manifestano maggiore carattere ionico:
(a) HCl, HI
(b) SO2, NO2
(c) CO2, CS2



Docenti: proff. Antonio Fiorentino – Anna Messere – Monica Scognamiglio

SSD: CHIM/06
CFU: 15
Periodo di erogazione: primo e secondo semestre
You must be logged in to post a comment.