REAZIONE DI CLAISEN
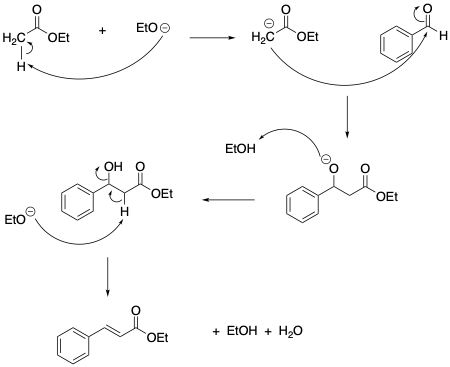
La rteazione tra un estere contenente un idrogeno attivo e un aldeide che ne sia priva, effettuata in presenza di una base, è conosciuta come reazione di Claisen (da non confondere con la condensazione di Claisen).
Il successo della reazione dipende dalla maggiore reattività verso i nucleofili del carbonio aldeidico rispetto a quello estereo. Le aldeidi che portano un idrogeno in alfa non sono reagenti adatti perchè danno di preferenza prodotti di autocondensazione.
REAZIONE DI REFORMATSKY
Sebbene non sia una reazione catalizzata dalle basi, essa viene inclusa in questo contesto in quanto riguarda la reazione di un enolato con un’aldeide o un chetone.
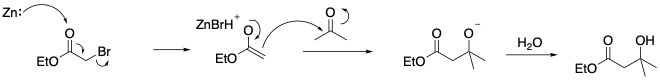
L’enolato si forma da un alfa-bromoestere con zinco in Et2O:
Contrariamente di quanto avviene nelle reazioni degli enolati con le aldeidi aromatiche, spesso seguite da eliminazione catalizzata da basi per dare composti alfabeta-insaturi, nella reazione di Reformatsky l’assenza di basi porta alla formazione di un beta-idrossiestere.
REAZIONE DI PERKIN
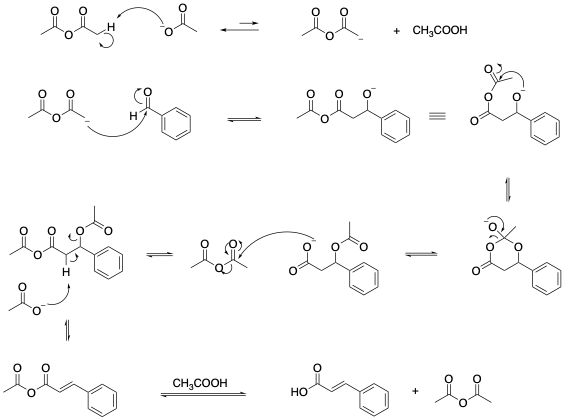
Questa reazione consiste nella condensazione, catalizzata dall’anione carbossilato, di un’anidride acida con un’aldeide aromatica. Sebbene il meccanismo sia molto complesso, la reazione procede secondo passaggi ben definiti.
Affinchè la reazione proceda sono richieste in genere temperature piuttosto elevate a causa della basicità relativamente modesta dello ione carbossilato.
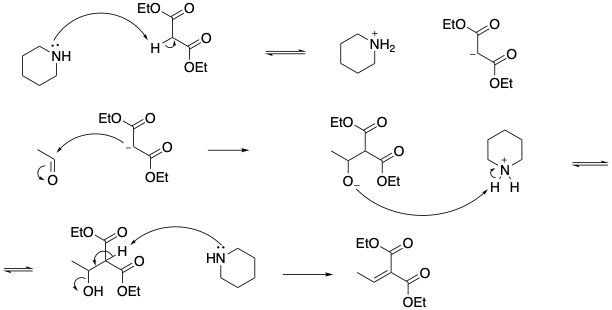
REAZIONE DI KNOEVENAGEL
Nei composti in cui un gruppo metilenico è legato a due gruppi carbonilici ( o anche nitrili o gruppi nitro) i legami C-H sono molto più acidi rispetto agli idrogeni in alfa ad un solo gruppo. Ciò permette di usare, nelle reazioni con le aldeidi e, in alcunio casi, con i chetoni, una base più debole di quelle usate nelle condensazioni aldoliche o di Claisen e di ottenere una concentrazione soddisfacente di ioni enolato, ad una velocità sufficientemente alta. Il processo prende il nome di reazione di Knoevenagel quando vengono usate ammine quali la piuperidina come catalizzatori.



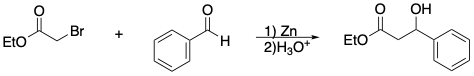


















You must be logged in to post a comment.