Struttura di Lewis – Acidità e basicità

Esercizio n. 1
Scrivete le formule di Lewis dei seguenti composti: (a) SOCl2; (b) COCl2; (c) C2HCl; (d) C2H3I; (e) PCl3; (f) POCl3.
Esercizio n. 2
Disegnate la struttura di Lewis e calcolare la carica formale di ogni atomo diverso dall’idrogeno nelle seguenti specie: (a) HNO2; (b) CH3OSO3H (c) CH3NH3+; (d) HCO3–
Esercizio n. 3
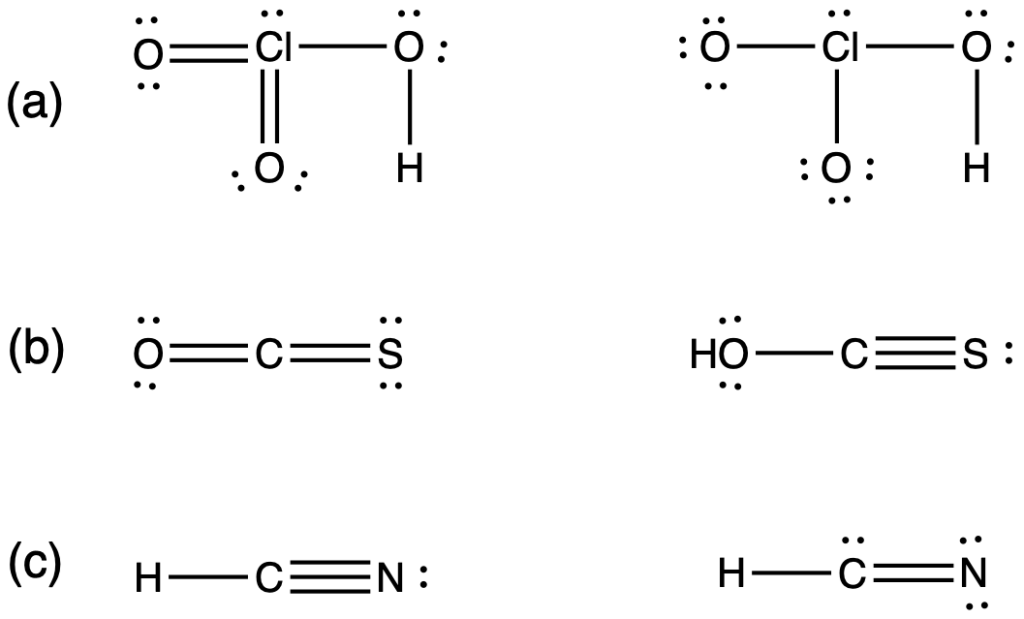
Quale, tra gli ossigeni evidenziati nelle seguenti specie, presenta una carica formale +1?
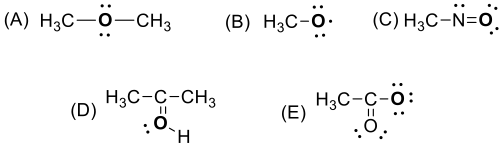
Esercizio n. 4
Disponete i legami indicati nei seguenti composti in ordine di lunghezza crescente, fornendo una adeguata spiegazione
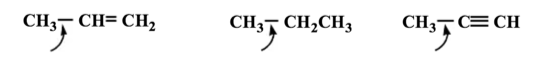
Esercizio n. 5
Indicare quale dei seguenti composti ha momento dipolare = 0: (a) NF3; (b) Cl2; (c) HBr; (d) BBr3; (e) CHCl3 (f) BeCl2.
Esercizio n. 6
Per ogni coppia di molecole o ioni, indicate la base o l’acido più forte e scrivere la sua struttura di Lewis:
(a) CH3S– o CH3O–
(b) CH3NH– o CH3O–
(c) CH3COO– e OH–
(d) CH3CH2O– e H–
(e) NH3 o OH–
(f) CH3COO– o HCO3–
(g) HSO4– o OH–
(h) OH– o Br–
Esercizio n. 7
Spiegate il fatto che l’acido nitroacetico O2NCH2COOH (pKa 1,68) è un acido nettamente più forte dell’acido acetico, CH3COOH (pKa 4,76).
Esercizio n. 8
Scrivete le equazioni relative alle reazioni che i composti elencati di seguito possono dare rispettivamente con AlCl3 (acido di Lewis) e con H2SO4 (acido protico forte): (a) CH3NHCH3; (b) H2C=O; (c) CH3OH; (d) CH3CH2SCH2CH3
Esercizio n. 9
In ciascuno dei seguenti gruppi, disponete i composti in ordine di acidità crescente
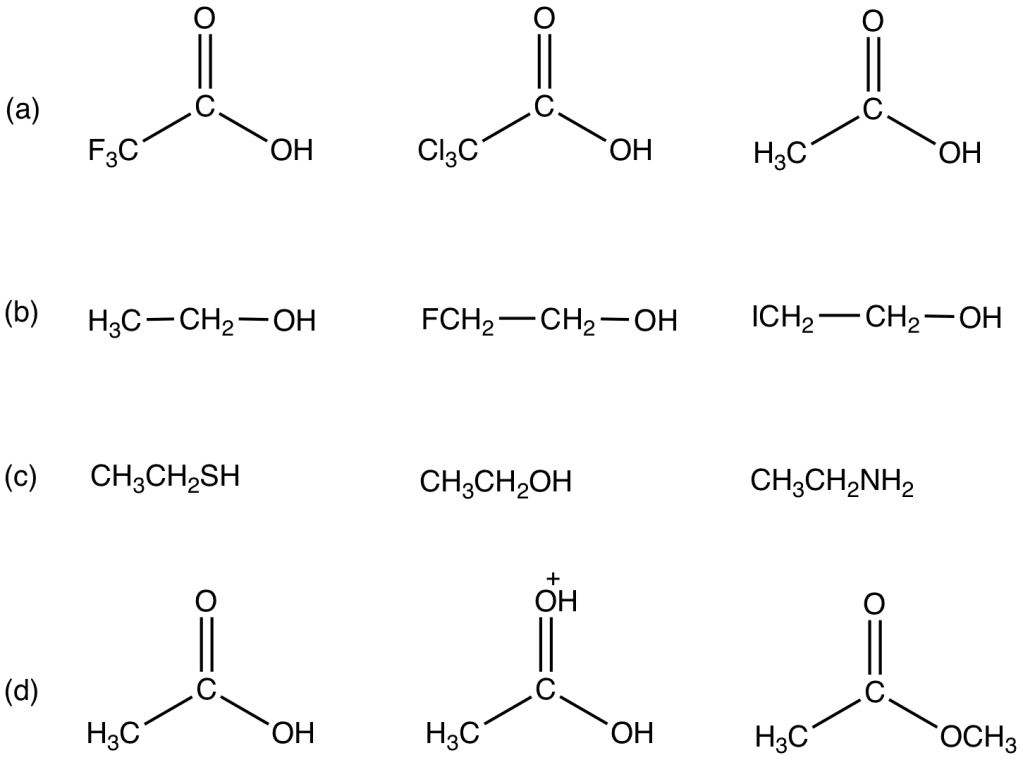
Esercizio n. 10
In ciascuno dei seguenti gruppi, disponete i composti in ordine di basicità crescente
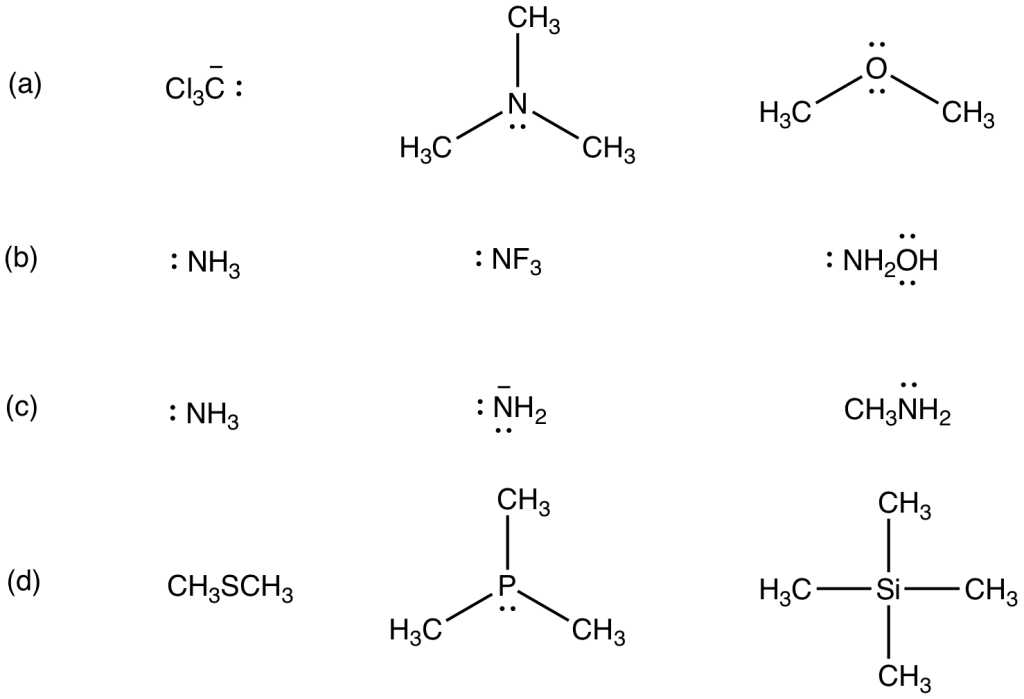

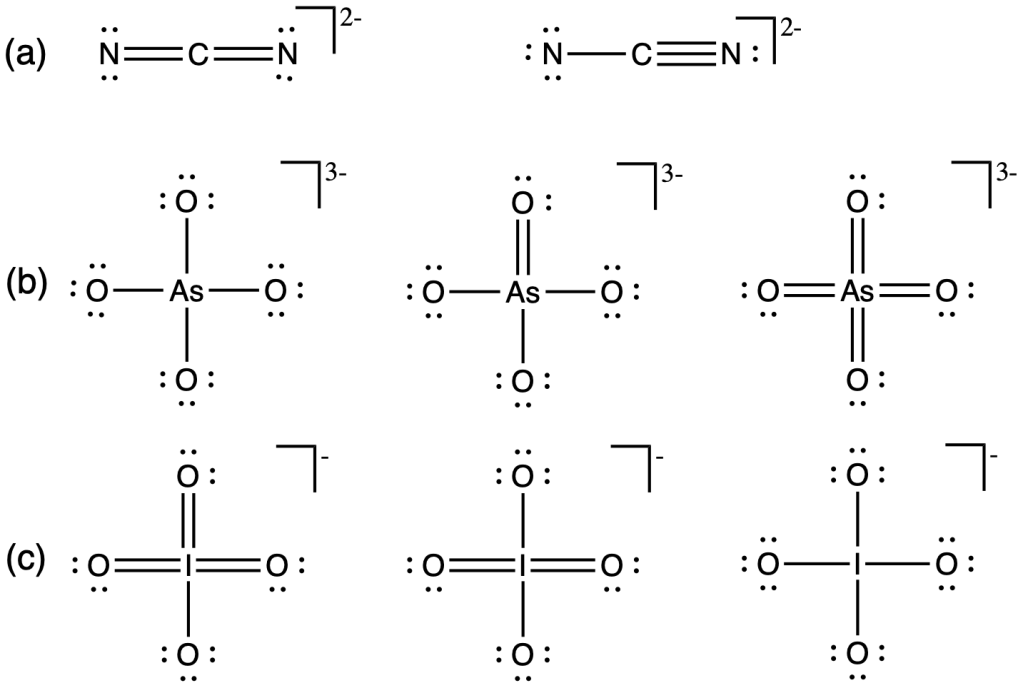











You must be logged in to post a comment.