I prova di recupero: esercitiamoci ancora un po’

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1) Proporre la struttura di una molecole che soddisfi i seguenti criteri: contiene 2 atomi di carbonio ibridati sp2 e 2 atomi di carbonio ibridati sp3. Dire quali sono la geometria e gli ancoli di legame di ciascun carbonio.
2) Scrivere la struttura di Lewis dello ione solfato. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza. Calcolare le cariche formali di ciascun atomo.
3) Rispondere ai seguenti quesiti:
a) A quale valore di pH la concentrazione della forma basica di un composto con pKa 5.2 è 100 volte maggiore rispetto alla forma acida?
c) A quale valore di pH il 50% di un composto con pKa 6.4 si troverà in soluzione nella forma basica?
4) Disporre i seguenti composti in ordine di acidità decrescente e spiegare sinteticamente il perché:
a) CH3CH2CH2SH b) CH3CH2CH2NH2 c) CH3CH2CH2CH3 d) CH3CH2CH2OH
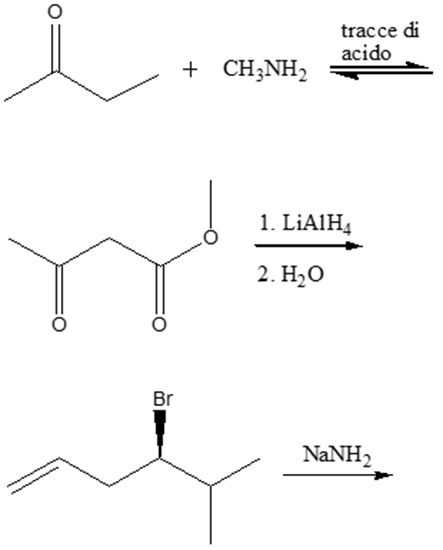
5) Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti

6) Rappresentare la struttura a segmenti e attribuire il nome IUPAC ad un composto di formula molecolare C10H20 che contiene solo H primari e terziari.
7) Scrivere i seguenti composti in proiezione di Fischer e rispondere alle domande I e II:
a) (2S,3S)-2,3-dibromobutano
b) (2R,3S)-2,3-dibromobutano
c) (2S,3R)-2,3-dibromobutano
d) (2R,3R)-2,3-dibromobutano
I) Quali composti sono otticamente attivi?
II) Dire qual è la relazione esistente tra le seguenti coppie di composti (enantiomeri/diastereoisomeri/ isomeri geometrici/isomeri conformazionali/ stesso composto/isomeri costituzionali/altro):
a e b sono_____________________
a e c sono_____________________
a e d sono_____________________
b e c sono_____________________
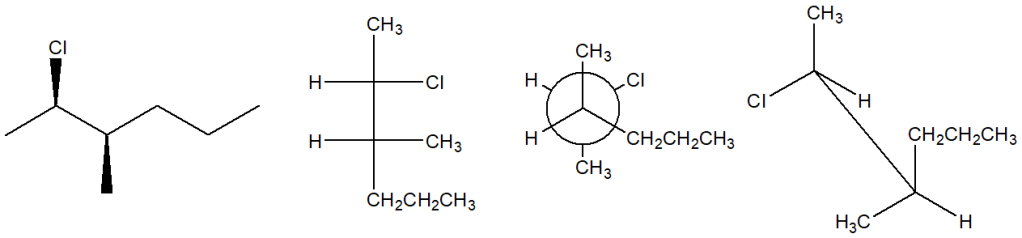
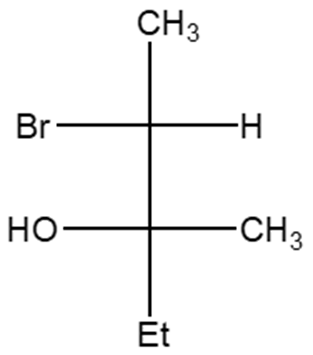
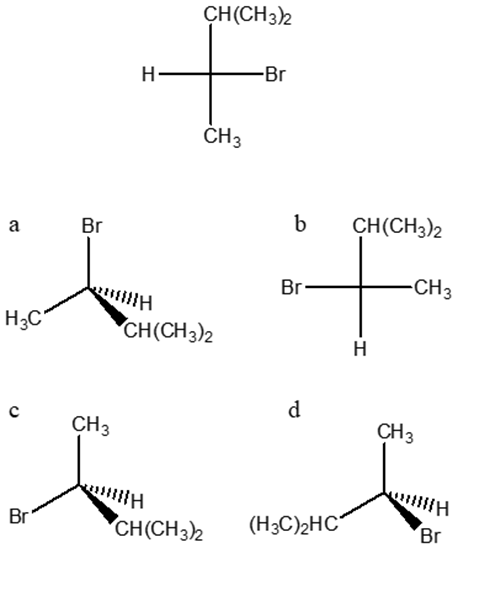
8) Quale delle seguenti strutture corrisponde al (2S,3S)-2-cloro-3-metilesano?
9) Disegnare il trans-1-isopropil-3-metilcicloesano in proiezione di Newman (rispetto ai legami C1-C6 e C3-C4). Effettuare l’inversione d’anello. Indicare qual è tra i due il conformero a più alta energia e spiegare perchè individuando le interazioni che lo rendono meno stabile rispetto all’altro
10) Scrivere le proiezioni di Newman della conformazione anti e delle due conformazioni
eclissate dell’1,2-diiodoetano. Quale delle due conformazioni eclissate ha energia maggiore?
SECONDO SET
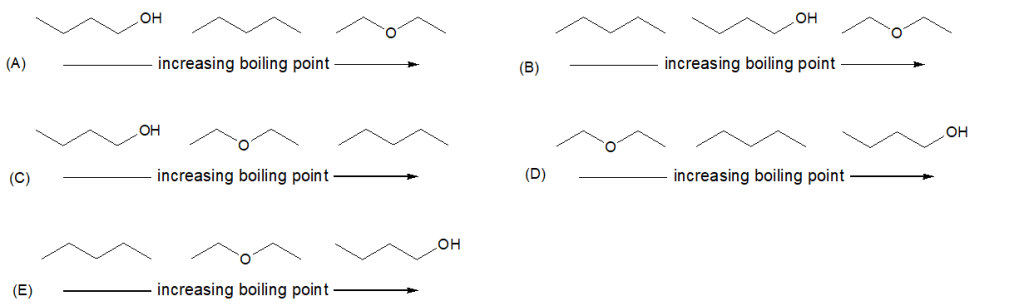
1) Ordina i seguenti alcani secondo il punto di ebollizione crescente:
I) esano
II) ottano
III) 2-metilpentano
IV) 2,2-dimetilbutano
2) Dire quali sono l’ibridazione, la geometria e l’angolo di legame del catione metile.
3) Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
e) può essere sia di legame sia di antilegame
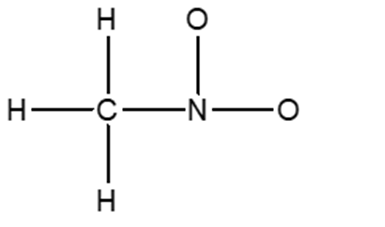
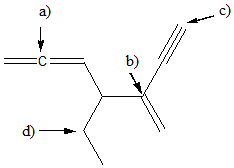
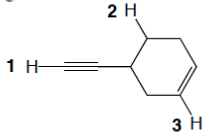
4. Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia. Dire qual è il legame singolo C-C più corto?

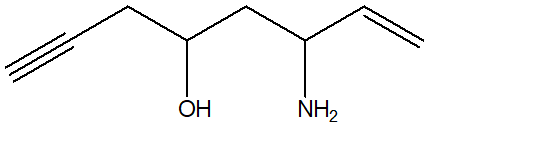
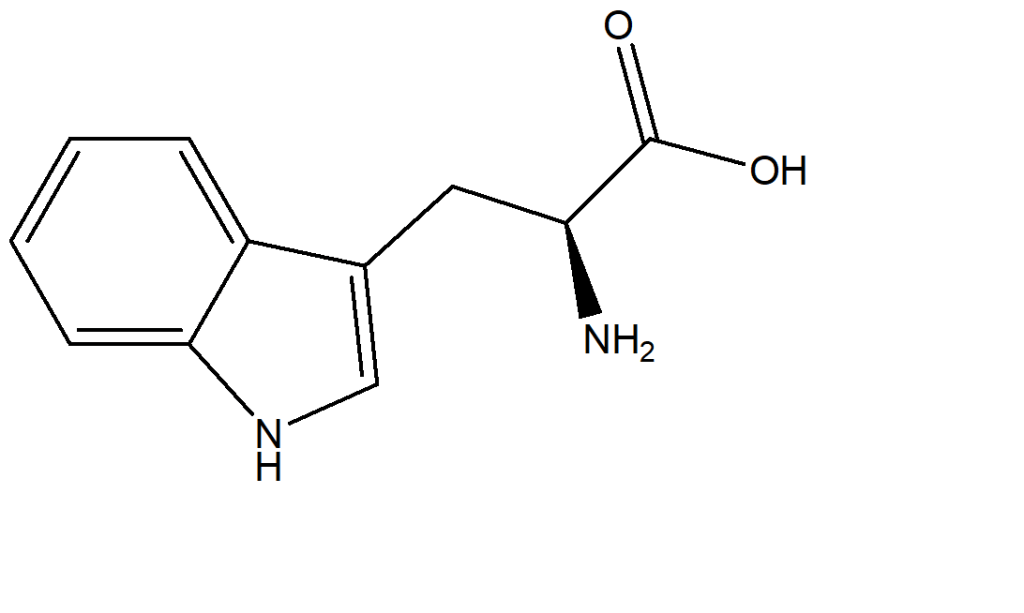
5) Dire quale atomo nella seguente molecola può essere più facilmente deprotonato
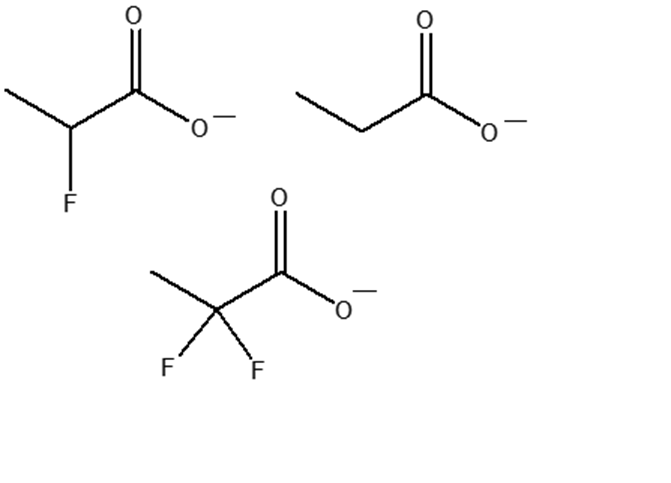
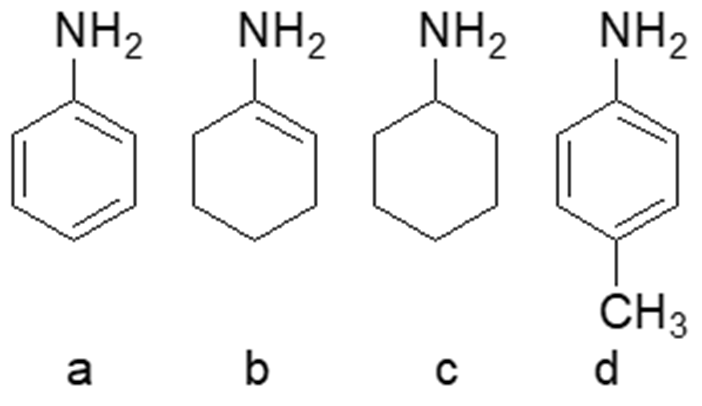
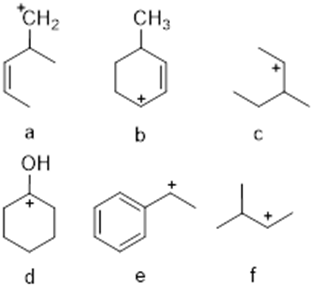
6) Metti i seguenti composti in ordine di basicità crescente e motivare la scelta

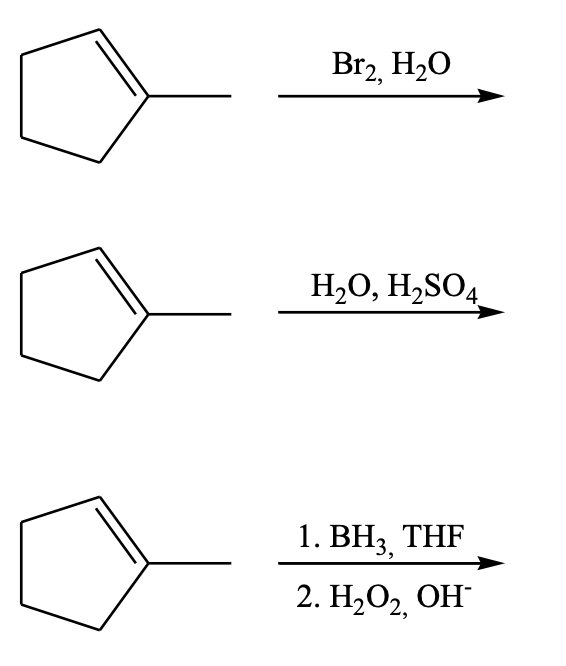
7) Scrivi il prodotto della seguente reazione acido-base e indica la direzione dell’equilibrio
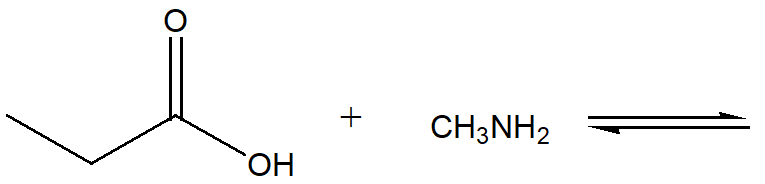
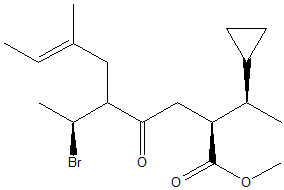
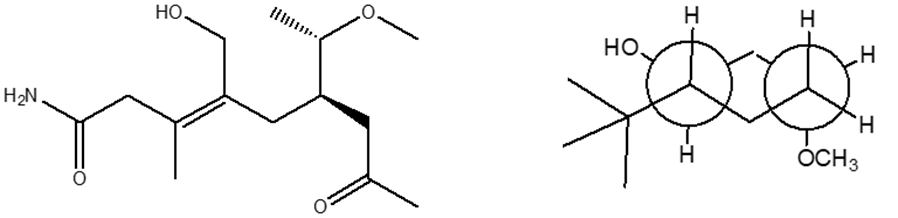
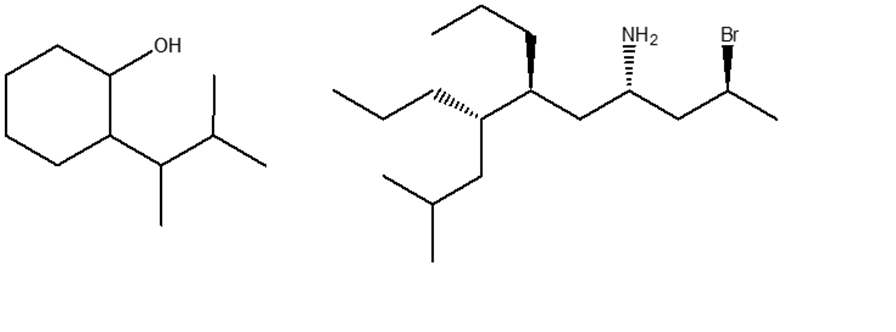
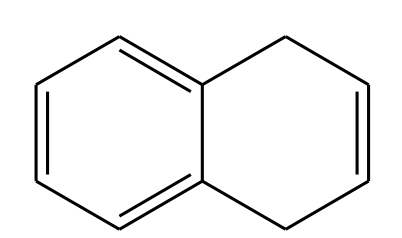
8) Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti

9) Rappresentare la struttura a segmenti dei seguenti composti:
a) 4-metil-2-metossi-3-esanolo
b) N,N,3-trietilciclopentanammina
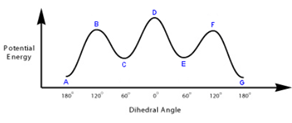
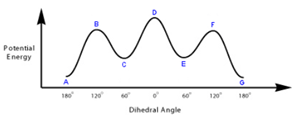
10) Il seguente grafico mostra l’energia potenziale al variare dell’angolo diedro, guardando il legame C-C della molecola di 1-bromo-1-cloro-2-fluoroetano. Completare le proiezioni di Newman ed elencare il tipo di tensione presente in ciascuna di esse

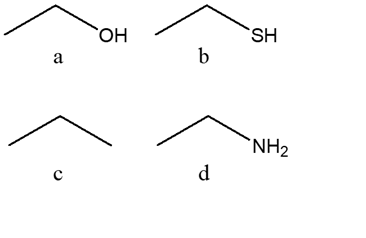
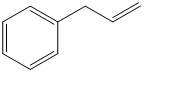
11) Dire quali dei seguenti composti ruotano il piano della luce polarizzata

12) Dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/ isomeri geometrici/isomeri conformazionali/ stesso composto/isomeri costituzionali/altro)

a e b sono________________________________
a e c sono________________________________
b e c sono________________________________
13) Quale delle seguenti affermazioni è vera per qualsiasi enantiomero S?

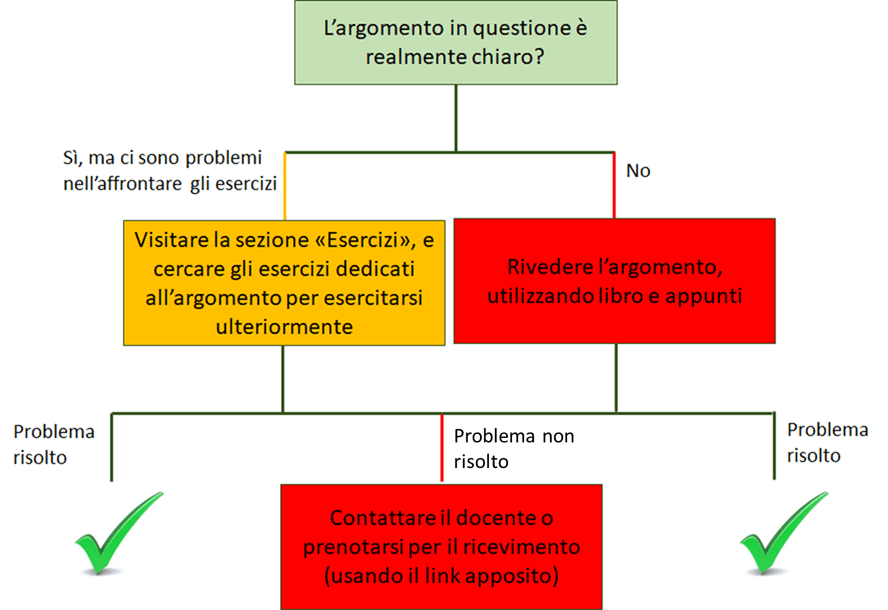
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate







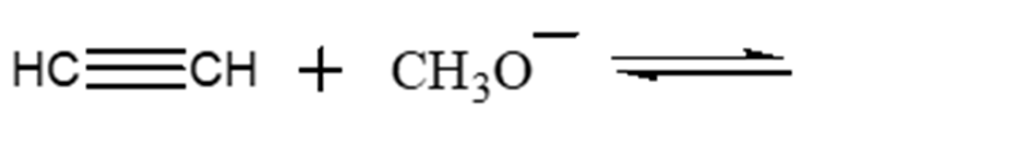







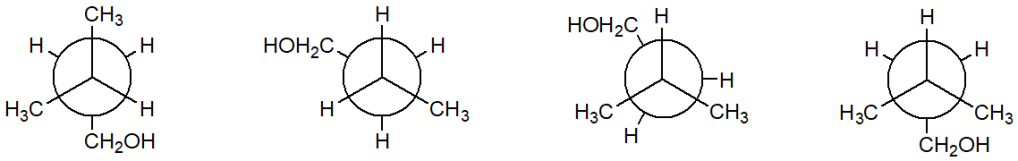

































You must be logged in to post a comment.