Training IV…

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomentii…e a breve altre saranno pubblicate. In ogni caso, potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti.
- Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto
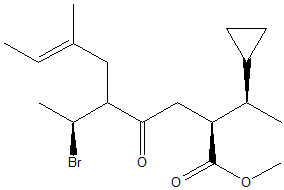
2. Quanti stereoisomeri sono possibili per il composto riportato in 1?
3. Disegna le proiezioni di Newman dei due conformeri a sedia del cis-1,3-dimetilcicloesano e del trans-1,3-dimetilcicloesano. Quali conformeri predominano all’equilibrio?
5. Scrivi la struttura del D-glucosio e attribuisci la configurazione assoluta a ciascuno dei carboni chirali.
6. Mostra la ciclizzazione del D-glucosio a D-glucopiranosio e spiega il fenomeno della mutarotazione.
7. Considerando che il galattosio è l’epimero in 4 del glucosio, cosa sono tra di loro, dal punto di vista della stereochimica, l’alfa-D-galattopiranosio e il beta-L-glucopiranosio?
8. Chiarisci a cosa fa riferimento la notazione D/L utilizzata sia per i carboidrati, sia per gli amminoacidi.
[Domande 9-11 eliminate poichè erano presenti degli errori]
12. Elencare i derivati degli acidi carbossilici in ordine di reattività crescente in una reazione di sostituzione nucleofila acilica, motivando la risposta.
13. I nitrili sono molto utili nella sintesi. Mostrare il meccanismo di idrolisi di un nitrile, in particolare del propanonitrile, indicando anche le condizioni di reazione.
14. A partire dal composto sintetizzato in 13, mostrare come, in più passaggi, è possibile ottenere il 2-metil-2-propossibutano utilizzando come ulteriore fonte di atomi di carbonio solo un reattivo di Grignard.
15. A partire dal composto sintetizzato in 13, ottenere un’aldeide, un estere, un chetone (NB: potrebbero essere necessari più passaggi). Poi, per ciascun composto, dindividuare l’idrogeno più acido. Infine, mettere i composti ottenuti e il composto iniziale in ordine di acidità crescente, motivando la scelta.
16. A partire dall’aldeide sintetizzata in 15, mostrare il meccanismo e il prodotto di condensazione aldolica.
17. A partire dall’estere e dal chetone sintetizzati in 15, mostrare il meccanismo e il prodotto della condensazione di Claisen mista.
18. Nel caso della condensazione aldolica, utilizziamo quantità catalitiche di base. Invece, nel caso della condensazione di Claisen ne utilizziamo quantità equivalenti. Spiegare perchè.
19. Il prodotto di addizione aldolica disidrata anche in condizioni basiche, riscaldando la soluzione. Se il prodotto ha un sistema coniugato esteso, la disidratazione avviene ancora più facilmente. Spiegare perchè.
20. A proposito di sistemi coniugati, spiegare la stabilità di un sistema coniugato (es. 1,3-butadiene) secondo la teoria degli orbitali molecolari.
21. Sia un carbocatione sia un radicale benzilico sono stabilizzati per risonanza. Mostare in che modo, disegnando un esempio di ciascuno e scrivendo tutte le possibili strutture di risonanza.
22. Spiegare perchè gli alogenuri vinilici e arilici non subiscono nè reazioni SN1 nè reazioni SN2.
23. A proposito di reazioni di sostituzione, gli alcoli possono essere trasformati in alogenuri alchilici, utilizzando le opportune condizioni di reazione. Illustrare tutti i metodi studiati.
24. Uno dei metodi cui si fa riferimento in 23 prevede l’utilizzo del cloruro di tionile. Questo, come altri metodi utilizzati, funziona bene con gli alcoli primari e secondari, mentre le reazioni con gli alcoli terziari danno rese molto scarse. Spiegare perchè.
25. Le reazioni di sostituzione e di eliminazione sono in competizione. Immaginiamo di avere un alogenuro alchilico terziario. Quali condizioni di reazione dobbiamo utilizzare per favorire la sostituzione? Con quale meccanismo avviene? E l’eliminazione?
26. Perchè parliamo di reazioni E1 ed E2?
27. Mostrare una strategia e un meccanismo di sintesi che da (R)-2-bromobutano porti alla sintesi di 2,3-diclorobutano non otticamente attivo, ma che può essere separato in due composti otticamente attivi mediante una classica analisi cromatografica (NB: sono necessari più passaggi ed è necessario seguire la stereochimica nel corso della reazione).
28. Quali altri prodotti si possono ottenere da 27? Questi ruoteranno il piano della luce polarizzata? Perchè?
29. Per ciascuna reazione effettuata in 27, disegnare il diagramma che mostra il livello di energia in funzione della coordinata di reazione, completo di intermedi di reazione e stati di transizione.
30. Introduci i lipidi.
You must be logged in to post a comment.