Allenamento per la seconda prova intercorso

Esercizio n. 1
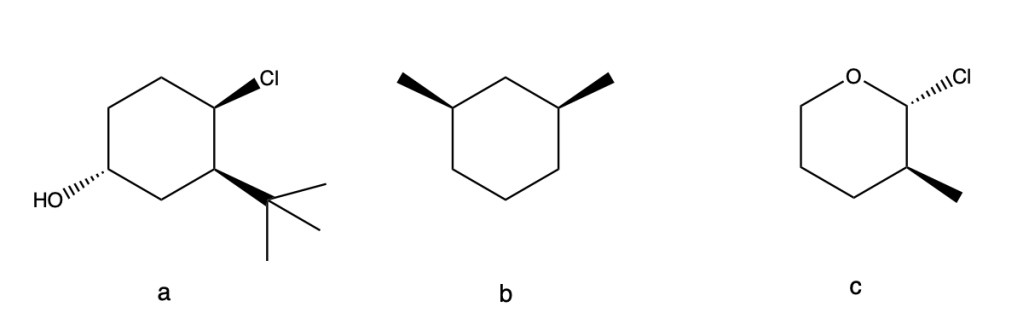
Identificare la relazione strutturale esistente tra i due termini di ciascuna delle 4 coppie di composti (enantiomeri, diastereoisomeri, isomeri costituzionali, conformeri, due rappresentazioni dello stesso composto)
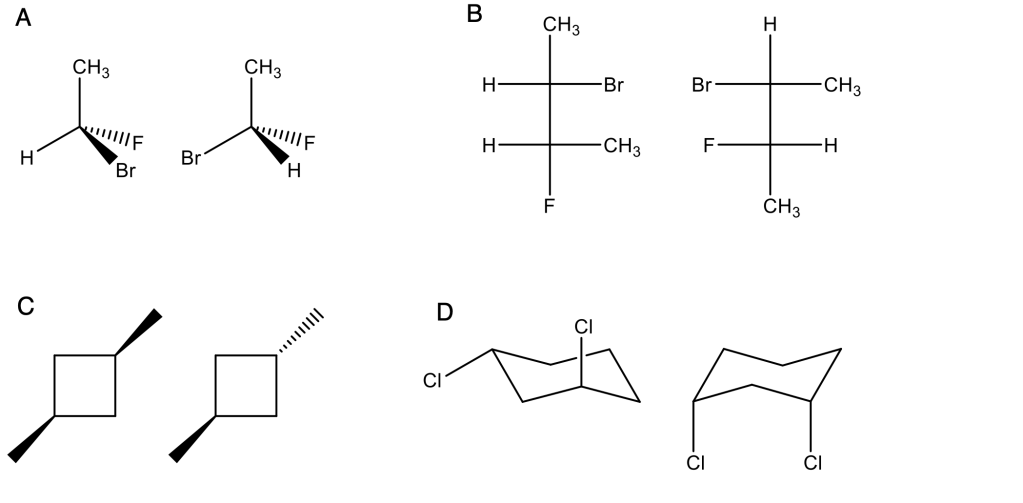
Esercizio n. 2
Assegnare la configurazione assoluta (R/S) ai carboni chirali delle seguenti molecole. Trasformare tutte le strutture in proiezioni di Fischer:
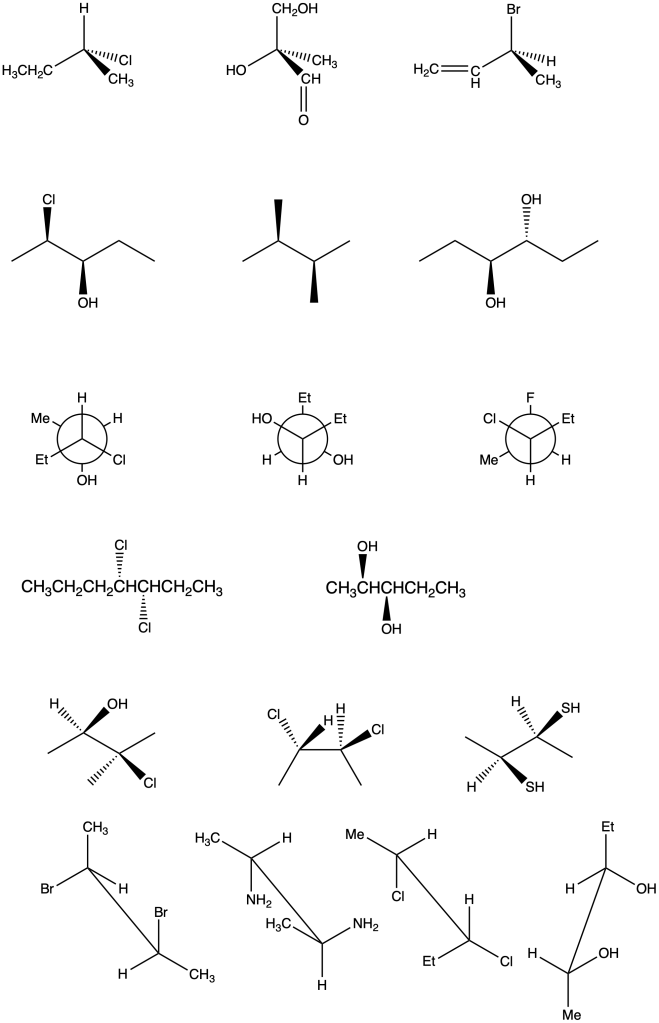
Esercizio n. 3
Attribuire le configurazioni R o S a ciascuno dei seguenti composti. Trasformare le strutture tridimensionali in proiezioni di Fischer
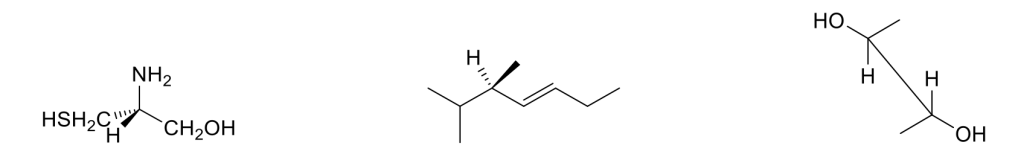
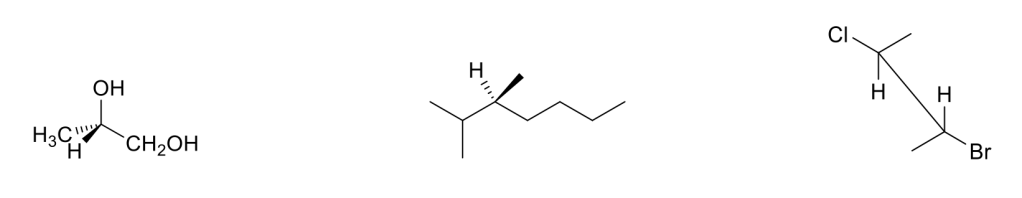
Esercizio n. 4
Scrivete almeno tutti i possibili isomeri (compresi gli stereoisomeri) del diclorociclobutano. Per ognuno di essi scrivere il nome IUPAC indicando se sono otticamente attivi.
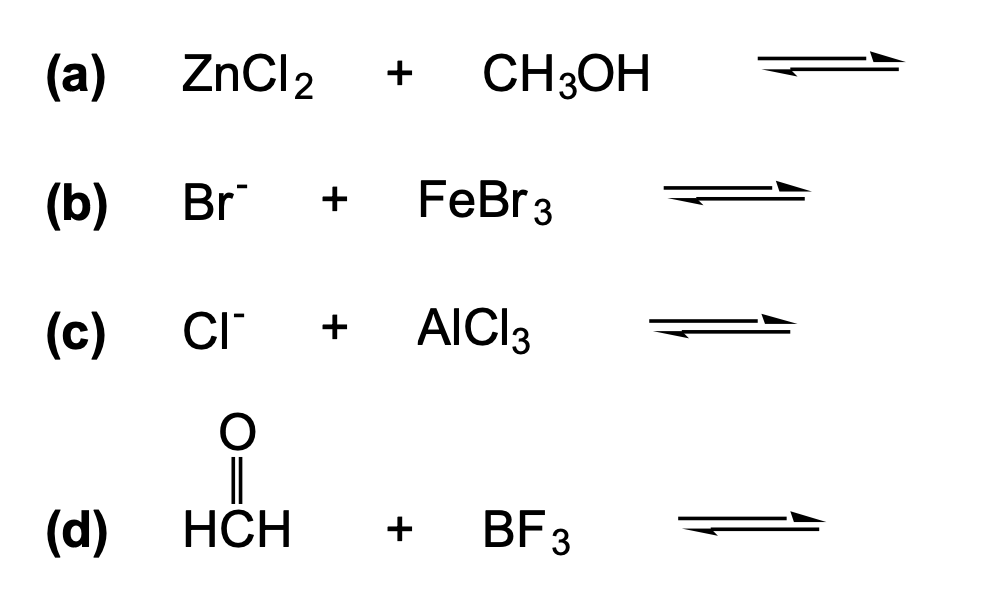
Esercizio n. 5
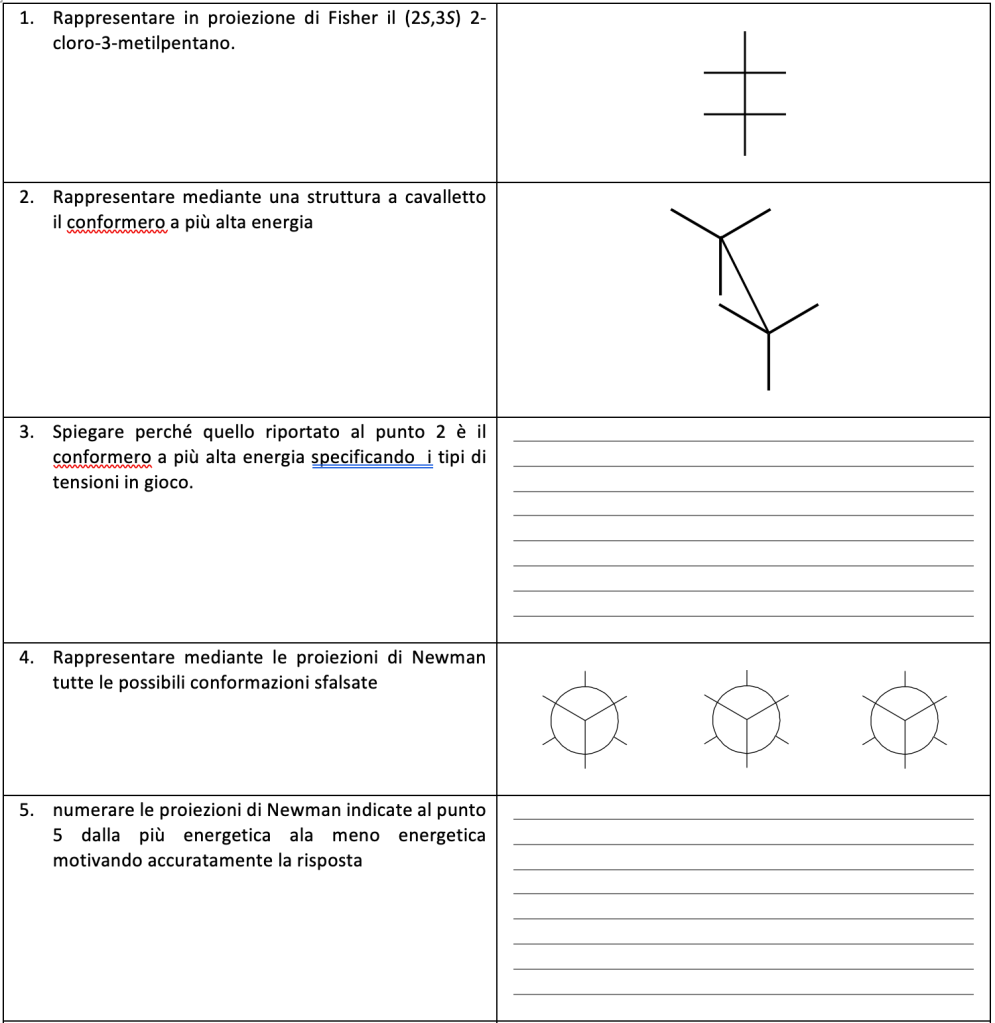
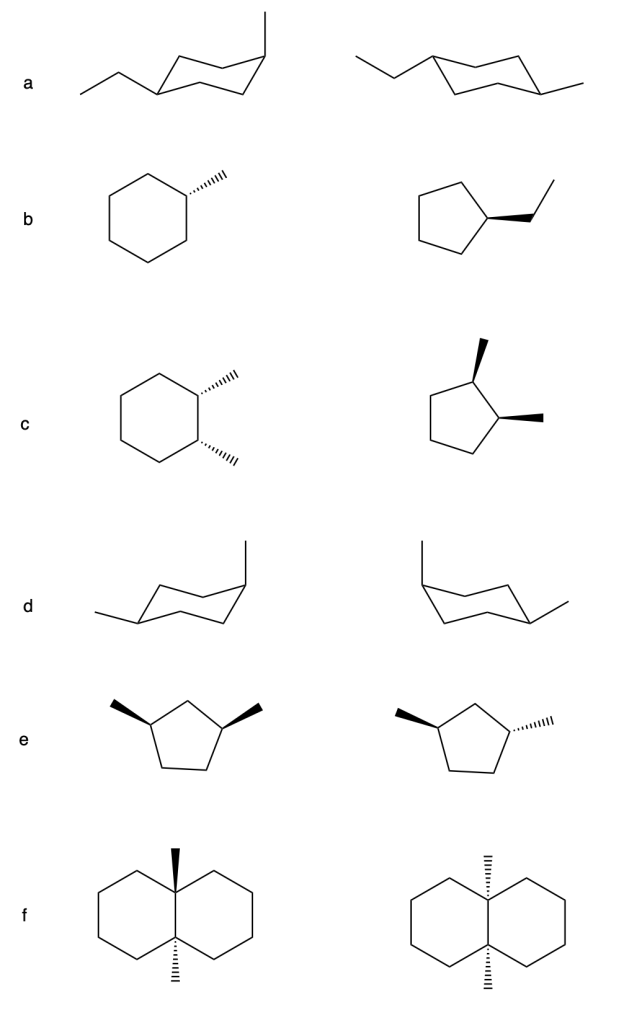
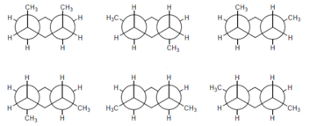
Esercizio n. 6
Per ognuna delle seguenti coppie di strutture indicare se i composti sono (a) identici (b) isomeri costituzionali (c) enantiomeri (d) diastereoisomeri (e) identici e composti meso (f) composti differenti non isomerici
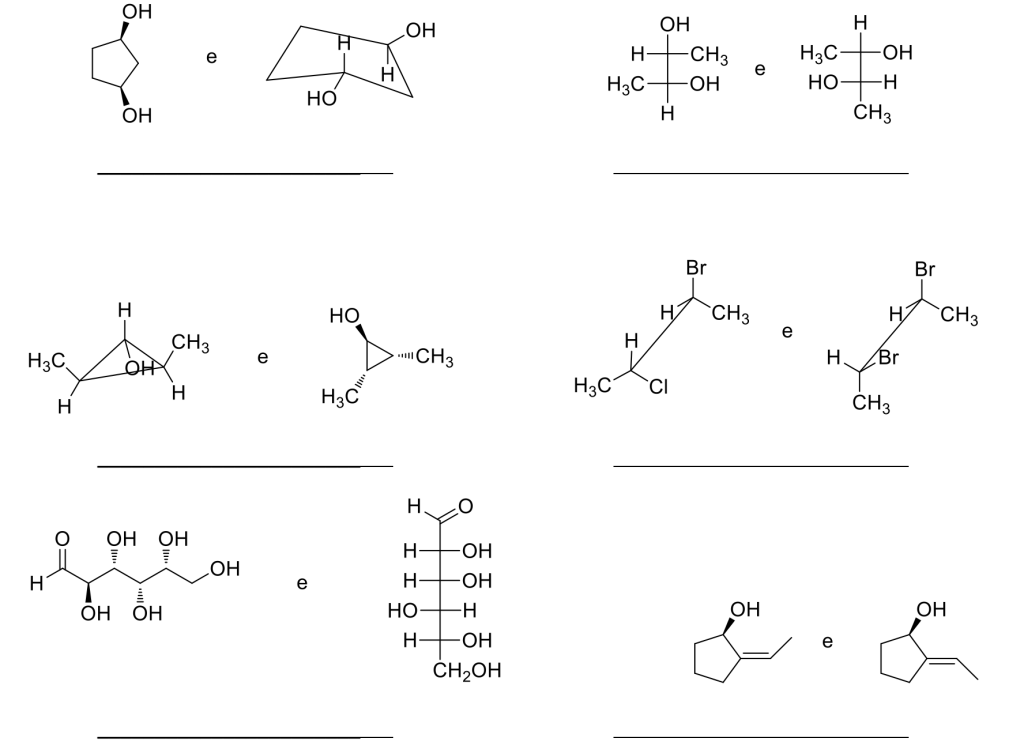
Esercizio n. 7
Rispondere alle seguenti domande relative ad un composto organico di formula bruta C3H4Cl2
- Qual è la struttura di un isomero che ammette isomeria cis/trans?
- Qual è la struttura di un suo isomero che non ammette isomeria cis/trans?
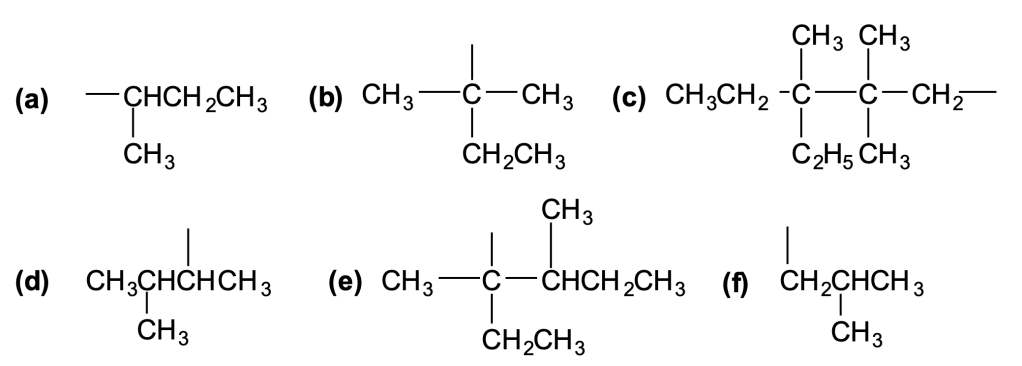
Esercizio n. 8
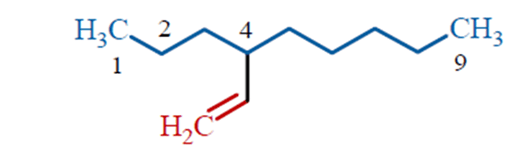
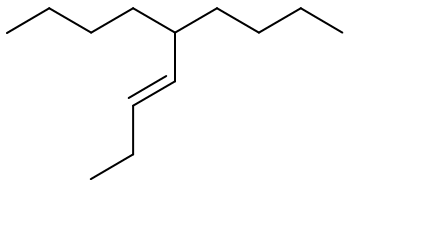
Assegnare il nome IUPAC ai seguenti composti
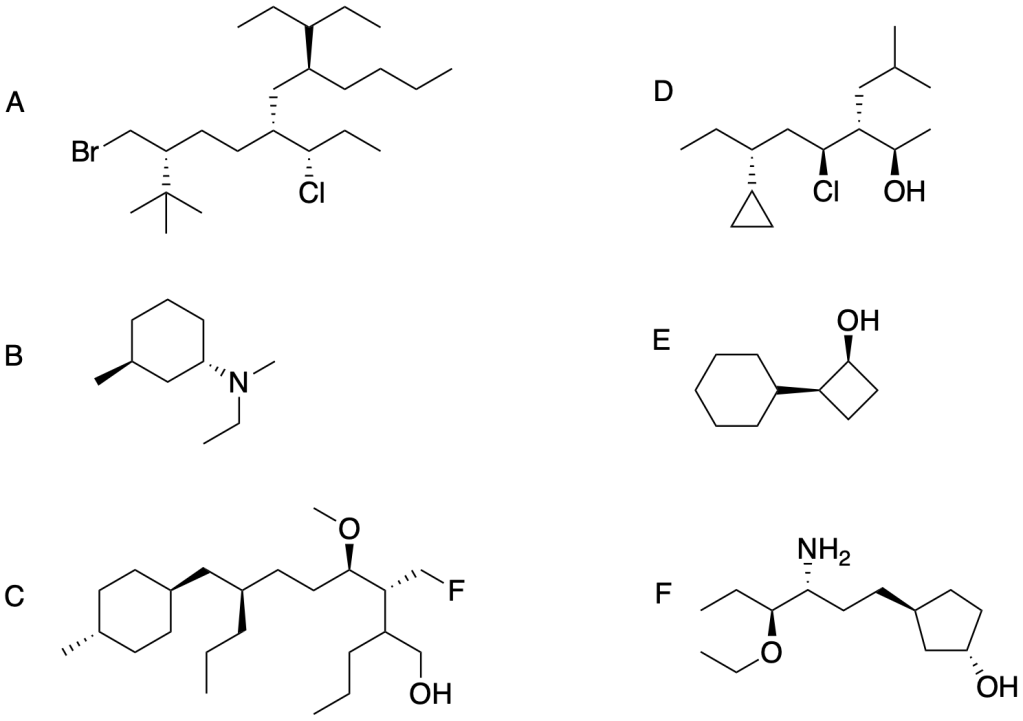
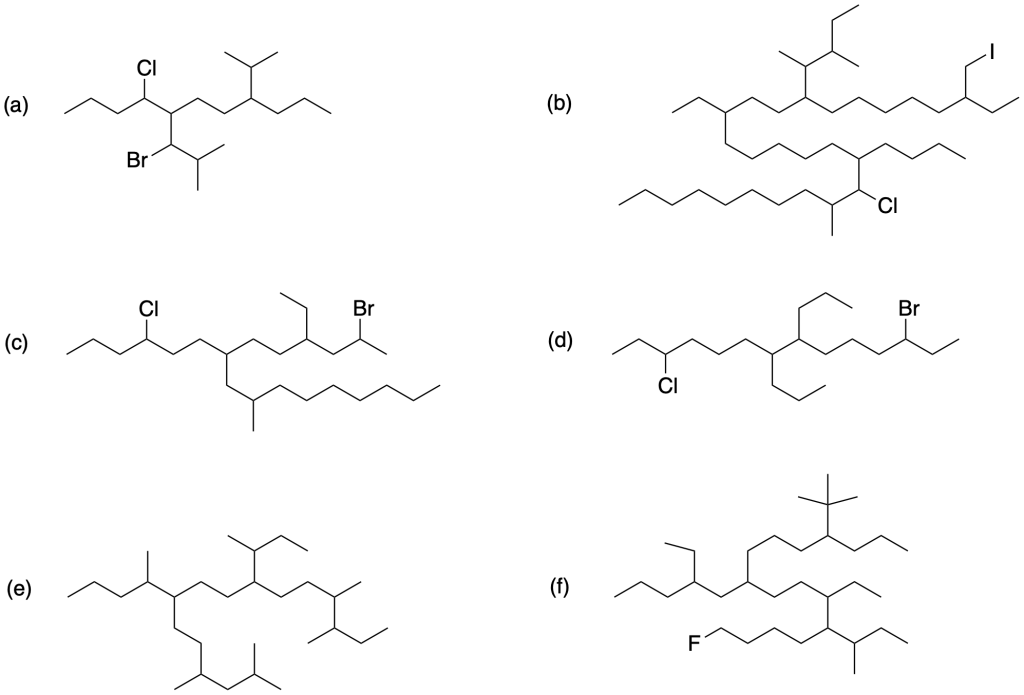
Esercizio n. 9
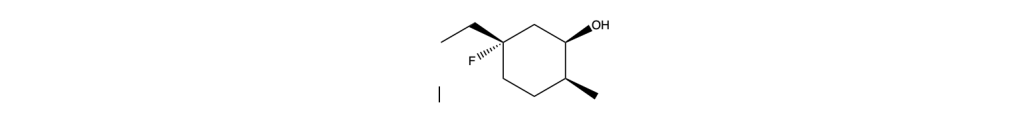
Assegnare il nome IUPAC (comprensivo si stereochimica) ai seguenti composti
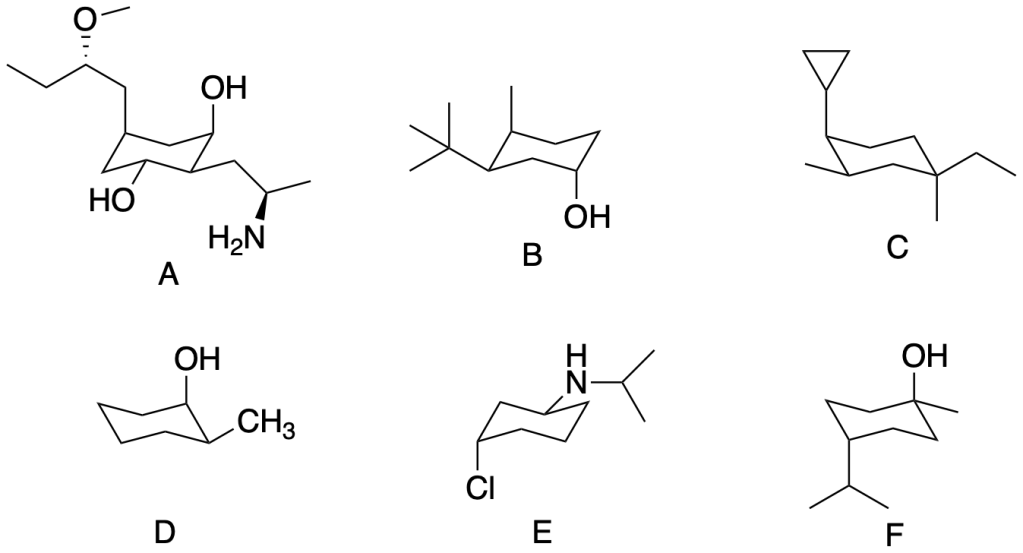




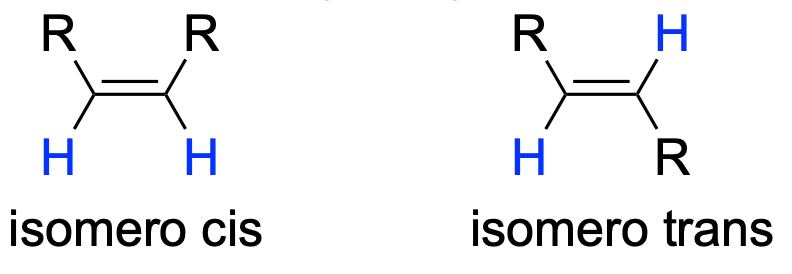



















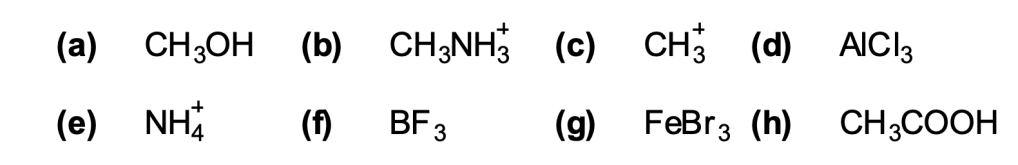

You must be logged in to post a comment.