Nomenclatura IUPAC: aggiornamenti relativi agli alcheni

![]() L’ultimo aggiornamento delle regole di nomenclatura IUPAC* prevede delle variazioni in relazione alla nomenclatura degli alcheni rispetto alle regole antecedenti, con particolare riferimento a quella che è la determinazione della catena principale.
L’ultimo aggiornamento delle regole di nomenclatura IUPAC* prevede delle variazioni in relazione alla nomenclatura degli alcheni rispetto alle regole antecedenti, con particolare riferimento a quella che è la determinazione della catena principale.
A differenza di quanto accadeva con le regole precedenti, ora la lunghezza della catena è più importante rispetto alla presenza del doppio legame.
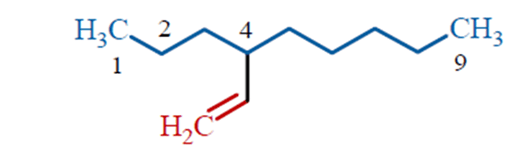
Ad esempio, il composto che segue, si chiama 4-etenilnonano: la catena più lunga è a 9 atomi di carbonio e non contiene il doppio legame. La porzione della molecola che contiene il doppio legame è dunque un sostituente, per il quale si usa il suffisso “-enil” (per indicare con “-en-” anche la presenza del doppio legame).
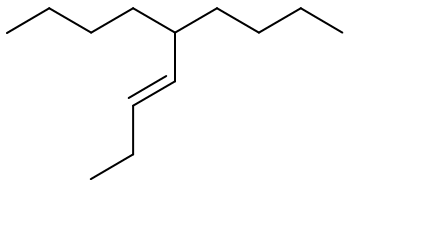
Se sono, invece, presenti due catene della stessa lunghezza, la catena principale sarà quella che contiene il doppio legame. Ad esempio, la molecola seguente sarà un 5-butilnon-3-ene.
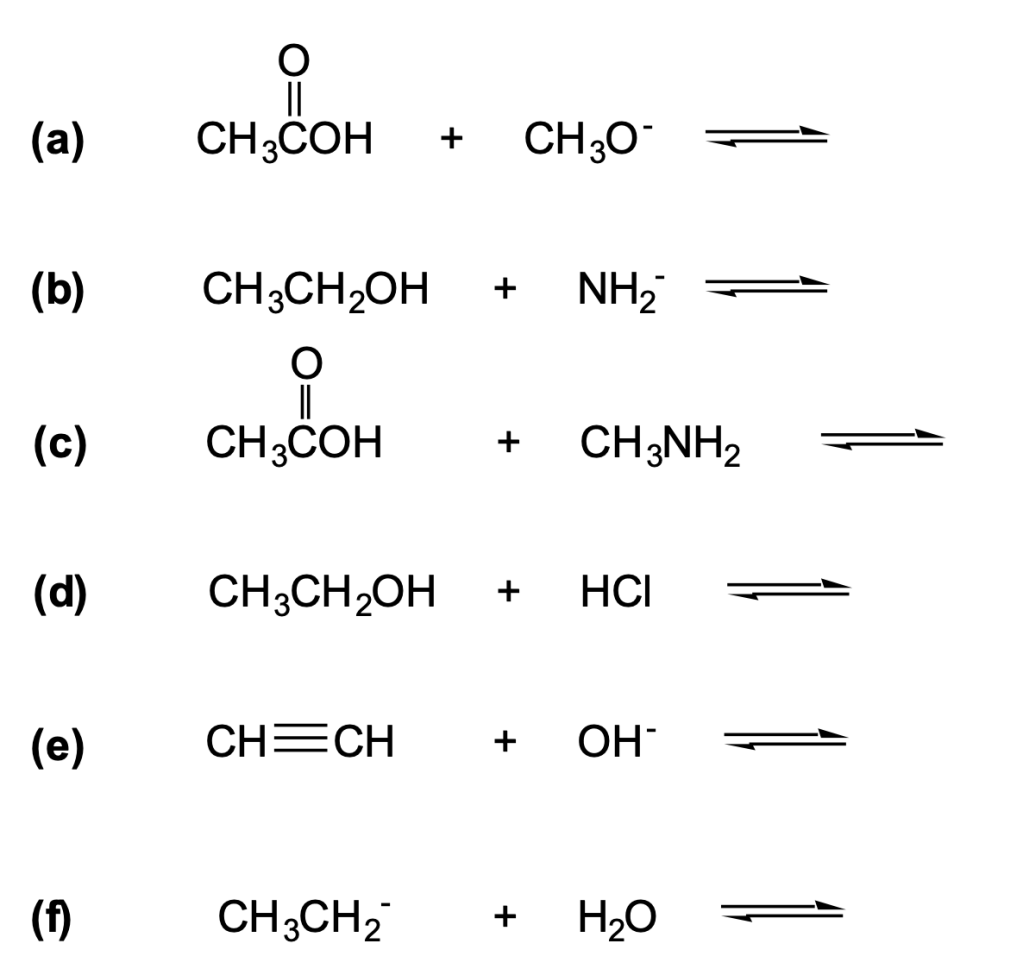
NB: Per sostituenti più lunghi di due atomi di carbonio, bisogna anche indicare la posizione del doppio legame. Esempi:

NB: a rigore, per il primo dei due composti, bisogna indicare anche la geometria del doppio legame
Una conseguenza di questo aggiornamento e di quello, precedentemente visto, relativo alla priorità del ciclo rispetto ad una catena aperta, è che se una molecola è un cicloalcano che lega una catena carboniosa che presenta un doppio legame, l’idrocarburo principale sarà il cicloalcano. Esempi:

Le slide della lezione relativa a questa parte possono essere scaricate qui.
Un ulteriore aggiornamento è relativo all’indicazione della geometria del doppio legame (E/Z). Secondo le indicazioni precedenti, non era necessario indicare tra parentesi la posizione cui faceva riferimento la notazione E/Z quando nella molecola era presente un solo doppio legame. Secondo le regole aggiornate, invece, il numero del carbonio cui fa riferimento la notazione E/Z va sempre indicata. Esempio: (2E)-2-butene.














You must be logged in to post a comment.