Alleniamoci per la prossima prova intercorso: reazioni degli alcheni

Esercizio n. 1
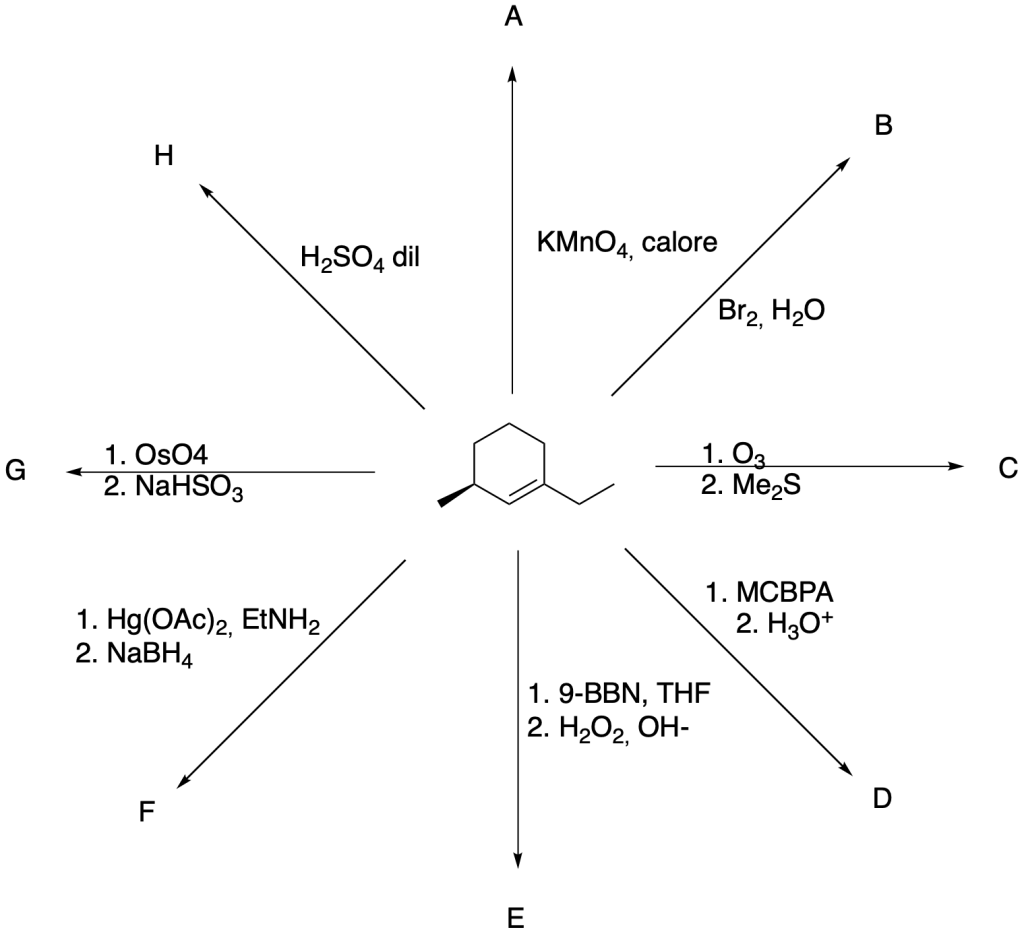
Scrivere il meccanismo delle reazioni elencate di seguito utilizzando l’(R)-6-fenil-1-metilcicloesene e qualsiasi altro reagente necessario. Per ogni reazione porre attenzione, dove appropriato, alla regioselettività, stereoselettività e alla stereospecificità. Assegnare, inoltre, il nome IUPAC ai prodotti di ogni reazione, specificandone la stereochimica e la relazione esistente tra loro (enantiomeri, diastereoisomeri, composto meso, ecc).
- Addizione di acidi alogenidrici
- Addizione di acqua, acido-catalizzata
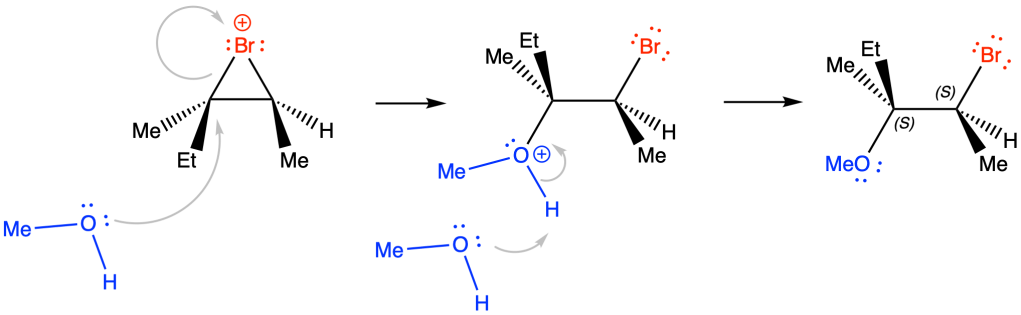
- Ossimercuriazione (o alcossimercuriazione)-demercuriazione
- Idroborazione-ossidazione
- Addizione di alogeni
- Addizione di alogeni in presenza di acqua (o alcol)
- Idrogenazione catalitica
- sin-Ossidrilazione
- Epossidazione
- Scissione ossidativa con permanganato di potassio
- Ozonolisi
Esercizio n. 2
Identificare i reagenti per ciascuna delle seguenti reazioni di addizione agli alcheni. Per le attuali conoscenze, trascurare le reazioni che porta alla formazione dell’1-bromo-2-metilcicloesano e dell'(1S,2S)-1-metil-1,2-cicloesandiolo

Esercizio n. 3
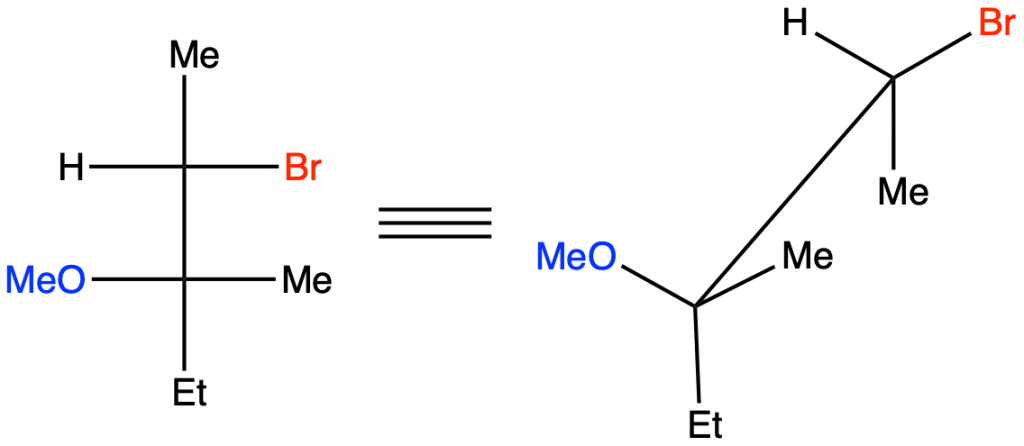
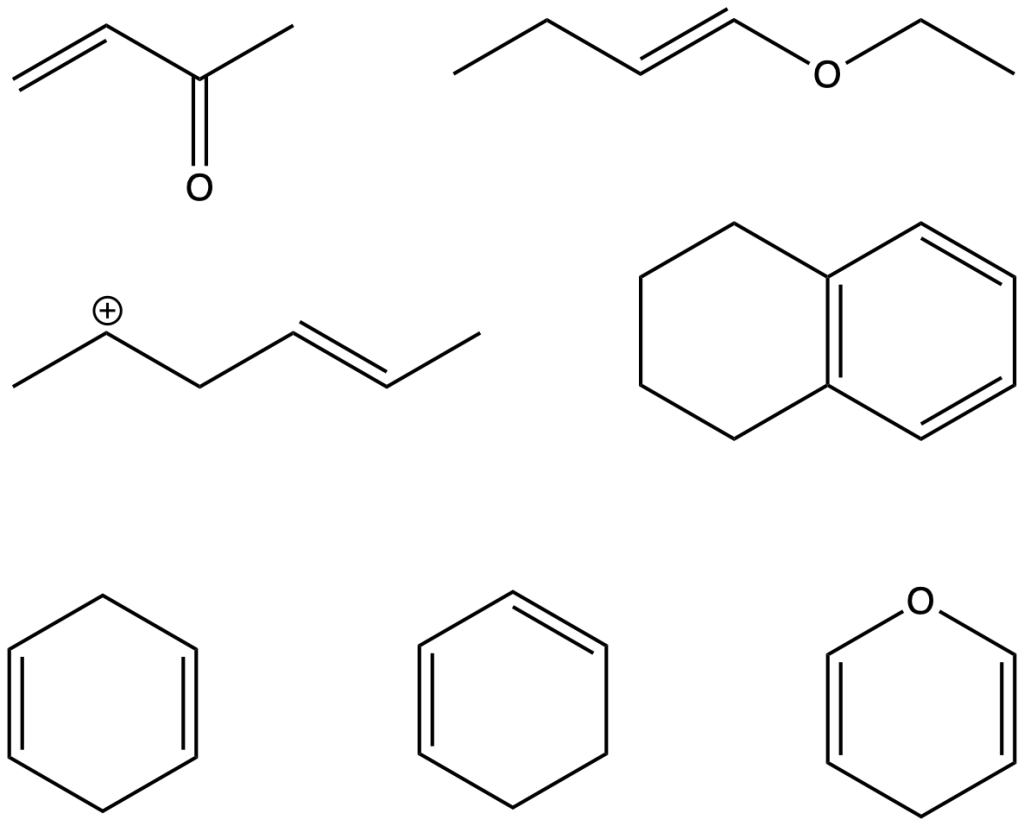
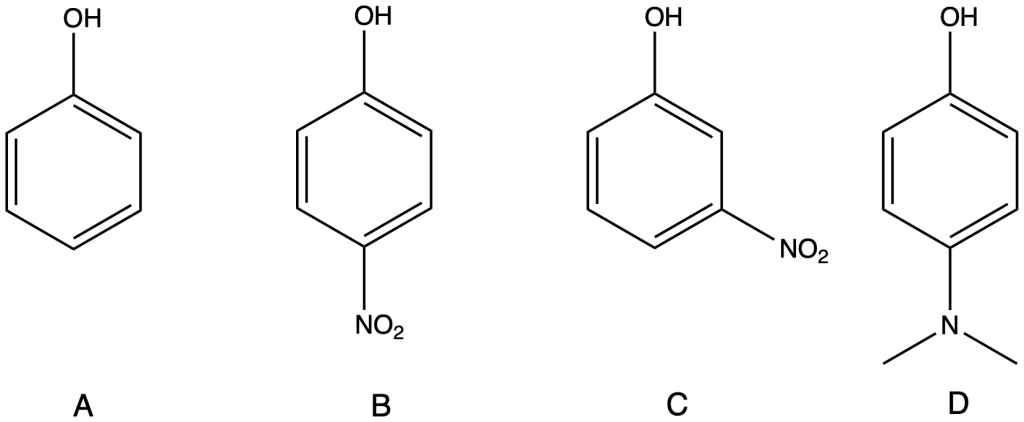
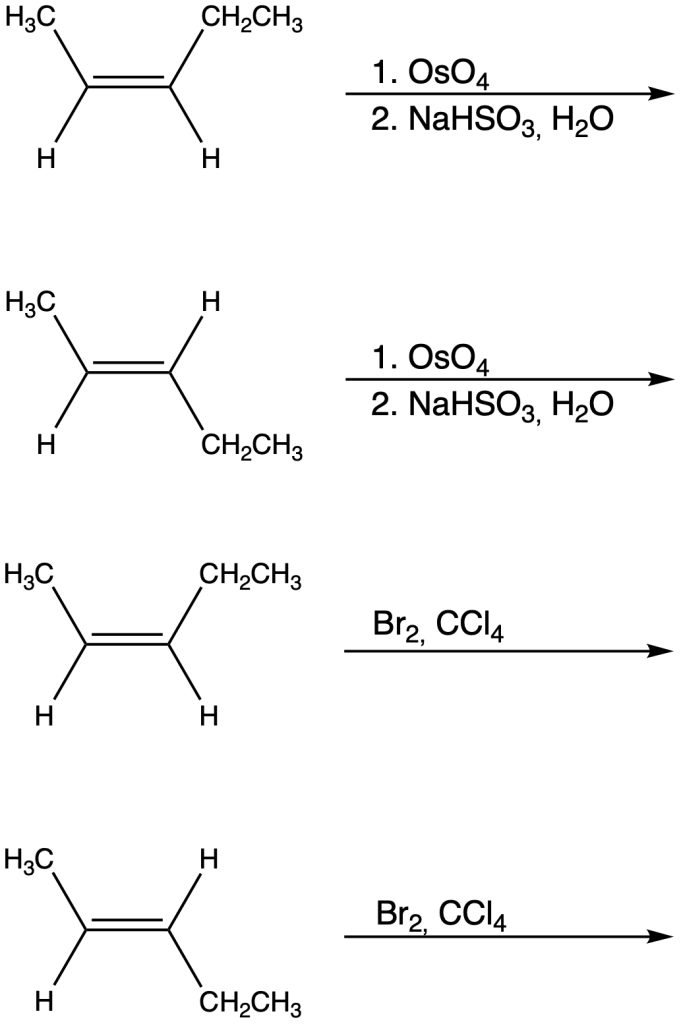
Determinare il prodotto per ognuna delle seguenti reazioni. fare attenzione alla regio- e stereoselettività delle reazioni
Esercizio n. 4
Per ciascuna reazione dell’esercizio n. 1, disegnare un diagramma di energia libera/coordinata di reazione e individuare lo stadio cinetico





























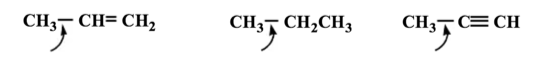
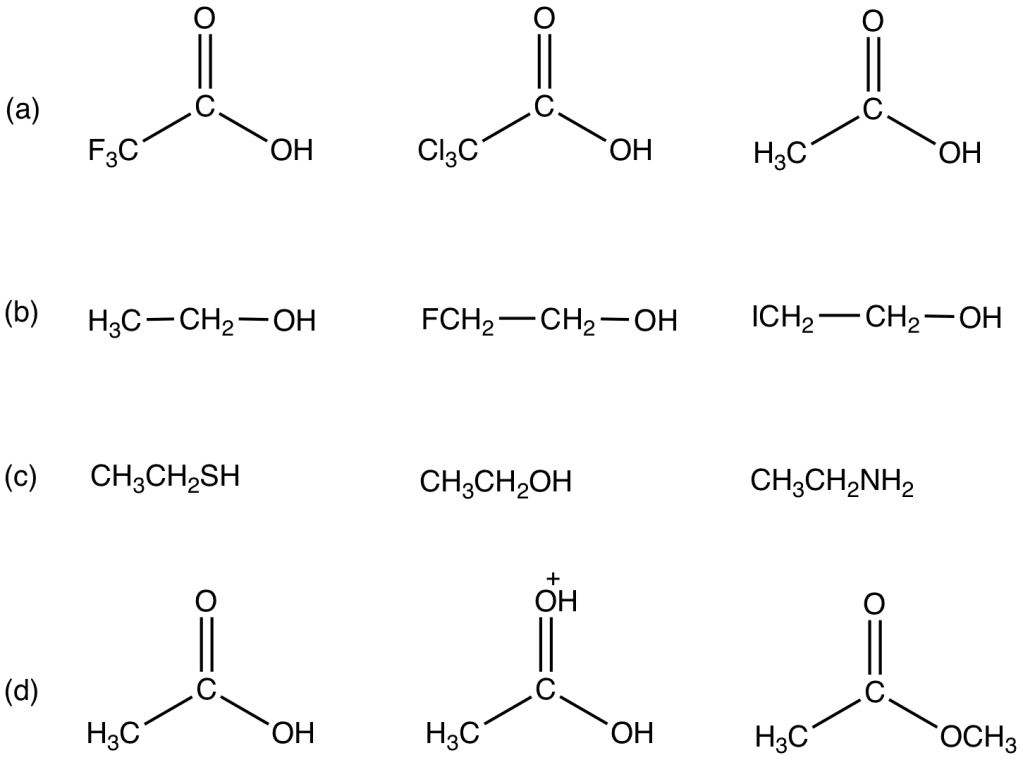
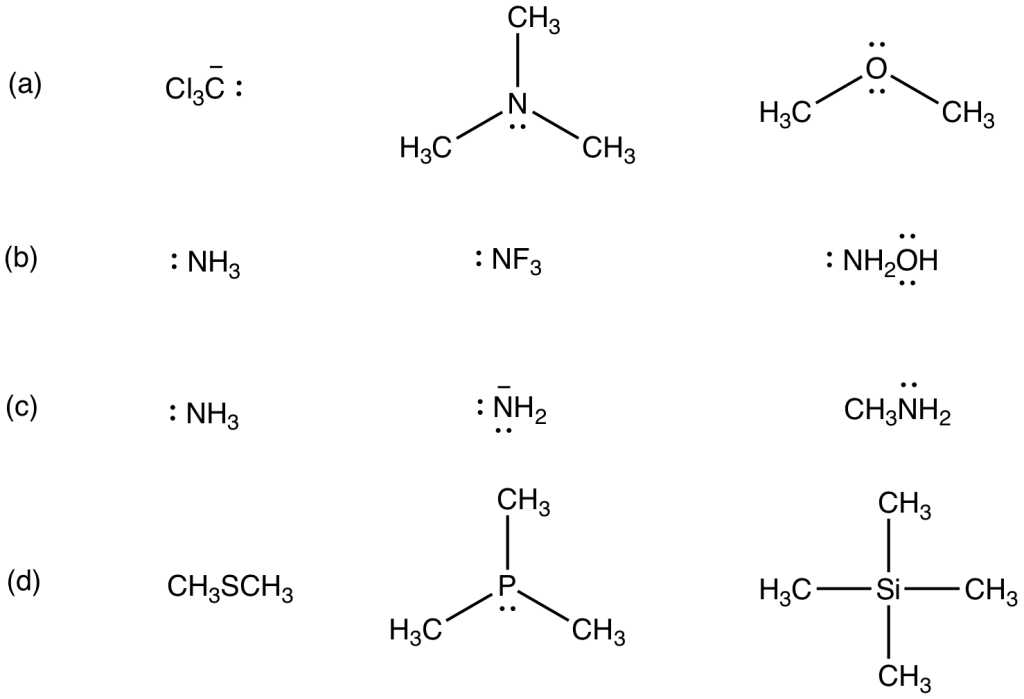
You must be logged in to post a comment.