Incontro per la discussione della prima prova intercorso

L’incontro con gli studenti per la discussione/correzione della prima prova intercorso si terrà LUNEDI’ 8 NOVEMBRE in aula A1 alle ore 14:50
Università degli Studi della Campania "Luigi Vanvitelli"

L’incontro con gli studenti per la discussione/correzione della prima prova intercorso si terrà LUNEDI’ 8 NOVEMBRE in aula A1 alle ore 14:50

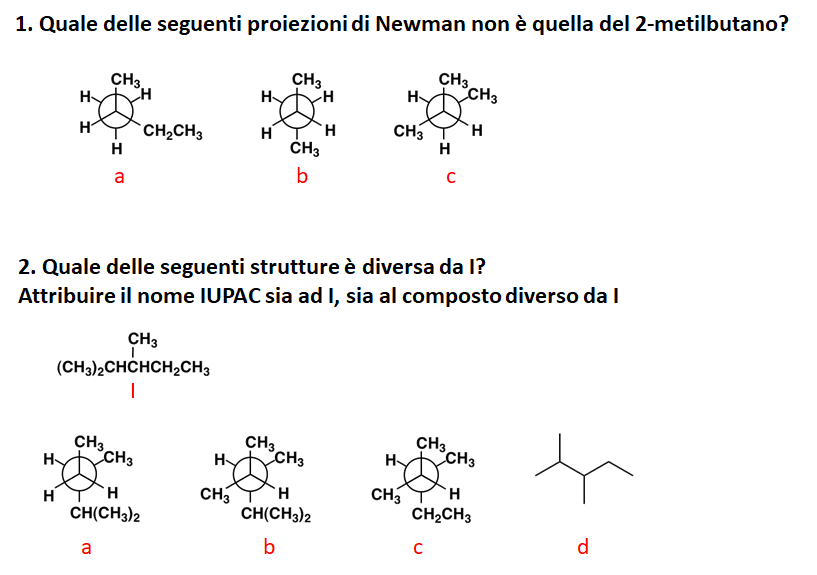
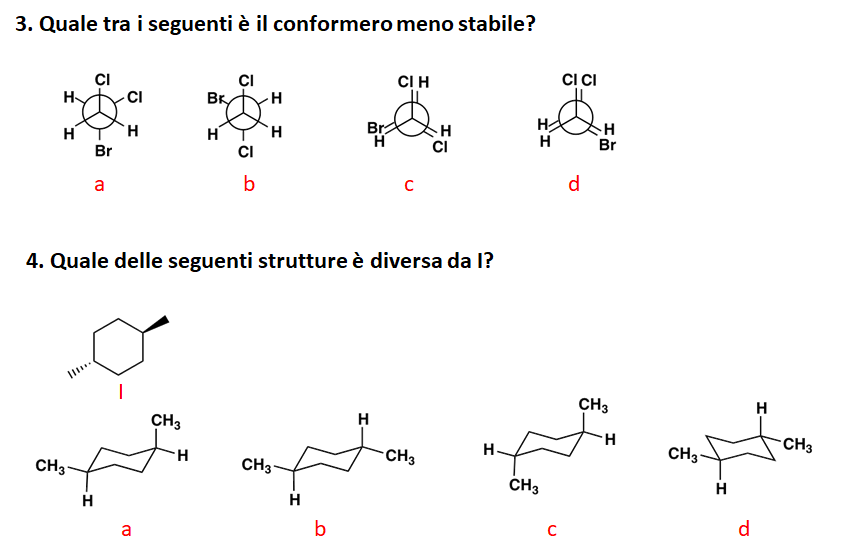
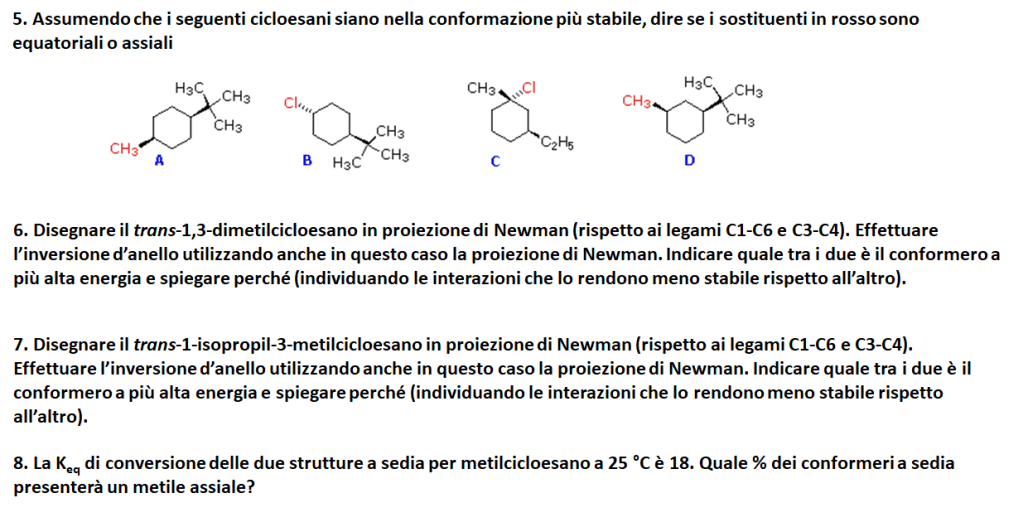


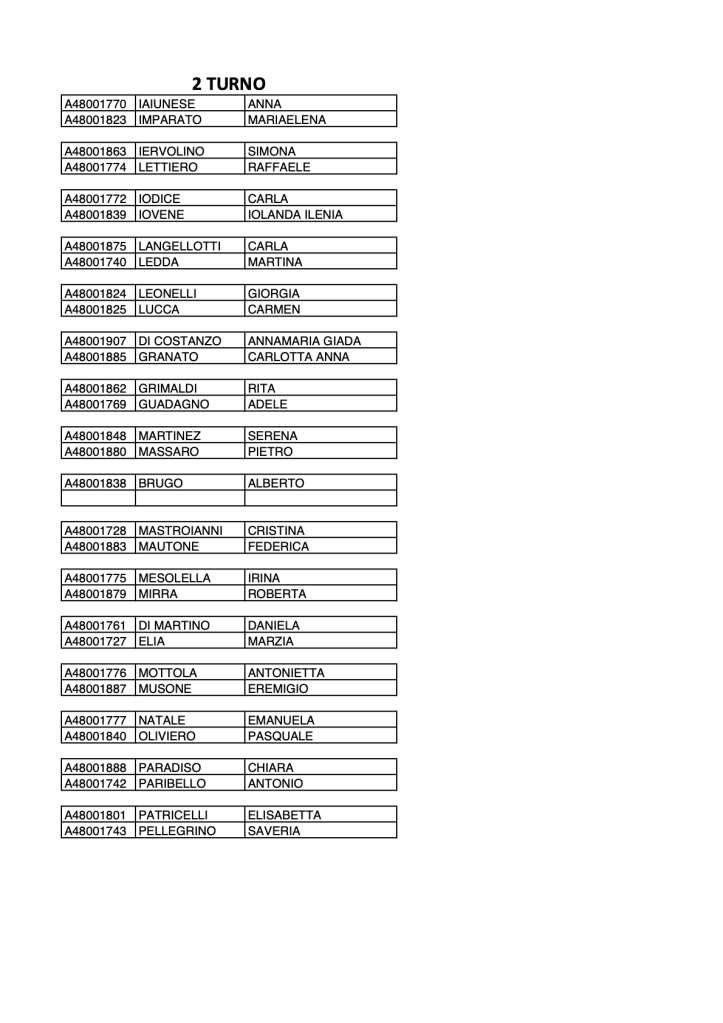
Di seguito sono riportati i risultati della prima prova intercorso.
Gli studenti identificati con il colore verde hanno superato la prova con sufficienza (verde scuro voti più alti).
Gli studenti identificati dal colore giallo hanno superato con riserva.
Per gli studenti indicati dai colori arancione e rosso, la prova si intende non superata.

NB: I BONUS ottenuti dalla vittoria della Weekend Organic Chemistry Challenge (e delle sfide a sorpresa) sono già stati aggiunti nel conteggio del punteggio finale.
Nella lezione di mercoledì 3 novembre saranno date indicazioni sul recupero della prova per coloro che non hanno potuto partecipare e per coloro che non hanno superato il compito del 28 ottobre.
Sarà possibile discutere gli argomenti del compito: seguiranno indicazioni del docente.

Di seguito sono riportati i risultati della prima prova intercorso. Gli studenti identificati con il colore verde hanno superato la prova con sufficienza (verde scuro, voti più alti).
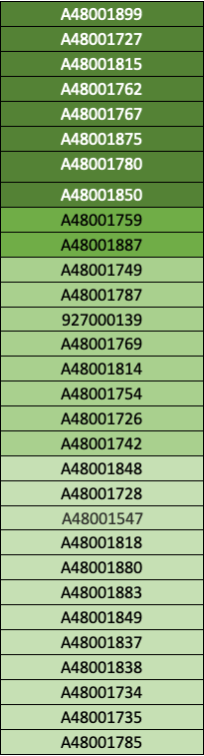
Gli studenti identificati dal colore giallo hanno superato con riserva.

Con il colore arancione/rosso s’intende prova non superata (rosso, grave insufficienza).

Nella lezione di mercoledì 3 novembre saranno date indicazioni sul recupero della prova per coloro che non hanno potuto partecipare e per coloro che non hanno superato il compito del 28 ottobre.
Sarà possibile discutere gli argomenti del compito: seguiranno indicazioni del docente

Regolamento:

…in preparazione della prossima (molto prossima!) prova intercorso
Esercizio n. 1
Disegnate un grafico che mostri in termini generali le variazioni di energia in funzione della rotazione intorno al legame C2-C3 del 2-metilbutano. disegnare i conformeri sfalsati ed eclissati utilizzando le proiezioni di Newman e le strutture a cavalletto.
Esercizio n. 2
a) Disegnate le proiezioni di Newman per tutte le possibili conformazioni sfalsate del 2-bromopentano.
b) Disegnate un grafico qualitativo dell’energia potenziale in funzione dell’angolo torsionale per la rotazione C2-C3 in questa molecola. ATTENZIONE: un atomo di bromo è. molto meno ingombrante, dal punto di vista sterico, di un gruppo metilico.
Esercizio n. 3
Scrivere le strutture degli isomeri cis e trans (se possono esistere) dei seguenti composti:
a) 1,,2-diclorociclopentano
b) 1,3-dibromociclobutano
c) 1,1-dibromociclobutano
Esercizio n. 4
a) Scrivere le formule di struttura per le due conformazioni a sedia del cis-1-isopropil-4-metilcicloesano
b) Le due conformazioni sono equivalenti?
c) In caso negativo, spiegate quale sia la più stabile
d) Qual è la conformazione preferita all’equilibrio?
Esercizio n. 5
a) Scrivere le due conformazioni dei seguenti composti e indicare se le due conformazioni hanno la stessa energia potenziale. IN caspo negativo indicare dov’è spostato l’equilibrio.
a) cis-1,2-dimetilcicloesamo.
b) trans-1,2-dimetilcicloesano
c) cis-1,3-dimetilcicloesamo.
d) trans-1,3-dimetilcicloesano
e) cis-1,4-dimetilcicloesamo.
f) trans-1,4-dimetilcicloesano
Esercizio n. 6
a) Scrivere tutti gli isomeri di formula C5H10. Trascurare tutti i composti con doppi legami.
b) assegnate il nome IUPAC a tutti i composti del punto a)
Esercizio n. 7
Disegnate una curva dell’energia potenziale simile a quella del problema n. 1 in funzione dell’angolo di rotazione intorno al legame C2-C3 per le seguenti molecole:
a) 2,3-dimetilbutano
b) 2,2,3,3,tetrametilbutano

1. Disegnare la proiezione di Newman del conformero più stabile del 2-metilpropano.
2. Disegnare il conformero a più bassa energia che deriva dalla rotazione intorno al legame C2-C3 del butano.
3. Disegnare il conformero gauche del butano.
4. Tra i conformeri del butano, quale si trova al minimo di energia su un diagramma di energia potenziale:
a) gauche
b) eclissato
c) gauche e anti
d)anti
5. Di seguito sono riportati dei composti in proiezione di Newman o rappresentati con le formule a cavalletto:
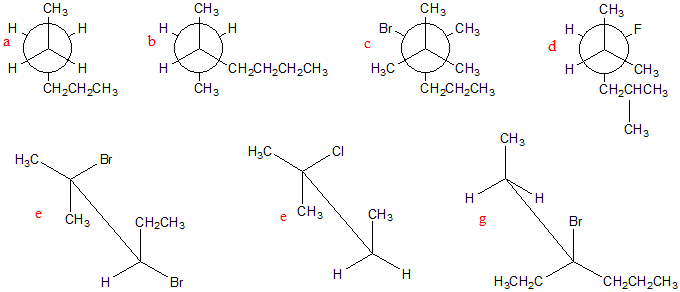
a) attribuire il nome IUPAC a ciascuno composto; b) per tutti i composti rappresentati in proiezione di Newman, scrivere le formule a cavalletto corrispondenti; c) per tutti i composti rappresentati con le formule a cavalletto, scrivere la proiezione di Newman corrispondete; d) dire, per ciascun composto, se quello rappresentato è il conformero più stabile.
6. Mediante le formule di Newman e quelle a cavalletto, rappresentare le conformazioni dell’1,2-dicloroetano corrispondenti ai minimi ed ai massimi di energia su un diagramma di energia potenziale.
7. Scrivere i conformeri sfalsati ed eclissati dei seguenti composti (formule proiettive di
Newman e formule a cavalletto):
a) metilbutano, rispetto al legame C2-C3;
b) tetrametilbutano, rispetto al legame C2-C3;
c) 1,2-dibromoetano;
d) 1,2-dicloro-1-fluoroetano;
e) esano, rispetto al legame C3-C4;
f) 2-cloro-3-metilpentano, rispetto al legame C2-C3;
g) 2-metilpentano, rispetto al legame C1-C2;
h) 2-metilpentano, rispetto al legame C2-C3; i) 2-metilpentano, rispetto al legame C3-C4.
8. Disegnare il diagramma di energia potenziale per le conformazioni di I) etano, II) neopentano e III) 2-cloro-3-metilpentano (prendere in considerazione il legame C2-C3). Indicare anche i conformeri che corrispondono ai massimi e ai minimi di energia.
9. Scrivere le proiezioni di Newman della conformazione anti e delle due conformazioni
eclissate dell’1,2-diiodoetano. Quale delle due conformazioni eclissate ha energia maggiore?
10. Disporre i seguenti cicloalcani in ordine di tensione d’anello crescente:
a) cicloesano
b) ciclopropano
d) ciclobutano
e) ciclopentano
11. Descrivere le fonti dell’energia torsionale e angolare presenti nel ciclopropano.
12. Quale delle seguenti affermazioni è una descrizione corretta del conformero più stabile del 1,1,3-trimetilcicloesano?
a) il metile al C-3 è equatoriale
b) C-1 è un carbonio terziario e C-3 è primario
c) C-1 è quaternario e C-3 è secondario
d) il metile al C-3 è assiale
13. Disegnare i due conformeri a sedia dei seguenti composti e dire qual è il più stabile dei due.
a) cis-2-bromo-1-metilcicloesano
b) cis-3-isopropil-1-metilcicloesano
c) trans-2-butil-1-isopropilcicloesano
d) trans-3-t-butil-1-metilcicloesano
e) trans-4-cloro-1-propilcicloesano.
Dire inoltre, se il nome è corretto. Nel caso in cui non lo fosse, attribuire il nome IUPAC corretto.
14. Per ciascuno dei seguenti composti I) disegnare il conformero a sedia più stabile dell’isomero geometrico più stabile II) dire se si tratta dell’isomero cis o trans:
a) 1-butil-2-metilcicloesano
b) 3-terz-butil-1-metilcicloesano
c) 1,4-dietilcicloesano
Dire inoltre, se il nome è corretto. Nel caso in cui non lo fosse, attribuire il nome IUPAC corretto.
15. Dire quali conformeri del cicloesano corrispondono ai minimi e ai massimi di energia (a-g) in questo grafico:
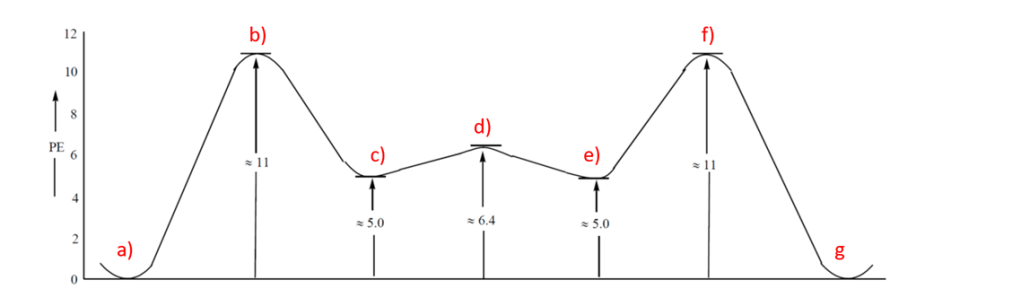
NB: per gli esercizi che richiedono il disegno di strutture o grafici, si potrà chiedere feedback a fine lezione per chi segue in presenza, oppure sarà possibile mostrarli a ricevimento o ancora inviando le immagini (chiare e ben leggibili) via chat di Teams.
ERRATA CORRIGE: per gli esercizi 13 e 14 manca un pezzo della traccia (che è stato aggiunto ora in rosso).



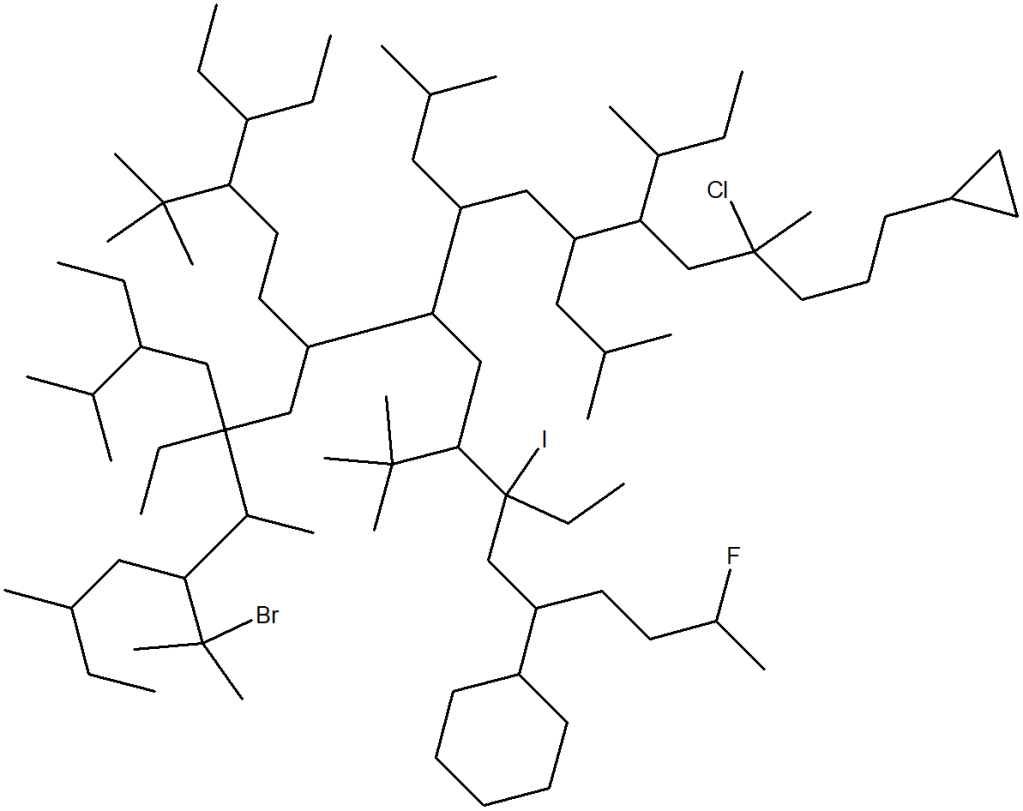
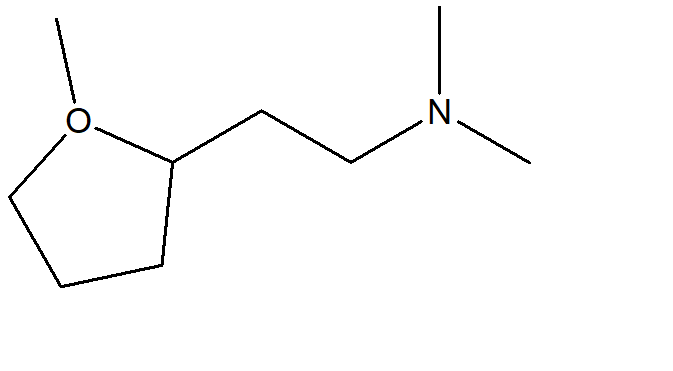
1. La struttura riportata di seguito è incompleta. Completare con le cariche e i doppietti elettronici non condivisi
2. Scrivere la formule molecolare del composto riportato in 1. Dire quanti C primari, secondari e quaternari ci sono.
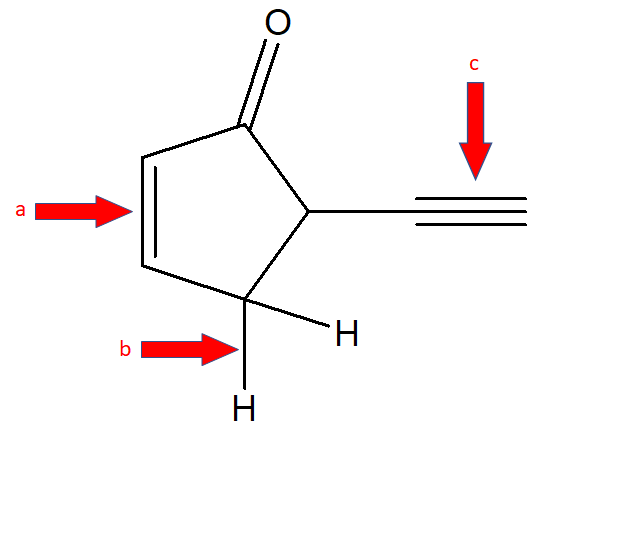
3. Etichettare i legami covalenti indicati da freccia nella seguente struttura come sigma o pi greco e dire quali orditali sono coinvolti nella formazione del legame.
4. Disporre i seguenti composti in ordine di acidità decrescente:
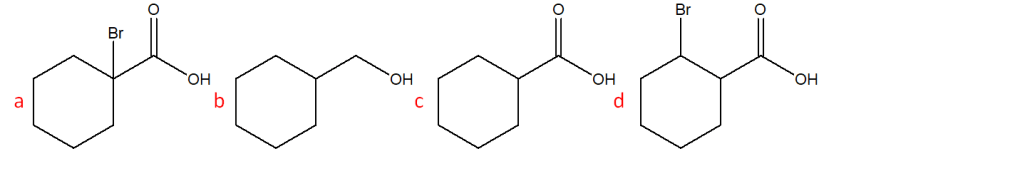
5. Disponi i seguenti composti in ordine di acidità crescente:

6. Dire quale tra i seguenti composti è la base più forte
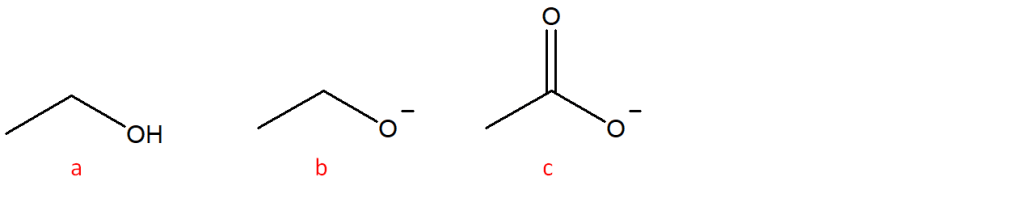
7. Assegnare il nome sistematico ai seguenti composti
Altri esercizi: Oltre agli esercizi presenti su questa pagina è possibile (per gli argomenti già studiati) svolgere anche gli esercizi pubblicati sulla pagina del corso di Chimica Organica per il CdS di Farmacia.

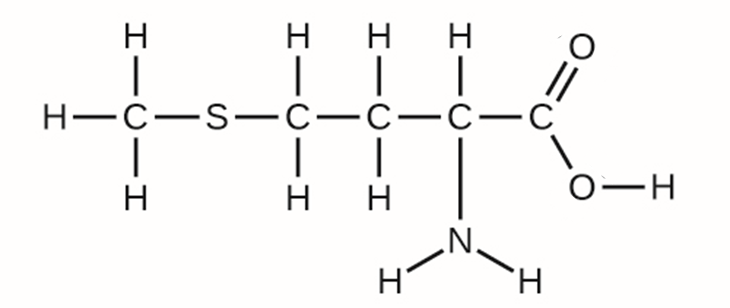
1. La struttura riportata di seguito è quella della metionina, uno degli amminoacidi che costituiscono le proteine.
a) Completare la struttura di Lewis con i doppietti elettronici non condivisi
b) Indicare l’ibridazione di ciascun atomo diverso dall’idrogeno
2. Completare la seguente struttura e determinare l’ibridazione di ciascun carbonio

3. Identificare la struttura di Lewis corretta per l’acido acetico (CH3COOH)
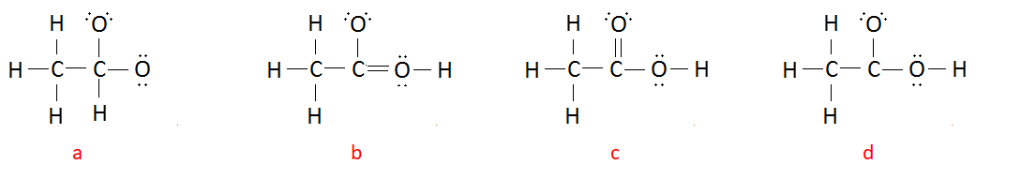
4. Calcolare le cariche formali per tutti gli atomi (esclusi gli atomi di idrogeno) dello ione acetato:
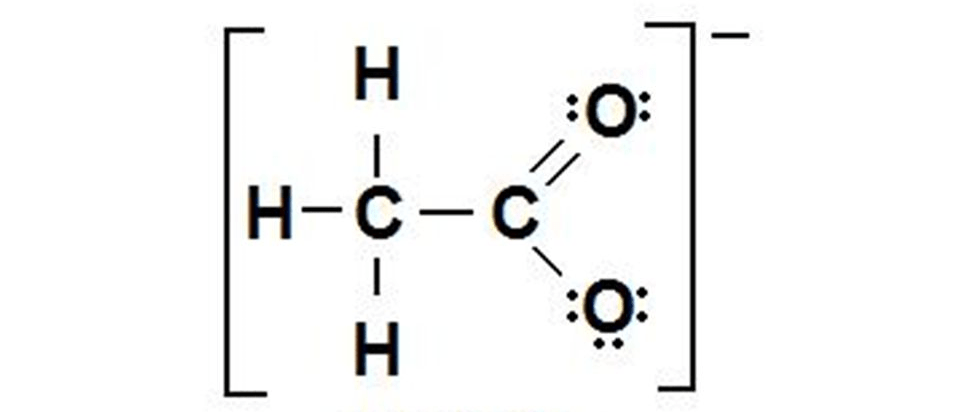
5. Completare le seguenti frasi:

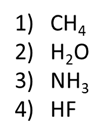
6. Associare i seguenti valori di pKa (approssimati) ai composti (1-4) sotto riportati:
pKa: a) 3 b)16 c) 38 d) 50
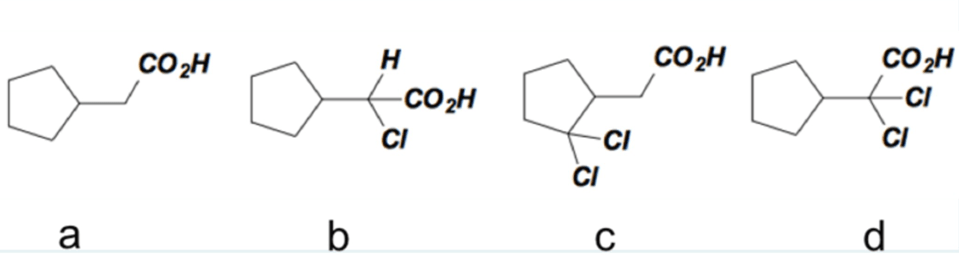
7. Disporre i seguenti composti in ordine di acidità decrescente:
8. Disponi i seguenti composti in ordine di acidità crescente:
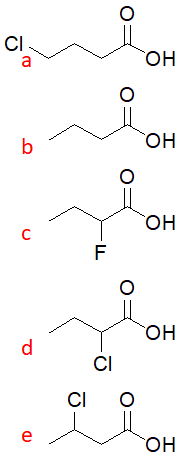
9. Dire quale tra i seguenti è l’acido più forte e spiegare perché:
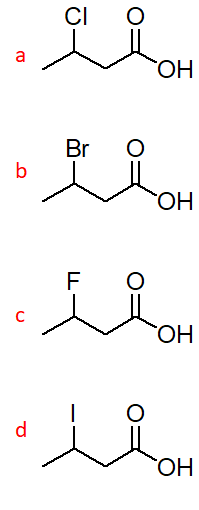
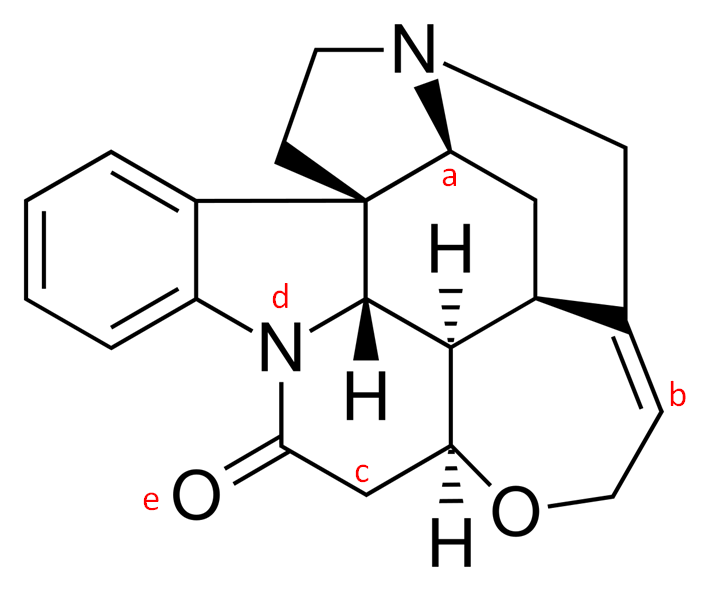
10. Quella riportata di seguito è la struttura della stricnina. Dire come sono ibridati gli atomi indicati dalle lettere a-e
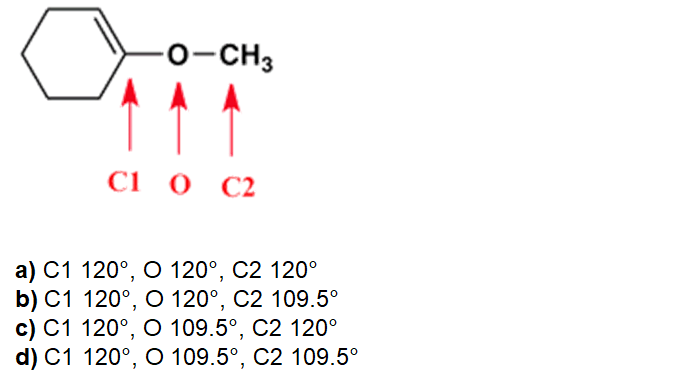
11. Qual è l’elenco corretto per gli angoli di legame per C1, O e C2 nella seguente molecola?
12 Dire per quale dei seguenti composti si prevede il punto di ebollizione più elevato e spiegare il perché:
a) 2-metilpentano
b) pentano
c) esano
d) butano
e) propano
13. Classificare i carboni indicati dalle lettere a-e come primari, secondari, terziari o quaternari:
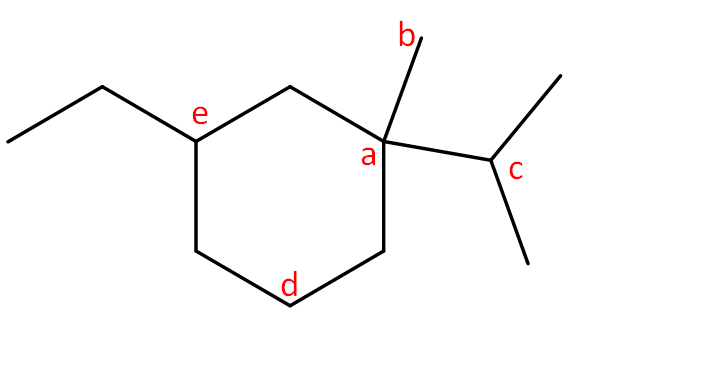
14. Scrivere un composto che corrisponda alla formula molecolare C9H18 che contenga solo idrogeni primari.
15. Dire se i seguenti nomi sistematici sono corretti. Se non lo sono, apportare le opportune correzioni:
a) 1-etil-3,4-dimetilcicloesano
b) 2-bromo-4-etil-6-metileptano
c) 3-isopropilesano
d) 3-metil-1-(3-metilesil)ciclopentano
e) 1-cloro-1,4-dimetilesano
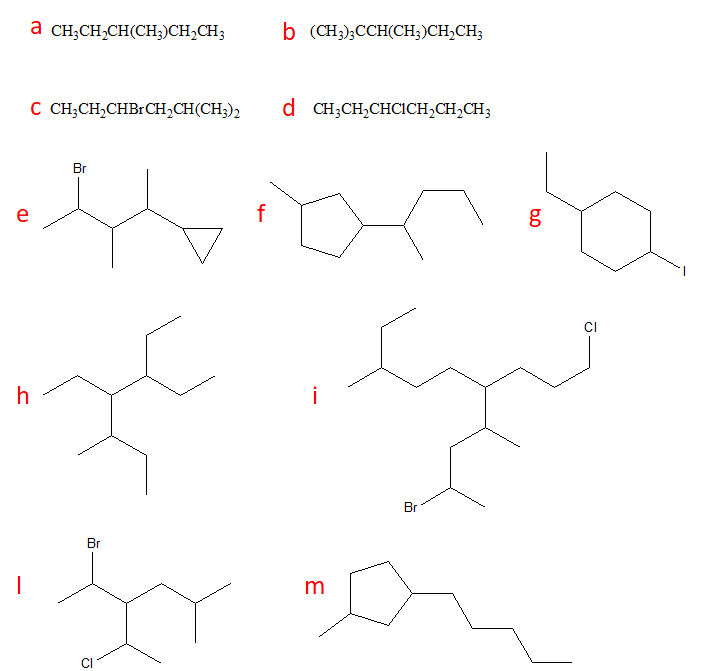
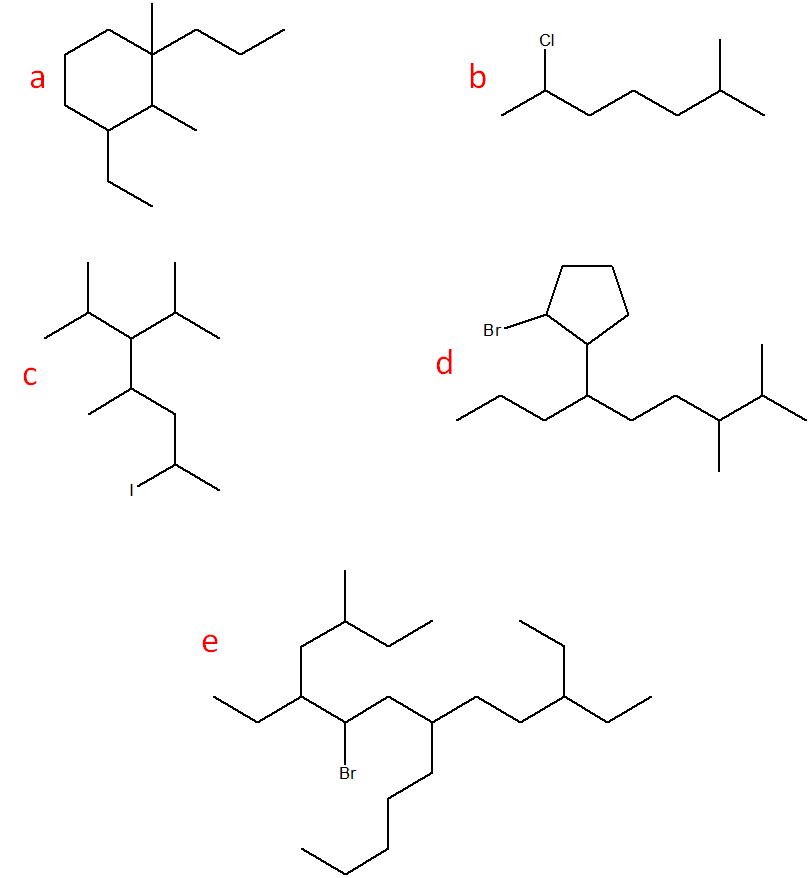
16. Assegnare il nome IUPAC ai seguenti composti
Altri esercizi: Oltre agli esercizi presenti su questa pagina è possibile (per gli argomenti già studiati) svolgere anche gli esercizi pubblicati sulla pagina del corso di Chimica Organica per il CdS di Farmacia.
You must be logged in to post a comment.