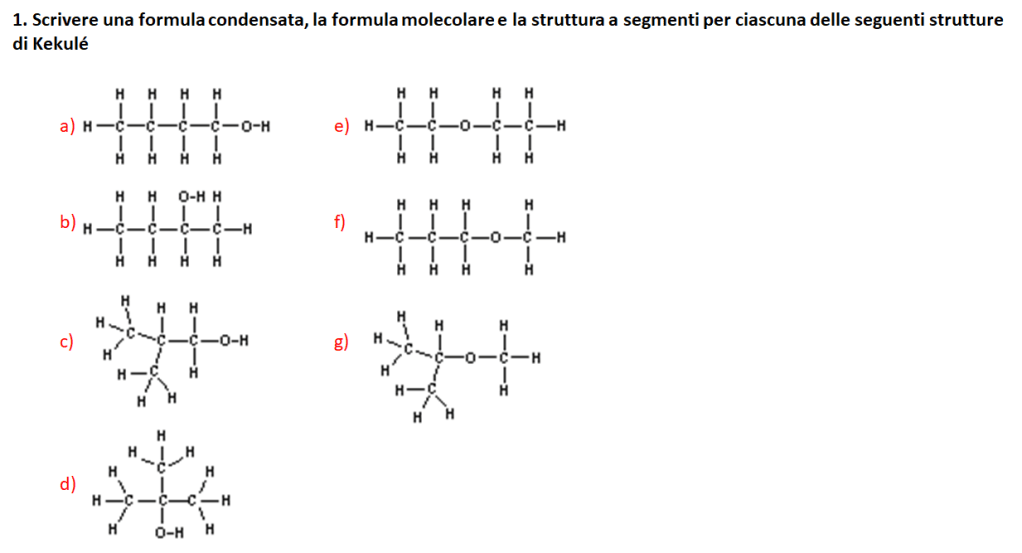
Legami nei composti organici: esercizi su orbitali atomici, orbitali ibridi e orbitali molecolari

1. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

2. Indicare il tipo di ibridazione per ognuno degli atomi (escluso l’H) dei seguenti composti

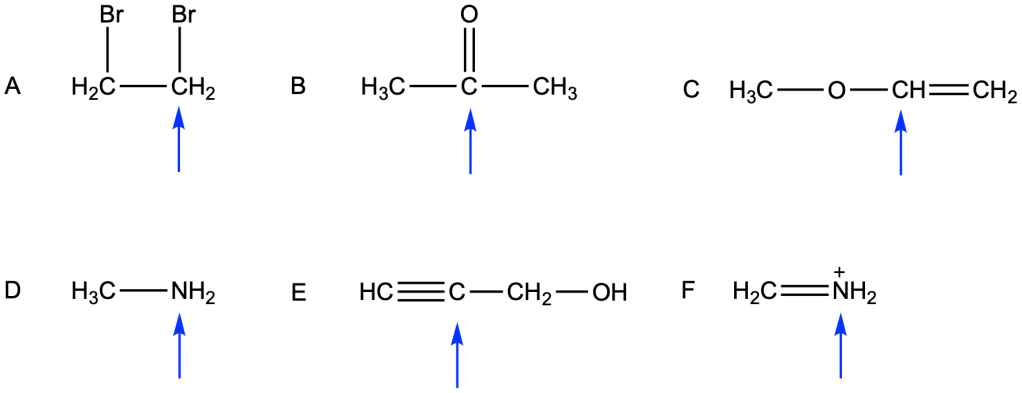
3. Per gli atomi indicati da una freccia nei seguenti composti, indicare:

4. Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

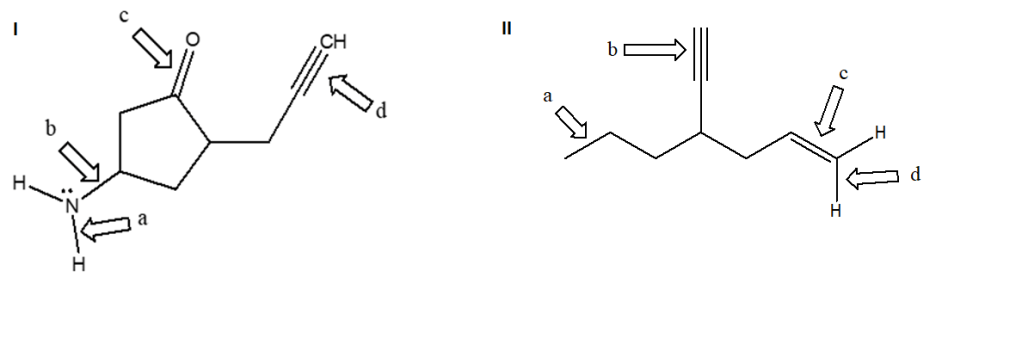
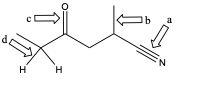
5. Nelle seguenti figure, alcuni dei legami sono indicati da freccia e da una lettera. a) Etichettare i legami a-d come singoli, doppi o tripli; b) Indicare (per qui legami) il tipo di orbitale/i molecolare/i; c) dire quali orbitali atomici sono coinvolti nella formazione del legame.
d) Considerando tutti i legami singoli della molecola (ed escludendo i legami C-H) qual è il legame più corto? (NB: in questo caso ci riferiamo a tutti i legami, non solo a quelli indicati da freccia e lettera)
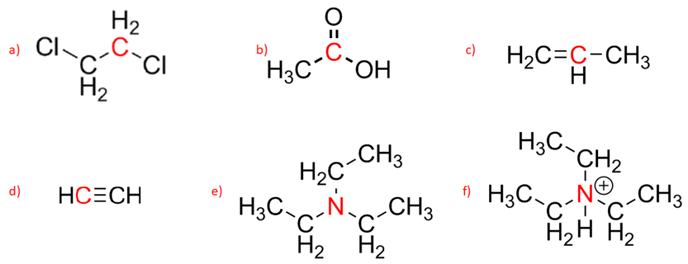
6. Per gli atomi mostrati in rosso nelle seguenti strutture, dire l’ibridazione, la geometria e l’angolo di legame. Dire, inoltre, quali orbitali molecolari formano (con ciascuno degli atomi con cui sono legati) e quali orbitali atomici e orbitali ibridi sono coinvolti nella formazione di ciascun orbitale molecolare.
7. Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
e) può essere sia di legame sia di antilegame
8. Gli orbitali molecolari di antilegame sono prodotti da:
a) interazione costruttiva (in fase) degli orbitali atomici
b) interazione distruttiva (fasi opposte) degli orbitali atomici
c) la sovrapposizione degli orbitali atomici di due ioni negativi
d) tutte le precedenti
e) nessuna delle precedenti
9. Quali orbitali ibridi si trovano nella molecola di acqua?
a) sp3
b) sp2
c) sp3d
d) sp
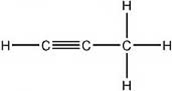
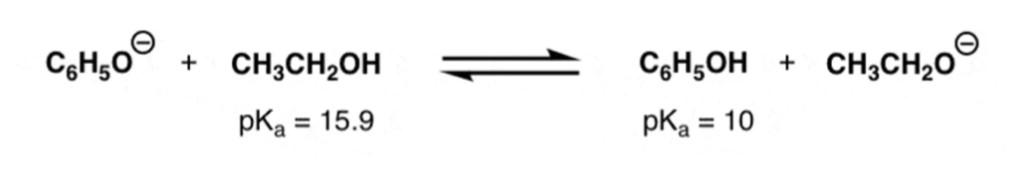
10. Quanti legami σ carbonio-carbonio ci sono nella seguente molecola?


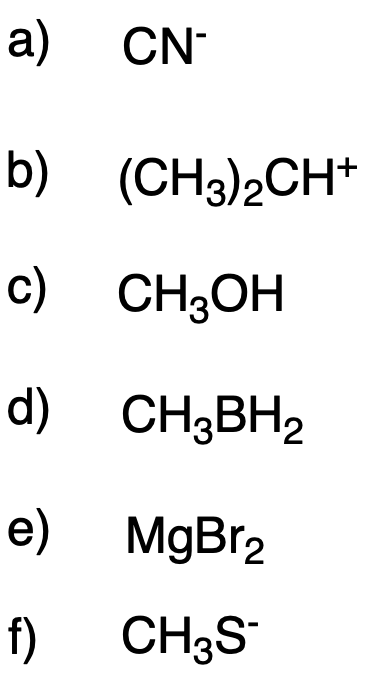














You must be logged in to post a comment.