CdL Scienze Biologiche: esercitazione su aromaticità, benzene e amminoacidi

In data 10/02 ore 10:00 si terrà un’esercitazione sugli argomenti in oggetto. L’esercitazione si terrà online sull’aula virtuale utilizzata per il corso
Università degli Studi della Campania "Luigi Vanvitelli"

In data 10/02 ore 10:00 si terrà un’esercitazione sugli argomenti in oggetto. L’esercitazione si terrà online sull’aula virtuale utilizzata per il corso

Abbiamo visto come il gruppo aldeidico degli aldosi possa essere ossidato a gruppo carbossilico in diversi modi. Uno di questi è mediante utilizzo del reattivo di Tollens. In virtù delle condizioni basiche utilizzate, anche i chetosi reagiranno col reattivo di Tollens. Infatti, essi andranno incontro a riarrangiamento enediolico.
Nel video seguente, è possibile vedere il saggio di Tollens effettuato su due monosaccaridi-glucosio (aldoso) e fruttosio (chetoso)- su due disaccaridi (maltosio e saccarosio) e su un polisaccaride (amido):
Di seguito è possibile guardare un video in cui si mostra invece l’utilizzo del saggio di Fehling per la determinazione degli zuccheri riducenti:
Attenzione: in condizione basica, il fruttosio non darà solo il glucosio come qui mostrato, ma anche il mannosio
Che succede se trattiamo il saccarosio con acido? Guardiamo il video seguente:

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
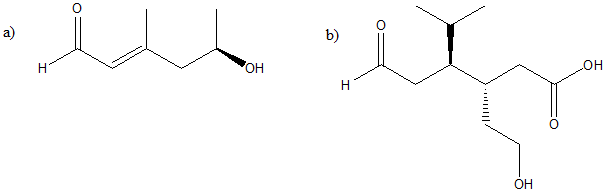
1. Attribuire il nome IUPAC, comprensivo di stereochimica, al seguente composto:
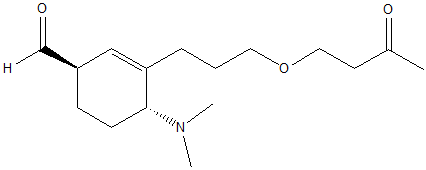
2) Scrivere l'(R)-3-bromo-5-ossoesanale
3) Il composto mostrato in figura è il paclitaxel. Indicare l’ibridazione dei carboni indicati dalle lettere A e B e dai numeri 1,2,3. Ai carboni indicati da numeri, attribuire anche la configurazione assoluta.

4) Disegnare la struttura di Lewis di ciascuna delle seguenti molecole: a) CH3CHO, b) CH3OCH3, c) CH3COO–, d) H2SO4. Scrivere anche enemtuali strutture di risonanza e indicare le cariche formali quando esse sono diverse da 0.
5) Quale tra il bromoetano e il bromoetene ha il legame C-Br più corto. Spiegare perchè.
6) Come sintetizzeresti il seguente composto mediante condensazione di Claisen?

7) Completare il seguente schema sintetico

8) L’arginina è un amminoacido con un gruppo ionizzabile in catena laterale. I valori di pKa per questo amminoacido sono i seguenti: pKa (COOH)=2,17; pKa (NH2) =9.04, pKa (gruppo in catena laterale)= 12,48. Quale sarà il pI per questo amminoacido?
SECONDO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
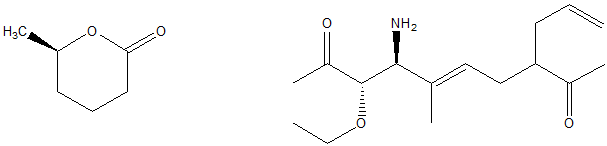
2. Dire quale/i tra i seguenti composti ha uno stereoisomero achirale: a) 1-etil-2-metilciclopentano, b)1,2-dimetilciclopentano, c) 2,3-diclorobutano, d) 2,3-dicloropentano. Disegnare le strutture degli stereoisomeri achirali.
3. Ordina i seguenti composti per acidità crescente e motivare la scelta

4. Quali sono l’ibridazione, la geometria e l’angolo di legame di un carbonio carbanionico? Quale sarà più stabile tra un carbanione primario e uno secondario? Perchè?
5) Quale dei due ioni mostrati di seguito è più stabile? Spiegare perchè

6) A partire dall’opportuno alchene, mostrare il meccanismo di sintesi del seguente composto. Indicare eventuali altri prodotti formati nel corso della reazione

7) Scrivere i prodotti delle seguenti reazioni. Indicare la stereochimica, quando opportuno

9) Scrivere la struttura di un generico L-amminoacido
TERZO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto:
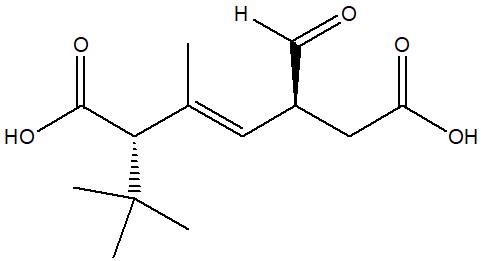
2. Scrivere 8 composti che abbiano formula molecolare C5H8O, almeno uno dei quali contenga un carbonio chirale.
3. Qual è il numero massimo di stereoisomeri per il seguente composto?
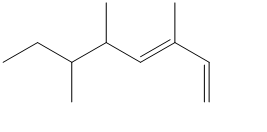
4. Quello riportato di seguito è il diagramma delle variazioni di energia potenziale rispetto all’angolo diedro per l’1,2-dicloroetano.

a) A cosa corrispondono A, C, E, G ? b) Disegnare le proiezioni di Newman di tutti i conformeri eclissati, indicandoli con la lettera corrispondente sul grafico. c) Discutere dei fattori che giustificano la minore energia potenziale dei conformeri più stabili.
5) Disporre i seguenti composti in ordine di acidità decrescente e spiegare sinteticamente il perché:
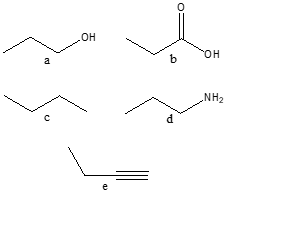
6) Disporre i seguenti composti in ordine di acidità crescente e giustificare la scelta

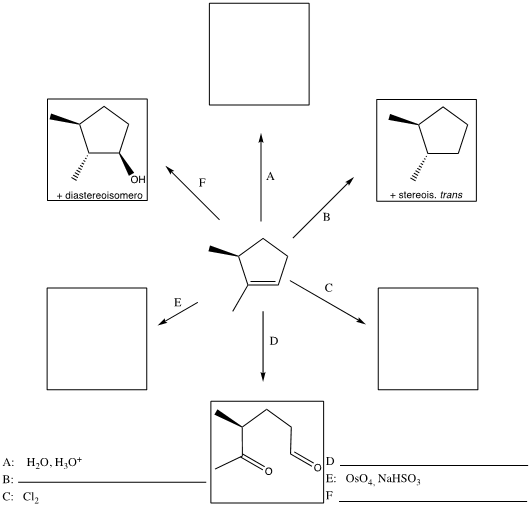
7) Completare il seguente schema inserendo le condizioni di reazioni o i prodotti mancanti. Evidenziare la stereochimica.
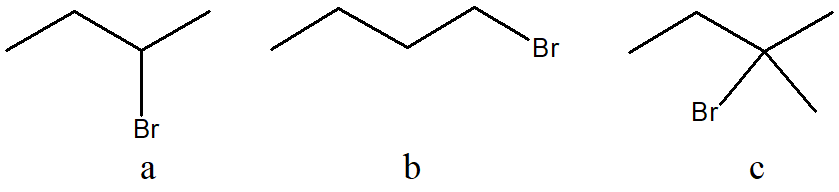
7) Ordina i seguenti composti per reattività crescente in una reazione a) E2 b) SN1
8) Mostrare il meccanismo di epimerizzazione e di arrangiamento enediolico catalizzato da base del D-glucosio
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomentii…e a breve altre saranno pubblicate. In ogni caso, potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti.
La molecola qui sotto riportata è il NAD+/NADP+, ossia il nicotinammide adenina dinucleotide/ nicotinammide adenina dinucleotide fosfato. Si tratta di due coenzimi comunemente usati dagli enzimi per catalizzare reazioni redox. Quella qui mostrata è la forma ossidata.


Di seguito sono riportati gli studenti che, sulla base della media dei punteggi delle quattro (I–II–III–IV) prove sostenute, sono ammessi a sostenere la prova orale in una delle date previste dal calendario. Si ricorda che è necessario prenotarsi (e che è assolutamente vietato prenotarsi per più di una data). La prenotazione sarà possibile a partire dalle 17 di oggi 4/02 e fino a due giorni prima della data prevista.
Gli studenti in giallo e arancione sono ammessi con riserva.

Si ricorda che le prove intercorso esonerano dallo scritto solo se si sostiene l’esame orale entro l’11 marzo (ultima data prevista).
Si ricorda, inoltre, che l’intero programma sarà oggetto di discussione alla prova orale.
Suggerimento: i risultati delle singole prove possono essere di supporto nel valutare quali argomenti è necessario approfondire ulteriormente prima di poter sostenere l’esame.
PROVA DI RECUPERO: coloro che non hanno potuto sostenere l’ultima prova per cause di forza maggiore potranno recuperarla il 16 febbraio. Sarà necessario contattare il docente per prenotarsi e produrre opportuna documentazione attestante i motivi che hanno reso impossibile la presenza in data 27/01.
Si ribadisce ancora una volta la disponibilità del docente a fornire ulteriori chiarimenti e si rende noto che è possibile, su richiesta, visionare le prove sostenute.

RISULTATI QUARTA PROVA INTERCORSO
Di seguito sono riportati i risultati della quarta prova intercorso.
Gli studenti identificati con il colore verde hanno superato la prova con sufficienza, quelli in giallo con riserva, quelli in rosso hanno ottenuto un punteggio che corrisponde ad un’insufficienza grave.

NB: I BONUS ottenuti dalla vittoria della Weekend Organic Chemistry Challenge (e delle sfide a sorpresa) sono già stati aggiunti nel conteggio del punteggio finale.
SI SOTTOLINEA LA DISPONIBILITA’ DEL DOCENTE A DARE CHIARIMENTI SUI VARI ARGOMENTI durante il ricevimento, prenotabile seguendo il solito link o inviando un messaggio via chat di Teams. Nel corso del ricevimento è anche possibile prendere visione della prova.
RISULTATI INTEGRAZIONE III PROVA INTERCORSO
Di seguito sono riportati i risultati relativi alla prova integrativa sulle reazioni degli alcheni. Coloro che sono riportati in verde, hanno risolto in maniera corretta almeno il 75% della prova; gli studenti in giallo in giallo tra il 50 e il 75%, quelli in rosso non hanno raggiunto il 50%

Seguirà la pubblicazione dell’elenco di coloro che sono ammessi alla prova orale

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
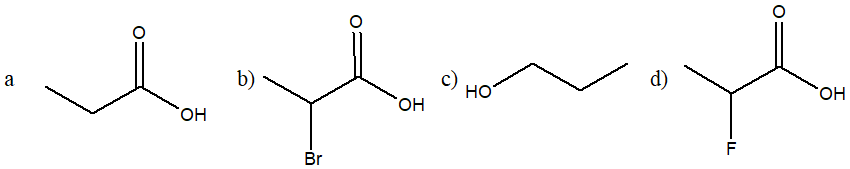
2) Indicare qual è la relazione (isomero strutturale, conformero, enantiomero, diastereoisomero, stesso composto, etc.) delle strutture a, b, c, d con il composto qui mostrato:

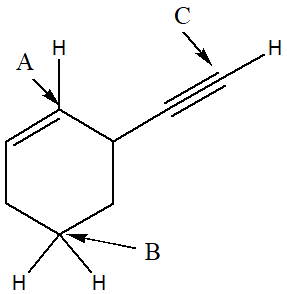
3) Per i carboni indicati da freccia (A, B, C) nella figura seguente, indicare: a) ibridazione, b) angolo di legame, c) geometria. Dire inoltre quale dei legami C-H degli idrogeni evidenziati è il più lungo spiegando sinteticamente perchè.
4) Scrivere il conformero più stabile del trans-1-bromo-4-isopropilcicloesano. Spiegare i fattori che lo rendono più stabile rispetto all’altro conformero. Dire, inoltre, quale tra l’isomero cis e l’isomero trans reagisce più velocemente in una reazione E2.
5) Disegnare il diagramma energetico per la reazione di addizione di acido bromidrico al propene.
6) Mostrare le condizioni e il meccanismo per la seguente trasformazione:

7) Completare le seguenti equazioni indicando le condizioni di reazione o i prodotti

8) Scrivere l’L-galattosio (il galattosio è l’epimero in 4 del glucosio)
SECONDO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2. Quale delle seguenti strutture è la (2S,3R)-3-bromo-2-butanammina? (NB: è possibile scegliere più di una opzione):

3. Ordina i seguenti composti per acidità crescente e motivare la scelta
4. Quali sono l’ibridazione, la geometria e l’angolo di legame di un carbonio carbocationico?
5) Scrivere tutte le strutture di risonanza dello ione carbossilato che si ottiene quando l’acido propanoico reagisce con una base. Confrontando il doppio legame C=O dell’acido propanoico con quello presente nel propanone, che considerazioni è possibile fare circa la lunghezza e forza dei legami in questione?
6) A partire dall’opportuno alchene, mostrare il meccanismo che porta alla formazione del seguente prodotto mediante una reazione di idroborazione-ossidazione. Indicare altri prodotti che si formano nel corso della reazione.

7) Le seguenti reazioni daranno, come prodotto principale, degli alcheni che non rispondono alla regola di Zeitzev. Disegnare i prodotti principali e argomentare.

8) Completare il seguente schema sintetico. Indicare la stereochimica quando opportuno

9) Quello mostrato di seguito è un disaccaride, il saccarosio. Dire se è o meno uno zucchero riducente spiegando brevemente perchè

TERZO SET
1. Scrivere il seguente composto e dire se il nome è corretto. Se non lo è, attribuire il nome IUPAC corretto.
4-(3-idrossipropil)-cicloesene
2. Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto:
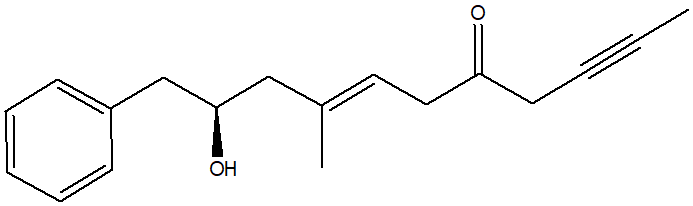
3. Dire se le seguenti molecole sono chirali

4. Qual è la relazione stereochimica che intercorre tra le seguenti strutture?
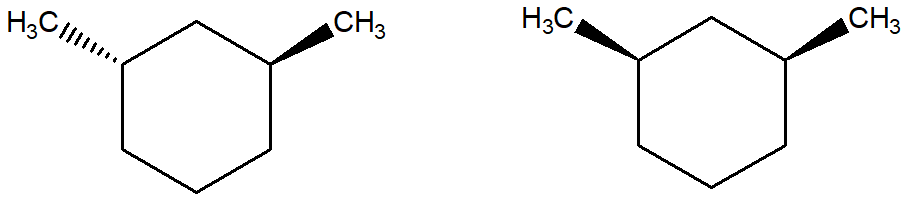
5) Giustificare il carattere aromatico, antiaromatico o non aromatico dei seguenti composti e ioni

6) Quale tra i seguenti è il conformero più stabile del 3-metil-1-butanolo?
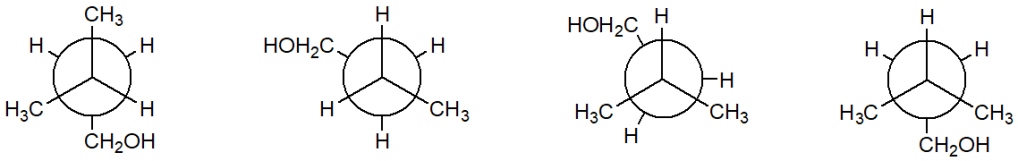
7) Individuare gli idrogeni più acidi per ognuno dei seguenti composti:
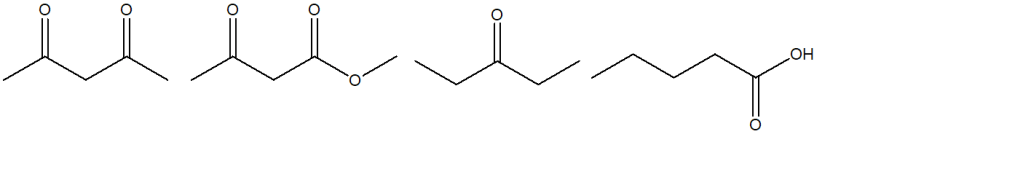
8) A partire da uno dei composti riportati nel riquadro e utilizzando qualsiasi altro reagente necessario, suggerire la sintesi del seguente prodotto, indicando sulle frecce le condizioni di reazione.


9) Mostrare la sintesi del 4-metil-3-penten-2-one a partire dal propanone.
10) Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica dei prodotti quando opportuno

12) Scrivere l’α-D-glucopiranosio in proiezione di Haworth
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate

Nessuno degli studenti che hanno sostenuto la prova scritta in oggetto è ammesso alla prova orale.
Di seguito sono riportati i risultati: in arancione è indicata un’insufficienza grave (voto<15), in rosso è indicata una insufficienza gravissima (voto<12). In rosso sono indicati anche coloro che si sono ritirati.

DISCUSSIONE PROVA SCRITTA
Tutti coloro che hanno sostenuto la prova sono invitati alla discussione della stessa, che si terrà online lunedì 7/02 alle 16:00.
Sarà cura del docente creare un’aula virtuale dedicata.
Alla fine dell’incontro dedicato alla discussione degli esercizi, sarà anche possibile, su richiesta, visionare la propria prova.

1) Un composto è aromatico se:
1) ha una nuvola ininterrotta di elettroni π (per cui il composto deve essere ciclico, planare e ogni atomo dell’anello deve possedere un orbitale p);
2) contiene 4n+2 elettroni π (ovvero un numero dispari di coppie di elettroni π).
Un composto è antiaromatico se soddisfa il primo ma non il secondo criterio per l’aromaticità. I composti antiaromatici sono quindi ciclici, planari, costituiti da una nube ininterrotta di elettroni π, ma hanno numero pari di coppie di elettroni π. I composti antiaromatici non possono riempire i loro orbitali molecolari di legame, per cui risultano molto instabili e altamente reattiviti:

Classifica i seguenti composti o ioni come aromatici, antiaromatici o non aromatici, giustificando la scelta:

2) Assegnare il nome IUPAC ai seguenti composti

3) Mostrare la sintesi delle molecole a-e dell’esercizio 2 a partire dal benzene.
4) In relazione ai composti sintetizzati nell’esercizio 3, che effetto hanno i sostituenti introdotti sulla reattività del benzene? Come orientano eventuali ulteriori sostituenti? Motivare la risposta.
5) Come sintetizzeresti il composto h dell’esercizio 3 a partire dal benzene?

Una delle tecniche utilizzate in metabolomica è la Spettroscopia di Risonanza Magnetica Nucleare (NMR).
Questa tecnica, che si basa sulle proprietà magnetiche dei nuclei di alcuni isotopi, ha tantissime applicazioni ed è certamente insostituibile quando si parla di caratterizzazione di composti organici. In questo contesto, ricordiamo che tra i nuclei attivi all’NMR ci sono l’idrogeno (1H) e il carbonio 13 (13C). La scarsa abbondanza naturale del 13C, insieme ad altre caratteristiche di questo nucleo, fanno sì che nel caso della metabolomica sia molto più pratico lavorare con 1H-NMR.
Dall’analisi NMR di un campione si possono dedurre tante informazioni diverse. Ma come si effettua un’analisi metabolomica mediante NMR?
A partire dal materiale liofilizzato, si ottengono gli estratti con una procedura molto semplice che prevede l’estrazione diretta in solventi deuterati (necessari per l’analisi NMR). Questi estratti vengono analizzati, ottenendo gli spettri, che saranno poi processati: questo processing prevede l’apodizzazione, la fasatura, la calibrazione rispetto allo standard intetno e la correzione della linea di base

A questo punto si procede con l’integrazione. Questa è effettuata attraverso il processo di bucketing o binnig: lo spettro si divide in tanti segmenti di lunghezza definita (in genere 0.02 o 0.04 ppm) e si procede ad integrare l’area sotto la curva di ogni bucket. Si ottiene in questo modo una matrice di dati in cui le osservazioni sono i singoli campioni analizzati e le variabili sono i vari bucket, che assumeranno quindi il valore dell’area per quella parte dello spettro in ciascun campione (NB: le aree sono in genere normalizzate rispetto allo standard interno a alla total intensity).

La matrice di dati così ottenuta è sottoposta ad analisi statistica multivariata. Questa sarà utile ad estrarre le informazioni significative dal nostro set di dati.
Una volta identificati i seganli NMR significativi per la nostra analisi, è necessario “tradurre” questi segnali in metaboliti. Si opera a questo punto per step successivi.
Il primo passaggio è quello del confronto con la letteratura e con i database. A questo proposito, è necessario sottolineare come l’NMR sia una metodica altamente riproducibile. In ogni caso, se questa ricerca non ci dà la risposta sperata, si può optare per l’analisi NMR bidimensionale (2D NMR).I metodi 2D NMR più utilizzati in metabolomica sono brevemente descritti di seguito.
COSY (COrrelation SpecroscopY)
Esperimento 2D omocorrelato. Permette di rilevare correlazioni omonucleari 1H-1H tra protoni vicinali e geminali

TOCSY (TOtal Correlation SpecroscopY)
Esperimento 2D omocorrelato. Permette di rilevare sistemi di spin (il trasferimento di magnetizzazione è interrotto da carboni quaternari).

HSQC (Heteronuclear Single Quantum Coherence)
Esperimento 2D eterocorrelato. Permette di rilevare le correlazioni dirette protone-carbonio. Permette quindi di attribuire il valore di chemical shift del carbonio per ciascun carbonio protonato presente nell’estratto (o nella molecola, quando lo spettro si riferisce ad un composto puro)
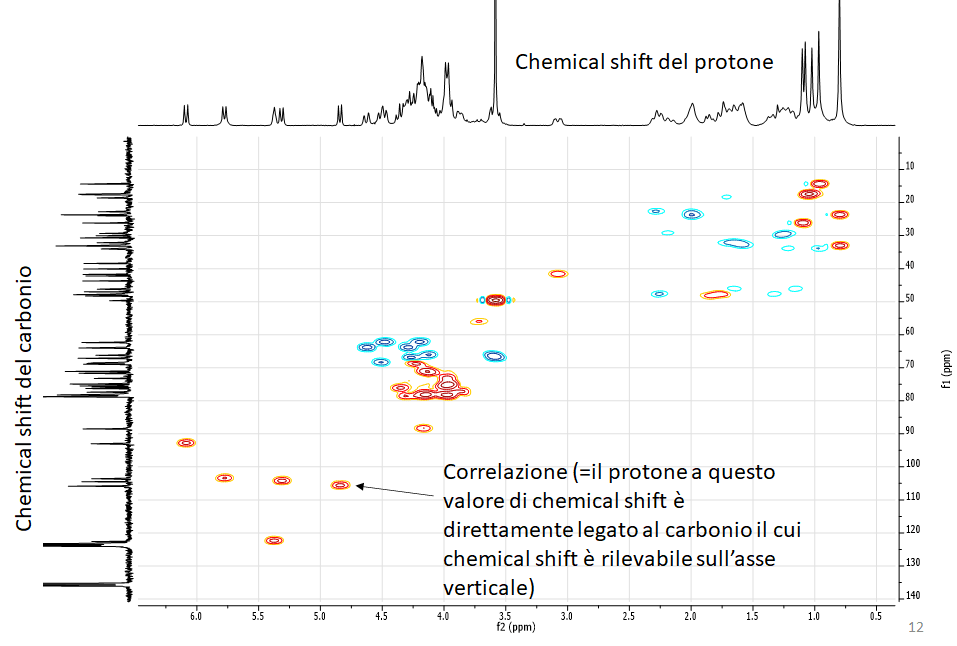
H2BC (Heteronuclear 2 bond correlation)
Esperimento 2D eterocorrelato. Permette di rilevare le correlazioni tra un protone e il carboni vicinale, a patto che quest’ultimo sia protonato.
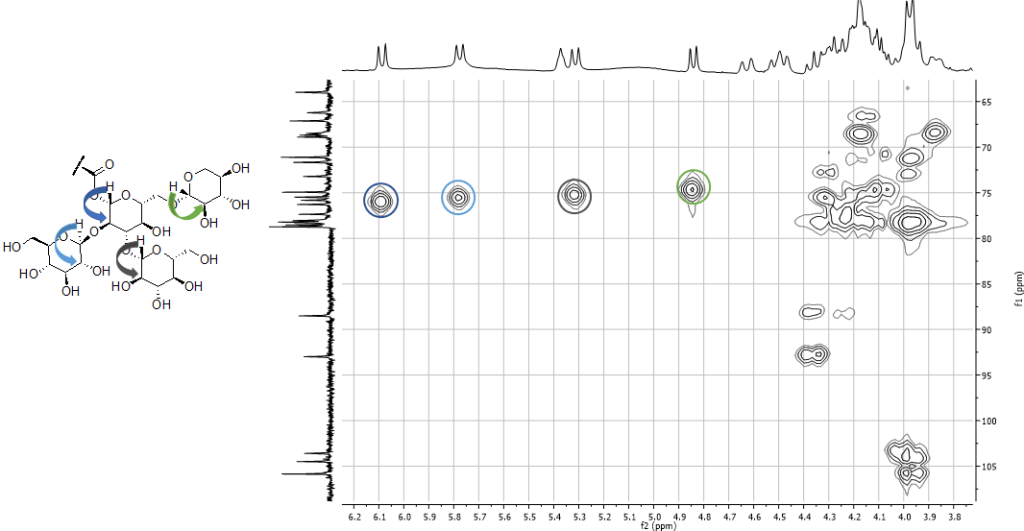
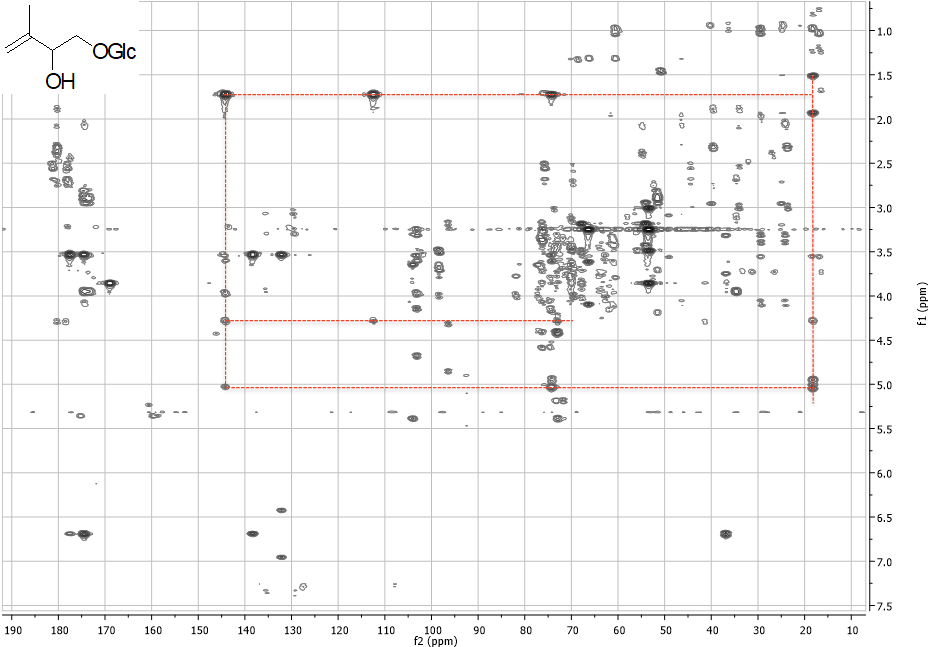
HMBC (Heteronuclear Multiple Bond Coherence)
Esperimento 2D eterocorrelato. Permette di rilevare le correlazioni tra un protone e carboni distanti due, tre o quattro legami. Un esperimento alternativo è noto come CIGAR-HMBC.
HSQC-TOCSY
Esperimento 2D eterocorrelato. Permette di rilevare sistemi di spin, che in questo caso includono sia i protoni sia i carboni.
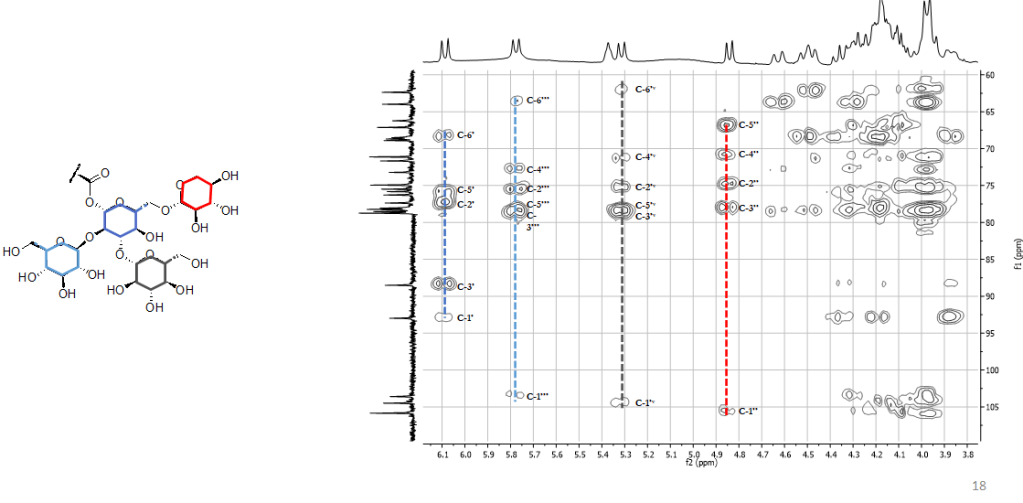
Grazie alla combinazione delle informazioni che si ottengono dai diversi spettri 2D NMR, è possibile identificare i costituenti dell’estratto anche in miscela. Per metaboliti già noti, a questo punto sarà possibile confrontare i dati NMR con quelli riportati in letteratura o con quelli degli standard (a patto che siano acquisiti nello stesso solvente). Per i composti identificati per la prima volta, al fine di confermare la struttura, saranno necessari l’isolamento (che a questo punto sarà facilitato dalle informazioni preliminari in nostro possesso circa la struttura del composto) e la completa caratterizzazione strutturale mediante tecniche spettroscopiche.
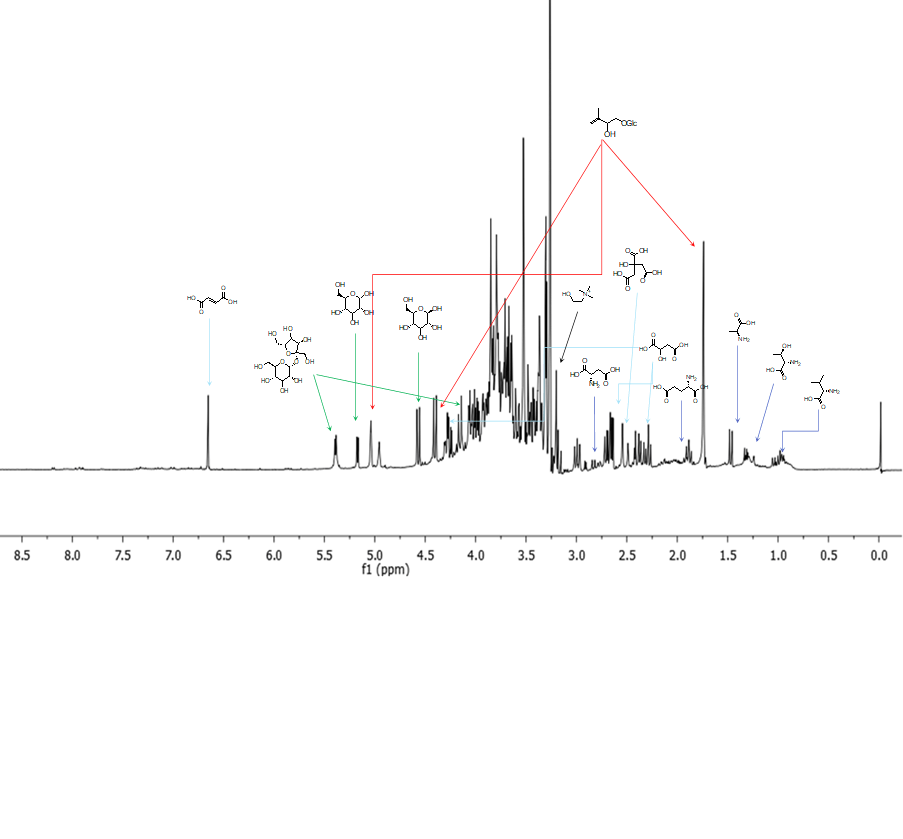
Va infine ricordato che oltre ad identificare i componenti dell’estratto, è anche possibile quantificarli dato che l’ 1H NMR è una tecnica quantitativa (se gli spettri sono acquisiti con determinati parametri) e che è sufficiente in questo caso utilizzare uno standard interno a concentrazione nota.
You must be logged in to post a comment.