Metabolomica: un approccio all’interfaccia tra la chimica e la biologia

A conclusione del corso di metabolomica, è qui presentata una panoramica di questo approccio analitico, che prevede l’analisi qualitativa e quantitativa di tutti i metaboliti presenti in un sistema biologico in determinate condizioni.
Innanzitutto, dobbiamo considerare l’ampio range di applicazioni di questo approccio allo studio dei sistemi biologici. Applicazioni che riguardano la chimica delle sostanze naturali, la chimica degli alimenti, la chimica farmaceutica, il metabolismo, la fisiologia e lo studio della risposta a stress da parte degli organismi e delle interazioni che tra essi intercorrono, la chimica ambientale, la ricerca biomedica e tantissimi altri campi.

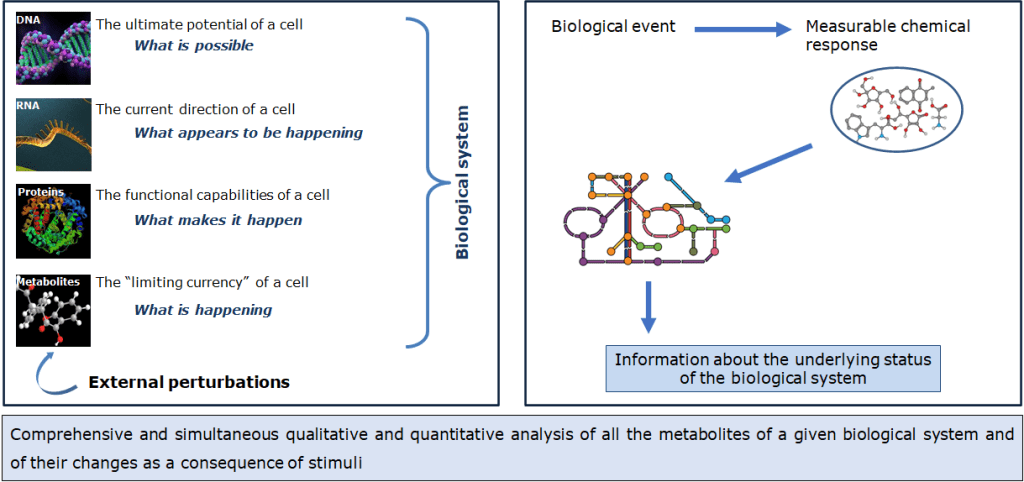
Del resto, la metabolomica si colloca all’interfaccia tra la chimica e la biologia, in quanto ciascun fenomeno biologico produrrà una risposta chimica misurabile e la determinazione delle variazioni osservate fornirà informazioni sullo stato del sistema biologico in analisi. Inoltre, andando a misurare quelli che sono i prodotti finali dell’espressione genica, ossia i metaboliti, fornisce informazioni essenziali su quello che è il fenotipo e la relazione di quest’ultimo col genotipo.
Uno step fondamentale nell’approccio metabolomico è la fase di disegno sperimentale. Al fine di ottenere dati che siano statisticamente e biologicamente significativi e che diano risposta alla nostra research question, è necessario definire a priori tutti i parametri sperimentali da considerare, le variabili da valutare e quelle da controllare. Sarà necessario inoltre prendere in considerazione l’utilizzo di un numero opportuno di replicati tecnici e biologici (tale numero varia sia in base al sistema biologico in analisi, sia in base alle tecniche analitiche utilizzate).
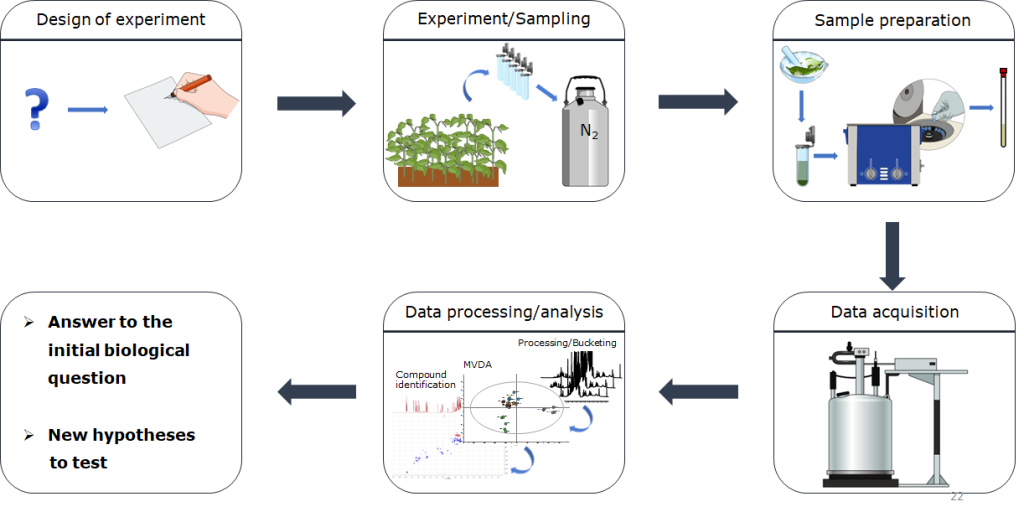
A questo punto, sarà necessario procedere all’esecuzione dell’esperimento e/o al campionamento. Le metodiche utilizzate variano a seconda del tipo di campione, ma un punto fondamentale e ineludibile, al fine di ottenere risultati che rispecchino il reale stato del sistema, è il quenching del metabolismo: sarà necessario bloccare tutte le reazioni, siano esse catalizzate da enzimi o meno. In genere, questo si ottiene con il metodo del deep freezing, congelando il campione immediatamente in azoto liquido (-196°C). I campioni sono poi conservati a -80°C fino al momento della liofilizzazione. Quest’ultimo processo, che allontana l’acqua dal campione, è necessario sia per una migliore conservazione (l’acqua è il mezzo per la maggior parte delle reazioni che avvengono nei campioni biologici) sia (in alcuni casi) per rendere compatibile il campione con le successive analisi.
La maggior parte delle tecniche analitiche usate in metabolomica richiede che il campione sia in soluzione, di conseguenza il passaggio successivo consisterà in una procedura di estrazione dei metaboliti. In questo caso le metodiche variano sia in base alla natura del campione, sia in base alla piattaforma analitica che si utilizzerà nella fase successiva. Fase successiva che consiste nell’analisi della composizione chimica degli estratti. Diverse tecniche sono disponibili, ma quelle più comunemente utilizzate in metabolomica sono la Spettroscopia di Risonanza Magnetica Nucleare (NMR) e la Spettrometria di Massa (MS). Quest’ultima richiede solitamente una separazione a monte dei metaboliti che compongono l’estratto ed è quindi in genere interfacciata con un sistema cromatografico (GC o HPLC/UPLC).
Una volta acquisiti i dati, il complesso dataset ottenuto è analizzato attraverso metodiche di analisi statistica multivariata (MVDA) al fine di estrarre le informazioni circa la classificazione dei campioni e circa i segnali e, in ultima analisi, i composti responsabili della classificazione osservata. A questo punto, si procede con la caratterizzazione strutturale dei composti che risultano essere significativi nell’analisi. Questa caratterizzazione si avvale, tra l’altro, di tecniche ad alta risoluzione e di spettrometria tandem, nel caso della MS. Nel caso dell’NMR una caratterizzazione dei metaboliti nell’estratto è possibile mediante l’utilizzo di tecniche NMR bidimensionali. Per entrambe le tecniche, un supporto notevole è fornito dai database.
Le informazioni estrapolate mediante MVDA vanno poi integrate con le conoscenze sul sistema biologico in analisi e forniranno la risposta alla domanda che sottende lo studio o forniranno nuove ipotesi da testare.




















You must be logged in to post a comment.