Acidi carbossilici e derivati

Esercizio n. 1
Assegna il nome IUPAC ai seguenti composti

Università degli Studi della Campania "Luigi Vanvitelli"

Esercizio n. 1
Assegna il nome IUPAC ai seguenti composti



Esercizio n. 1
Assegnare il nome IUPAC, comprensivo di stereochimica, ad ognuna delle seguenti molecole:
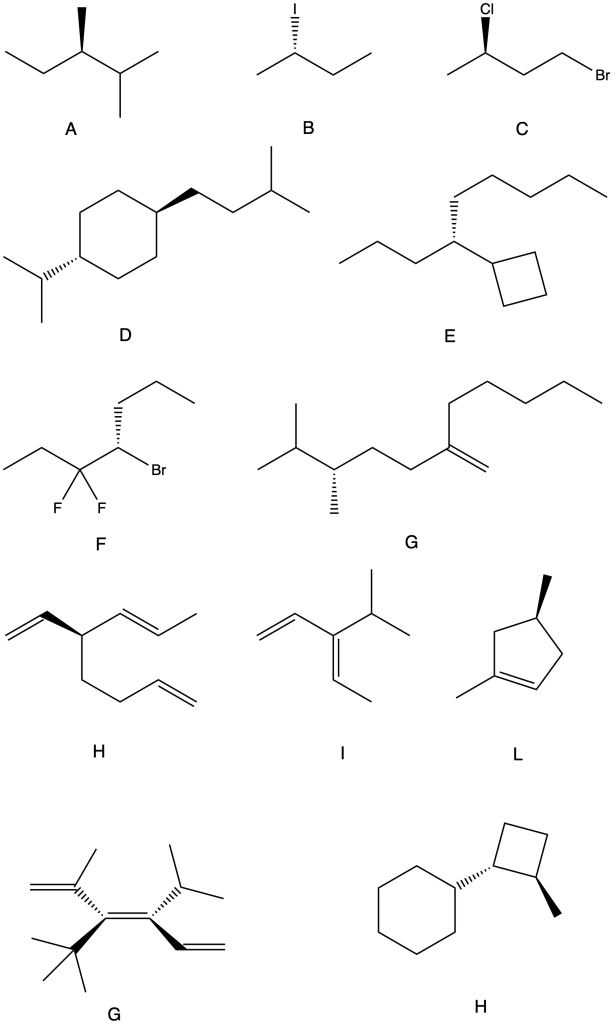
Esercizio n. 2
Per ciascuna delle seguenti coppie di strutture, indicate la relazione stereochimica esistente tra i due composti.
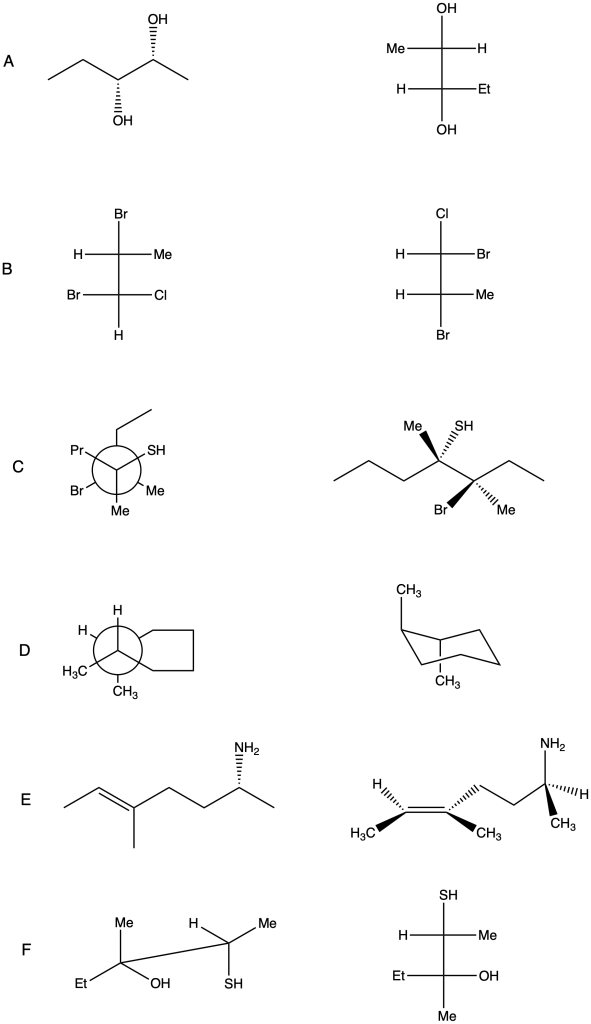
Esercizio n. 3
Disegnate le rappresentazioni strutturali di ciascuna delle seguenti molecole. Controllate che la vostra formula strutturale mostri chiaramente la configurazione allo stereocento.
a) (R)-3-bromometilesano
b) (3R,5S)-3,5-dimetilpentano
c) (2S,3S)-2-bromo-3-metilpentano
d) (S) 1,1,2-trimetilciclopropano
e) (1S,2S)-1-cloro-1-trifluorometil-2-m3tilbutano
f) 1R,2R,3S)-1,2-dicloro-3-etilciclopentano
Esercizio n. 4
Scrivete tutti i possibili stereoisomeri dei seguenti composti
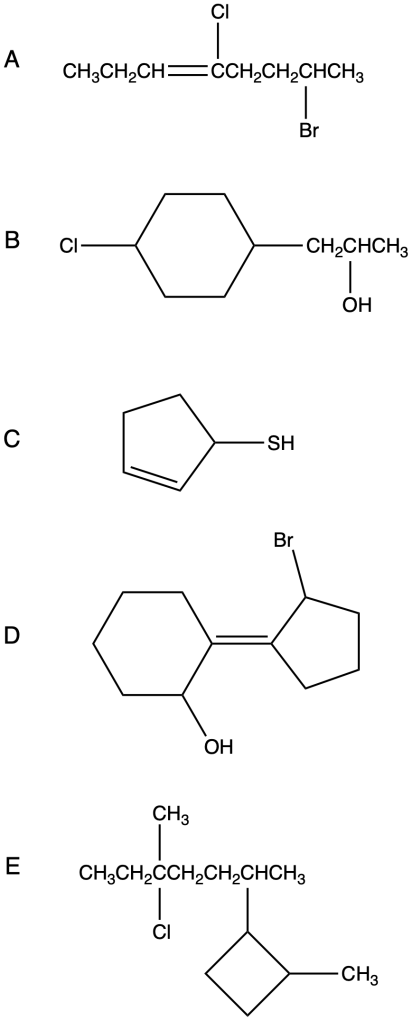

Esercizio n. 1
Assegna il nome ai seguenti composti

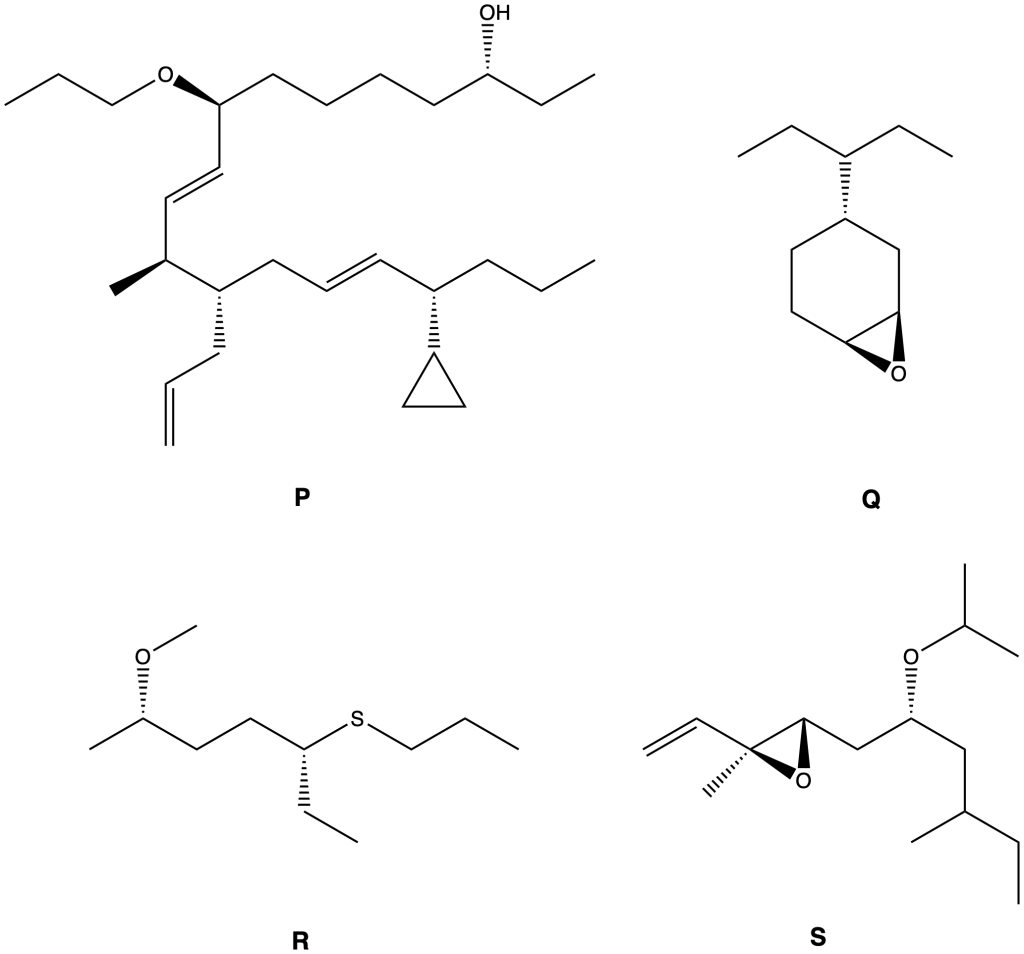
Esercizio n. 2
Assegna il nome IUPAC ai seguenti monoterpeni:


Esercizio n. 1
b.
In questo caso, abbiamo un’addizione coniugata:
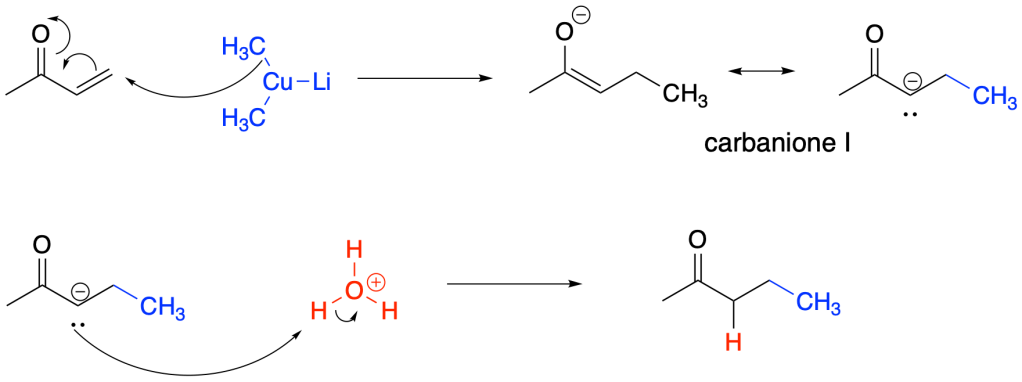
d:
Avviene un’addizione coniugata, come illustrata nella prima parte dell’esercizio 1b. Se il carbanione I è posto in presenza di un elettrofilo (es. un alogenuro alchilico) avviene anche un’alchilazione in alfa.
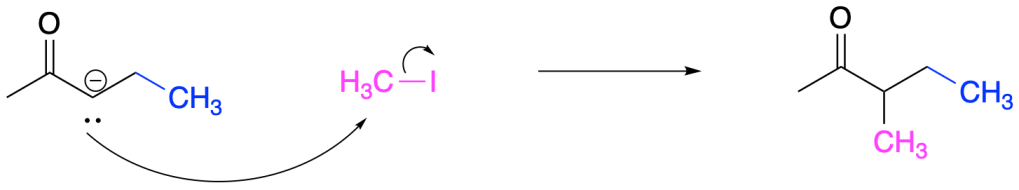
Esercizio n. 2 (reazioni di Michael)
Quando uno ione enolato reagisce con un composto carbopnilico alfa,beta-insaturo si ha sempre un’addizione coniugata (reazione di Michael)
c.
in questo caso il reagente di Gilman (divinilcuprato di litio) si addizione al carbonio beta del ciclopentenone. Successivamente, l’anione enolato che si forma, andrà a dare una reazione di Michael al 3-buten-2-one:
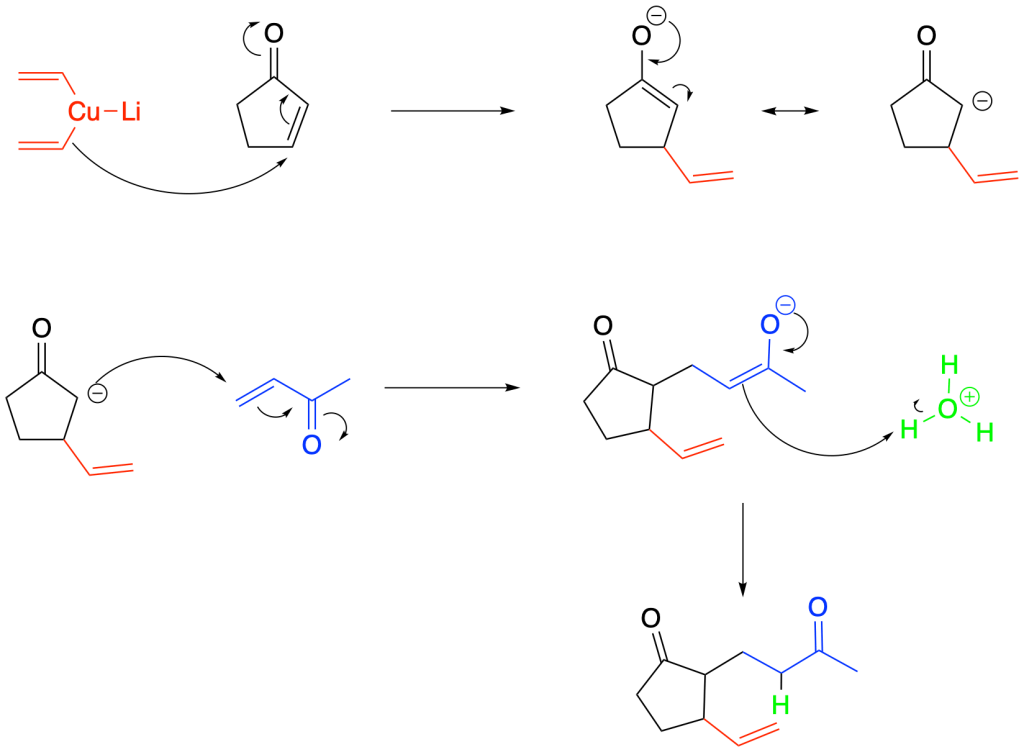
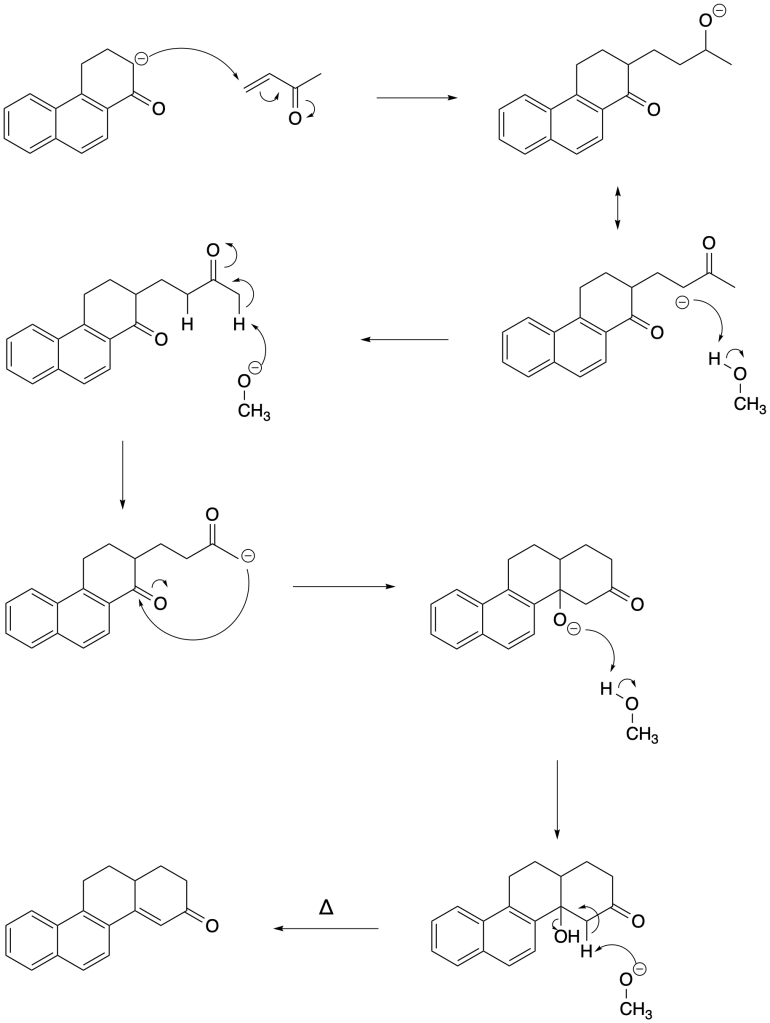
Esercizio n. 3 (reazioni di anellazione di Robinson)
a:
Gli idrogeni in gamma al carbonile sono meno acidi perchè lo ione enolato che si forma utilizza elettroni p del sistema aromatico naftalenico
La base strappa un protone dal carbonio alfa.
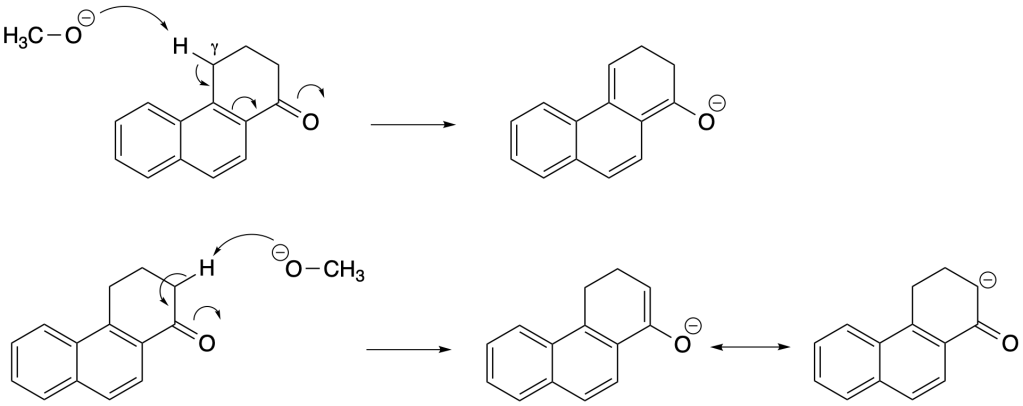
L’anione (donatore di Michael) reagisca con il composto carbonilico alfa,beta-insaturo (accettore di Michael) per dare un 1,5-dichetone (prodotto di Michael).
Quest’ultimo, in presenza di una base dà luogo ad una condensazione aldolica intramolecolare il cui prodotto, in presenza di calore, disidrata per dare un nuovo composto carbonilico alfa,beta-insaturo.

Si avvisano gli studenti del corso di laurea magistrale in Farmacia che :
MERCOLEDI’ 20 APRILE la lezione di Chimica organica non si terrà, pertanto l’orario delle lezioni sarà il seguente:
GIOVEDI’ 21 APRILE il laboratorio di Chimica organica non si terrà e riprenderà giovedì 28
VENERDI 22 APRILE la lezione di Chimica analitica e analisi dei medicinali 1 non si terrà. Le lezioni inizieranno alla terza ora con il seguente orario:

Esercizio n. 1
Indicate il prodotto o i prodotti attesi dalla reazione del 3-pentanonr con 1 equivalente di LDA, seguita dall’addizione di 1 equivalente di:

Esercizio n. 2
Indicare i prodotti delle seguenti reazioni:
A. etanale + 1. pirrolidina, H3O+; 2. 1-cloro-3-metil-2-butene; 3. H3O+, H2O.
B. feniletanale + 1. pirrolidina, H3O+; 2. bromuro di benzile; 3. H3O+, H2O.
Esercizio n. 3
Scrivere il meccanismo e la struttura dei prodotti della reazione di condensazione aldolica di:
A. feniletanale
B. ciclopentanone
C. 3-metilbutanale
Esercizio n. 4
Scrivere le strutture dei prodotti principali attesi dalla reazione tra benzaldeide (in eccesso) e i seguenti composti:
A. 1-feniletanone (acetofenone)
B. 2,2-dimetilciclopentanone
C. 3-pentanone
Esercizio n. 5
Scrivere i prodotti delle seguenti reazioni:
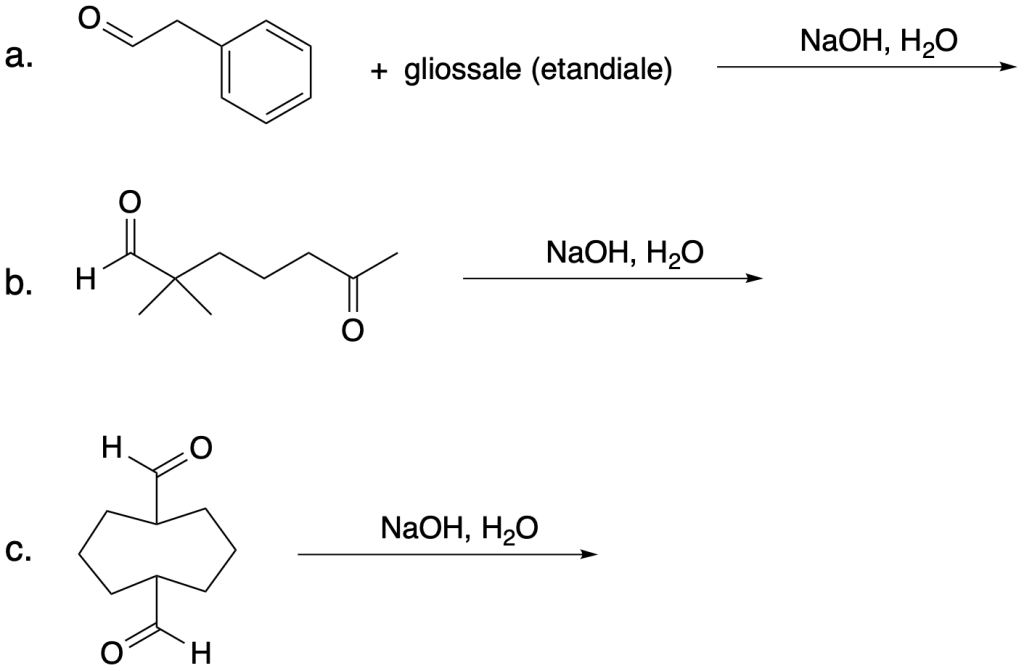
Esercizio n. 6
Proporre i reagenti necessari per convertire il butanale in ciascuno dei seguenti prodotti:
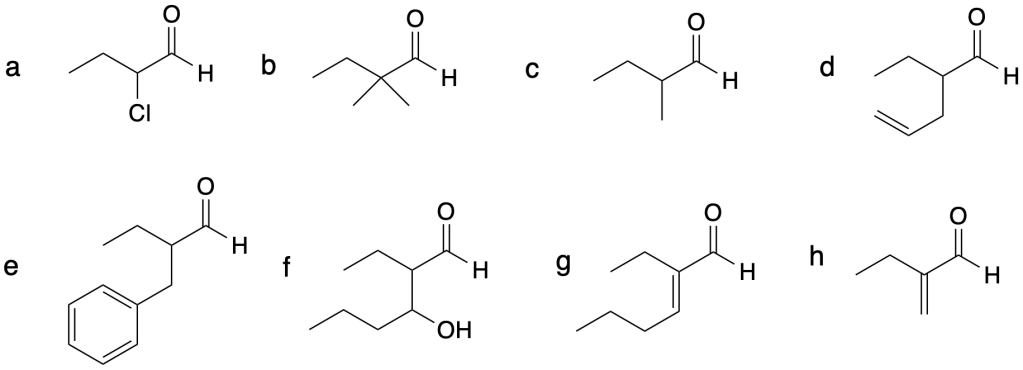
Esercizio n. 7
Proporre i reagenti necessari per convertire l’acetofenone in ciascuno dei seguenti prodotti:
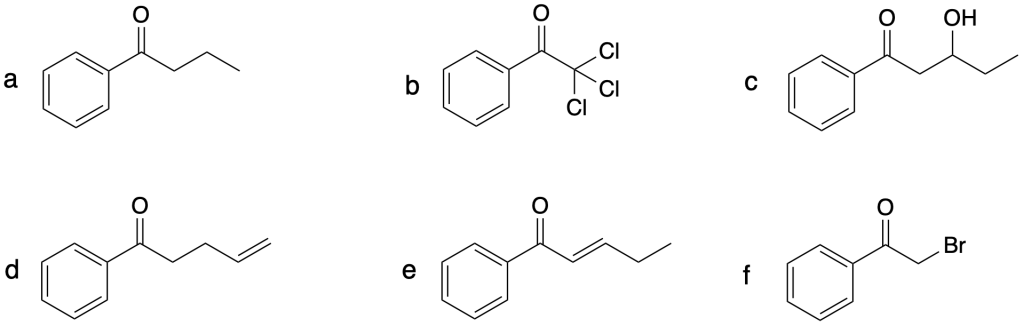

La I prova intercorso di Chimica organica per il corso LMCU in Farmacia si terrà mercoledì 6 aprile alle ore 14:30 in aula B2
Gli studenti ammessi, che hanno superato le prove del I semestre sono i seguenti:

Gli studenti in debito dell’esame di Chimica Organica 2 (vecchio ordinamento) che si sono iscritti al corso nel secondo semestre, possono richiedere al docente di essere inseriti nell’elenco

Esercizio n. 1
Suggerire gli opportuni reagenti necessari per convertire ciascuno dei seguenti materiali di partenza nel prodotto indicato:
a) cloruro di acetile in anidride acetica esanoica
b) esanoato di metile in N-metilesanammide
c) cloruro di esanoile in esanale
d) esanonitrile in acido esanoico
e) esanammide in esanammina
f) esanoato di etile in 3-etil-3-ottanolo
g) esanonitrile in 1-fenil-1-esanone
Esercizio n. 2
Indicare il prodotto di ciascuna delle seguenti reazioni:

Esercizio n. 3
Scrivere la reazione del pentanoato di etile con ciascuno dei seguenti reagenti nelle condizioni indicate:
a) NaOH, H2O, calore; poi H3O+, H2O
b) (CH3)2CHCH2CH2OH (eccesso), H3O+
c) (CH3CH2)2NH, calore
d) CH3MgI (eccesso), Et2O; poi H3O+, H2O
e) LiAlH4 (eccesso), Et2O; poi H3O+, H2O
f) DIBAL, toluene, -78°C; poi H3O+, H2O
Esercizio n. 4
Scrivere la reazione del γ-valerolattone con ciascuno dei reagenti dell’esercizio n. 3
Esercizio n.5
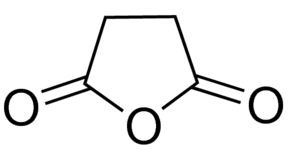
Scrivere il prodotto (o i prodotti) della reazione dell’anidride butandioica (anidride succinica) con i seguenti reagenti:
a) 2-propanolo
b) ammoniaca
c) bromuro di fenilmagnesio in THF; poi H3O+, H2O
d) LiAlH4 in etere etilico; poi H3O+, H2O
Esercizio n.6
Illustrare una sintesi per i seguenti acidi carbossilici. Quale tra essi potrebbe essere sintetizzato alternativamente via Grignard (reattivo di Grignard + CO2) e via nitrili?
a) acido fenilacetico
b) acido 3-butenoico
c) acido esanoico
d) acido 2,2-dimetilpentanoico
e) acido 4-metilbenzoico
Esercizio n. 7
Quale sintesi, via Grignard o via nitrile, potrebbe essere utile per sintetizzare l’acido 5-idrossipentanoico a partire dal 4-bromo-1-butanolo? Perchè?
Esercizio n. 8
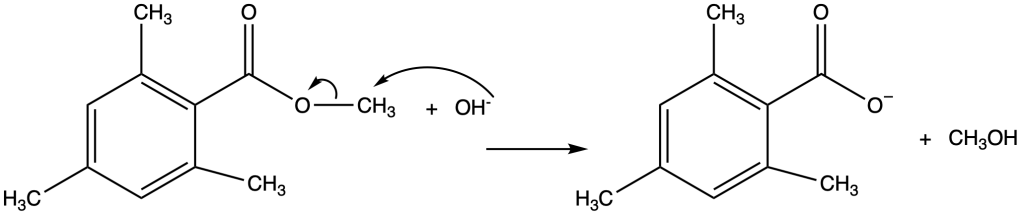
L’idrolisi basica del mesitoato di metile ha luogo attraverso un attacco promosso dallomione alcossido a livello del carbonio alcolico anzicchè acilico. Quale potrebbe essere una motivazione che giustifichi questo comportamento inusuale?

Il laboratorio di Chimica organica nel secondo semestre si terrà tutti i giovedì.
La prima esercitazione si terrà GIOVEDI’ 24 marzo
1° Turno: ore 9,00
2° Turno: ore 14,00
You must be logged in to post a comment.