Corso di Metabolomica: si parla di noi
Pubblicato su ATENEAPOLI un articolo sul nostro corso di Metabolomica

Università degli Studi della Campania "Luigi Vanvitelli"
Pubblicato su ATENEAPOLI un articolo sul nostro corso di Metabolomica


Pronti per la sfida di questo fine settimana?
Come annunciato a lezione, in questo fine settimana si terrà la prima Weekend Organic Chemistry Challenge di quest’anno.
Ricordatevi che vincerà chi risponderà per primo in maniera corretta!
LA sfida potrà riguardare tutti gli argomenti affrontati fino ad ora!
Le vecchie challenge sono disponibili in archivio (a fine pagina).

Risolvi i seguenti quesiti




1. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

2. Indicare il tipo di ibridazione per ognuno degli atomi (escluso l’H) dei seguenti composti

3. Per gli atomi indicati da una freccia nei seguenti composti, indicare:

4. Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

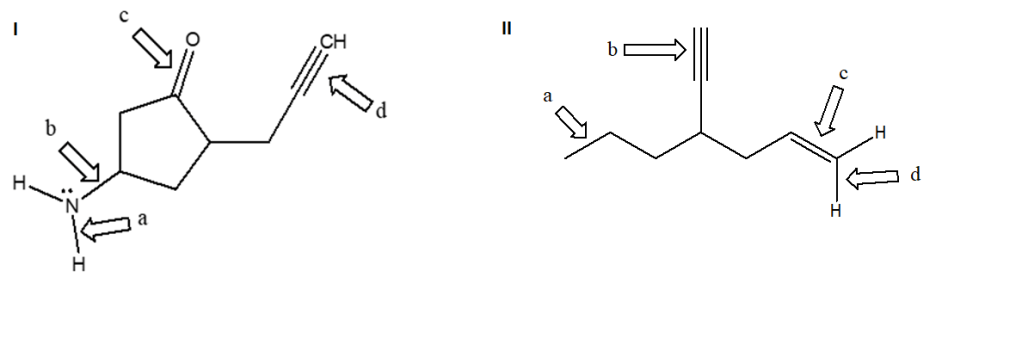
5. Nelle seguenti figure, alcuni dei legami sono indicati da freccia e da una lettera. a) Etichettare i legami a-d come singoli, doppi o tripli; b) Indicare (per qui legami) il tipo di orbitale/i molecolare/i; c) dire quali orbitali atomici sono coinvolti nella formazione del legame.
d) Considerando tutti i legami singoli della molecola (ed escludendo i legami C-H) qual è il legame più corto? (NB: in questo caso ci riferiamo a tutti i legami, non solo a quelli indicati da freccia e lettera)
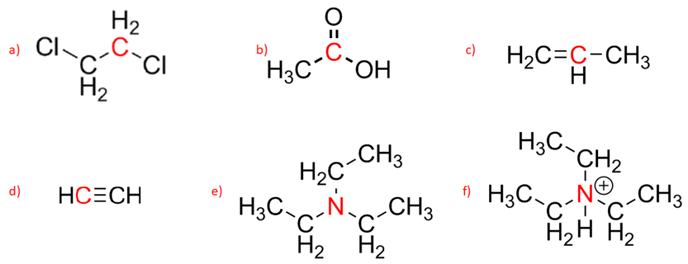
6. Per gli atomi mostrati in rosso nelle seguenti strutture, dire l’ibridazione, la geometria e l’angolo di legame. Dire, inoltre, quali orbitali molecolari formano (con ciascuno degli atomi con cui sono legati) e quali orbitali atomici e orbitali ibridi sono coinvolti nella formazione di ciascun orbitale molecolare.
7. Quale delle seguenti affermazioni è falsa?
Un orbitale molecolare sigma
a) può derivare dalla sovrapposizione laterale di due orbitali atomici p
b) può derivare dalla sovrapposizione testa-testa di due orbitali atomici p
c) può derivare dalla sovrapposizione di due orbitali atomici s
d) può derivare dalla sovrapposizione di un orbitale atomico s e un orbitale atomico p
e) può essere sia di legame sia di antilegame
8. Gli orbitali molecolari di antilegame sono prodotti da:
a) interazione costruttiva (in fase) degli orbitali atomici
b) interazione distruttiva (fasi opposte) degli orbitali atomici
c) la sovrapposizione degli orbitali atomici di due ioni negativi
d) tutte le precedenti
e) nessuna delle precedenti
9. Quali orbitali ibridi si trovano nella molecola di acqua?
a) sp3
b) sp2
c) sp3d
d) sp
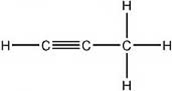
10. Quanti legami σ carbonio-carbonio ci sono nella seguente molecola?

Il Premio Nobel 2022 per la Chimica è stato assegnato ieri a Carolyn Bertozzi (Università di Stanford), Barry Sharpless (The Scripps Research Institute, La Jolla California) e Morten Meldal (Università di Copenhagen) per i loro studi sulla click chemistry e le applicazioni di quest’ultima in campo biologico (chimica bioortogonale).
La click chemistry è una metodologia sintetica che permette di connettere due molecole, anche molto complesse come biomolecole e biopolimeri in modo semplice (del resto il termine onomatopeico “click” rende l’idea) e selettivo. Inoltre, fondamentale per le applicazioni biologiche è la possibilità di far avvenire queste reazioni in condizioni blande e in solvente acquoso e che le tali reazioni non interferiscano con i processi biochimici.
La click chemistry ha avuto un enorme impatto in tante aree, inclusa la biologia e la medicina. Ha permesso, tra le altre cose, di capire il ruolo di alcune biomolecole coinvolte in importanti processi cellulari e lo sviluppo di nuove terapie di precisione per la cura del cancro e altre patologie.
Per saperne di più: The Nobel Prize in Chemistry 2022

Si ricorda che le lezioni di Chimica Organica del CdL in Scienze Biologiche si tengono in Aula A1 il venerdì e in A3 il lunedì e il mercoledì!

Due video per visualizzare e capire l’ibridazione del carbonio e la formazione dei legami nei composti organici!

Il ricevimento è uno dei tanti strumenti messi a vostra disposizione! Può essere utilizzato per chiarire i vostri dubbi, confrontandovi direttamente con il docente. Sulla pagina del nostro corso trovate sia gli orari di ricevimento del docente, sia un link per prenotare il ricevimento stesso. Seguendo il link, e dopo aver scelto la data e l’orario per il ricevimento, si aprirà una pagina simile a quella qui riportata:
Come anticipato a lezione, ora è possibile indicare anche se volete fare ricevimento in gruppo. In tal caso, basterà che una sola persona compili il form di prenotazione e indichi nell’ultimo campo (quello facoltativo) il numero di persone interessate.




In che modo gli atomi formano legami covalenti?
Secondo la teoria degli orbitali molecolari, i legami covalenti vengono fuori dalla combinazione di orbitali atomici per formare orbitali molecolari.
Su ChemTube 3D, è possibile visualizzare gli orbitali molecolari di diverse molecole, come ad esempio dell’ H2 o dell’etene.
You must be logged in to post a comment.