Atomi e molecole: ulteriori esercizi

Esercizio n.1
Calcolare la carica formale per tutti gli atomi (tranne idrogeno) delle seguenti specie.

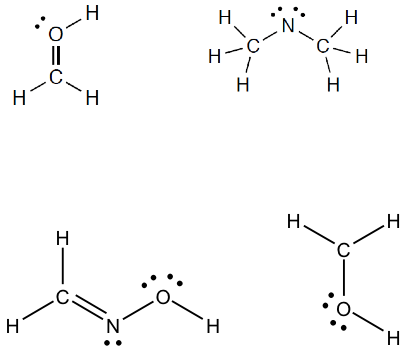
Esercizio n. 2
Scrivere la struttura di Lewis dell’anione nitrato
Esercizio n. 3
Rappresentare la struttura di Lewis dello ione idrogenosolfato. Calcolare le cariche formali e scrivere almeno due strutture di risonanza.
Esercizio n. 4
Rappresentare la struttura di Lewis, comprendendo i tipici contributi alla struttura di risonanza (ove appropriato) in relazione a: (a) cloruro di ammonio; (b) ipoclorito di calcio.
Esercizio n. 5
Scrivere tre strutture di risonanza a differente energia dello ione periodato. Determinare la carica formale di ciascun atomo ed identificare la struttura di energia minima
Esercizio n. 6
Rappresentare la struttura di Lewis dello:
(a) ione solfato
(b) ione solfito
Calcolare le cariche formali e scrivere almeno due strutture di risonanza per ogni specie














You must be logged in to post a comment.