Weekend Organic Chemistry Challenge

Regolamento:
- Vincerà la sfida chi risponderà per primo CORRETTAMENTE al seguente quesito.
- La risposta dovrà essere postata nel seguente modo: bisognerà inserire nei commenti al post la descrizione sintetica del meccanismo proposto e contestualmente inviare una foto del meccanismo via chat di teams. Risposte per le quali mancherà una delle due cose non saranno ritenute valide.
- Ognuno può rispondere solo una volta (anche in presenza di più di un commento pubblicato dalla stessa persona, soltanto il primo sarà preso in considerazione).
- Il tempo massimo a disposizione sarà di 48h dalla pubblicazione del post.
- Il vincitore (4 pt) sarà annunciato a lezione.
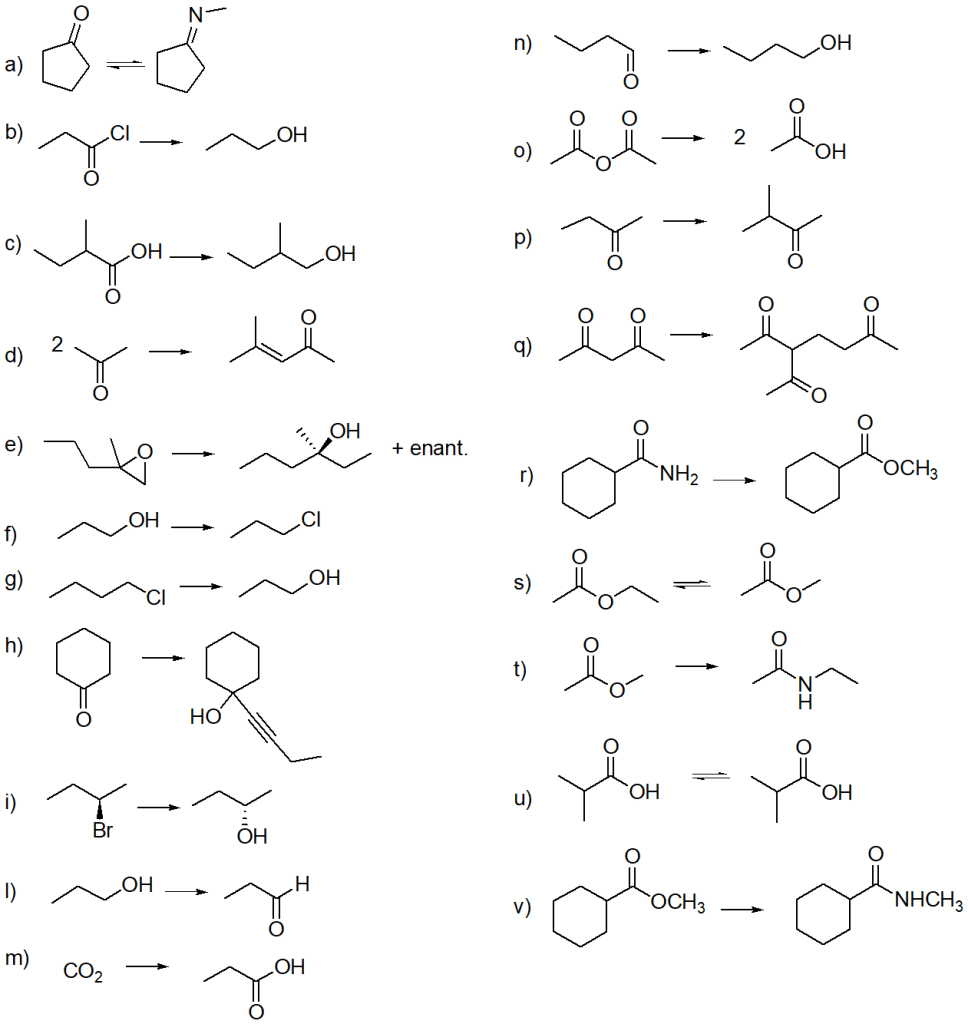
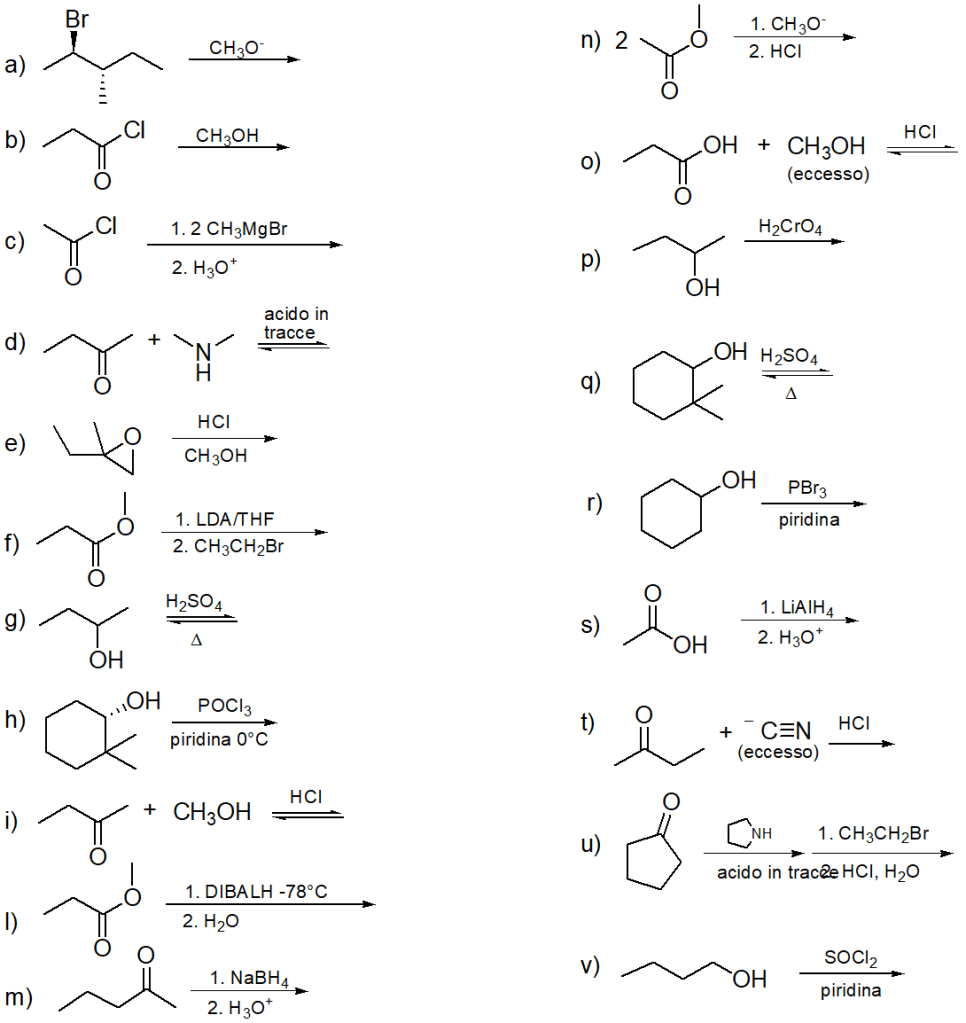
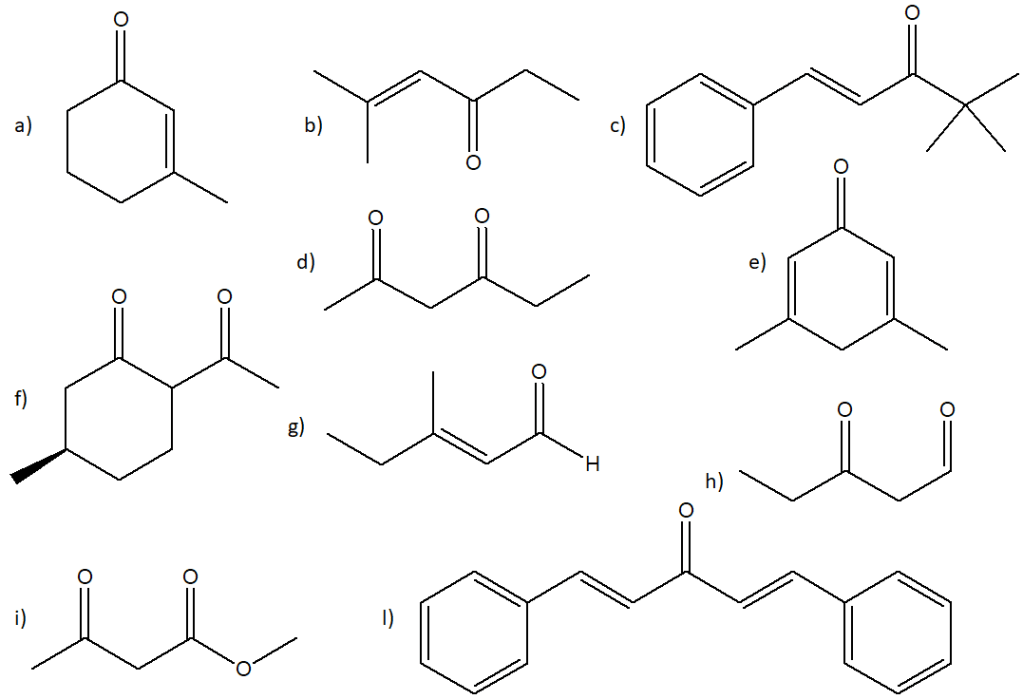
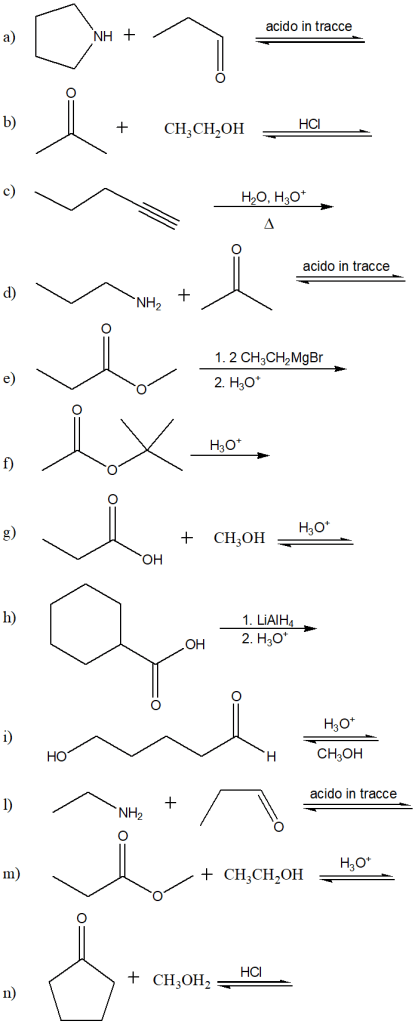
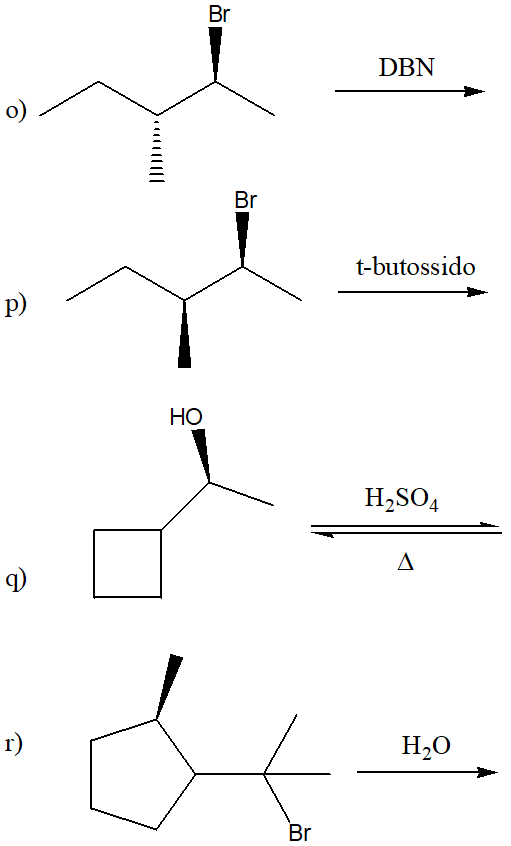
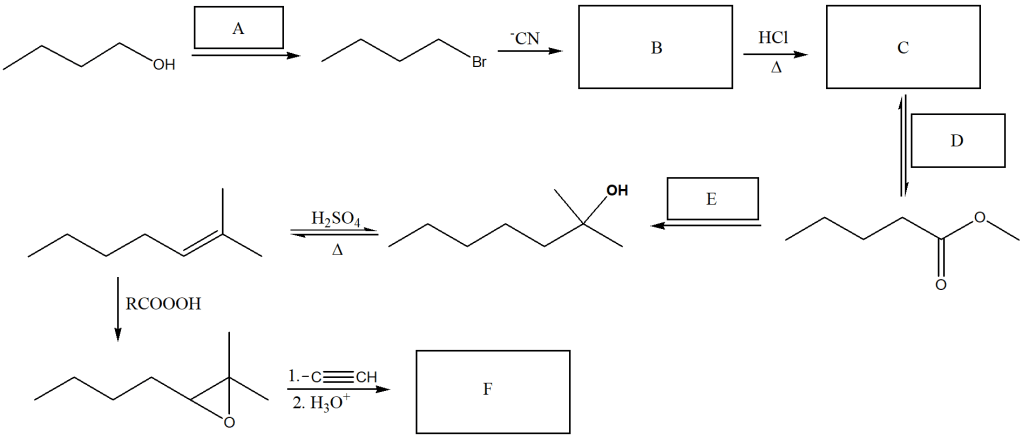
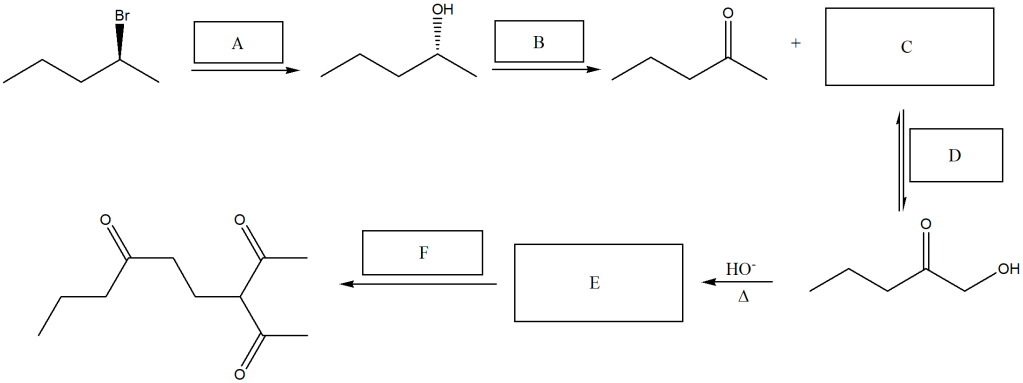
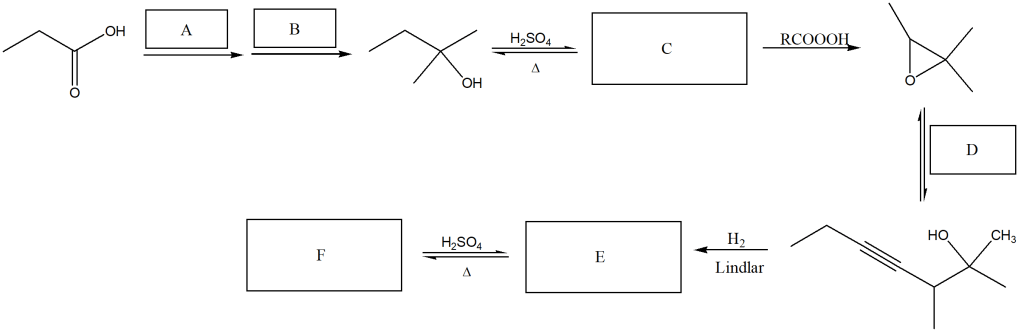
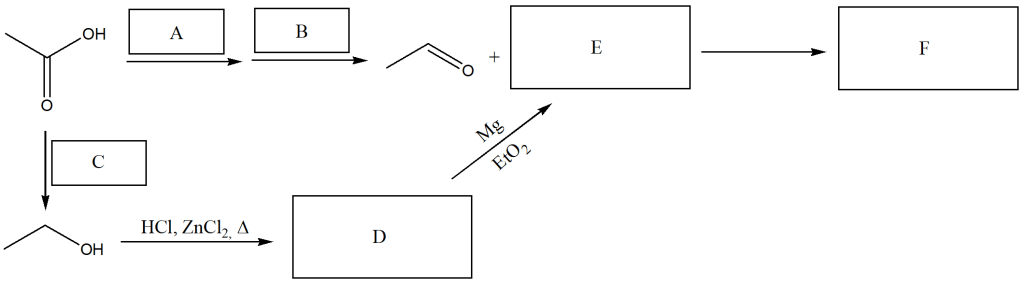
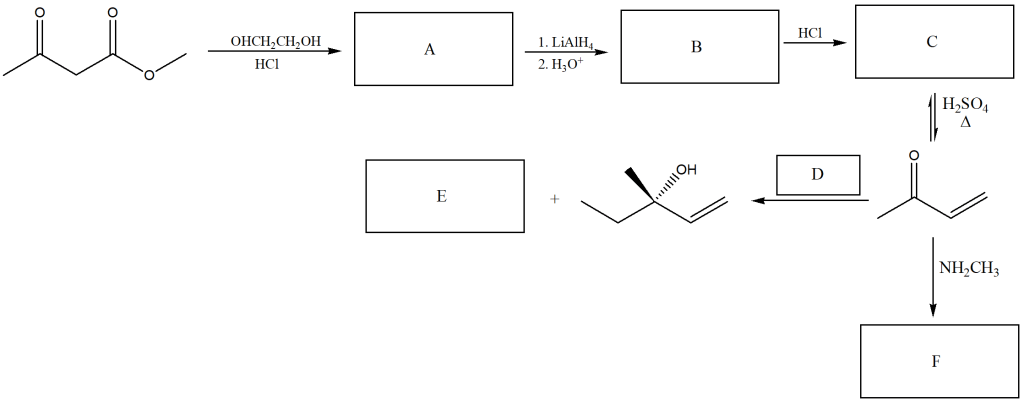
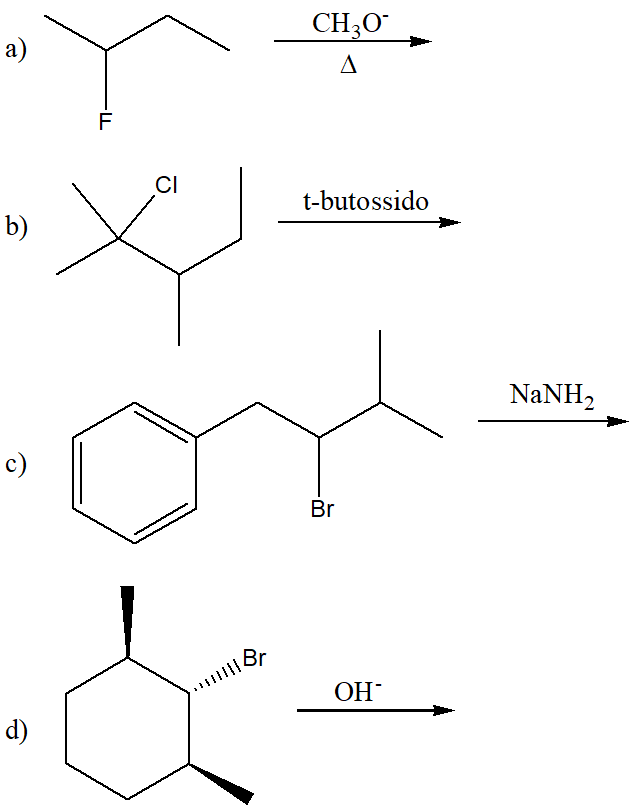
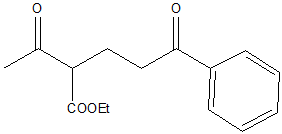
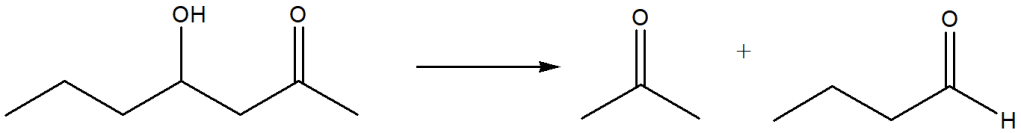
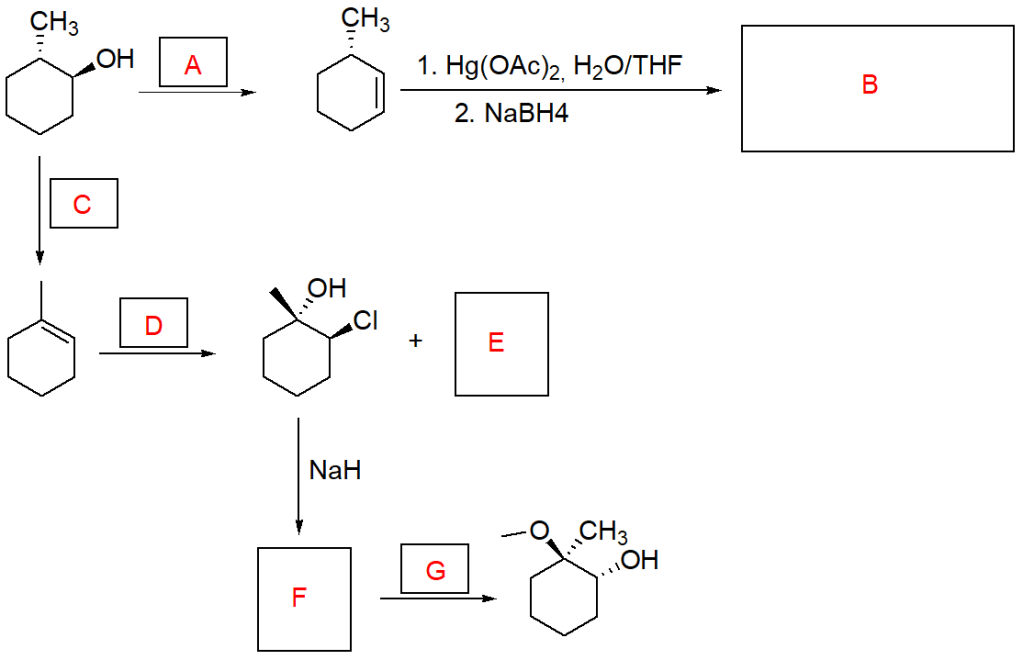
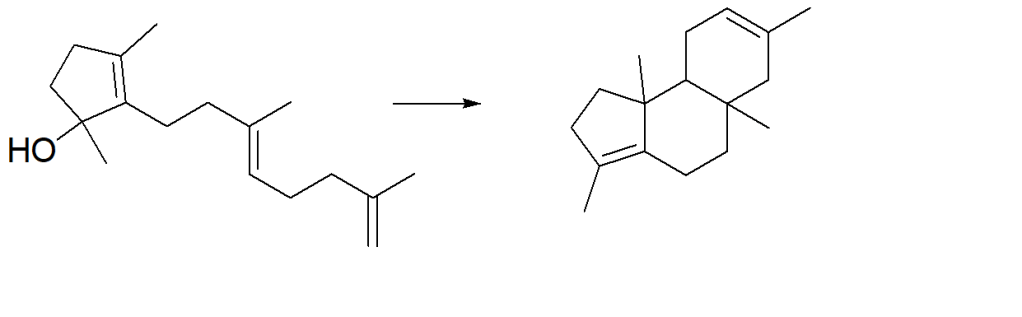
Proporre un meccanismo per la seguente reazione:
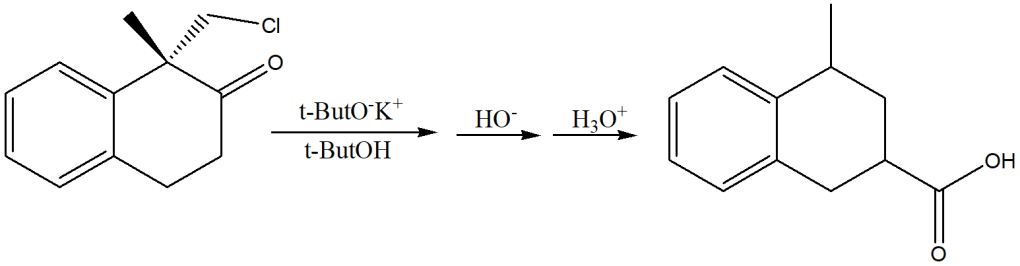
Suggerimenti:
1. Mostrare i primi passaggi della reazione utilizzando una rappresentazione a sedia della porzione della molecola costituita dal cicloesanone. Potete anche “sottintendere” la presenza dell’altro anello in questa fase, indicandolo nel modo seguente:

2. Ragionare sempre in riferimento alla reazione tra un nucleofilo ed un elettrofilo piuttosto che per schemi predefiniti. Analogamente, considerare eventuali reazioni acido-base che possono avvenire.
3) Considerare anche i vari fattori che possono stabilizzare o, al contrario, rendere meno stabili gli intermedi eventualmente formati nel corso della reazione!
NB:l’abbreviazione sulla prima freccia sta per t-butossido

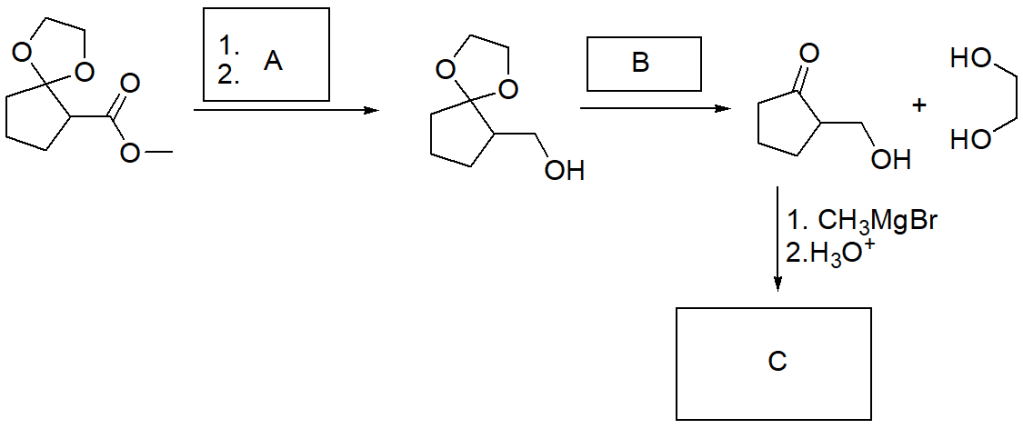
SUGGERIMENTO II
Ecco a voi un piccolo suggerimento…ma i punti scendono a 3. Se entro 12 ore non avremo la soluzione, pubblicherò un ulteriore suggerimento (che porterà ad una ulteriore diminuzione dei punti che saranno assegnati in caso di vittoria).
Scriviamo la molecola nel modo seguente:
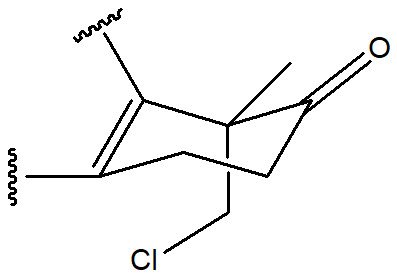
La base utilizzata nel primo passaggio andrà a strappare uno degli idrogeni più acidi…cosa si forma?
A quel punto, chi può subire un attacco nucleofilo?

SUGGERIMENTO III
Ora i punti scendono a 2… Ultima chance:
A seguito dell’attacco nucleofilo di cui si parla nel suggerimento II, si forma un nuovo ciclo caratterizzato da una notevole tensione d’anello e quindi molto reattivo. Lo ione idrossido attaccherà il carbonio carbonilico, formando un intermedio tetraedrico. Successivamente, una coppia solitaria dell’ossigeno riforma il legame pi-greco e a questo punto si romperà un legame apparentemente inaspettato (bisogna valutare tutti quei fattori che rendono più o meno stabile un intermedio rispetto ad un altro per capire perchè la reazione procede in tal senso)…

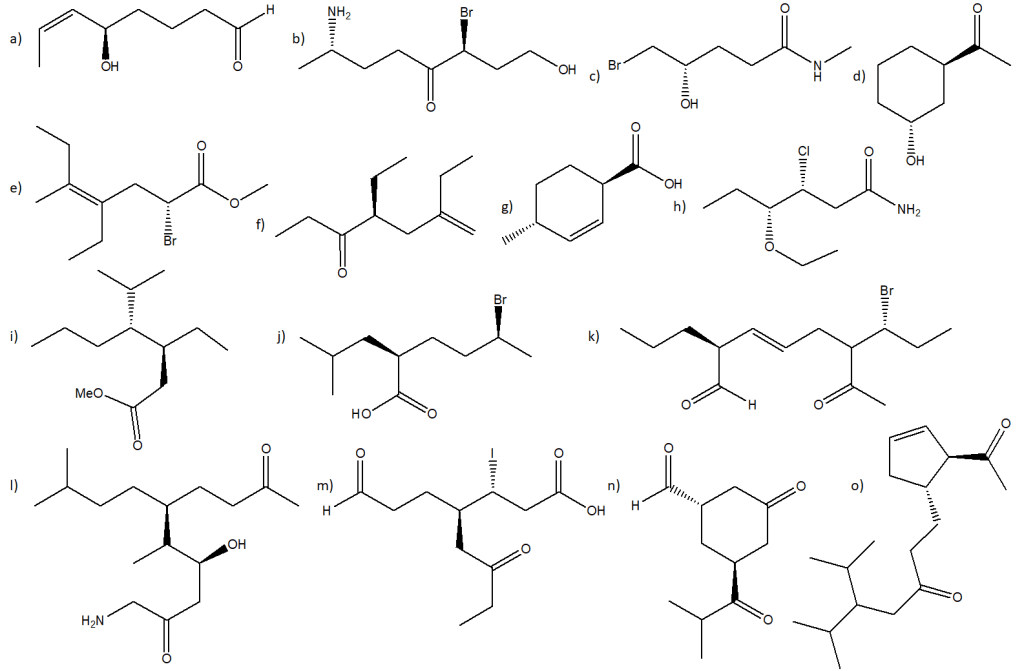














You must be logged in to post a comment.