Introduzione alla nomenclatura sistematica IUPAC

Il primo impatto con le regole di nomenclatura IUPAC può essere difficile, ma dobbiamo assolutamente conoscere questo sistema che ci permette di evitare di imparare a memoria migliaia e migliaia di nomi di composti organici.
Cerchiamo di esercitarci insieme in maniera graduale.
Occorrente: libro (in particolare Bruice), carta e penna, tanta pazienza e la totale attenzione…
Suggerimento: seguire l’ordine con cui gli esercizi sono presentati.
Vedrete che sul libro le regole sono numerate. I seguenti gruppi di esercizi devono essere svolti applicando le regole indicate nella traccia. Prima di svolgerli, leggete e capite bene le regole in questione. Se alla fine di ciascun set non avete dubbi, allora passate al successivo. Se avete dubbi, rivolgetevi alla docente per chiarimenti.
PRIMO SET: assegnare il nome sistematico IUPAC ai seguenti composti, applicando le regole 1 e 2
Individuiamo la catena continua di atomi di carbonio più lunga (che non è necessariamente quella lineare) e definiamo il nome dell’idrocarburo genitore (o catena principale). La catena va numerata a partire dall’estremità che dà al sostituente il numero più basso possibile. Il nome del sostituente alchilico va messo prima del nome dell’idrocarburo genitore, insieme al numero che indica il carbonio cui è legato.

SECONDO SET: assegnare il nome sistematico IUPAC ai seguenti composti, applicando le regole 1, 2, 3 e 4
Regole aggiunte: Se ci sono più sostituenti, si numera la catena principale a partire dall’estremità che dà il numero più basso al sostituente che si incontra per primo (3). I sostituenti si elencano in ordine alfabetico.
Che succede se le due direzioni portano allo stesso numero per il sostituente che ha il numero più piccolo? Si numera nella direzione che dà il numero più basso possibile al sostituente successivo (4).

TERZO SET: assegnare il nome sistematico IUPAC ai seguenti composti, applicando le regole 1, 2, 3, 4 e 5
Regole aggiunte: Cosa si fa se non è possibile decidere da quale estremità cominciare a numerare perchè si ottengono gli stessi numeri per i sostituenti sia in una direzione sia nell’altra? In questo caso (e SOLO in questo caso) il gruppo citato per primo (quello che viene prima in ordine alfabetico) riceve il numero più basso.

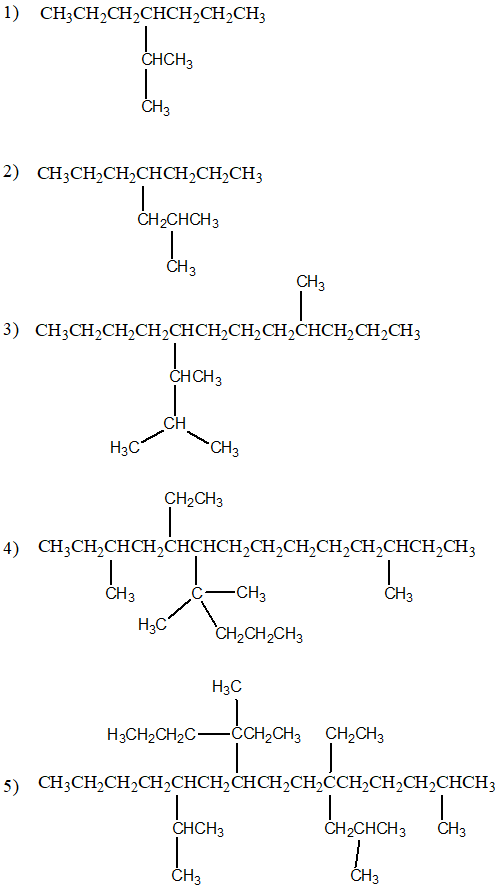
QUARTO SET: assegnare il nome sistematico IUPAC ai seguenti composti, applicando le regole 1,2,3,4,5,6
Regole aggiunte: Se ci sono sostituenti ramificati, attribuire ad essi il nome numerando il sostituente a partire dal carbonio legato all’idrocarburo genitore. Il carbonio 1 è, dunque, quello legato alla catena principale. Il nome del sostituente viene messo tra parentesi. Non bisogna dimenticare di scrivere, fuori dalla parentesi, il numero che indica la posizione del sostituente ramificato sulla catena principale.
QUINTO SET: assegnare il nome sistematico IUPAC ai seguenti composti, applicando le regole 1,2,3,4,5,6,7
Regole aggiunte: Che succede se ci sono due o più catene della stessa lunghezza? Quale dovremo scegliere come catena principale? La catena principale sarà quella con il maggior numero di sostituenti.
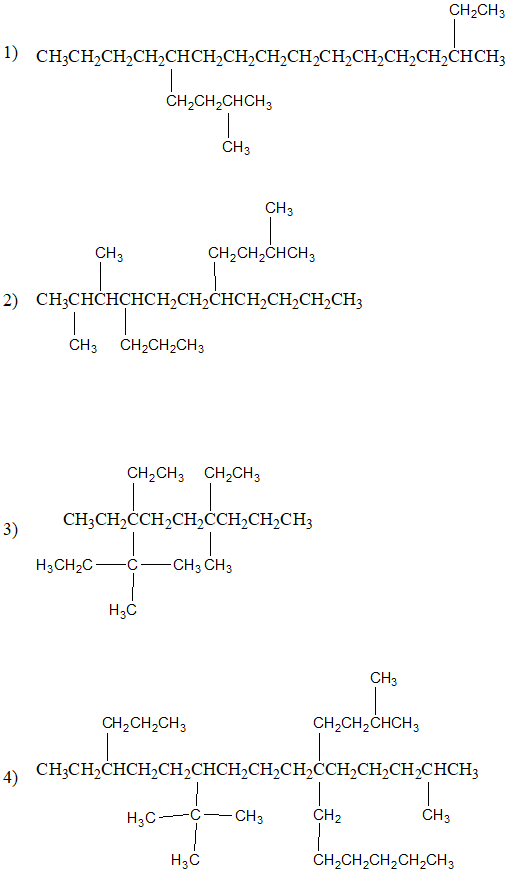
NB: I numeri cui si fa riferimento nella traccia di ciascun set sono quelli usati nel Bruice, ultima edizione.
Notate come, man mano che aggiungiamo regole, non dobbiamo dimenticare quelle precedenti.
Seguiranno altri esercizi…







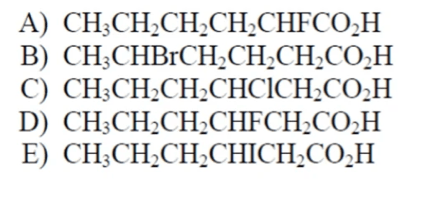


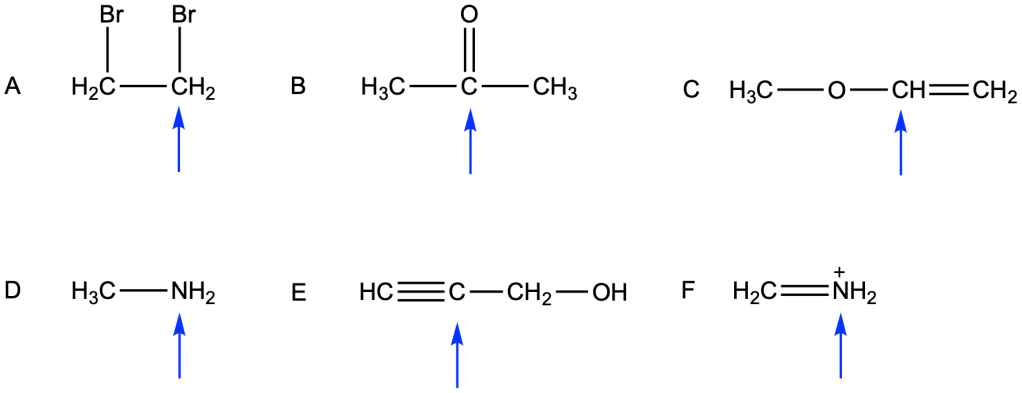

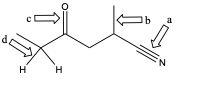


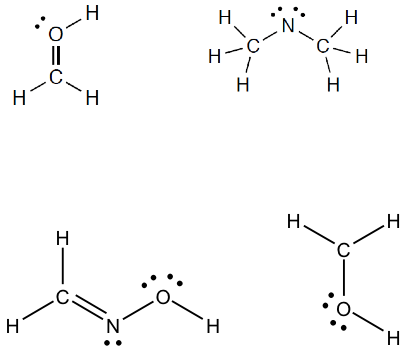


You must be logged in to post a comment.