Esercitazione Stereochimica



Università degli Studi della Campania "Luigi Vanvitelli"





REGOLE DI CHAN-INGOLD-PRELOG (Regole CIP)
Nel 1950 i chimici Cahn, Ingold e Prelog proposero una serie di regole universali e non ambigue per specificare la configurazione assoluta (R/S) delle molecole che presentano un centro chirale. Le stesse regole sono utilizzate per stabilire la configurazione E/Z di un doppio legame.
Per assegnare una configurazione R o S a un carbonio chirale (oppure una configurazione E/Z ad un doppio legame) si seguono precise regole di priorità, vale a dire si stabilisce quale atomo o gruppo prevale per le sue caratteristiche sugli altri (o sull’altro).
Regole CIP:
1. Tra gli atomi legati al centro stereogenico, quelli che hanno numero atomico più alto hanno priorità più alta.

2. Se due atomi legati al centro stereogenico sono identici, per assegnare la priorità si tiene conto del numero atomico dell’atomo successivo a quello dei due atomi considerati

3. A tutti gli atomi, con eccezione dell’idrogeno, viene formalmente data una valenza pari a 4. Se la valenza reale è inferiore, (come nel caso dell’azoto, dell’ossigeno o di un carbanione), per raggiungere la tetravalenza si utilizzano “atomi fantasma” (phantom atoms). Agli atomi fantasma viene assegnato un numero atomico pari a 0.

4. Gli atomi legati con un doppio o triplo legame sono trasformati in «legami singoli equivalenti» aventi come sostrituenti 3 atomi «fantasma» che servono solo per l’assegnazione della priorità. Gli atomi fantasma non sono legati ad altri atomi. Ogni doppio legame è duplicato e ogni triplo legame è triplicato.

5. Quando ci sono cicli come sostituenti è necessario convertire la struttura in una versione aciclica. Se consideriamo l’esempio del ciclopropano, bisogna considerare la sequenza C1-C2-C3-(C1) e la sequenza C1-C3-C2-(C1), dove l’ultimo termine di ogni sequenza è un carbonio duplicato (C1) che si intende legato a tre atomi fantasma.



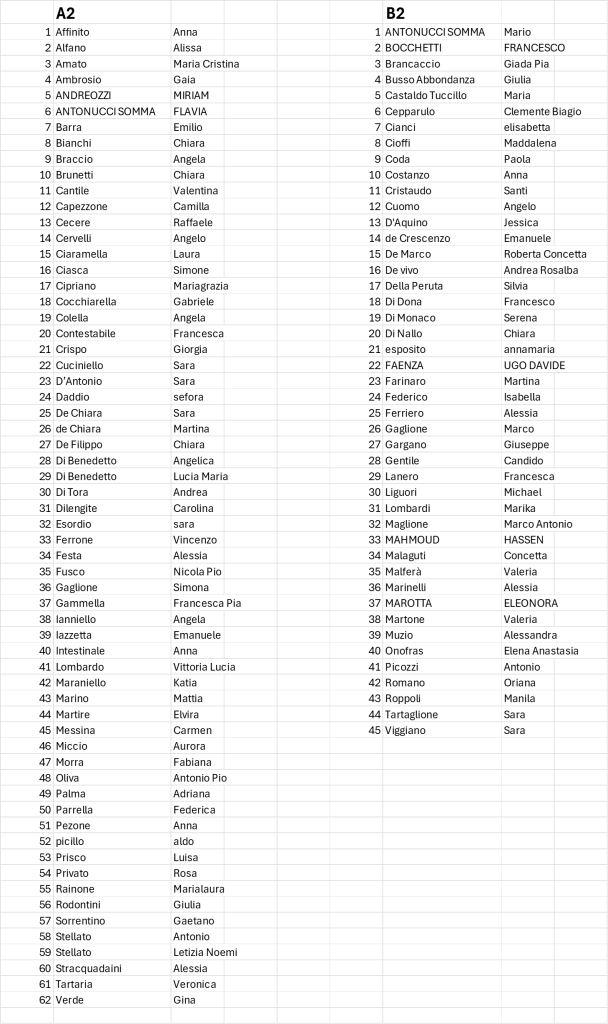
Nel corso della II prova intercorso è consentito l’utilizzo dei modellini
DI seguito la distribuzione nelle aule
NB: se qualcuno non ha intenzione di sostenere la II prova intercorso, è invitato a darne tempestiva comunicazione alla docente

Separazione di una miscela a due componenti mediante estrazione liquido-liquido e analisi cromatografica dell’efficienza di estrazione.

Diapositive della lezione:

PROIEZIONI DI NEWMAN, A CAVALLETTO E DI FISCHER
In chimica la proiezione (o formula proiettiva) è un modo di rappresentazione bidimensionale della struttura tridimensionale di una molecola. Riveste una notevole importanza per quanto riguarda la rappresentazione degli isomeri.
Nelle formule prospettiche, due dei legami del carbonio asimmetrico sono disegnati come segmenti che giacciono sul piano del foglio, un terzo come un cuneo pieno, che rappresenta un legame che viene avanti fuori dal piano, verso l’osservatore e il quarto legame viene disegnato come un cuneo tratteggiato che rappresenta un legame che si estende dietro al piano, lontano dall’osservatore.
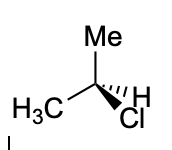
I legami C-Me e C-Et giacciono nel piano; il legame C-Cl punta in avanti, fuori dal piano, verso l’osservatore; il legame C-H affonda nel piano, lontano dall’osservatore.
Nelle proiezioni di Fischer le linee orizzontali rappresentano dei legami che emergono dal piano del foglio, mentre quelle verticali indicano legami che affondano sotto il piano del foglio. Per trasformare una formula prospettica in una proiezione di Fischer, bisogna osservare la molecola in modo che due gruppi legati al carbonio chirale siano rivolti verso l’osservatore lungo una linea orizzontale, mentre gli altri due siano rivolti lontano dall’osservatore lungo una linea verticale.

Per una data formula prospettica è possibile scrivere diverse proiezioni di Fischer, cambiando il punto di osservazione. Attenzione a guardare sempre la struttura in modo da avere due gruppi verso l’osservatore lungo una linea orizzontale.

La proiezione di Newman è un metodo utilizzato per la rappresentazione grafica di una struttura molecolare che consiste in una proiezione frontale lungo l’asse di un certo legame C-C. Il carbonio anteriore viene rappresentato come un punto (il punto in cui si incontrano i tre legami), mentre il carbonio posteriore è rappresentato da un cerchio, sono indicati parzialmente.

La proiezione di Newman è particolarmente sfruttata nello studio della conformazione dei composti aciclici, in quanto riesce a evidenziare facilmente i diversi conformeri sfalsati o eclissati considerando semplicemente l’effetto della rotazione lungo l’asse di legame in cui è effettuata la proiezione. Graficamente è possibile mettere in relazione in modo chiaro i vari conformeri ottenibili e la loro energia associata, in modo tale da evidenziarne il diverso livello di stabilità.

Le strutture a cavalletto mostrano il legame C-C in modo prospettico.
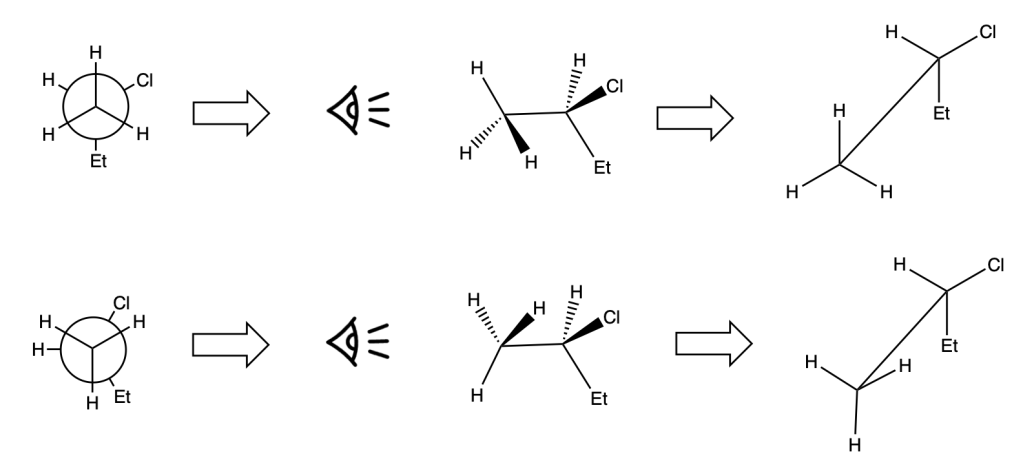
Molecole con due carboni asimmetrici possono essere rappresentate mediante proiezioni di Newman o strutture a cavalletto:

Per passare dalla struttura a cavalletto alla proiezione di Fischer, dobbiamo ruotare uno dei due carboni della struttura a cavalletto in modo da avere una conformazione eclissata. Questo è essenziale in quanto per poter scrivere una proiezione di Fischer, i sostituenti sulla linea orizzontale devono essere tutti rivolti verso l’osservatore, mentre i sostituenti sulla linea verticale devono essere tutti rivolti lontano dall’osservatore:


ISOMERI OTTICI



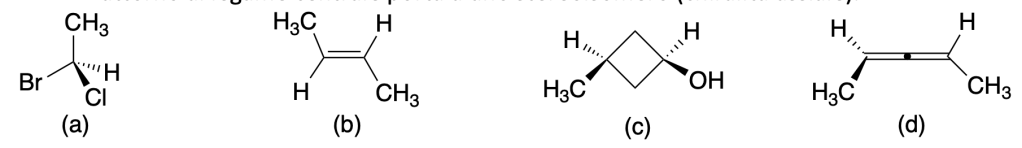

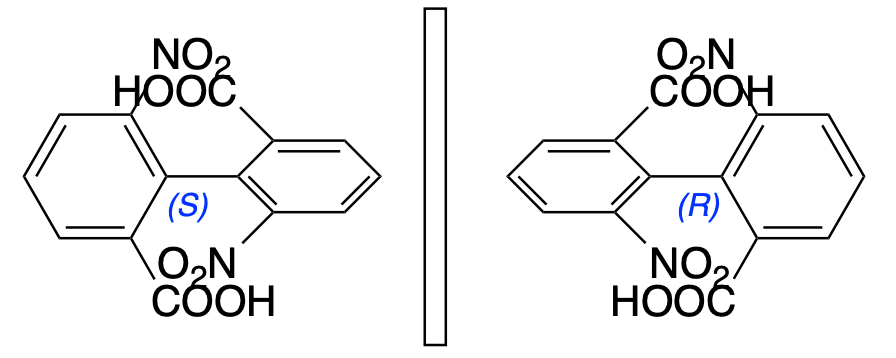
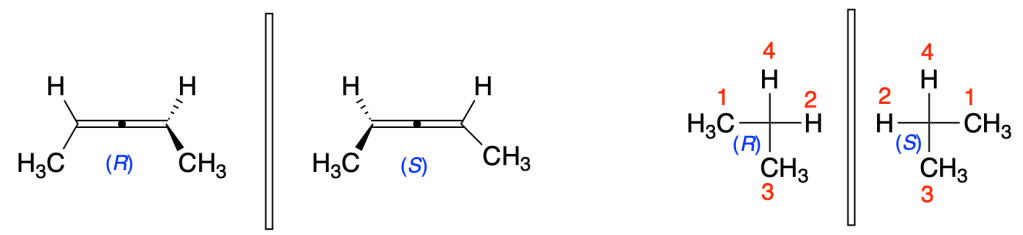



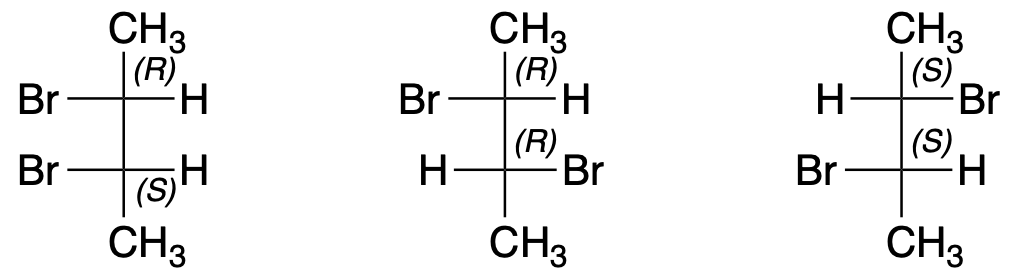
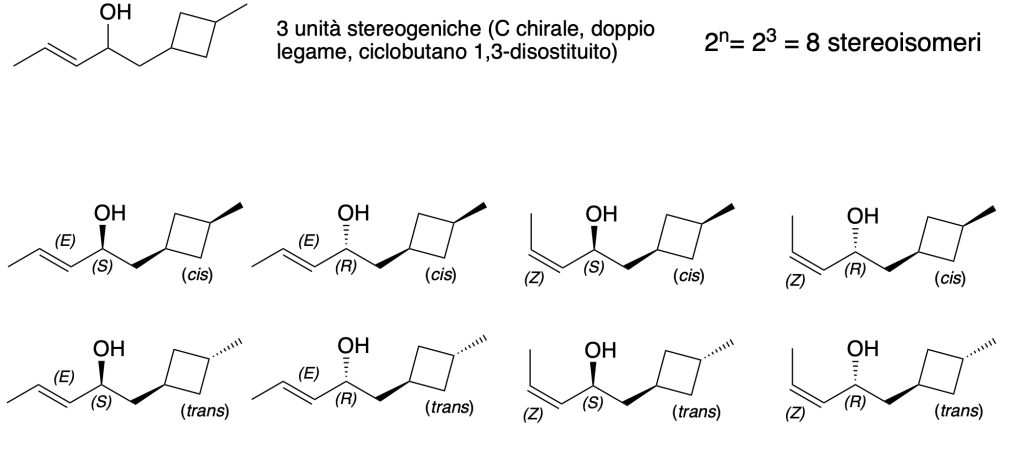

Esercizio n. 1
Identificare la relazione strutturale esistente tra i due termini di ciascuna delle 4 coppie di composti (enantiomeri, diastereoisomeri, isomeri costituzionali, conformeri, due rappresentazioni dello stesso composto)
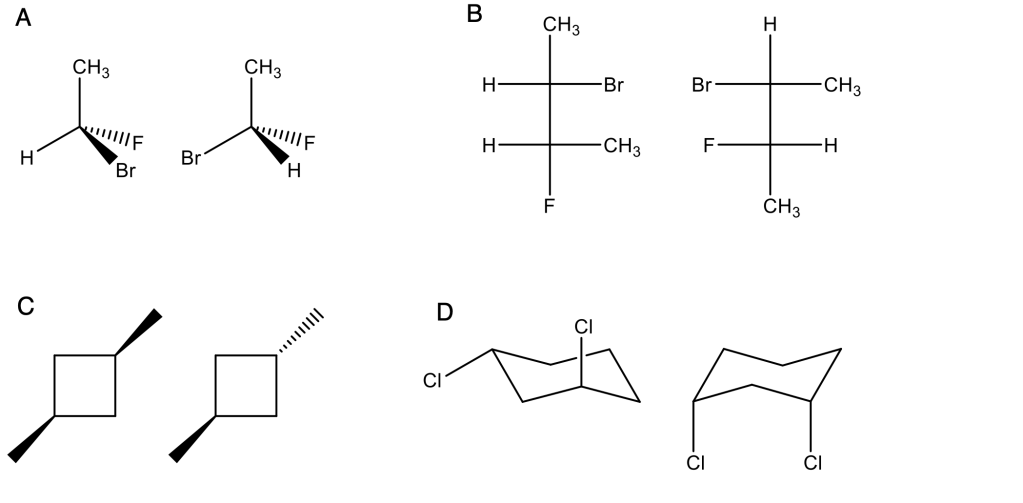
Esercizio n. 2
Assegnare la configurazione assoluta (R/S) ai carboni chirali delle seguenti molecole. Trasformare tutte le strutture in proiezioni di Fischer:
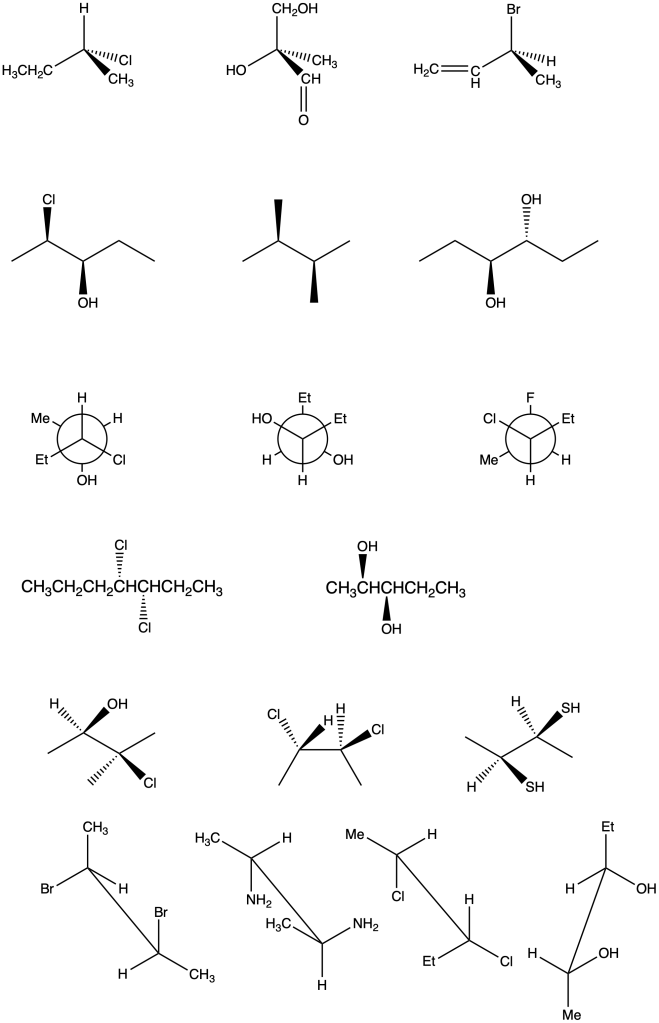
Esercizio n. 3
Attribuire le configurazioni R o S a ciascuno dei seguenti composti. Trasformare le strutture tridimensionali in proiezioni di Fischer
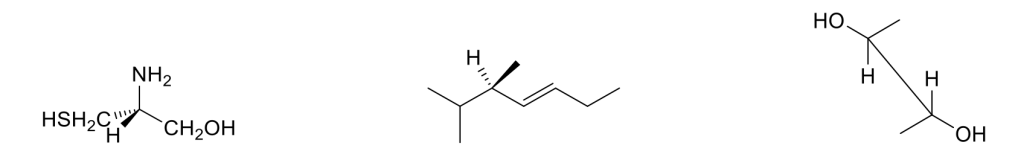
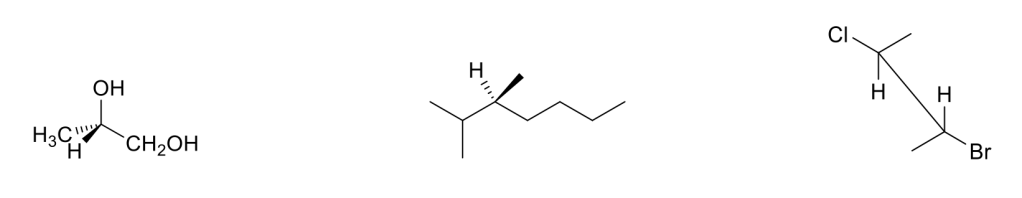
Esercizio n. 4
Scrivete almeno tutti i possibili isomeri (compresi gli stereoisomeri) del diclorociclobutano. Per ognuno di essi scrivere il nome IUPAC indicando se sono otticamente attivi.
Esercizio n. 5
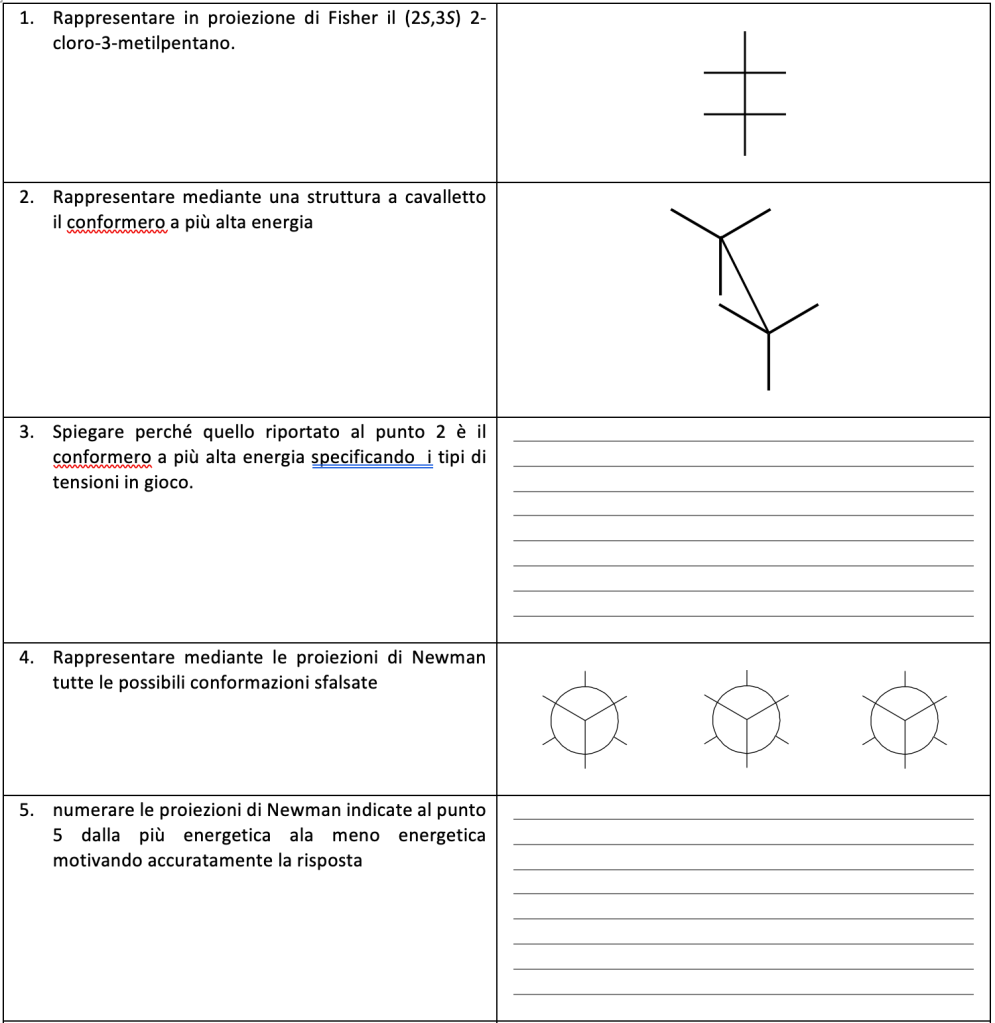
Esercizio n. 6
Per ognuna delle seguenti coppie di strutture indicare se i composti sono (a) identici (b) isomeri costituzionali (c) enantiomeri (d) diastereoisomeri (e) identici e composti meso (f) composti differenti non isomerici
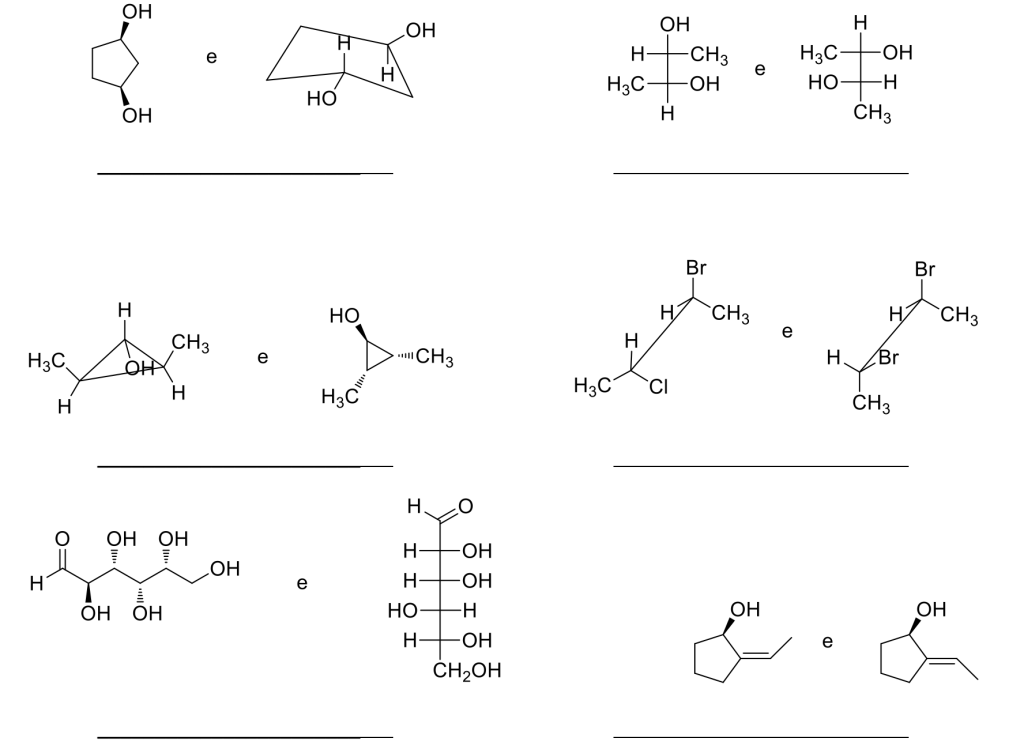
Esercizio n. 7
Rispondere alle seguenti domande relative ad un composto organico di formula bruta C3H4Cl2
Esercizio n. 8
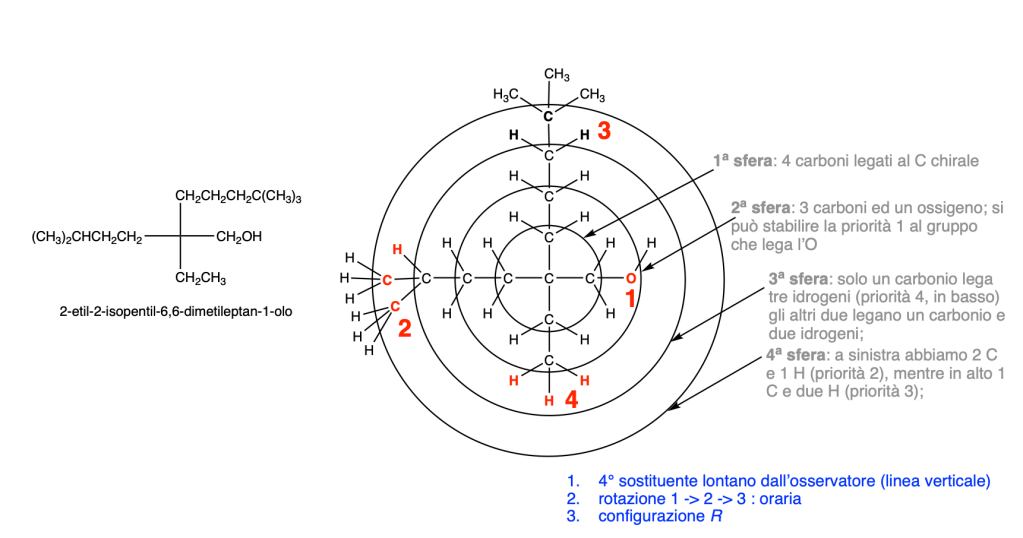
Assegnare il nome IUPAC ai seguenti composti
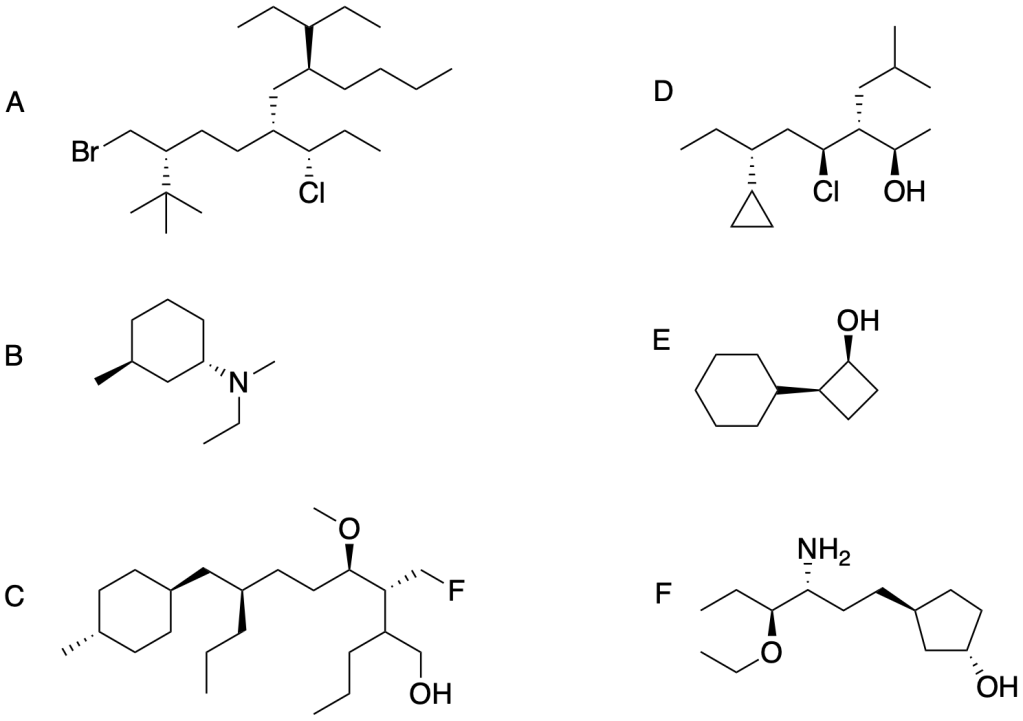
Esercizio n. 9
Assegnare il nome IUPAC (comprensivo si stereochimica) ai seguenti composti
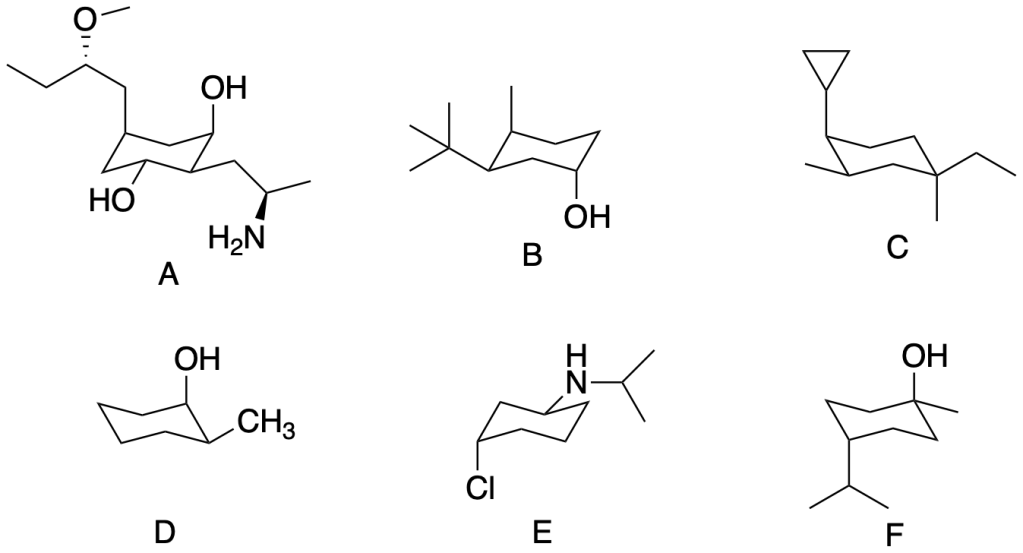

Esercizio n. 1
Indicare la relazione esistente tra le seguenti coppie di composti (identici, enantiomeri o diastereoisomeri)
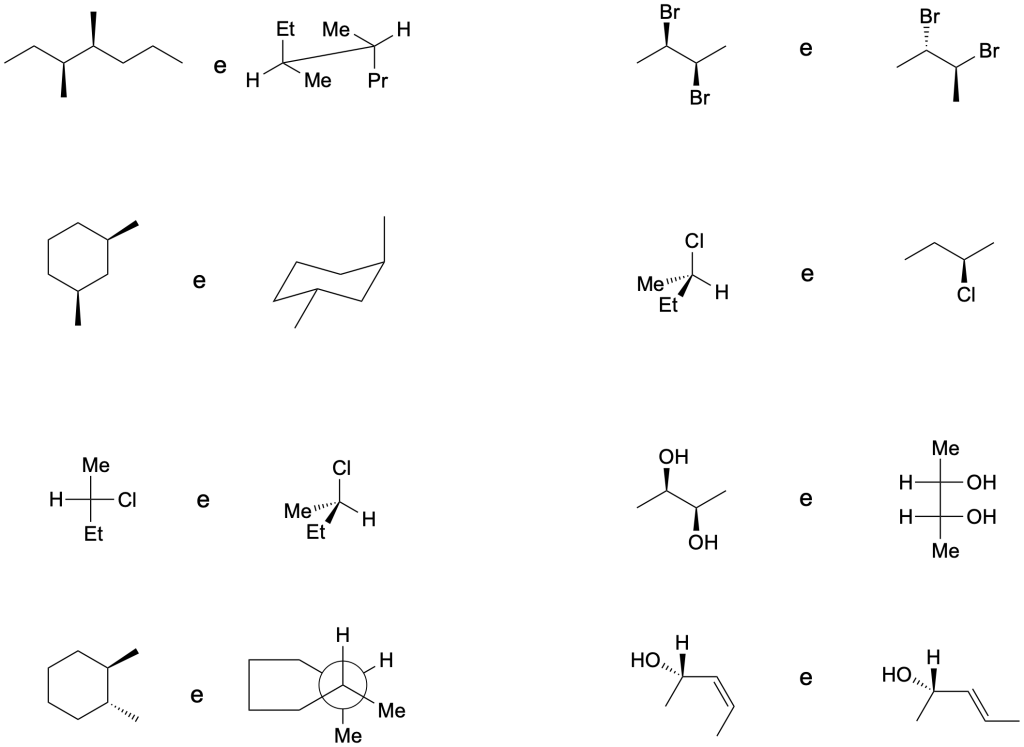
Esercizio n. 2
Qual è il numero massimo di stereoisomeri che è possibile scrivere per i seguent composti?

Esercizio n. 3
Di seguito è riportata la struttura della pravastatina, principio attivo dei farmaci utilizzati per abbassare il livello di colesterolo nel sangue

Esercizio n. 4
Indicare se le seguenti coppie di strutture sono enantiomeri, diastereoisomeri, isomeri strutturali o composti identici.
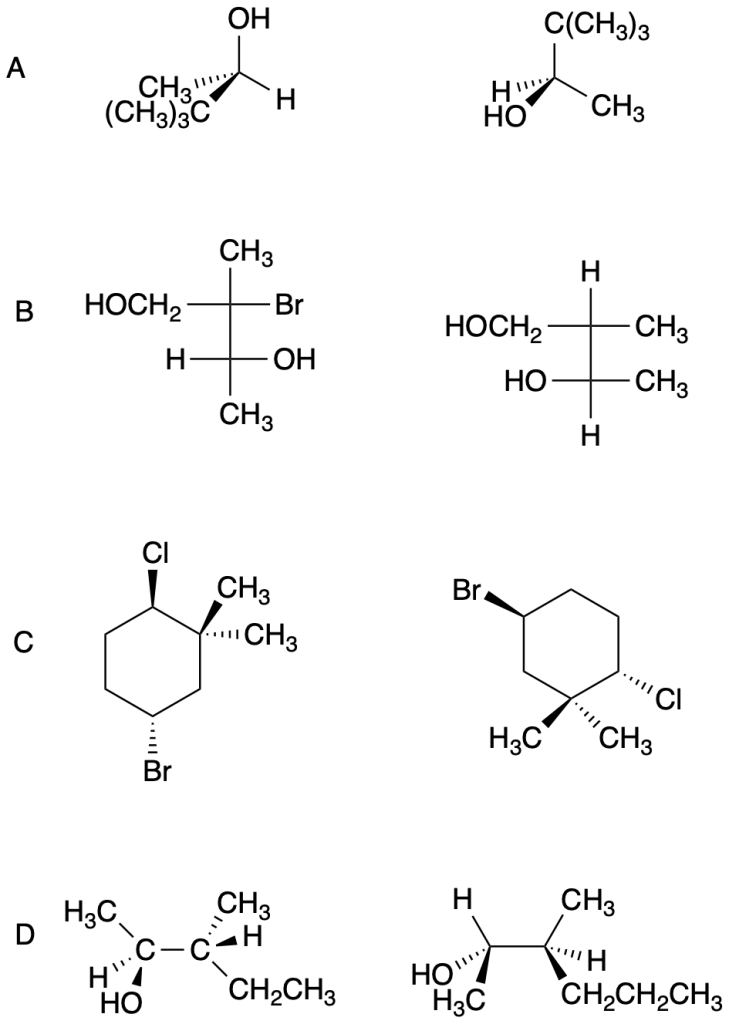
Esercizio n. 5
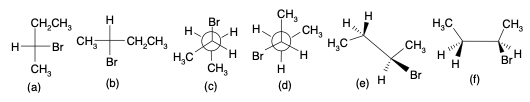
Quale delle seguenti strutture corrisponde al (2R,3S)-2-bromo-3-metilesano?
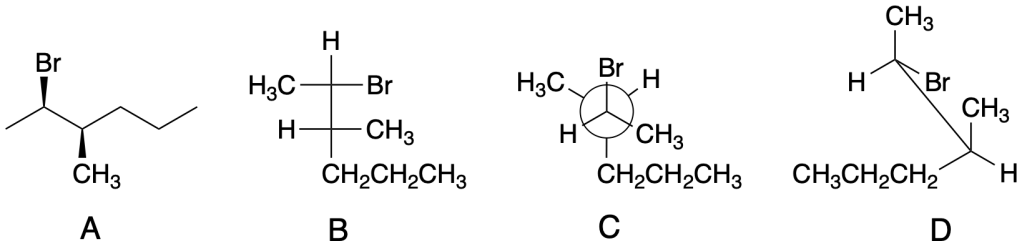
Esercizio n. 6
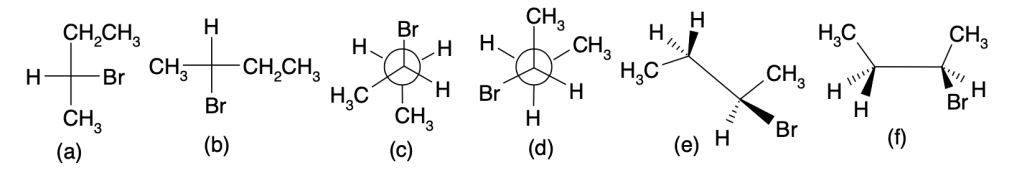
Quale tra le strutture a-d rappresenta l’enantiomero del seguente composto ?

Esercizio n. 7
Quali dei seguenti composti è otticamente attivo? (è possibile scegliere più opzioni)
a) (2R,3S)-2,3-dibromobutano
b) (2R,3S)-2,3-dibromoesano
c) (2R,3R)-2,3-dibromobutano
d) (1S,2S)-1,2-dibromocicloesano
Esercizio n. 8
A quale delle strutture a “cavaletto” A-D corrisponde la struttura prospettica del (2R,3S)-3-bromo-2-butanolo

Esercizio n. 9
Trasformare le seguenti molecole in strutture a cavalletto. Individuare quale di esse è un composto meso

Esercizio n.10
Attribuire le configurazioni R o S a ciascuno dei seguenti composti. Trasformare le strutture tridimensionali in proiezioni di Fisher

Esercizio n. 11
Quali tra i seguenti derivati del cicloesano sono chirali? (Per la determinazione della chiralità, l’anello può essere trattato come se fosse planare).

Esercizio n. 12
Data la proiezione di Fischer scritta a destra, dire se è di serie R o S.

Determinare se le strutture scritte sotto con una simbologia diversa, corrispondono di volta in volta alla struttura inizialmente scritta o al suo enantiomero.
Esercizio n. 13
Identificare le unità stereogeniche dei seguenti composti ed assegnare ad ognuna di esse la configurazione (R/S, E/Z o cis/trans). individuare, inoltre, i composti otticamente inattivi.


Esercizio n. 1
Per ognuna delle seguenti molecole indicare se è chirale o achirale. Nel caso di molecole chiari, indicare il numero di centri chirali

Esercizio n. 2
Classificare le seguenti coppie di strutture come stereoisomeri, conformeri o isomeri strutturali
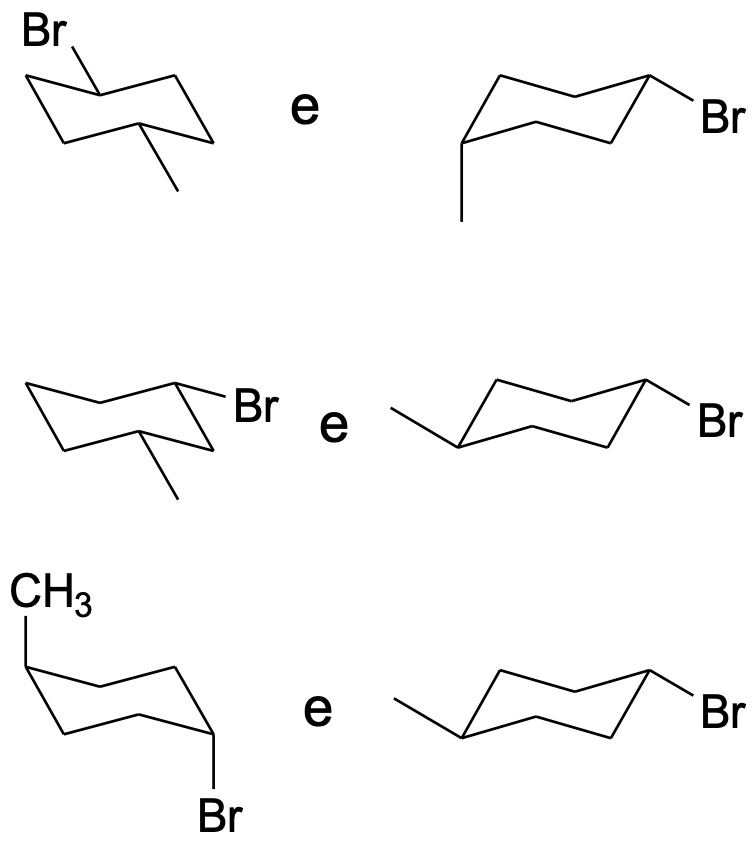
Esercizio n. 3
Per ciascuna delle seguenti coppie di molecole, indicare se i suoi membri sono tr loro identici, isomeri strutturali, conformeri o stereoisomeri.

Attribuire le configurazioni R o S a ciascuno dei seguenti composti. Trasformare le strutture tridimensionali in proiezioni di Fisher.
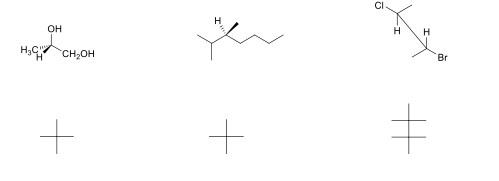
Esercizio n. 4
Assegnare la configurazione assoluta ai carboni chiari evidenziati nelle seguenti strutture tridimensionali

Esercizio n. 5
Assegna la configurazione E/Z ai doppi legami presenti nelle seguenti molecole

Esercizio n. 6
Assegna la configurazione E/Z ai doppi legami dei seguenti composti
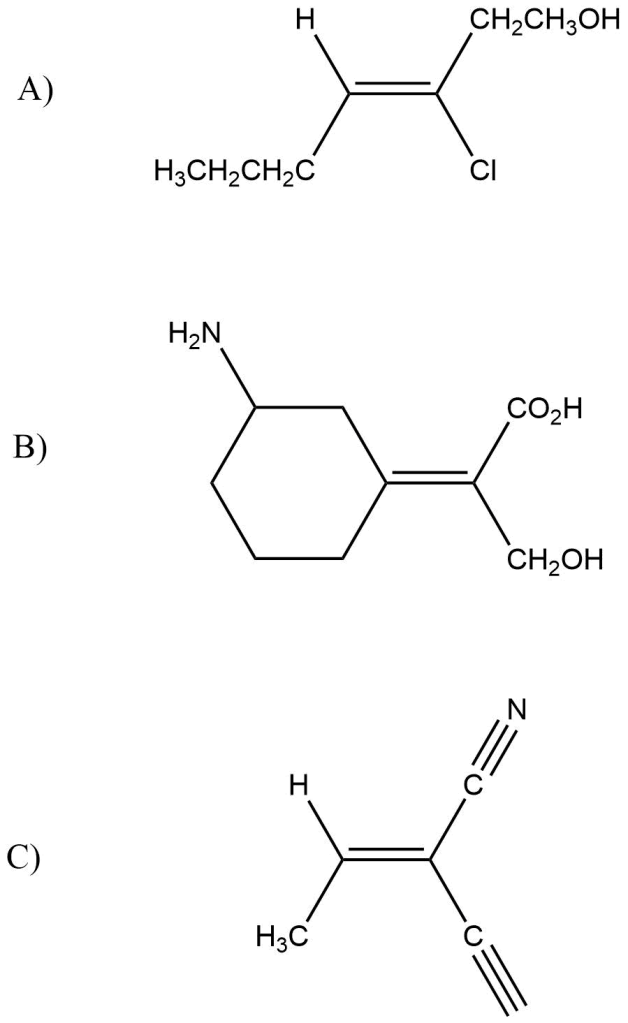

Esercizio n. 1
Per ognuna delle seguenti coppie, indicare se si tratta di stereoisomeri, isomeri strutturali, o dello stesso composto:
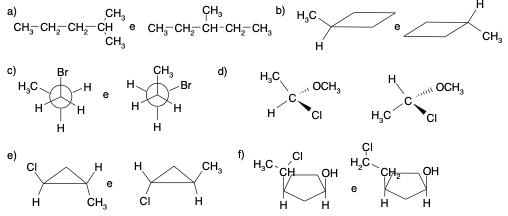
Esercizio n. 2
Per ognuna delle seguenti coppie di strutture dire se sono una coppia di enantiomeri o due rappresentazioni dello stesso composto.
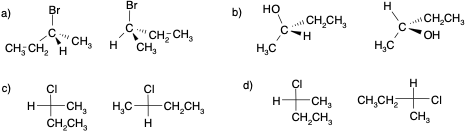
Esercizio n. 3
Indicare con un asterisco gli atomi di carbonio chirali (se ce ne sono) nei seguenti composti:
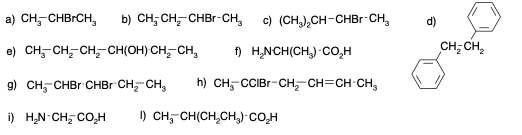
Esercizio n. 4
Quali tra i seguenti composti sono chirali? (indicare gli stereocentri); a) 2-metileptano; b) 3- metileptano; c) 4-metileptano; d) 1,1-dibromopropano; e) 1,3-dibromopropano; f) 1,2- dibromopropano; g) 2,3-dimetilpentano; h) metilcicloesano; i) 1,3-dimetilciclobutano;
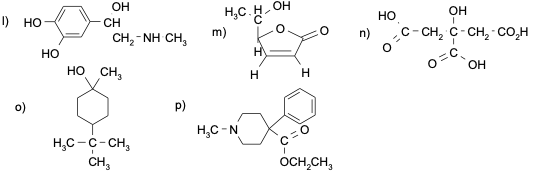
Esercizio n. 5
Alcune delle molecole elencate di seguito sono chirali, altre no. Scrivere le formule tridimensionali e quelle proiettive (Fischer) per gli enantiomeri delle molecole con C chirale, attribuendo a ciascun enantiomero la configurazione, secondo la notazione R,S: a) 1-cloropropano; b)1-bromo-1-cloropropano; c) bromocloroiodometano; d) 1-cloro-2- metilpropano; e) 2-cloro-2-metilpropano; f) 2-cloro-2-metilbutano; g) 2-bromobutano; h) 1-cloropentano; i) 2- cloropentano: l) 3-cloropentano.
Esercizio n. 6
Data la seguente proiezione di Fischer, dire se è di serie R o S.
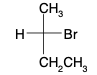
Determinare se le strutture scritte sotto con una simbologia diversa, corrispondono di volta in volta alla struttura inizialmente scritta o al suo enantiomero.
You must be logged in to post a comment.