CdLM Biologia-Chimica Bioorganica

Domani 19 marzo 2026 alle ore 14, in aula B1, si terrà la lezione di recupero relativa alla settimana in corso.
Università degli Studi della Campania "Luigi Vanvitelli"

Domani 19 marzo 2026 alle ore 14, in aula B1, si terrà la lezione di recupero relativa alla settimana in corso.

Esercizio n. 1
Mostrare i reagenti e le condizioni necessarie per effettuare la conversione del cicloesanolo in ciascuno dei seguenti prodotti:

Esercizio n. 2
Partendo dal cicloesanone, mostrare come preparare i composti (a) – (l)
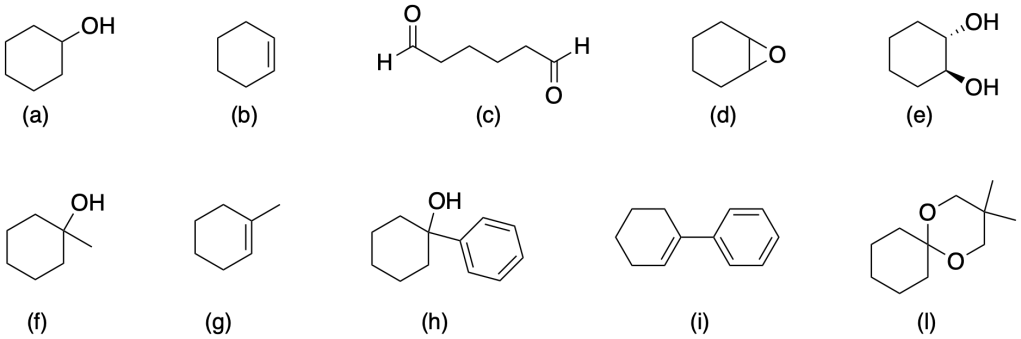
Esercizio n. 3
Mostrare come effettuare le seguenti trasformazioni.
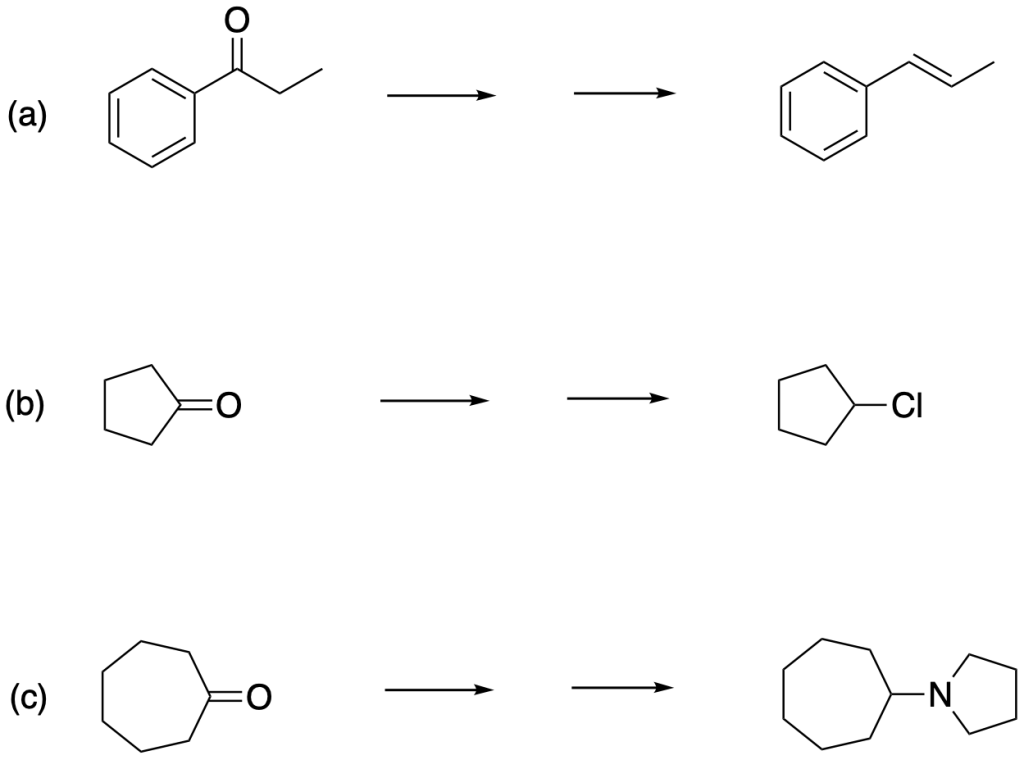
Esercizio n. 4
La procaina è stato uno dei primi anestetici topici ad essere utilizzato per l’anestesia locale tramite infiltrazione. Proporre il meccanismo della procaina partenco dall’acido 4-amminobenzoico, ossido di etilene e dietilammina.
Esercizio n. 5
Nella procaina vi sono due atomi di azoto. Quale dei due ha maggiore carattere casico? Disegnare la struttura del sale che si forma quando la procaina viene trattata con 1 mole di HCl acquoso.
Esercizio n. 6
L’N,N-dietil-m-toluammide (Deet), oil principio attivo di bdiversi comuni repellenti di insetti, può essere sintetizzato dall’acido 3-metilbenzoico e dalla dietilammina. Mostrare come può essere effettuata la sintesi.
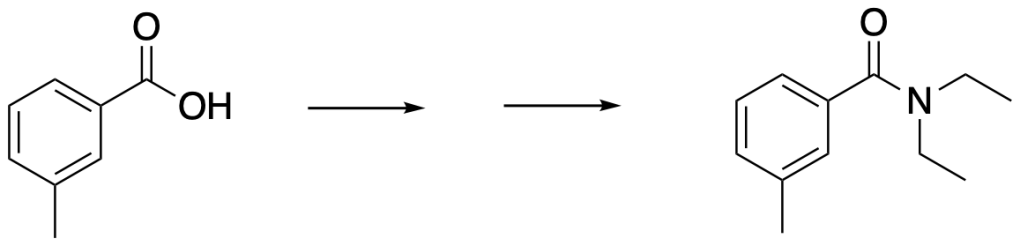
Esercizio n. 7
Assumendo di avere a disposizione solo alcoli o esteri aventi non più di 4 tomi di carbonio, mostrare come si potrebbe sintetizzare ciascuno dei seguenti composti. Scrivere l’analisi retrosintetica di ognuno. In uno stadio della sintesi bisogna utilizzare un reattivo di Grignard. Se necessario sarà possibile utilizzare l’ossirano (1,2-epossietano) o il bromobenzene, per gli altri eventuali composti organici bisogna mostrarne la sintesi a partire da un alcol o da un estere a non più di quattro atomi di carbonio. è possibile usare qualsiasi composto inorganico, compresi agenti ossidanti e riducenti.

Esercizio n. 8
Il seguente alcol trova impiego in profumeria. Scrivere un’analisi retrosintetica e poi le reazioni di sintesi che si potrebbero utilizzare per preparare l’alcol a partire dal bromobenzene e dall’1-butene.
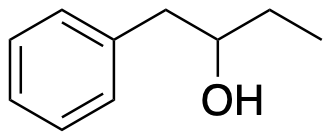
Esercizio n. 9
La struttura del feromone sessuale delle femmine della mosca tse-tse è stata dimostrata dalla seguente sintesi. Il composto C sembra essere identico al feromone naturale da ogni punto di vista, inclusa la risposta del maschio della mosca tse-tse. Fornire le strutture per A, B e C
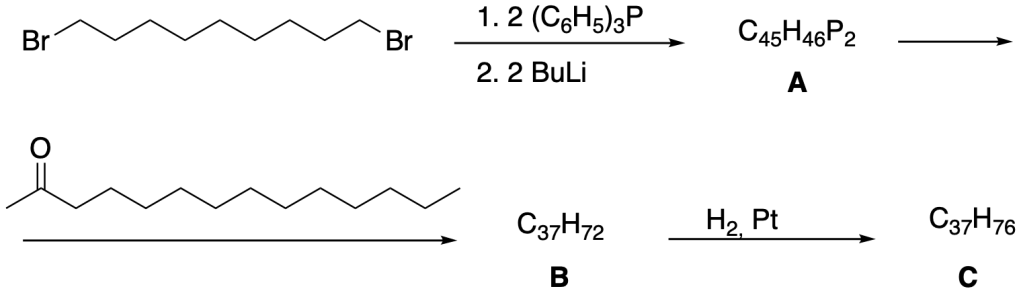

Esercizio n. 1
Sono riportati gli stadi finali della sintesi industriale dell’acetato della vitamina A.

(a) proporre un meccanismo per la ciclizzazione catalizzata da acidi nello stadio 1
(b) indicare i reagenti che permettono la reazione dello stadio 2
(c) proporre un meccanismo pe rla formazione del sale di fosfonio dello stadio 4
(d) indicare i reagenti che permettono la reazione dello stadio 3
(e) mostrare come lo stadio 5 possa essere completato con la reazione di Wittig
Esercizio n. 2
Proporre un meccanismo per la seguente isomerizzazione:
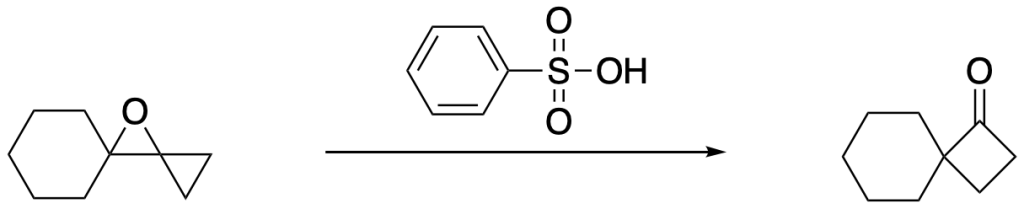
Esercizio n. 3
Sia gli 1,2- sia gli 1,3-dioli possono essere protetti per trattamento con il 2-metossipropene secondo la seguente reazione:

(a) proporre un meccanismo per la formazione di questo diolo protetto
(b) suggerire una procedura sperimentale con cui questo gruppo protettore può essere rimosso per rigenerare l’alcol non protetto.
Esercizio n. 4
Utilizzando l’1-butanolo come unica fonte di carbonio indicare come si può trasformare l’1-butanolo in 4-ottanolo racemico

Esercizio n. 5
Il difepanolo è un sedativo della tosse. Mostrare come si può trasformare l’1-idrossi-1-fenil-2-propanone in difepanolo, utilizzando il bromuro di fenilmagnesio e la piperidina come uniche fonti di atomi di carbonio.
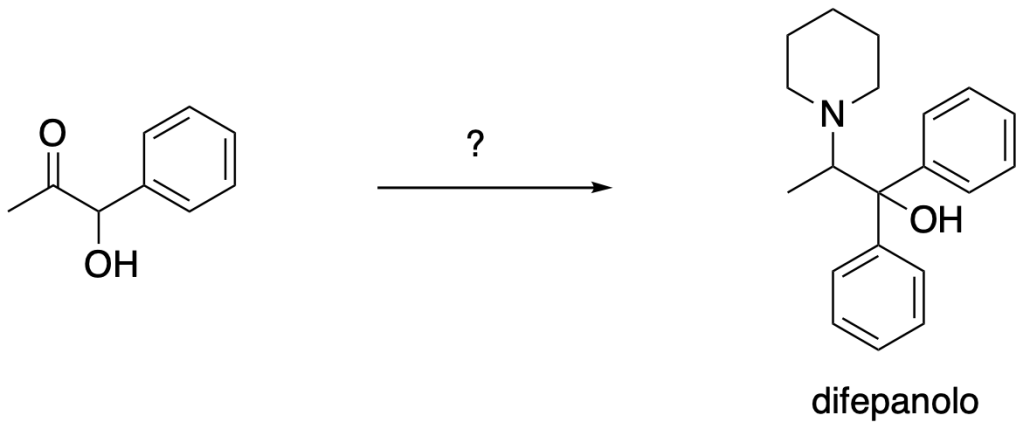
Esercizio n. 6
Quella che segue è l’analisi retrosintetica della dietilcarbamazina, un antielmintico.
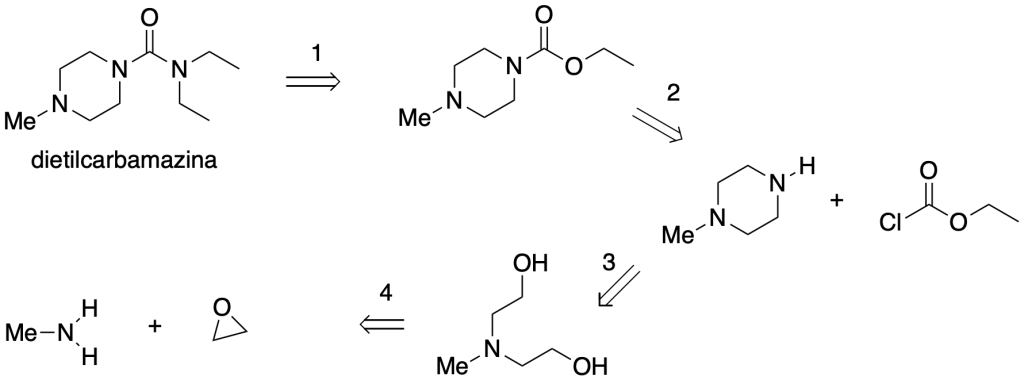
Sulla base di questa analisi retrosintetica, proporre una sintesi della dietilcarbamazina dai quattro precursori indicati

Esercizio n. 1
Quale combinazione di estere e reattivo di Grignard può essere usato per preparare i seguenti composti:
a. 2-metil-2-butanolo
b. 3-fenil-3-pentanolo
c. 1,1-difeniletanolo
Esercizio n. 2
La reazione di un’ammina primaria o secondaria con carbonato dietilico in condizioni controllate genera un estere carbammico. Proporre un meccanismo per la sintesi del seguente composto:
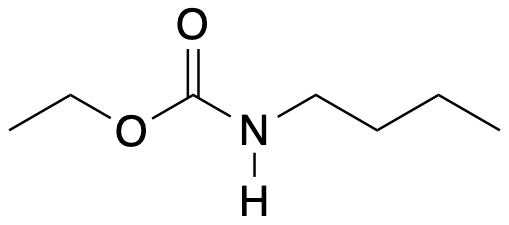
Esercizio n. 3
I barbiturici vengono preparati per trattamento del dietil 2,2-dietilmalonato o di un suo derivato con urea in presenza di etossido di sodio come catalizzatore. Proporre un meccanismo per questa reazione.

Esercizio n. 4
Proporre un meccanismo per la sintesi del fenobarbital

Esercizio n. 5
La sintesi della clorpromazina e metà del secolo scorso e la scoperta della sua attività antipsicotica, aprirono la moderna era dell’applicazione della biochimica alla farmacologia del sistema nervoso centrale. Uno dei composti preparati nella ricerca di antipsicotici più efficaci fu l’amitriptilina.

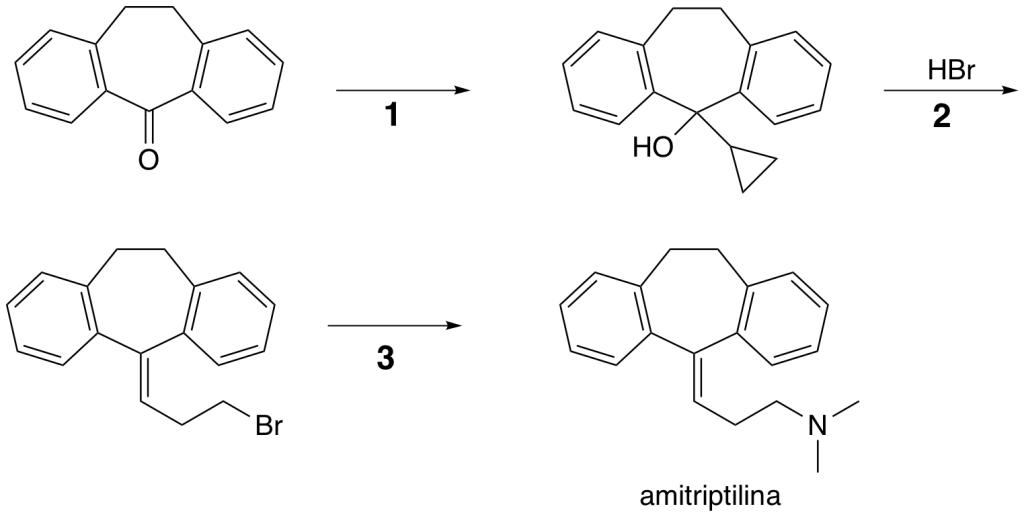
a. indicare i reagenti per lo stadio (1)
b. proporre un meccanismo per lo stadio (2)
c. indicare il reagente dello stadio (3)
Esercizio n. 6
Molti tumori del seno dipendono daghli estrogeni. I farmaci che interferiscono con gli estrogeni hanno attività antitumorale e possono anche aiutare a prevenire l’instaurarsi dei tumori. Un antiestrogeno ampiamente usato è il tamoxifene.

a. quanti stereoisomeri sono possibili per il tamoxifene?
b. specificare la configurazione di quello mostrato
c. ipotizzare un meccanismo per la sintesi indicata sopra

Esercizio n. 1
Mostrare come può essere sintetizzata la benzaldeide (benzencarbaldeide) da ciascuno dei seguenti reagenti:
a) alcol benzilico
b) feniletino
c) benzoato di metile (benzencarbossilato di metile)
d) stirene (feniletene)
e) acido benzoico
f) benzonitrile (benzencarbonitrile)
Esercizio n. 2
Il riscaldamento del piperonale con HCl diluito acquoso lo converte in un composto di formula C7H6O3. Qual è questo composto e che tipo di reazione è coinvolta? Mostrare il meccanismo.

Esercizio n. 3
Fornire una struttura per i composti A–D
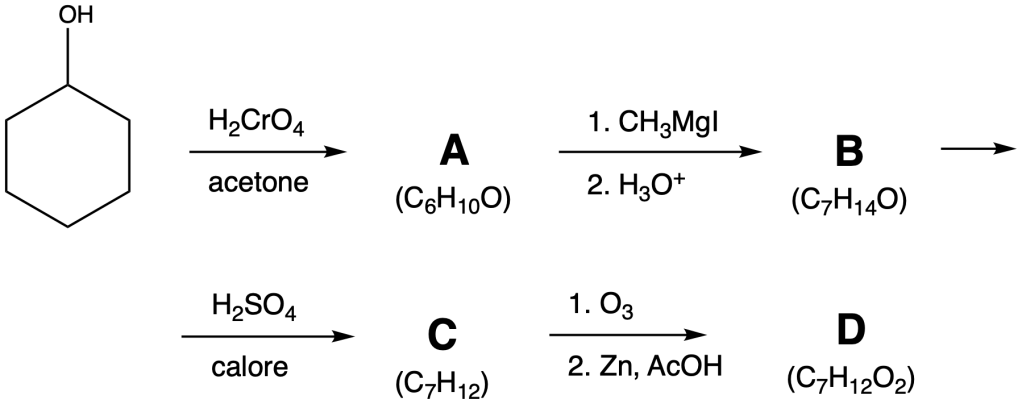
Esercizio n. 4
Partendo dal bromuro di benzile, mostrare come si potrebbe sintetizzare ciascuno dei seguenti composti:

Esercizio n. 5
In ciascuna selle seguenti disconnessioni retrosintetiche, mostrare le reazioni che servono a formare i legami C-C indicati.

Esercizio n. 6
Proporre una sequenza sintetica per convertire l’acido carbossilico A nel sesquiterpene di origine naturale alfa-curcumene
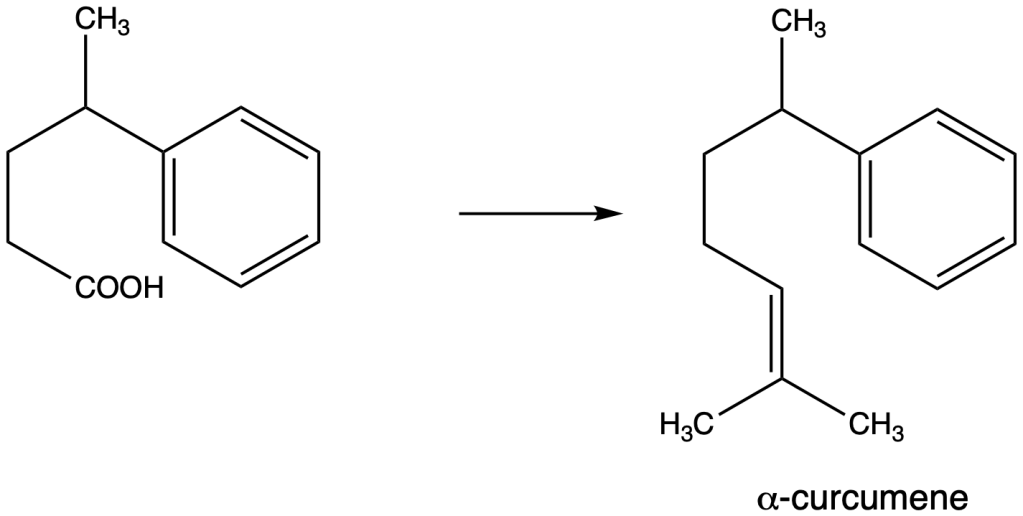
Esercizio n. 7
Proporre una sintesi del beta-selinene, un membro di una famiglia molto comune di sesquiterpeni, partendo dall’alcol mostrato in basso. Nella sintesi, impiegare un nitrile. Usare un modello melecolare per ottenere la stereochimica sediserata. Il gruppo 1-metiletilene è assiale o equatoriale?


Esercizio n. 1
Assegna il nome IUPAC ai seguenti composti

Esercizio 2
Assegnare il nome IUPAC ai seguenti composti:
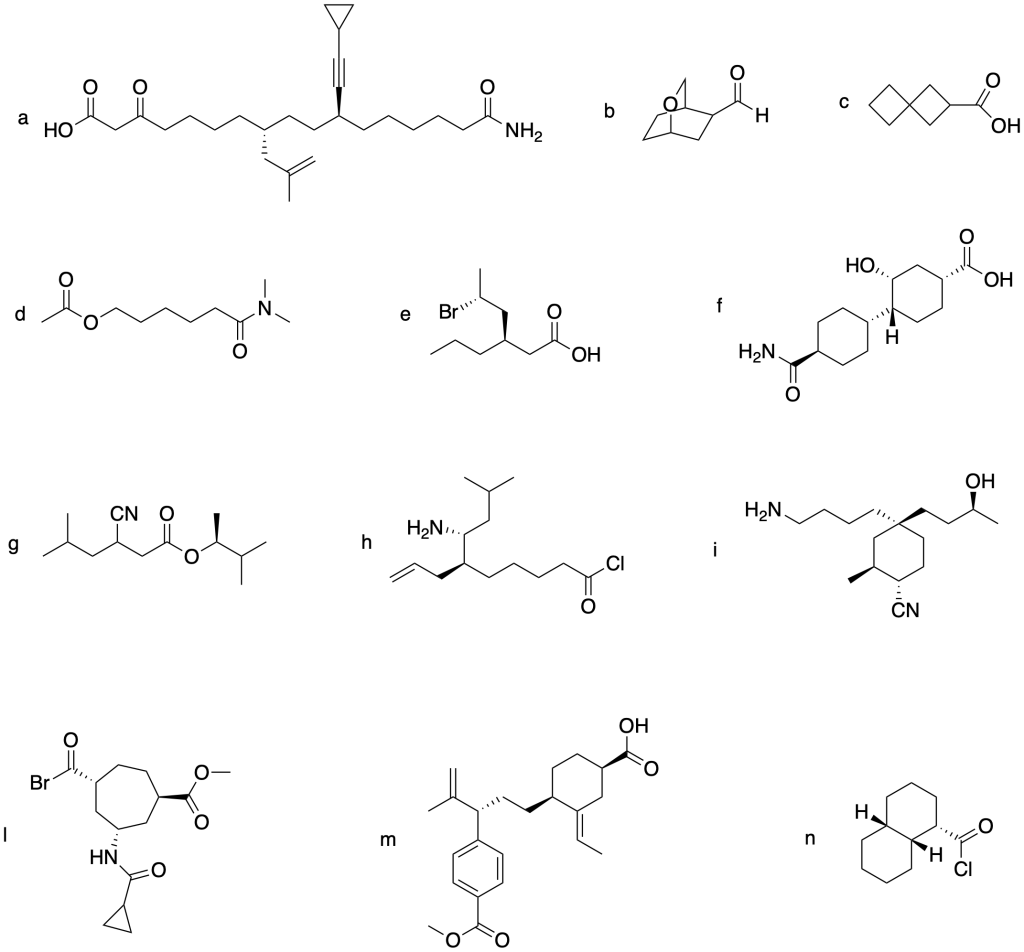
Esercizio n. 3
Assegnare il nome IUPAC ai seguenti composti


Esercizio n. 1
Completare le seguenti trasformazioni ipotizzando uno o più passaggi:

Esercizio n. 2
Quali tra le seguenti trasformazioni non produrranno butanammide?
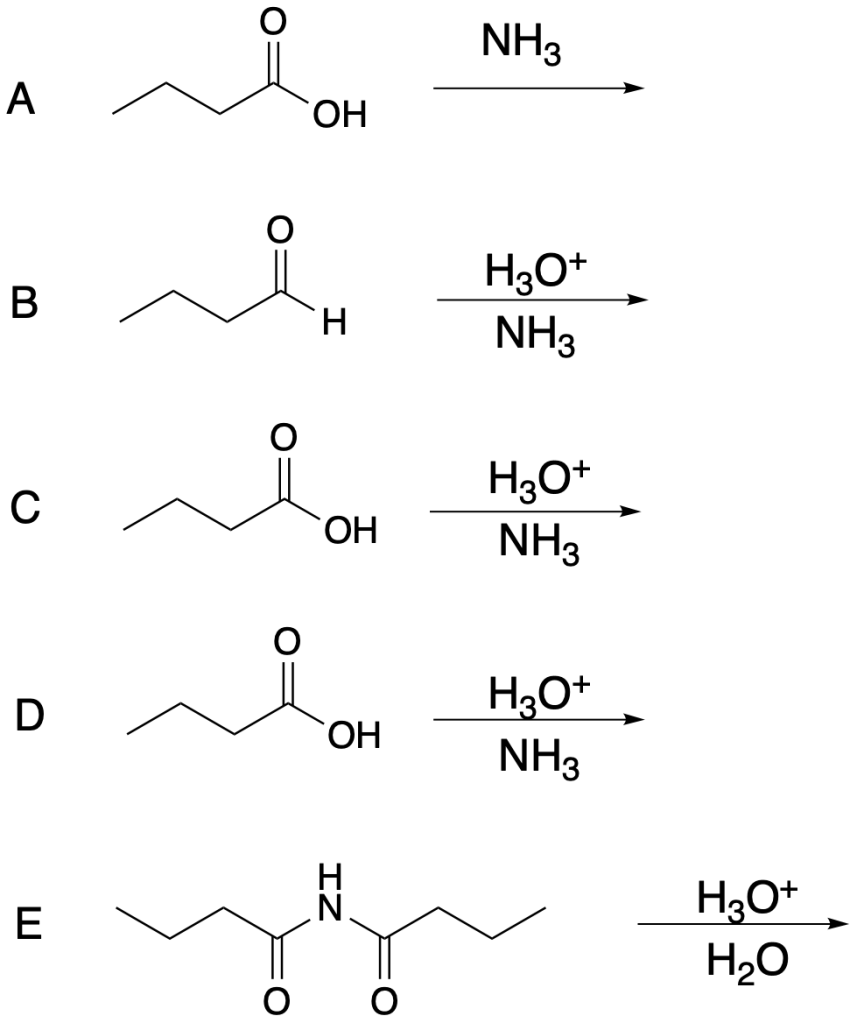
Esercizio n. 3
Proporre un meccanismo per la seguente trasformazione

Esercizio n. 4
I feromoni sono composti organici importanti in agricoltura, in quanto rappresentano uno dei mezzi per attrarre e intrappolare gli insetti che potrebbero essere dannosi per i raccolti. L’oleano, il feromone sessuale per la mosca dell’ulivo, Dacus oleae, può essere sintetizzato dall’etere idrossienolico mostrato mediante trattamento di quest’ultimo con un acido.
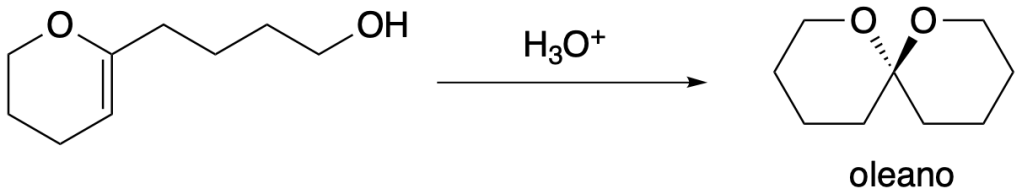

Esercizio n. 1
L’isoniazide, un farmaco usato per curare la tubercolosi, viene preparata dall’acido 4-piridin carbossilico. Come potrebbe essere effettuata la sintesi?

Esercizio n. 2
Suggerire come trasformare il fenilacetilene in fenilacetato di allile
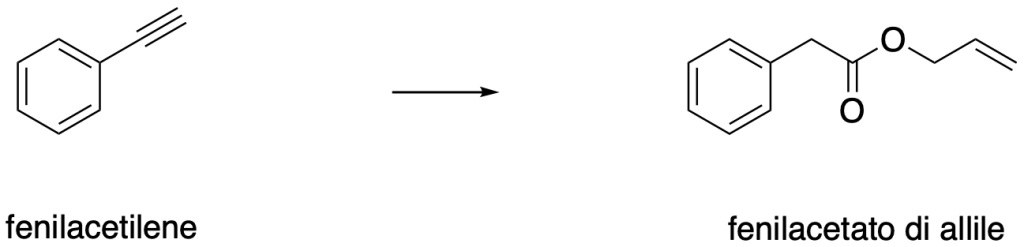
Esercizio n. 3
La reazione di un cicloesene trisostituito con bromo per formare un bromolattone è uno dei passaggi nella sintesi della PGE1 (prostaglandina E1, alprostadil). Proporre un meccanismo per la formazione di questo bromolattone e giustificare la stereochimica osservata per ciascun sostituente sull’anello cicloesanico.

Esercizio n. 4
I barbiturici sono preparati mediante una reazione di un derivato del dietilmalonato con urea in presenza di etossido di sodio come catalizzatore. Viene mostrata qui di seguito un’equazione per la preparazione del barbitale, un ipnotico e sedativo di lunga durata, partendo ad dietilmalonato dietilico e urea. Proporre un meccanismo per questa reazione.

Esercizio n. 5
Il seguente composto appartiene alla famiglia delle β-clorammine, molte delle quali hanno attività antitumorale. Descrivere una sintesi di questo composto da acido antranilico e ossido di etilene.


Esercizio n. 1
Suggerire gli opportuni reagenti necessari per convertire ciascuno dei seguenti materiali di partenza nel prodotto indicato:
a) cloruro di acetile in anidride acetica esanoica
b) esanoato di metile in N-metilesanammide
c) cloruro di esanoile in esanale
d) esanonitrile in acido esanoico
e) esanammide in esanammina
f) esanoato di etile in 3-etil-3-ottanolo
g) esanonitrile in 1-fenil-1-esanone
Esercizio n. 2
Indicare il prodotto di ciascuna delle seguenti reazioni:

Esercizio n. 3
Scrivere la reazione del pentanoato di etile con ciascuno dei seguenti reagenti nelle condizioni indicate:
a) NaOH, H2O, calore; poi H3O+, H2O
b) (CH3)2CHCH2CH2OH (eccesso), H3O+
c) (CH3CH2)2NH, calore
d) CH3MgI (eccesso), Et2O; poi H3O+, H2O
e) LiAlH4 (eccesso), Et2O; poi H3O+, H2O
f) DIBAL, toluene, -78°C; poi H3O+, H2O
Esercizio n. 4
Scrivere la reazione del γ-valerolattone con ciascuno dei reagenti dell’esercizio n. 3
Esercizio n.5
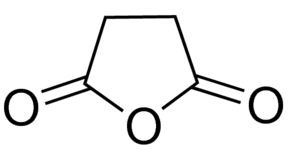
Scrivere il prodotto (o i prodotti) della reazione dell’anidride butandioica (anidride succinica) con i seguenti reagenti:
a) 2-propanolo
b) ammoniaca
c) bromuro di fenilmagnesio in THF; poi H3O+, H2O
d) LiAlH4 in etere etilico; poi H3O+, H2O
Esercizio n.6
Illustrare una sintesi per i seguenti acidi carbossilici. Quale tra essi potrebbe essere sintetizzato alternativamente via Grignard (reattivo di Grignard + CO2) e via nitrili?
a) acido fenilacetico
b) acido 3-butenoico
c) acido esanoico
d) acido 2,2-dimetilpentanoico
e) acido 4-metilbenzoico
Esercizio n. 7
Quale sintesi, via Grignard o via nitrile, potrebbe essere utile per sintetizzare l’acido 5-idrossipentanoico a partire dal 4-bromo-1-butanolo? Perchè?
Esercizio n. 8
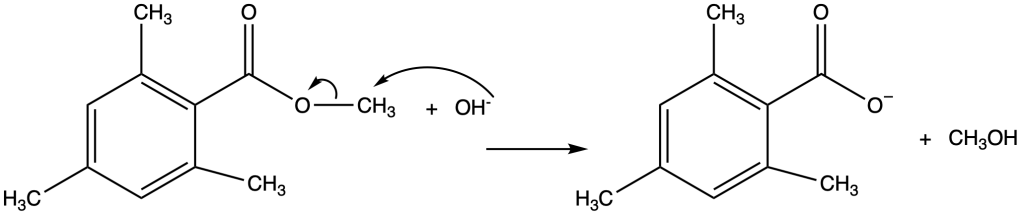
L’idrolisi basica del mesitoato di metile ha luogo attraverso un attacco promosso dallomione alcossido a livello del carbonio alcolico anzicchè acilico. Quale potrebbe essere una motivazione che giustifichi questo comportamento inusuale?
You must be logged in to post a comment.