Riconoscimento degli zuccheri riducenti con il saggio di Fehling

Determinazione qualitativa degli zuccheri riducenti e non riducenti.
Esclusivamente per questa esperienza di laboratorio i turni saranno 2:

Università degli Studi della Campania "Luigi Vanvitelli"

Determinazione qualitativa degli zuccheri riducenti e non riducenti.
Esclusivamente per questa esperienza di laboratorio i turni saranno 2:


Mercoledì 5 aprile tutti i gruppi devono completare l’esperienza della condensazione aldolica con la misura del peso del prodotto della reazione,
Gli studenti del 1 TURNO sono convocati alle 14,30
Gli studenti del 2 TURNO sono convocati alle 15,00
Gli studenti del 3 TURNO sono convocati alle 15,30

Di seguito sono riportati i risultati della SESTA prova intercorso (nella colonna 6 l’esito della prova).
Gli studenti identificati con il colore verde nella colonna “MATR” hanno superato la prova con sufficienza (verde scuro, voti più alti).
Gli studenti identificati dal colore giallo/arancione hanno superato con riserva (arancione, voti più bassi)


Esercizio n. 1
Quale combinazione di estere e reattivo di Grignard può essere usato per preparare i seguenti composti:
a. 2-metil-2-butanolo
b. 3-fenil-3-pentanolo
c. 1,1-difeniletanolo
Esercizio n. 2
La reazione di un’ammina primaria o secondaria con carbonato dietilico in condizioni controllate genera un estere carbammico. Proporre un meccanismo per la sintesi del seguente composto:
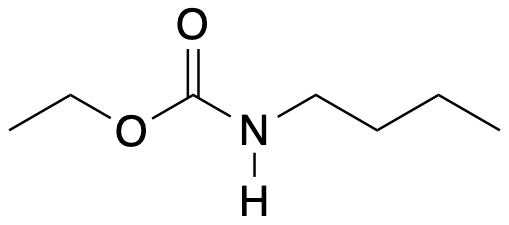
Esercizio n. 3
I barbiturici vengono preparati per trattamento del dietil 2,2-dietilmalonato o di un suo derivato con urea in presenza di etossido di sodio come catalizzatore. Proporre un meccanismo per questa reazione.

Esercizio n. 4
Proporre un meccanismo per la sintesi del fenobarbital

Esercizio n. 5
La sintesi della clorpromazina e metà del secolo scorso e la scoperta della sua attività antipsicotica, aprirono la moderna era dell’applicazione della biochimica alla farmacologia del sistema nervoso centrale. Uno dei composti preparati nella ricerca di antipsicotici più efficaci fu l’amitriptilina.

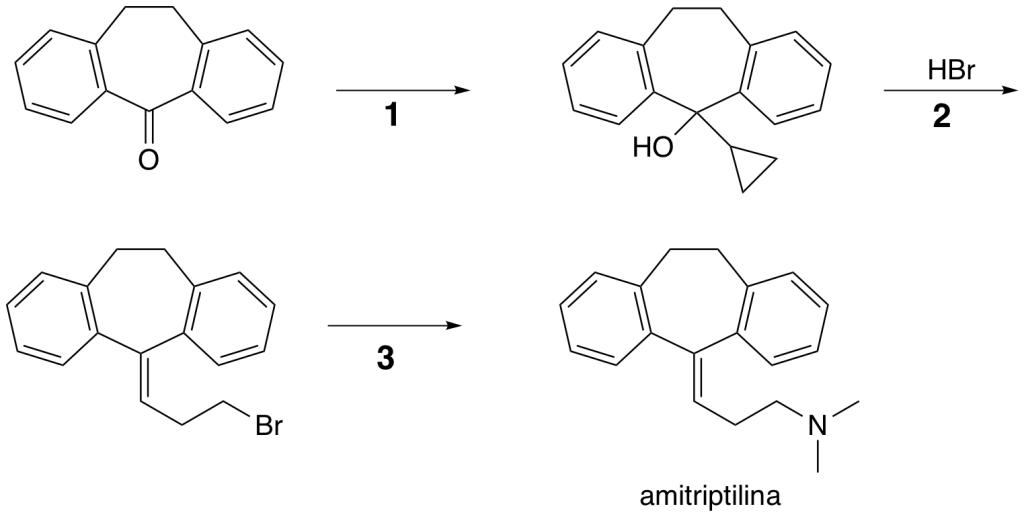
a. indicare i reagenti per lo stadio (1)
b. proporre un meccanismo per lo stadio (2)
c. indicare il reagente dello stadio (3)
Esercizio n. 6
Molti tumori del seno dipendono daghli estrogeni. I farmaci che interferiscono con gli estrogeni hanno attività antitumorale e possono anche aiutare a prevenire l’instaurarsi dei tumori. Un antiestrogeno ampiamente usato è il tamoxifene.

a. quanti stereoisomeri sono possibili per il tamoxifene?
b. specificare la configurazione di quello mostrato
c. ipotizzare un meccanismo per la sintesi indicata sopra

Esercizio n. 1
Mostrare come può essere sintetizzata la benzaldeide (benzencarbaldeide) da ciascuno dei seguenti reagenti:
a) alcol benzilico
b) feniletino
c) benzoato di metile (benzencarbossilato di metile)
d) stirene (feniletene)
e) acido benzoico
f) benzonitrile (benzencarbonitrile)
Esercizio n. 2
Il riscaldamento del piperonale con HCl diluito acquoso lo converte in un composto di formula C7H6O3. Qual è questo composto e che tipo di reazione è coinvolta? Mostrare il meccanismo.

Esercizio n. 3
Fornire una struttura per i composti A–D
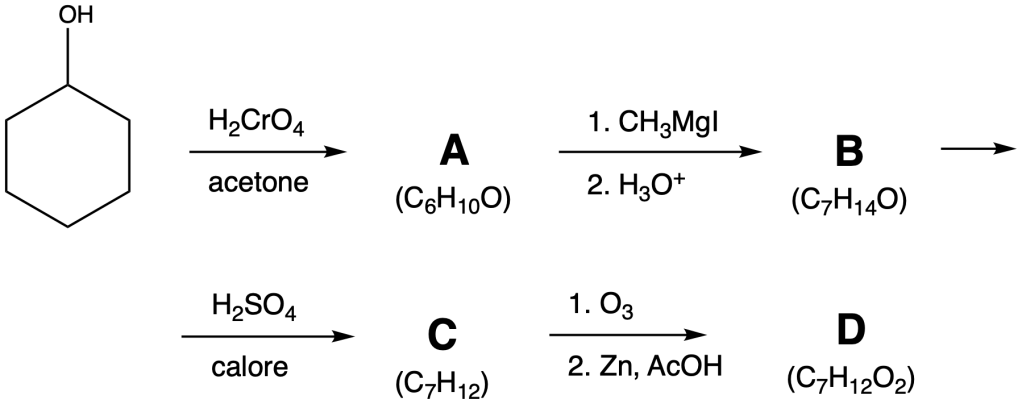
Esercizio n. 4
Partendo dal bromuro di benzile, mostrare come si potrebbe sintetizzare ciascuno dei seguenti composti:

Esercizio n. 5
Completare le seguenti reazioni


Esercizio n. 6
Preparare con la reazione di Wittig i seguenti composti:


Esercizio n. 1
Suggerire gli opportuni reagenti necessari per convertire ciascuno dei seguenti materiali di partenza nel prodotto indicato:
a) cloruro di acetile in anidride acetica esanoica
b) esanoato di metile in N-metilesanammide
c) cloruro di esanoile in esanale
d) esanonitrile in acido esanoico
e) esanammide in esanammina
f) esanoato di etile in 3-etil-3-ottanolo
g) esanonitrile in 1-fenil-1-esanone
Esercizio n. 2
Indicare il prodotto di ciascuna delle seguenti reazioni:

Esercizio n. 3
Scrivere la reazione del pentanoato di etile con ciascuno dei seguenti reagenti nelle condizioni indicate:
a) NaOH, H2O, calore; poi H3O+, H2O
b) (CH3)2CHCH2CH2OH (eccesso), H3O+
c) (CH3CH2)2NH, calore
d) CH3MgI (eccesso), Et2O; poi H3O+, H2O
e) LiAlH4 (eccesso), Et2O; poi H3O+, H2O
f) DIBAL, toluene, -78°C; poi H3O+, H2O
Esercizio n. 4
Scrivere la reazione del γ-valerolattone con ciascuno dei reagenti dell’esercizio n. 3
Esercizio n.5
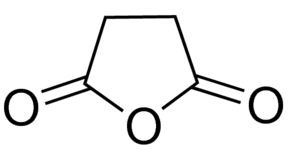
Scrivere il prodotto (o i prodotti) della reazione dell’anidride butandioica (anidride succinica) con i seguenti reagenti:
a) 2-propanolo
b) ammoniaca
c) bromuro di fenilmagnesio in THF; poi H3O+, H2O
d) LiAlH4 in etere etilico; poi H3O+, H2O
Esercizio n.6
Illustrare una sintesi per i seguenti acidi carbossilici. Quale tra essi potrebbe essere sintetizzato alternativamente via Grignard (reattivo di Grignard + CO2) e via nitrili?
a) acido fenilacetico
b) acido 3-butenoico
c) acido esanoico
d) acido 2,2-dimetilpentanoico
e) acido 4-metilbenzoico
Esercizio n. 7
Quale sintesi, via Grignard o via nitrile, potrebbe essere utile per sintetizzare l’acido 5-idrossipentanoico a partire dal 4-bromo-1-butanolo? Perchè?
Esercizio n. 8
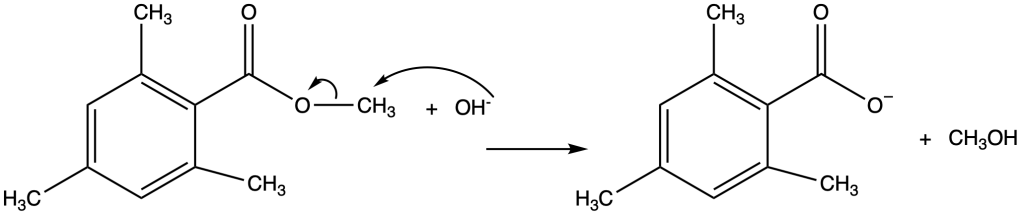
L’idrolisi basica del mesitoato di metile ha luogo attraverso un attacco promosso dallomione alcossido a livello del carbonio alcolico anzicchè acilico. Quale potrebbe essere una motivazione che giustifichi questo comportamento inusuale?

Calendario delle esercitazioni di Laboratorio di Chimica Organica – II semestre:
| I TURNO | II TURNO | III TURNO |
| 15 marzo | 22 marzo | 29 marzo |
| 5 aprile | 12 aprile | 19 aprile |
| 26 aprile | 3 maggio | 10 maggio |
| 17 maggio | 24 maggio | 31 maggio |
Turni Laboratorio II semestre


Di seguito sono riportati i risultati della prova intercorso di recupero.
Gli studenti identificati con il colore verde hanno superato la prova con sufficienza (verde scuro, voti più alti).
Gli studenti identificati dal colore arancione hanno superato con riserva


Ammessi alle prove del secondo semestre
Di seguito sono riportati i risultati della quinta prova intercorso.
Gli studenti identificati con il colore verde nella colonna “MEDIA” hanno superato la prova con sufficienza (verde scuro, voti più alti).
Gli studenti identificati dal colore giallo/arancione hanno superato con riserva (arancione, voti più bassi)
Nelle colonne 1, 2 , 3, 4 e 5, i colori indicano, rispettivamente, i risultati della prima, della seconda, della terza, della quarta e della quinta prova intercorso
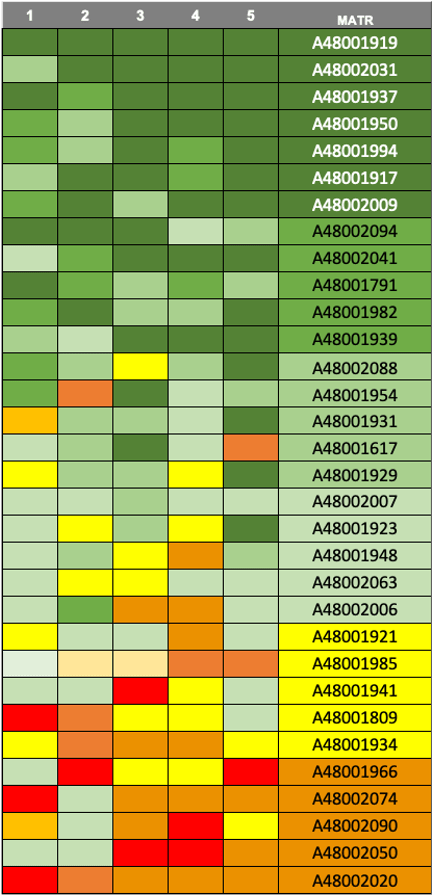
Gli studenti non presenti nell’elenco possono sostenere la prova di recupero su tutti gli argomenti del primo semestre il giorno 22 febbraio

TUTORIAL REAZIONI
REAZIONI DEGLI ALCHENI


Esercizio n. 1
Disegnare un diagramma per una reazione che avviene con i seguenti criteri:
Indicare nel grafico reagenti (R) e prodotti (P), i tre stati di transizione (ST1, ST2, ST3) i due intermedi (I1 e I2); illustrare, inoltre, il DG° dell’intera reazione e i DG‡ dei tre stadi.
Esercizio n. 2
Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica

Esercizio n. 3
Completare il seguente schema inserendo le condizioni di reazioni o i prodotti mancanti. Evidenziare la stereochimica

Esercizio n. 4
Mostrare il meccanismo della seguente trasformazione

Esercizio n. 5
Partendo dall’opportuno stereoisomero del 3-metil-2-pentene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica

Esercizio n. 6
Il prodotto principale della reazione di idratazione del seguente composto è diverso rispetto al prodotto principale della reazione di ossimercuriazione/riduzione. Mostrare il meccanismo delle due reazioni, mettendo in evidenza i fattori che determinano la formazione di due prodotti diversi.
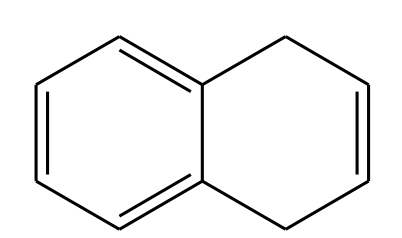
Esercizio n. 7
Scrivere i prodotti principali delle seguenti reazioni.
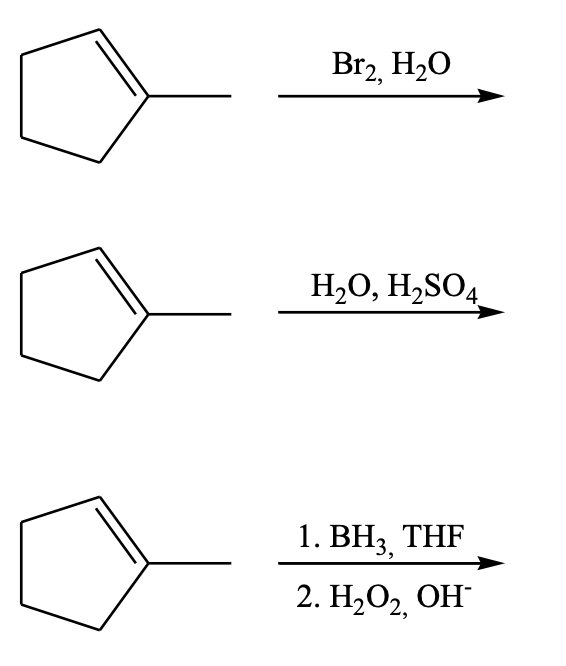
Esercizio n. 8
Quale, tra i seguenti prodotti A-D, si può ottenere dalla reazione dell’ (E)-3-metil-2-pentene con bromo in acqua?

Esercizio n. 9
Proporre la sintesi del (2S,3S)-2,3-epossipentano e del suo enantiomero a partire dall’etino. Utilizzare un approccio retrosintetico
Esercizio n. 10
A partire da uni dei composti riportati nel riquadro e utilizzando qualsiasi altro reagente necessario, suggerire la sintesi di ciascuno dei prodotti A-I, indicando sulle frecce le condizioni di reazione


Esercizio n. 11
Ipotizzare un meccanismo che spieghi la seguente trasformazione

Esercizio n. 12
Proponi un meccanismo per ciascuna delle seguenti reazioni:

Esercizio n. 13
Ognuno dei seguenti alcheni viene trattato prima con diborano in tetraidrofurano (THF) a formare un trialchilborano e quindi con perossido di idrogeno in idrossido di sodio acquoso. Disegna la formula di struttura dell’alcol che si forma. Nel caso, specifica la stereochimica.

You must be logged in to post a comment.