Caratterizzazione del dibenzalacetone sintetizzato

analisi del grado di purezza mediante TLC, misurazione del punto di fusione e calcolo del coefficiente di estinzione molare del dibenzalacetone sintetizzato nell’esperienza precedente.
Università degli Studi della Campania "Luigi Vanvitelli"

analisi del grado di purezza mediante TLC, misurazione del punto di fusione e calcolo del coefficiente di estinzione molare del dibenzalacetone sintetizzato nell’esperienza precedente.

Esercizio n. 1
Proporre la sintesi del 4-fenil-2-butanone a partire dall’estere acetoacetico e dalla benzaldeide.
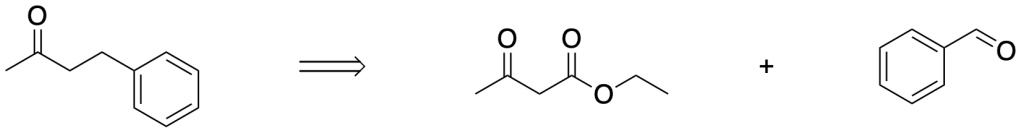
Esercizio n. 2
L’anticoagulante warfarina (coumadin) viene sintetizzato a partire da 4-idrossicumarina, benzaldeide e acetone. Mostrare come effettuare la sintesi.
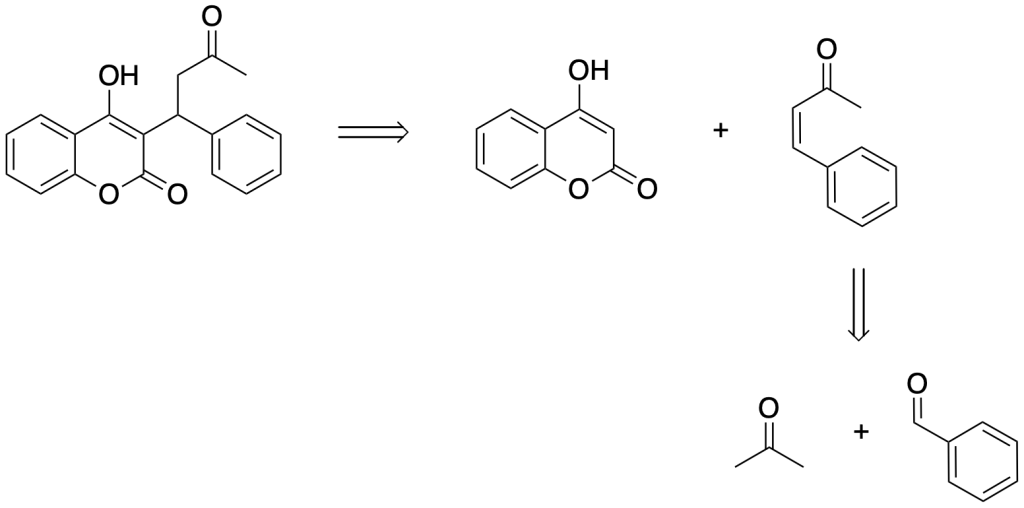
Esercizio n. 3
L’ossanammide è un blando sedativo appartenente a una classe di molecole chiamate ossanammidi. Proporre una sintesi di questo composto partendo dal solo butanale.
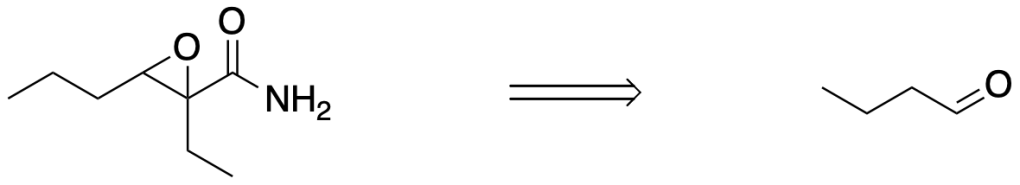
Esercizio n. 4
Il 3,5,5-trimetil-2-cicloesenone può essere preparato usando acetone e acetato di etile come fonti di atomi di carbonio. IN questa sintesi i nuovi legami carbonio-carbonio si formano per combinazione di reazioni aldolica, di Claisen e di Michael. Mostrare la sintesi di questo composto.
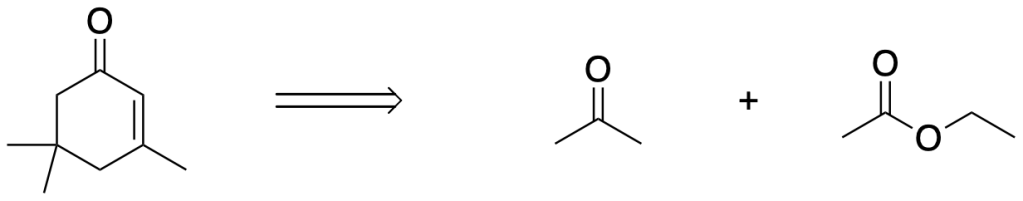
Esercizio n. 5
Facendo uso delle reazioni dei carbonio in alpha, suggerire i materiali di partenza A-L necessari per preparare ciascuna delle strutture che seguono (1-6). Mostrare il meccanismo di ciascuna reazione.
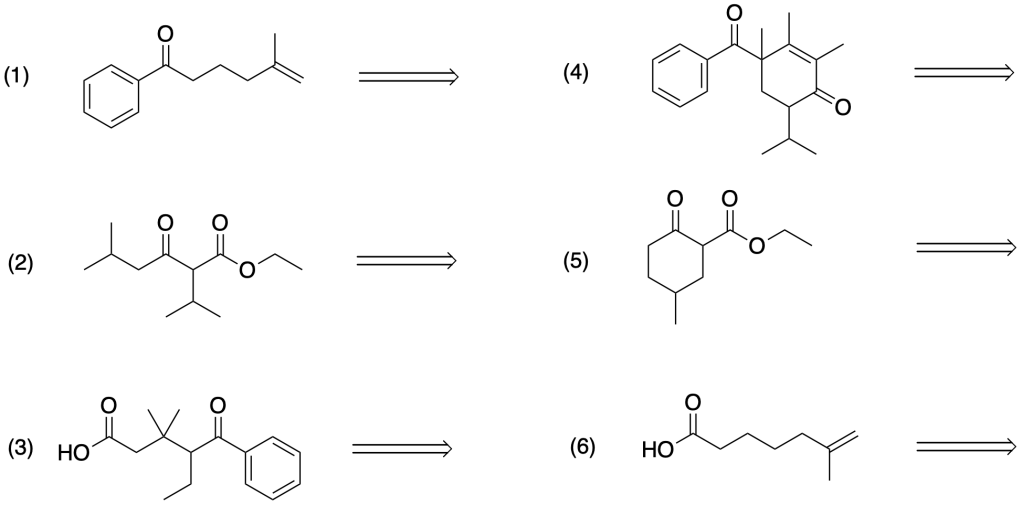
materiali di partenza:
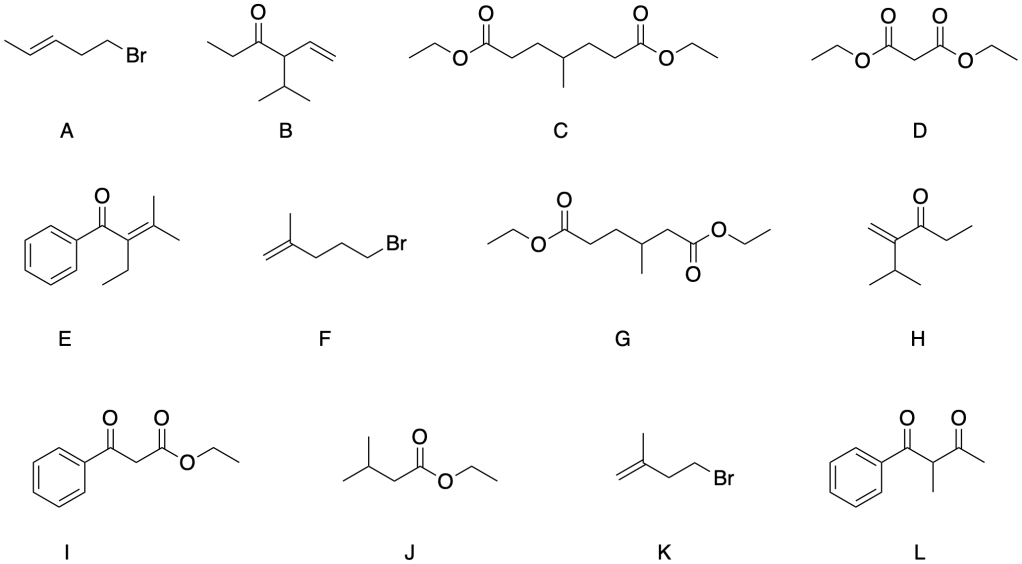

SINTESI
Quando si progetta una sintesi, il primo passaggio è confrontare il reagente con il prodotto. In particolare, bisogna:
ANALISI RETROSINTETICA
La freccia ⇒ indica la retrosintesi
A ⇒ B
la molecola B è la molecola più semplice che mediante una reazione porterà alla formazione della molecola A.
Nella progettazione della sintesi è fondamentale padroneggiare un gran numero di reazioni organiche: più reazioni si conoscono, più è probabile realizzare una sintesi con successo. Il principio guida nella pianificazione è semplificarla il più possibile. Un progetto di sintesi semplice ha una maggiore possibilità di avere esito positivo.
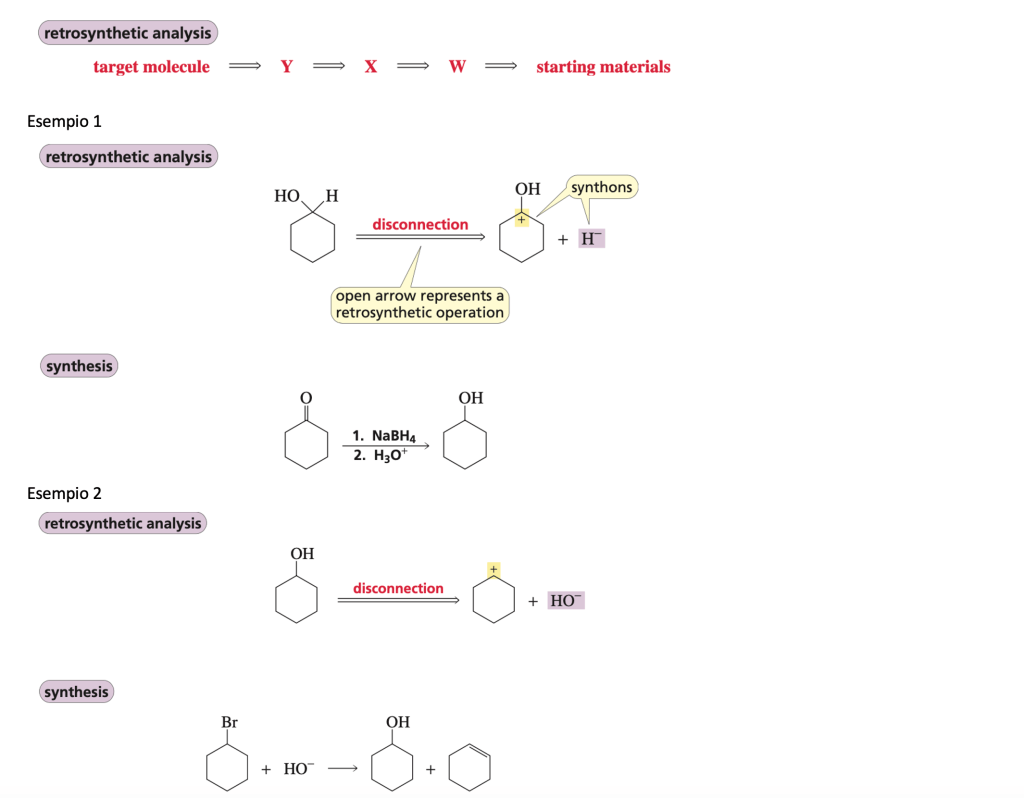
Disconnessione: La disconnessione implica la rottura di un legame all’interno della molecola target per generare due frammenti più semplici che potrebbero costituire i precursori della sintesi desiderata. Questo concetto aiuta a semplificare la complessità della sintesi, consentendo ai chimici di identificare i punti chiave di rottura per ottenere i precursori desiderati.
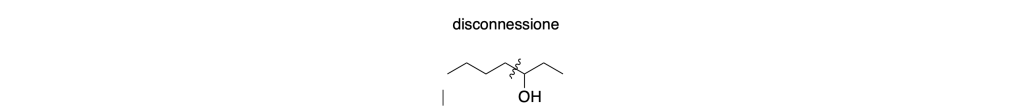
Sintoni: I sintoni sono frammenti ideali generati attraverso la disconnessione di un legame. Sono considerati ideali poiché rappresentano unità strutturali che facilitano la progettazione della sintesi. I sintoni possono essere utilizzati come guida per individuare i precursori necessari per la sintesi della molecola bersaglio.

Equivalenti Sintetici: Gli equivalenti sintetici sono specie chimiche effettive che svolgono la stessa funzione dei sintoni durante il processo di sintesi. Poiché i sintoni sono spesso specie ideali o transitorie e non possono essere impiegati direttamente, gli equivalenti sintetici vengono utilizzati al loro posto. Essi sono capaci di partecipare attivamente alle reazioni chimiche, generando gli intermedi di sintesi necessari per la formazione del prodotto finale.
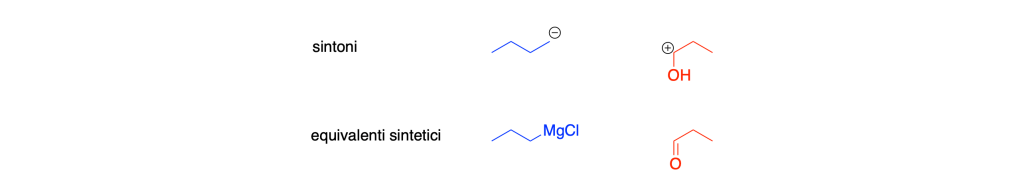
Reagenti: I reagenti sono i composti chimici effettivi che reagiscono con gli equivalenti sintetici per avviare le reazioni di sintesi. Essi forniscono gli atomi o i gruppi funzionali necessari per la formazione degli intermedi di sintesi o della molecola bersaglio stessa. I reagenti sono fondamentali per la trasformazione dei precursori in prodotti desiderati durante il processo di sintesi.
INTERCONVERSIONE DI GRUPPI FUNZIONALI
Quando si progetta una sintesi, il primo passaggio è comparare, tra il reagente e il prodotto, sia lo scheletro di atomi di carbonio sia la posizione dei gruppi funzionali. Se essi non variano, si deve semplicemente capire come convertire il gruppo funzionale del reagente in quello del prodotto.
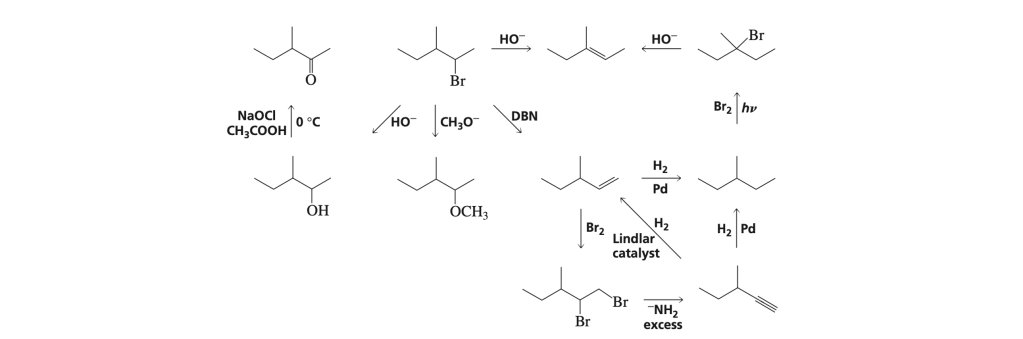
FUNZIONALIZZAZIONE DI UN CARBONIO
Può essere effettuata mediante una reazione radicalica

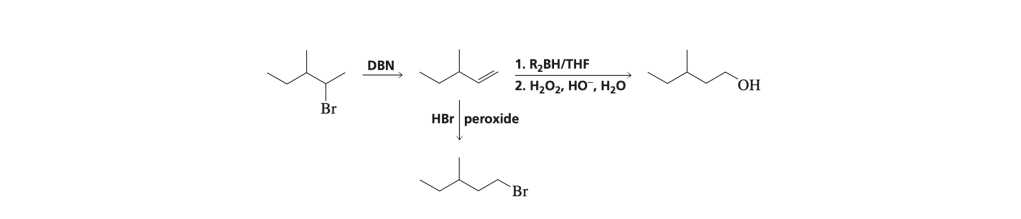
MODIFICA DELLA POSIZIONE DI UN GRUPPO FUNZIONALE
Se lo scheletro di atomi di carbonio non è modificato ma la posizione del gruppo funzionale è diversa, si devono prendere in considerazione le reazioni che modificano la posizione del gruppo funzionale.
MODIFICA DELLO SCHELETRO DI ATOMI DI CARBONIO
Se lo scheletro di atomi di carbonio è modificato, ma il numero di atomi di carbonio è lo stesso, si devono prendere in considerazione le reazioni che portano alla formazione di intermedi carbocationici.

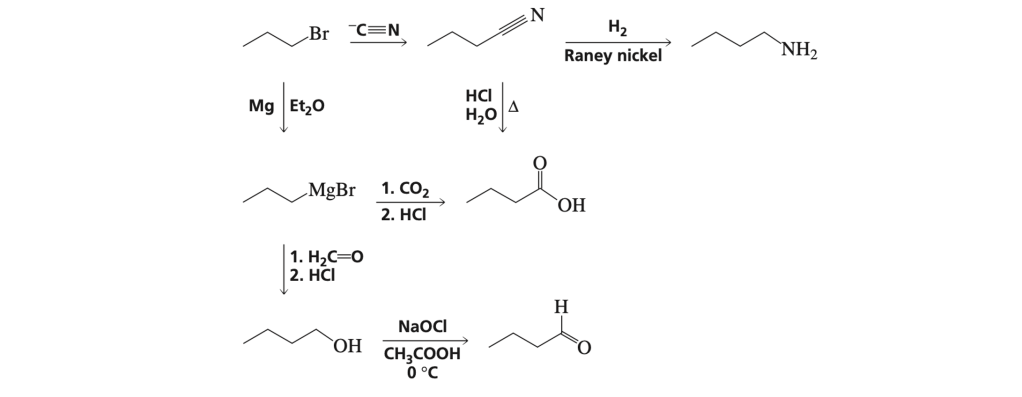
AGGIUNTA DI UN CARBONIO ALLO SCHELETRO DELLA MOLECOLA
Le reazioni con cui è possibile introdurre un atomo di carbonio allo scheletro della molecola sono diverse. Il metodo che si sceglie dipende dal gruppo funzionale che si desidera avere nel prodotto.
AGGIUNTA DI PIÙ DI UN CARBONIO ALLO SCHELETRO DELLA MOLECOLA
Le reazioni con cui è possibile introdurre Più un atomo di carbonio allo scheletro della molecola sono diverse. Ioni acetiluro, epossidi, reattivi di Grignard, addizione aldolica, reazione di Wittig e reazioni di accoppiamento sono alcuni esempi.
Per una visione d’insieme delle reazioni che possono essere utilizzate nel progettare una sintesi organica è possibile consultare il post “Mappe delle reazioni in Chimica Organica“
Esempio 3
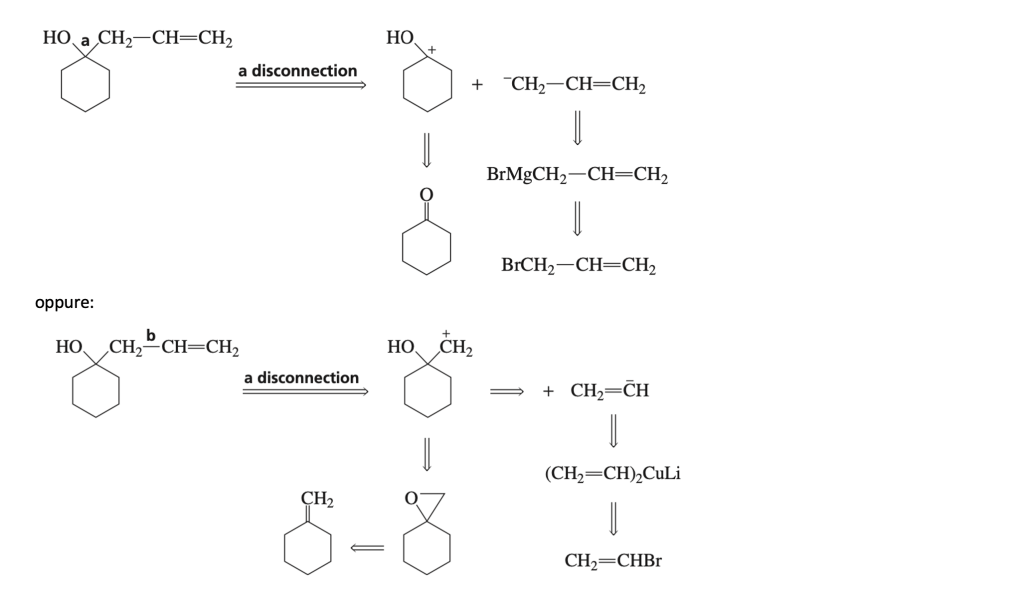
POSIZIONE RELATIVA DI DUE GRUPPI FUNZIONALI PER PROGETTARE UNA SINTESI
Se un composto contiene due gruppi funzionale, la loro posizione relativa può formìnire un buon suggerimento su come affrontare la sintesi.
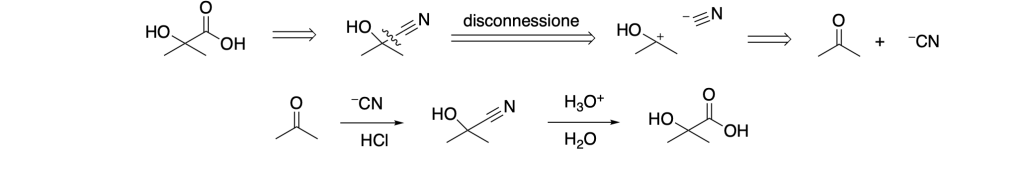
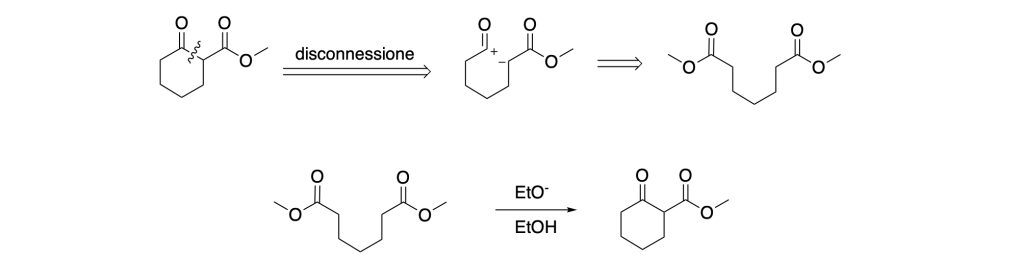
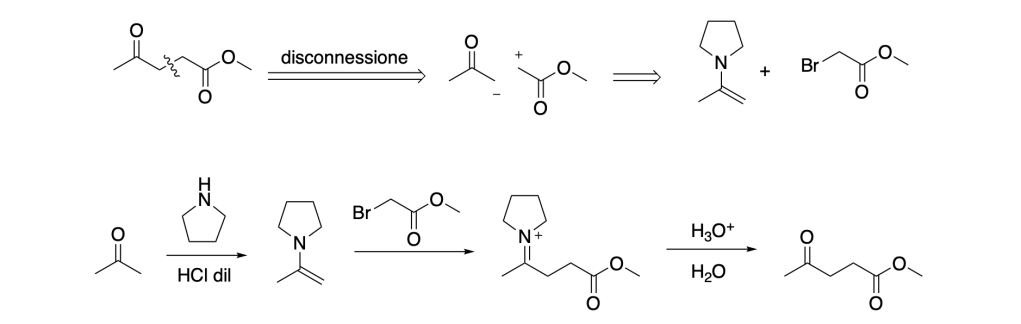

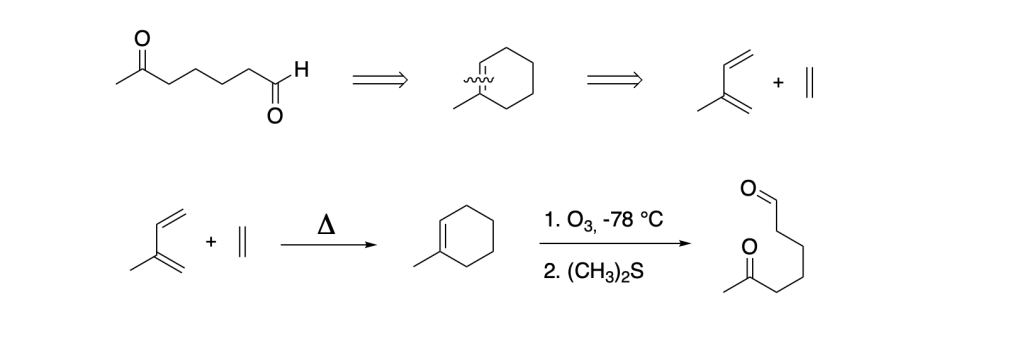
Esempio 1.
Sintetizzare il 3-esanone a partire dall’1-butino

Contando i carboni dei due composti, è evidente che bisogna aggiungere 2 carboni. In questo caso, dovendo partire dal butino, sfruttiamo l’acidità dell’idrogeno terminale per formare uno ione acetiluro da utilizzare come nucleofilo in una reazione SN2.

L’idratazione del 3-esino porta alla formazione di un enolo che tautomerizza immediatamente a chetone, quindi l’analisi retrosintetica è la seguente:

Per individuare i reagenti necessari, si parte dalle disconnessioni:
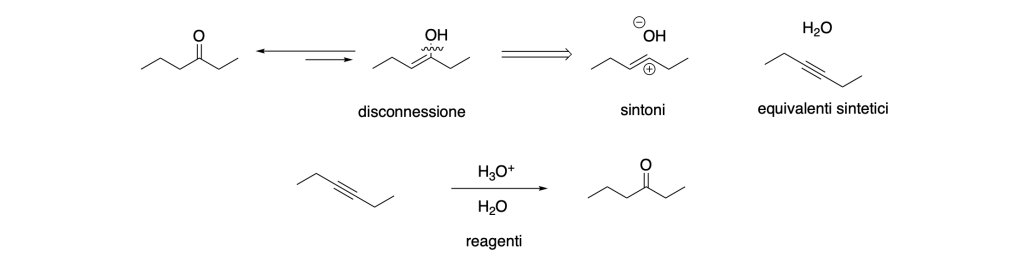
Per il primo passaggio dobbiamo disconnettere il legame C-C tra il C2 e il C3 del 3-esino:
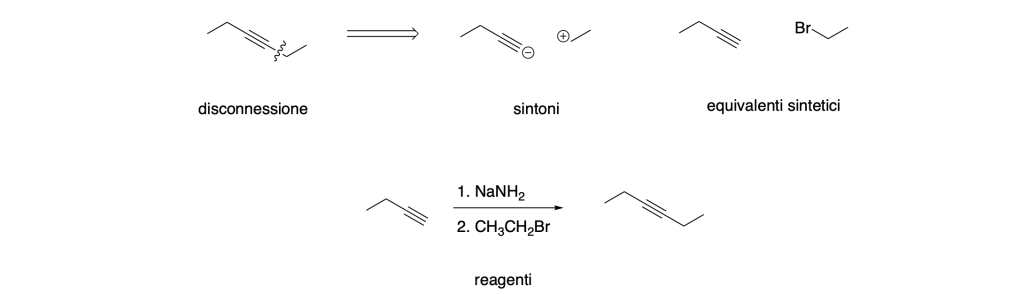
Pertanto, lo schema sintetico è:
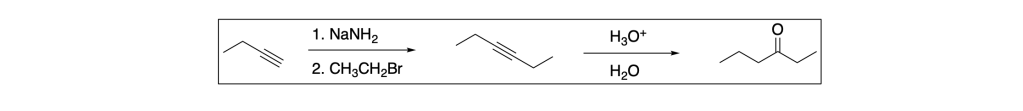
Esempio n. 2
Sintetizzare l’acido cicloesancarbossilico a partire dal bromocicloesano:
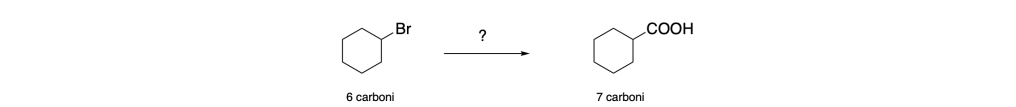
Partendo dalle disconnessioni possiamo avere due possibilità:
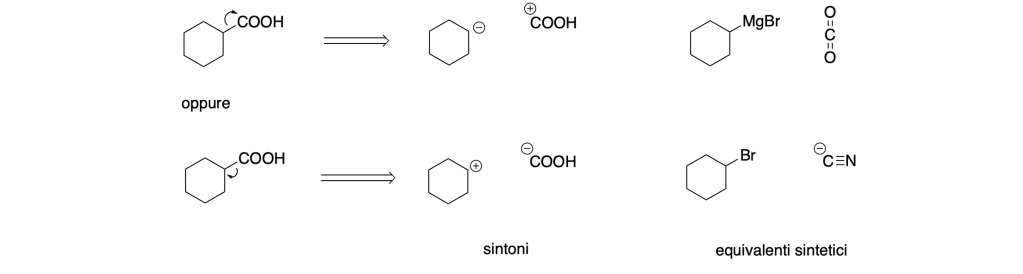
Le analisi retrosintetiche sono:
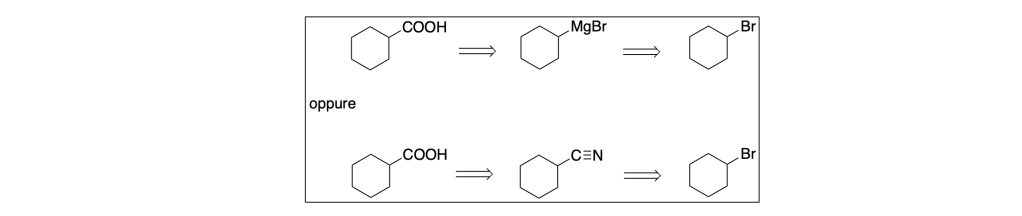
Gli schemi di sintesi sono:
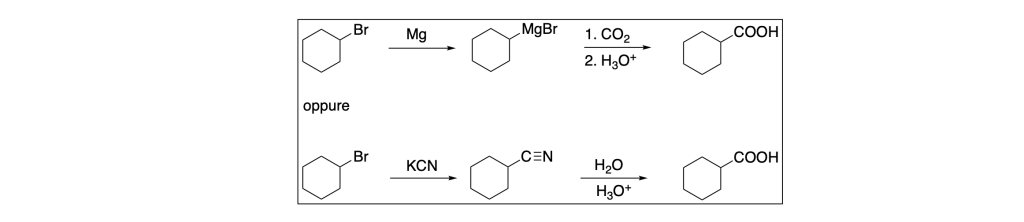
Esempio n. 3
Sintetizzare l’1-metil-1-cicloesene a partire dal bromocicloesano
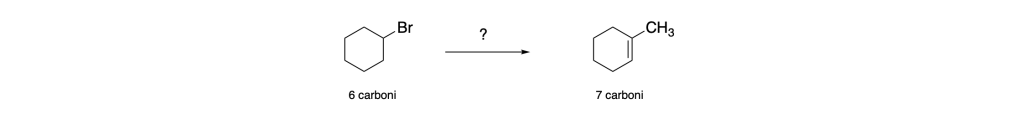
IN questo caso il prodotto da sintetizzare ha un carbonio in più e una insaturazione. Il doppio legame si può formare attraverso una reazione di disidratazione:
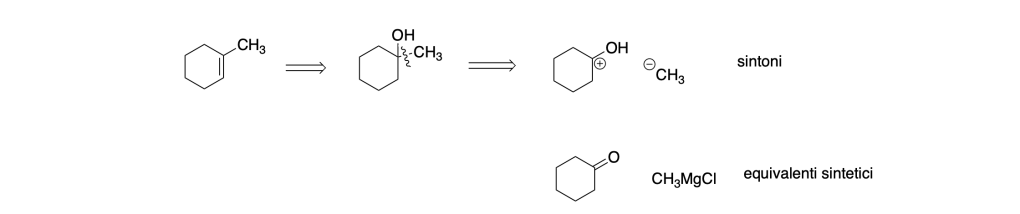
Il cicloesanone si può ottenere dall’ossidazione del cicloesanolo che si può ottenere dal bromocicloesano attraverso una reazione SN2

Quindi l’analisi retrosintetica è la seguente:

Lo schema di sintesi è dunque il seguente:


Per autovalutazione, provare a svolgere la simulazione della prova in due ore.
Esercizio n. 1
Assegnare il nome IUPAC completo di stereochimica ai seguenti composti:
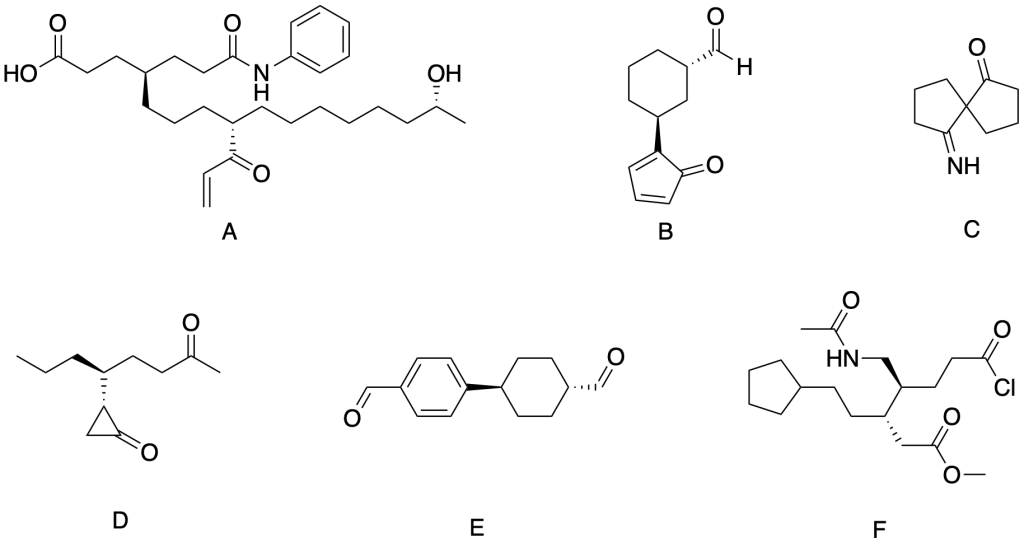
Esercizio n. 2
Proporre un meccanismo per la seguente reazione:
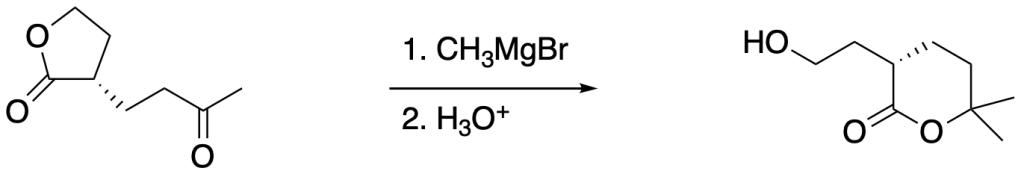
Esercizio n. 3
Proporre un meccanismo per la seguente trasformazione. E’ possibile usare il ciclopentanone e qualsiasi composto inorganico, compresi agenti ossidanti o riducenti.

Esercizio n. 4
La sintesi di Kiliani-Fischer, a partire dall’aldopentoso D-ribosio, produce una miscela di D-allosio e D-altrosio. Il 2,6-dideossi-D-altrosio, noto anche come D-digitossosio, è un monosaccaride ottenuto per idrolisi della digitossina, un prodotto naturale estratto dalla digitale (Digitalis purpurea). La digitossina trova largo impiego in cardiologia poichè riduce la velocità delle pulsazioni, regolarizza il ritmo e rinforza il battito cardiaco. Disegnare la proiezione di Fischer del 2,6-dideossi-D-altrosio. Disegnare la struttura del beta-L-digitossopiranosio nella conformazione a sedia più stabile.
Esercizio n. 5
Proporre una sintesi efficiente della 4-idrossi-4-metilcicloesan-1-carbaldeide a partire da 4-idrossicicloesan-1-carbaldeide. Partendo dallo stesso reagente, proporre la sintesi dell’1-ciclesil-1-etanone

Esercizio n. 1
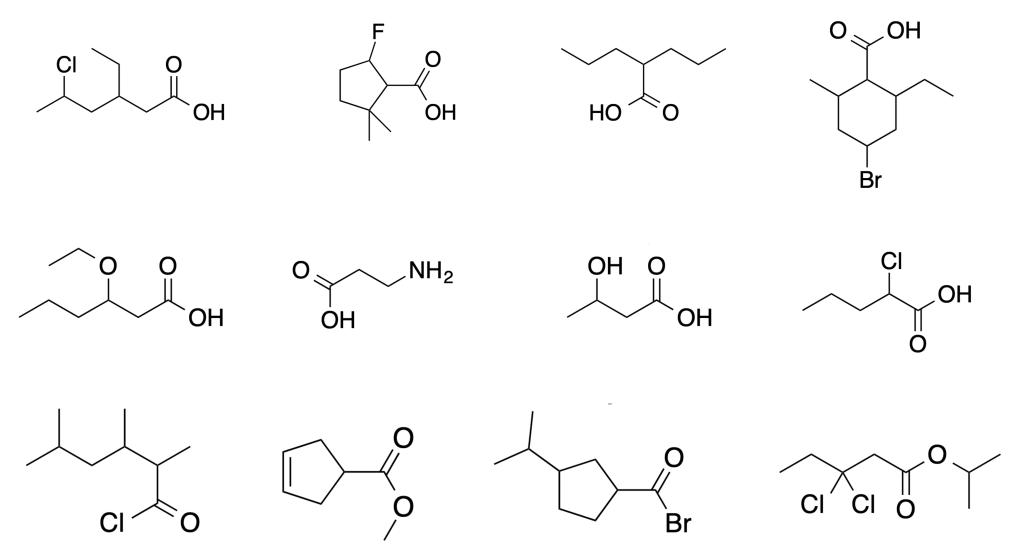
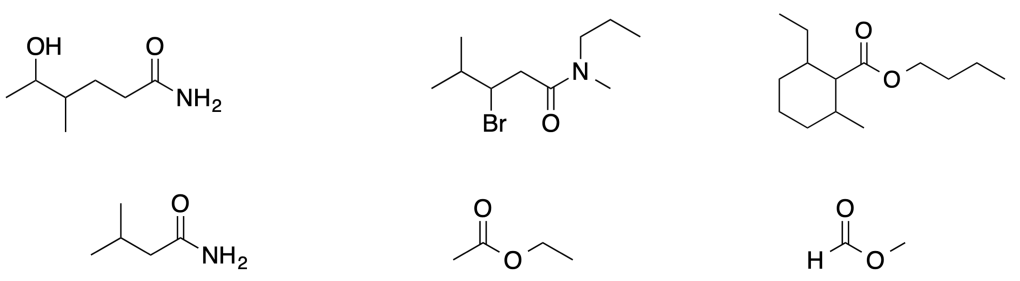
Assegna il nome IUPAC ai seguenti derivati degli acidi carbossilici


Le esercitazioni di laboratorio di Chimica organica si terranno tutti i lunedì come di seguito specificato:
Primo turno – inizio attività 9:30 nel Laboratorio didattico di Chimica 2

Secondo turno – inizio attività 14:30 nel Laboratorio didattico di Chimica 2



Lunedì 10 marzo inizieranno le esercitazioni di laboratorio per gli studenti iscritti al secondo anno del Corso di Laurea Magistrale a Ciclo Unico in Farmacia per l’aa 2024/25.
Le esercitazioni di laboratorio hanno frequenza obbligatoria. Gli studenti che devono iscriversi al corso di labopratorio possono farlo utilizzando il seguente link:
Le esercitazioni si svolgeranno tutti i lunedì con due turni: il primo alle 9:30 e il secondo alle 14:30.
Ogni studente deve portare un camice (ignifugo e antiacido), un quaderno di laboratorio (computisteria a quadretti), penna, matita, righello.
Prima di entrare il laboratorio, ogni studente deve STUDIARE la dispensa e gli argomenti teorici spiegati nella lezione teorica che precederà sempre ogni esercitazione pratica. Gli studenti che risulteranno assenti a lezione teorica non potranno svolgere l’esercitazione e l’assenza sarà conteggiata nel 25% di assenze massime consentite.
All’ingresso in laboratorio, ogni studente deve aver elaborato, sul proprio quaderno, la scheda pre-Lab, così come riportato di seguito:
In questa elaborazione non serve e non si devono copiare informazioni dalla dispensa dell’esperienza. Per comodità è possibile incollare l’esperienza nelle pagine precedenti la scheda pre-Lab.
Le schede saranno controllate dal docente durante l’esercitazione.

Di seguito sono riportati i risultati della prova intercorso di recupero.
Gli studenti riportati nella tanbella hanno superato la prova e sono ammessi a sostenere le prove intercorso del secondo semestre.

LA PROVA SI TERRA’ IL GIORNO 27 GENNAIO 2025 ALLE ORE 15:00
Le prenotazioni potranno esserer fatte, a partire dalle ore 17 del 6 gennaio fino alle ore 18 del 25 gennaio, al seguente link

You must be logged in to post a comment.