CONCETTI IMPORTANTI 2: ISOMERI CONFORMAZIONALI

ISOMERIA E STEREOISOMERIA:
- Isomeri di struttura: composti che presentano la stessa formula molecolare ma diverso ordine di connessione fra gli atomi.
- Stereoisomeri: isomeri i cui atomi sono collegati nello stesso ordine, ma presentano diversa disposizione spaziale. Si dividono in:
- Isomeri conformazionali: diverse conformazioni dello stesso composto in equilibrio tra loro grazie alla veloce convertibilità (rotazione intorno ad un legame singolo). Non possono essere separati l’uno dall’altro
- Isomeri configurazionali: sono degli stereoisomeri che, pur mantenendo la medesima connettività (i collegamenti tra i singoli atomi rimangono i medesimi), possono essere trasformati l’uno nell’altro solo rompendo legami chimici. Sono composti diversi e possono essere separati l’uno dall’altro. Gli isomeri configurazionali si dividono in:
- Isomeri geometrici (isomeri cis-trans): composti che non presentano libera rotazione attorno al legame tra i due atomi di carbonio, ognuno dei quali è legato a due gruppi diversi
- Isomeri ottici: composti in cui sono presenti degli elementi stereogenici, cioè elementi a causa dei quali la molecola ammette due isomeri che sono uno la forma speculare non sovrapponibile dell’altro.
ISOMERI CONFORMAZIONALI:
Le proiezioni di Newman sono uno strumento molto utile in chimica organica per rappresentare la conformazione di molecole attorno a un legame singolo, visualizzando come gli atomi sono orientati nello spazio rispetto a quel legame. Vediamo come costruire una proiezione di Newman passo per passo.
Il legame C-C
Immagina una molecola di etano (C₂H₆), che ha un legame singolo tra due atomi di carbonio (C-C). In una proiezione di Newman, osserviamo la molecola guardando lungo l’asse di un legame carbonio-carbonio.

atomo di carbonio frontale: L’atomo di carbonio più vicino a te.
atomo di carbonio posteriore: L’atomo di carbonio più lontano da te.
Ogni atomo di carbonio ha tre legami con gruppi sostituenti (come atomi di idrogeno o gruppi alchilici) disposti in modo tetraedrico.
Immagina la vista dal davanti
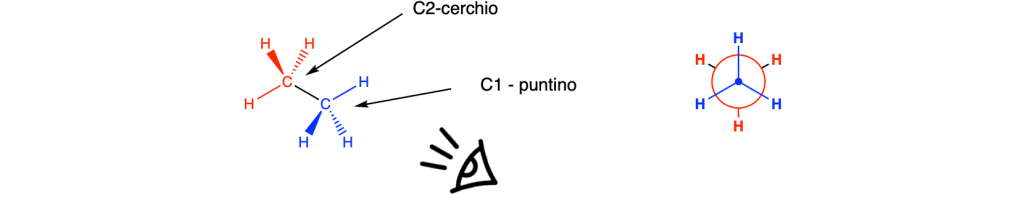
Nella proiezione di Newman, guardi il legame C-C come se tu fossi posizionato lungo la linea del legame, con il primo carbonio (C1) direttamente davanti a te e il secondo carbonio (C2) nascosto dietro di esso.
Il carbonio frontale (C1) viene rappresentato da un punto.
Il carbonio posteriore (C2) viene rappresentato da un cerchio.
Ogni molecola può essere rappresentata da più proiezioni di Newman. Infatti, possiamo guardare la molecola mettendoci di fronte al carbonio rosso che diventa così il carbonio frontale mentre il carbonio blu quello posterione:

- Disegna la proiezione di Newman dell’1-bromo-2-cloroetano
Passo 1: Il carbonio frontale
– Disegna un punto al centro del foglio, che rappresenta l’atomo di carbonio più vicino (C1).
– Da questo punto, disegna tre linee che si irradiano in direzioni diverse (idealmente a 120° l’una dall’altra). Queste linee rappresentano i legami tra il carbonio frontale e i suoi tre sostituenti
– Aggiungi i sostituenti: il bromo rivolto verso l’alto e i due idrogeni verso il basso.

Passo 2: Il carbonio posteriore
– Ora disegna un cerchio attorno al punto centrale, che rappresenta il secondo atomo di carbonio (C2), dietro al primo.
– Dal cerchio esterno, disegna altre tre linee (anch’esse distanziate di 120°) che indicano i legami tra il carbonio posteriore e i suoi tre sostituenti. Queste linee dovrebbero apparire dietro le linee disegnate per il carbonio frontale.
– Aggiungi i sostituenti: il bromo rivolto verso l’alto e i due idrogeni verso il basso.

.
- Rappresentare le diverse conformazioni
Le proiezioni di Newman sono utili per visualizzare le conformazioni della molecola. Due conformazioni comuni sono:
Conformazione eclissata: I sostituenti del carbonio frontale e posteriore sono allineati, ovvero si sovrappongono l’uno all’altro. Questo crea una configurazione meno stabile a causa della repulsione sterica tra i sostituenti.
Conformazione sfalsata: I sostituenti del carbonio posteriore sono sfalsati rispetto a quelli del carbonio frontale, cioè distanti il più possibile. Questa è la conformazione più stabile perché minimizza la repulsione tra i gruppi.


- Il conformero sfalsato è più stabile del conformero eclissato a causa dell’iperconiugazione
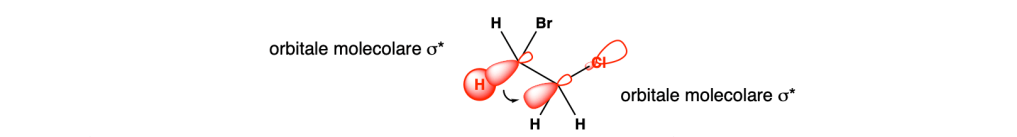
- Un conformero sperimenta una tensione quando la sua struttura chimica subisce un qualche sforzo che innalza la sua energia interna rispetto a un conformero privo di tensione o con una minore tensione.
- La tensione torsionale dovuta all’eclissamento dei legami C-H.
- La tensione sterica è il risultato della repulsione tra le nuvole elettroniche di atomi o gruppi
- La tensione angolare si manifesta quando gli angoli di legame deviano dal valore ideale
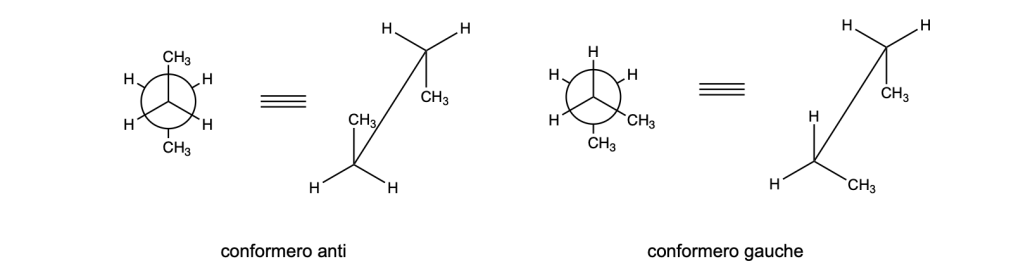
- Il conformero anti (o antiperiplanare) presenta due gruppi alchilici che formano un angolo diedro di 180° è più stabile del conformero gauche (angolo diedro 60°)a causa della tensione sterica
- Il cicloesano interconverte rapidamente tra le due conformazioni a sedia ugualmente stabili. Questo processo è chiamato inversione di anello
- I legami che sono assiali in un conformero sono equatoriali nell’altro e viceversa

- Il conformero a sedia con un sostituente in posizione equatoriale ha meno tensione sterica ed è perciò più stabile del conformero con il sostituente assiale
- Un sostituente in posizione assiale ha interazioni 1,3-diassiali sfavorevoli

Rappresentare il cicloesano mediante le proiezioni di Newman è un ottimo modo per visualizzare la disposizione spaziale dei legami e la conformazione della molecola, in particolare la conformazione a sedia, che è la più stabile per il cicloesano.
Nella rappresentazione tramite proiezioni di Newman, ci concentriamo su due legami carbonio-carbonio alla volta, osservando l’orientamento dei gruppi attaccati.
Vista lungo i legami C-C
Per disegnare una proiezione di Newman del cicloesano, bisogna osservare lungo l’asse di un legame carbonio-carbonio. Iniziamo con una parte della conformazione a sedia, osservando un legame tra due carboni adiacenti:
- I carboni 1 e 2 (o qualsiasi altra coppia di carboni adiacenti) e i carboni 5 e 4.
- Vedrai il primo carbonio frontalmente e il secondo dietro di esso.
Questa rappresentazione ti permette di visualizzare come gli idrogeni e altri sostituenti (se presenti) sono orientati rispetto ai due carboni che stai osservando.
- Disegna la proiezione di Newman dell’1-clorocicloesano
Passo 1: Il carbonio frontale C1
- Disegna un punto per rappresentare il carbonio frontale (C1).
- Dal punto centrale, disegna tre linee che si irradiano a 120° l’una dall’altra. Queste linee rappresentano i legami tra C1 e i suoi sostituenti
Per il cicloesano, in conformazione a sedia:
- Un legame sarà assiale, puntando verso l’alto o verso il basso (rispetto all’anello).
- Gli altri due legami saranno equatoriali, orientati lateralmente e distanti tra loro.
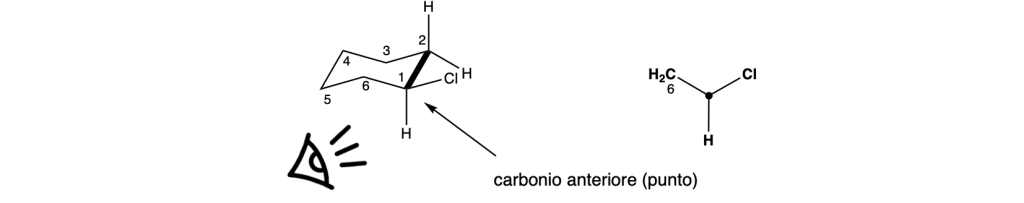
Passo 2: Il carbonio posteriore C2
- Disegna un cerchio più grande dietro il punto del carbonio frontale per rappresentare il carbonio posteriore (C2).
- Anche per C2, disegna tre linee distanziate di 120° tra loro che rappresentano i suoi legami. Una linea sarà orientata assialmente (opposta all’assiale del C1), e le altre due saranno equatoriali.

Passo 3: Il carbonio frontale C5
- Disegna un punto per rappresentare il carbonio frontale (C5).
- Dal punto centrale, disegna tre linee che si irradiano a 120° l’una dall’altra. Queste linee rappresentano i legami tra C5 e i suoi sostituenti

Lo stesso vale per il carbonio posteriore. Ricorda che i legami assiali tra carboni adiacenti sono opposti (se un assiale punta in alto, l’altro punta in basso).

- Disegna la proiezione di Newman del conformero dell’1-clorocicloessano dell’esempio precedente:

Passo 1: Il carbonio frontale C1 e C5
- Per disegnare la proiezione di Newman del conformero, bisogna sclissare gli stessi legami presi in considerazione precedentemente: legame C1-C2 e C-5-C4).
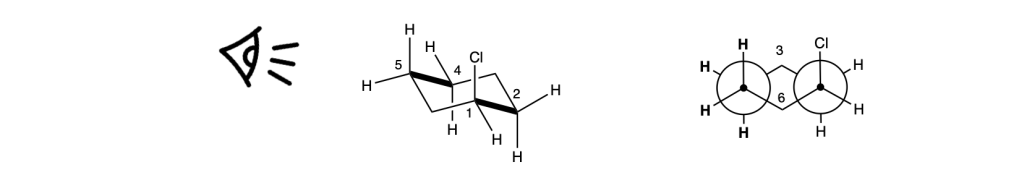
Le proiezioni di Newman applicate al cicloesano ti permettono di visualizzare meglio l’orientamento spaziale dei gruppi legati ai carboni e di valutare la stabilità conformazionale, specialmente in molecole sostituite dove la presenza di gruppi voluminosi può influenzare la conformazione preferita:



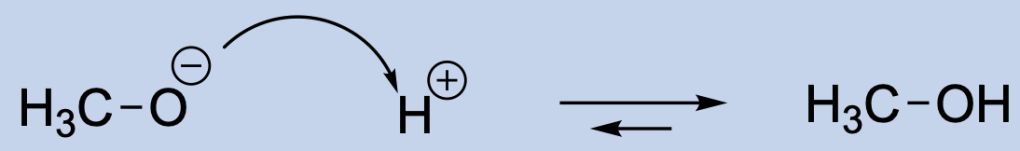

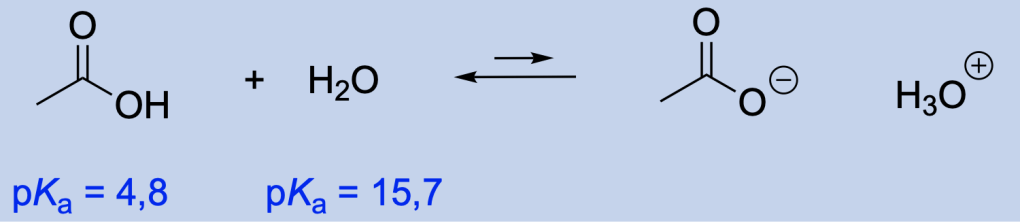
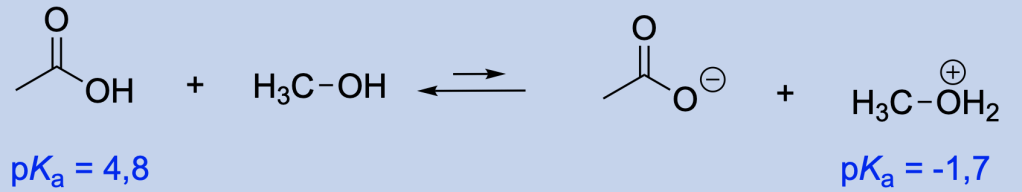



























































You must be logged in to post a comment.