Calendario appuntamenti della prossima settimana

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 24/02 | 14:00 | ESAME ORALE | Da definire | |
| 25/02 | 14:30 | ESAME ORALE | B1 | |
| 26/02 | 14:30 | ESAME ORALE | B1 |
Università degli Studi della Campania "Luigi Vanvitelli"

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 24/02 | 14:00 | ESAME ORALE | Da definire | |
| 25/02 | 14:30 | ESAME ORALE | B1 | |
| 26/02 | 14:30 | ESAME ORALE | B1 |

Si comunica che a partire da lunedì 23 febbraio sarà possibile sostenere esami solo nel corso del pomeriggio. Il numero massimo di prenotazioni per ogni data sarà quindi modificato a 5.
Sono state pertanto aggiunte nuove date, che è possibile consultare nel calendario in basso.
Gli studenti già prenotati in una delle prossime date sono invitati a riconsiderare la prenotazione, dato che in presenza di un numero di prenotati significativamente superiore a 5 sarà molto probabilmente necessaria una modifica che sarà eventualmente stabilita d’ufficio dalla docente.
Gli esami orali cominceranno alle 14:30, se non diversamente indicato su esse3 e sul calendario degli appuntamenti settimanali.
Sarà possibile prenotarsi per le nuove date già a partire da oggi pomeriggio. SI raccomanda di eliminare la vecchia prenotazione in caso di modifica.


| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 18/02 | 10:00 | ESAME ORALE | Da definire |
NB: come riportato in tabella, gli esami cominceranno alle 10:00

Si ricorda che le prove intercorso sono valide solo entro l’attuale finestra di esami.
Molti studenti, pur essendo stati ammessi alla prova orale, non risultano prenotati per nessuna delle date disponibili.
Data la presenza di posti liberi in suddette date, NON SONO PREVISTE DATE AGGIUNTIVE RISPETTO A QUELLE INDICATE NEL CALENDARIO.
Dunque, siete invitati ad individuare la data più consona in base alla vostra preparazione e a prenotarvi. Nel caso in cui dovessero essere esauriti i posti in detta data, potrete essere aggiunti da me: dovrete inviarmi una mail indicando la data (che dovrà sempre essere ESCLUSIVAMENTE tra quelle indicate nel calendario https://chimicaorganicadistabif.com/2026/01/06/calendario-esami-sessione-anticipata-a-a-2025-2026/

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 10/02 | 9:30 | ESAME ORALE | C1 | |
| 11/02 | 9:30 | ESAME ORALE | L |
L’incontro pre-esame orale (inizialmente previsto per lunedì 16) non potrà essere tenuto in quella data, a causa della vacanza accademica prevista per quel giorno. Di conseguenza, si terrà in data 13/02 (orario da programmare) se E SOLO SE ci saranno risposte al seguente form: Questionario in preparazione all’incontro pre-esame – Fill out form Il form si chiuderà domenica a mezzanotte.

Di seguito sono riportati i risultati della prova in oggetto.
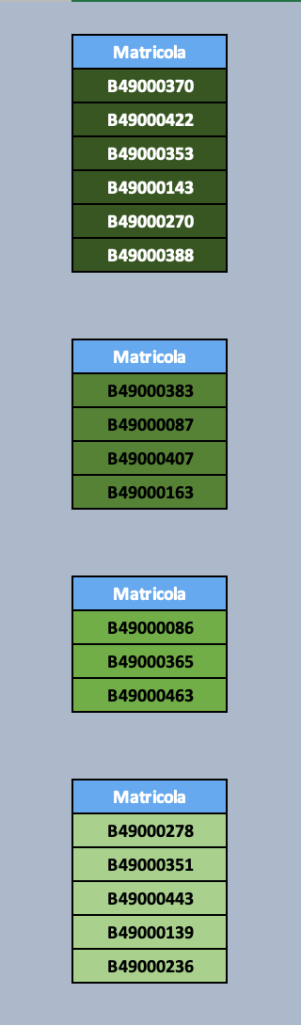
Gli studenti in verde e giallo hanno superato la prova (giallo con riserva) e sono dunque ammessi a sostenere la prova orale in data 10/02/2026 alle 9:30 in aula C1.
Per gli altri studenti la prova si intende NON superata.
Arancione: voto inferiore a 15
Rosso: voto inferiore a 12
Nero: voto pari a 0.5

Tutti coloro che hanno sostenuto la prova potranno prenderne visione prenotandosi per il ricevimento utilizzando l’apposito link
Si ricorda, infine, che il superamento dell’esame prevede che si raggiungano dei requisiti minimi di sufficienza e non di certo una “collezione” di un certo numero di “tentativi”.

Di seguito sono riportati i risultati della terza prova intercorso di Chimica Organica. I colori indicano il punteggio della media delle quattro prove intercorso.

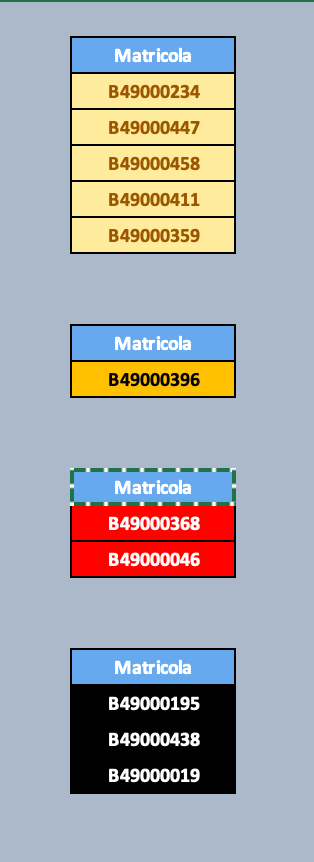
Di seguito sono riportati i risultati della prova di recupero di Chimica Organica.

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 03/02 | 15:30 | PROVA SCRITTA | A1 | |
| 04/02 | 9:30 | ESAME ORALE | L |

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, alle seguenti molecole
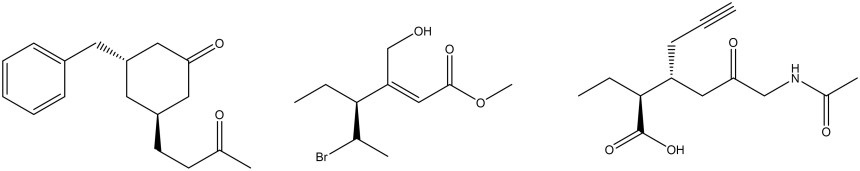
2. Rispondi alle domande sulla seguente molecola:
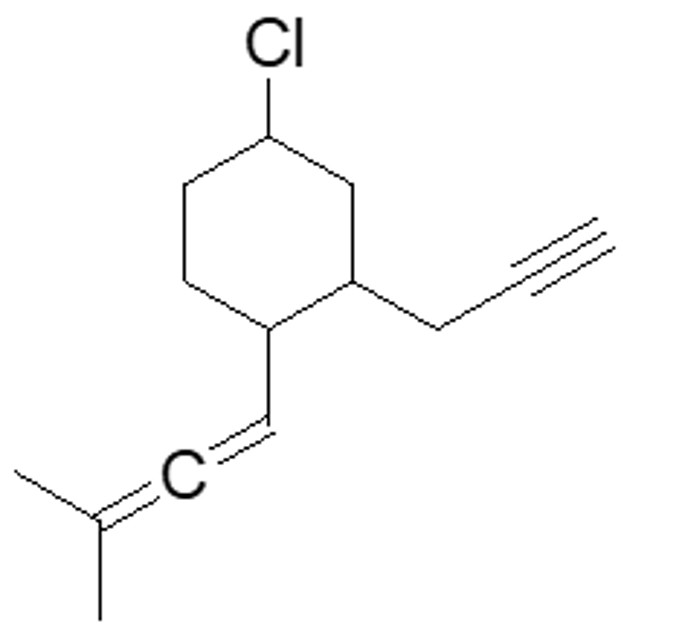
a) Come è ibridato l’atomo di cloro ____________________
b) Prendere in considerazione i doppi legami cumulati: com’è ibridato il carbonio centrale? Descrivere il tipo di legami che fa tale carbonio e gli orbitali molecolari coinvolti
c) Individuare l’idrogeno più acido in questa molecola
3.Disporre i seguenti composti in ordine di acidità crescente (dal meno acido al più acido) e spiegare sinteticamente il perché
a) CH3BrCH2SH
b) CH3CH2SH
c) CH3CH2OH
d) CH3CH2NH2
4. Il mentolo di origine naturale ha il seguente nome IUPAC: (1R,2S,5R)-2-isopropil-5-metilcicloesanolo. Qual è il nome IUPAC del suo enantiomero?
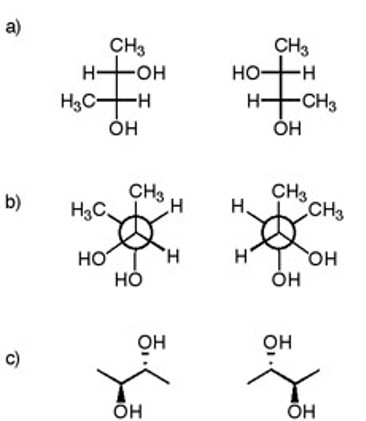
5. Dire se le seguenti coppie di composti sono enantiomeri, diastereoisomeri o lo stesso composto
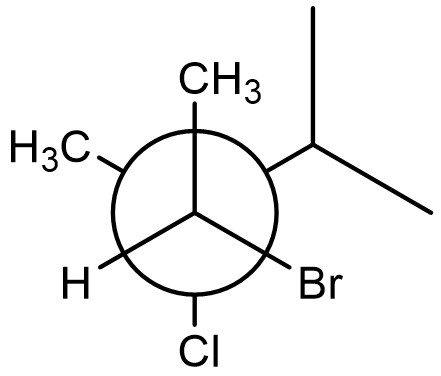
6. Scrivere a) un isomero di struttura del seguente composto, b) un diastereoisomero del seguente composto, c) l’enantiomero del seguente composto. Attribuire il nome IUPAC a ciascun di essi
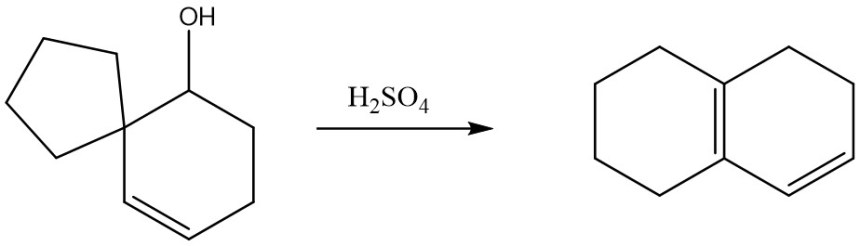
7. Proporre un meccanismo per la seguente reazione:
8. Chi reagirà più velocemente in una reazione E1 tra 3-bromo-3-metil-1-cicloesene e 4-bromo-4-metil-1-cicloesene? Spiegare sinteticamente perché.
9. Disporre i seguenti composti in ordine di basicità decrescente, fornire una spiegazione e dimostrare gli effetti che concorrono a determinare l’ordine indicato
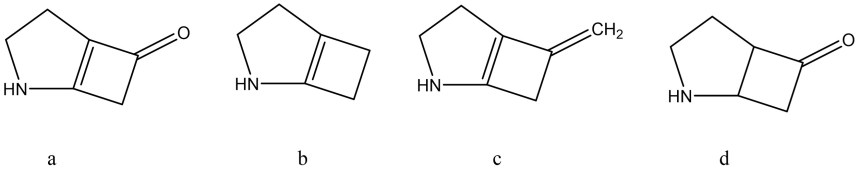
10. Quanti prodotti si formano dalla seguente reazione? Quale relazione stereochimica esiste tra questi pdotti?
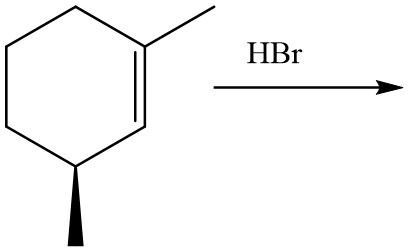
11. Fornire una definizione di punto isoelettrico. Come può essere calcolato?
SECONDO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
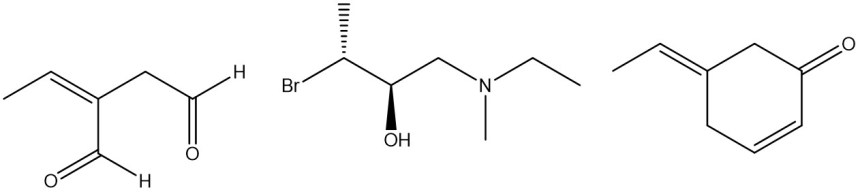
2. Disporre i seguenti composti in ordine di acidità decrescente e spiegare sinteticamente il perché
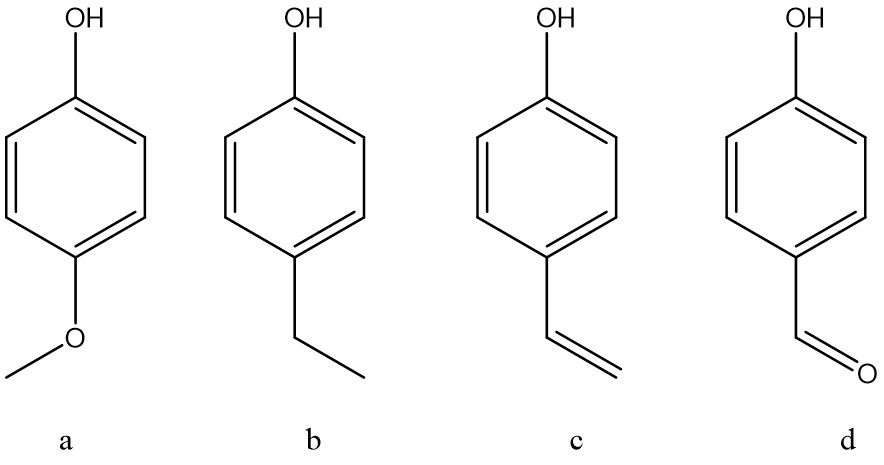
3. Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
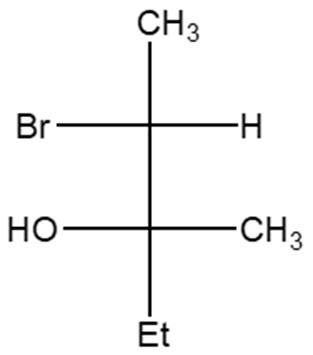
4. Quale dei seguenti è un composto meso?
a) (2R,3S)-diclorobutano
b) (2R,3R)-diclorobutano
c) (2R,3S)-3-cloro-2-butanolo
d) (2R,3R)-3-cloro-2-butanolo
5. Confrontare i seguenti composti e definirne le relazioni stereochimiche. In particolare, dire se sono enantiomeri, diastereoisomeri o isomeri conformazionali.
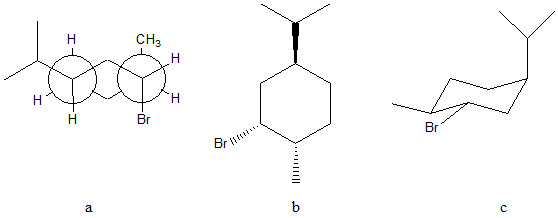
a e b sono___________________
a e c sono___________________
b e c sono___________________
6. Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal 3-metil-1-butene. Se quello ottenuto non è l’unico prodotto di reazione, indicare gli ulteriori altri prodotti formati, dire in che relazione sono col prodotto riportato e indicare se si formano o meno in quantità equimolari rispetto a quest’ultimo. NB: se non si formano ulteriori prodotti, scrivere “nessuno” nella casella dedicata
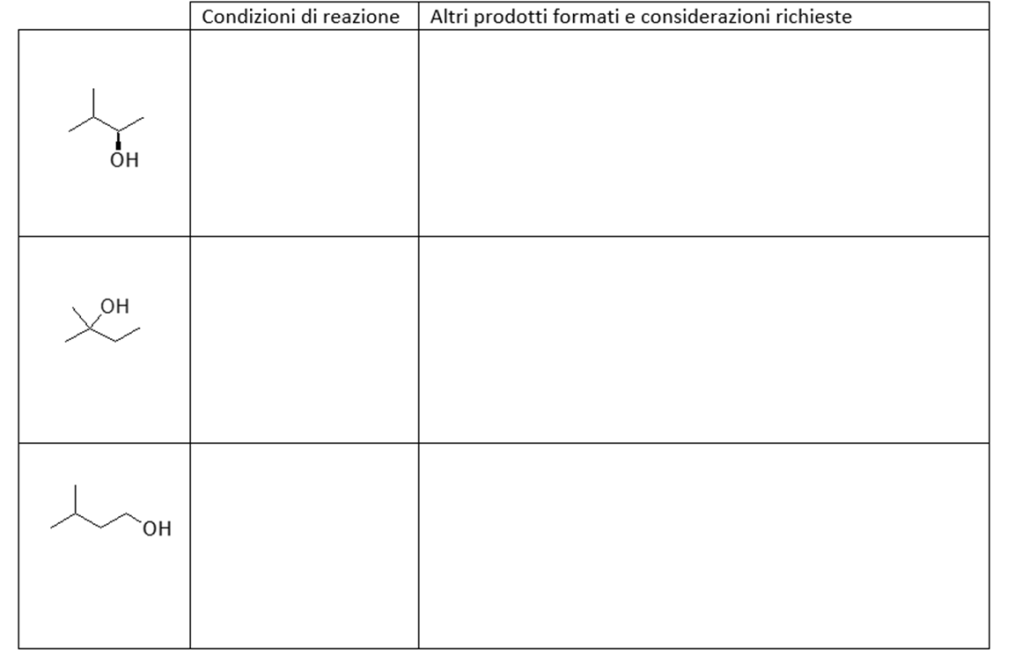
7. Mostrare il meccanismo e scrivere il prodotto della seguente reazione
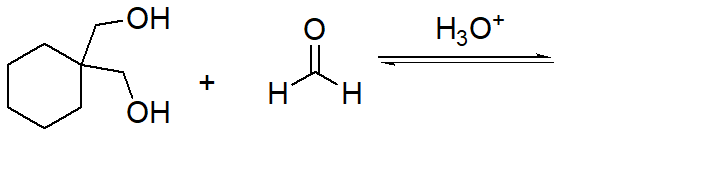
8. Scrivere i due anomeri del D-galattopiranosio, sapendo che il galattosio è l’epimero in 4 del glucosio
9 Scrivere il dipeptide Ala-Ala sapendo che la catena laterale dell’alanina è -CH3
TERZO SET
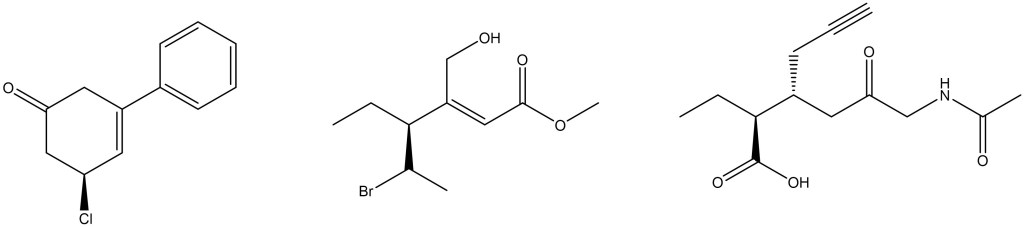
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
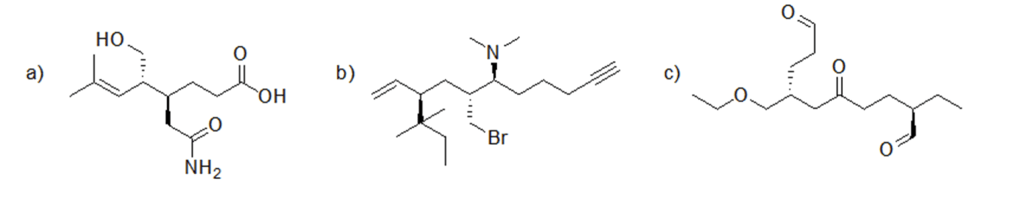
2.
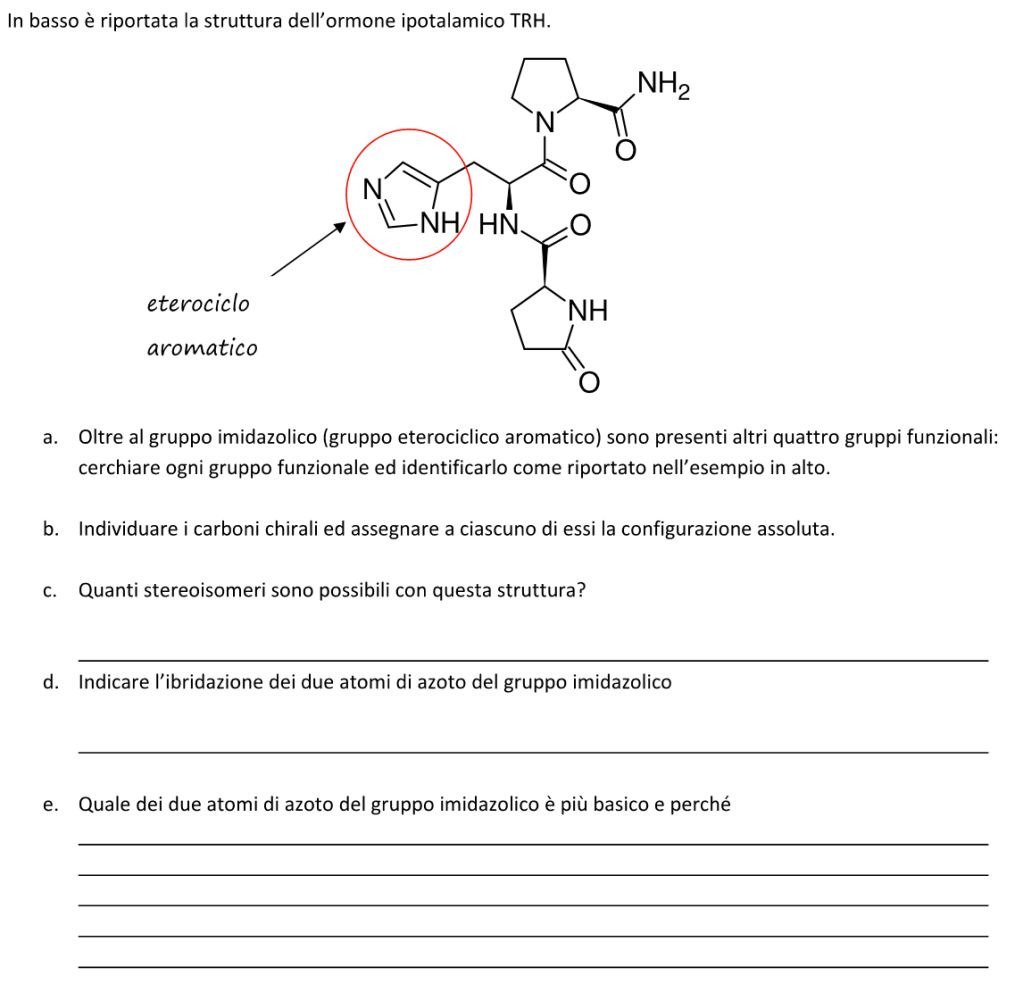
3. Ordinare i seguenti acidi carbossilici dal più acido al meno acido, giustificando la risposta data
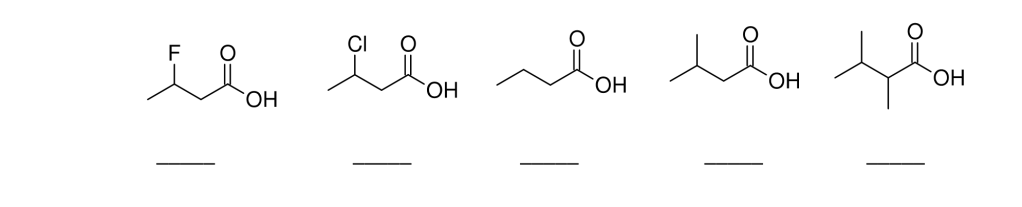
4. Quale dei seguenti composti è meno solubile in acqua?
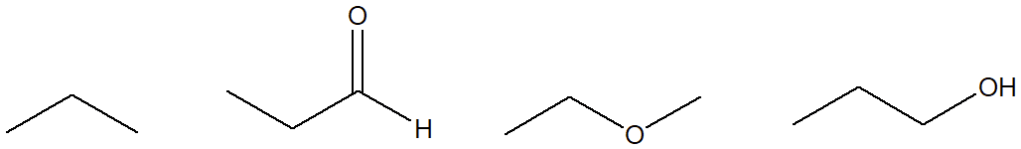
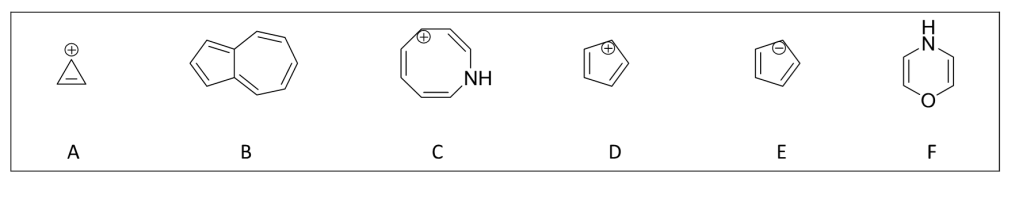
5. Giustificare il carattere aromatico, antiaromatico o non aromatico dei seguenti composti e ioni
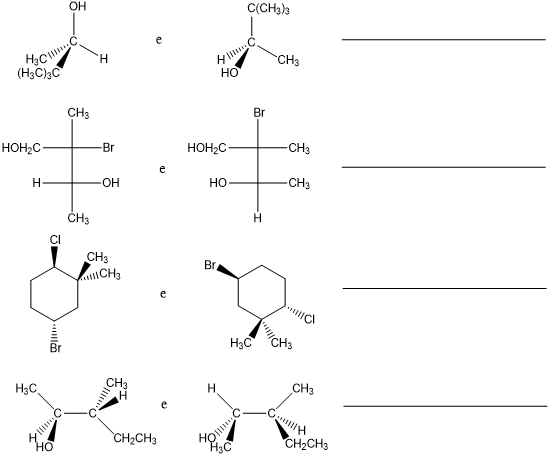
6. Indicare se le seguenti coppie di strutture sono enantiomeri, diastereoisomeri, isomeri strutturali o composti identici
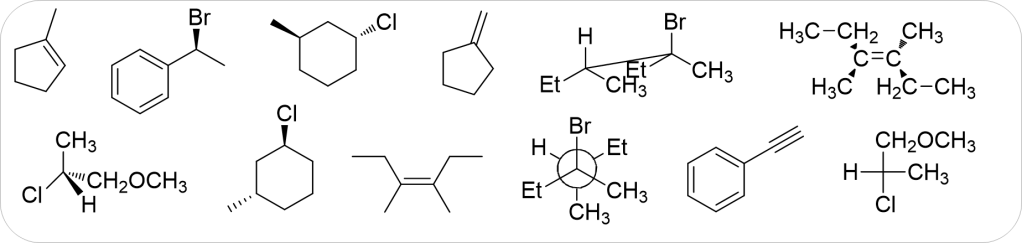
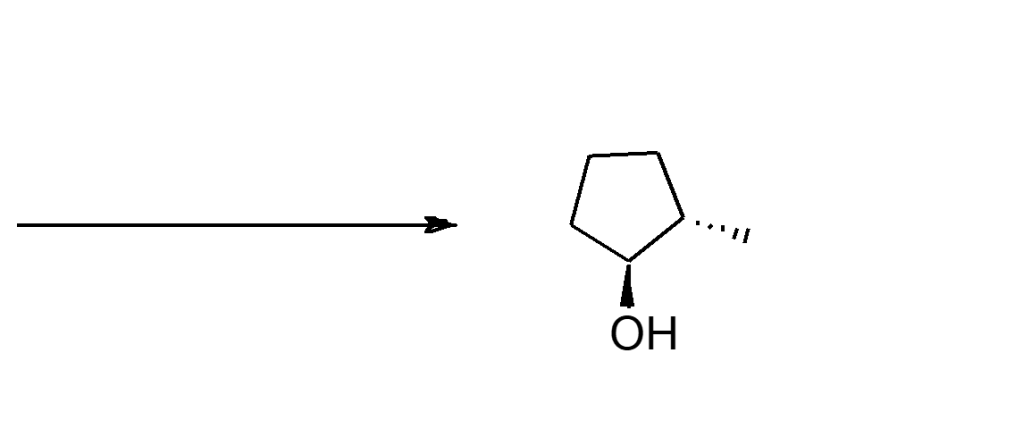
7. A partire da uno dei composti riportati nel riquadro e utilizzando qualsiasi altro reagente necessario, suggerire la sintesi di ciascuno dei seguenti prodotti, indicando sulle frecce le condizioni di reazione. Mostrare, inoltre, il meccanismo di reazione.
8. La reazione di (1R,2S)-1-bromo-2-metilcicloesano con etossido di sodio, dà come prodotto principale di eliminazione un prodotto diverso rispetto a quello che si ottiene dalla stessa reazione dello stereoisomero (1R,2R). Dare una spiegazione.
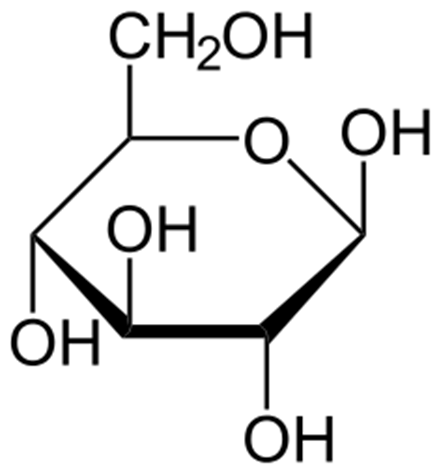
9. Il composto di seguito mostrato è il β-D-glucopiranosio, scrivere: a) l’anomero α; b) il β-D-galattopiranosio (epimero in 4); β -L-glucopiranosio
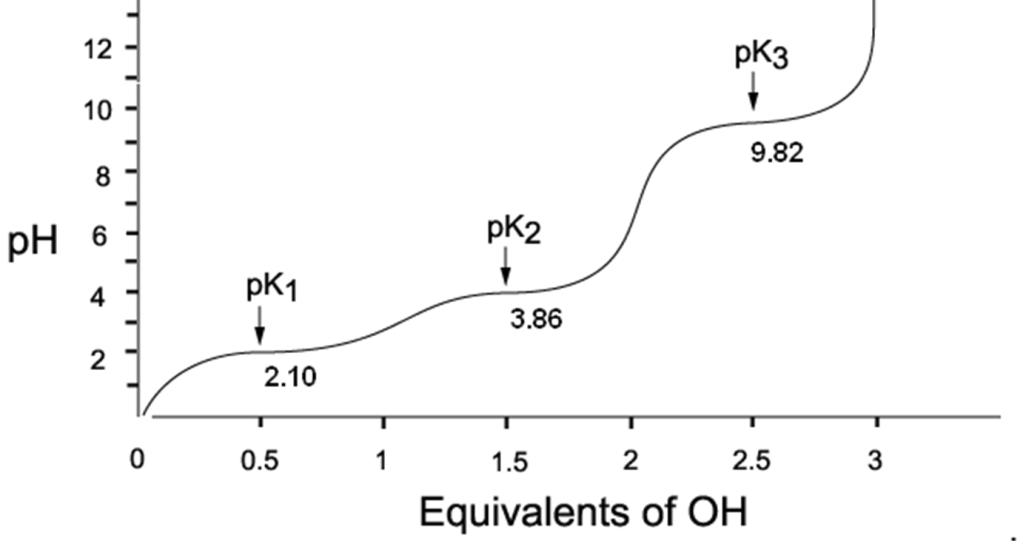
10. In basso è riportata la curva di titolazione dell’acido aspartico, un amminoacido acido.
Qual è il punto isoelettrico dell’acido aspartico?

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomenti…e a breve altre liste di domande saranno pubblicate. In ogni caso, potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti. In fondo alla lista, troverete anche una classifica del livello di difficoltà delle domande.
Grado di difficoltà delle domande:
Alto (richiedono più passaggi e/o notevole padronanza della disciplina): 17
Medio (domande che vanno al di là della mera esposizione/applicazione di concetti teorici): 5, 8, 24, 30
Basso (domande che riguardano l’esposizione di concetti teorici, la dimostrazione di semplici meccanismi di reazione, l’applicazione diretta di concetti teorici di base): tutte le domande non incluse nelle due liste precedenti.
You must be logged in to post a comment.