Attribuzione della configurazione assoluta al carbonio chirale

Definire la configurazione assoluta dei seguenti composti. Per ogni set, è disponibile un esercizio guidato
PRIMO SET: Gruppo a priorità minore lontano dall’osservatore
Esercizio guidato

La prima cosa da fare è attribuire le priorità relative agli atomi o ai gruppi legati al carbonio chirale, secondo quanto riportato a pag. 148 del Bruice.
Gli atomi direttamente legati al carbonio sono O, C, C, C. L’ossigeno ha numero atomico maggiore del carbonio, per cui possiamo già dire che avrà priorità 1. Dei tre carboni, quello del gruppo metile lega HHH, quello dell’etile lega CHH, quello dell’isopropile lega CCH. Sapendo che il carbonio ha numero atomico maggiore dell’idrogeno, possiamo dedurre che l’isopropile ha priorità rispetto all’etile, che avrà a sua volta priorità rispetto al metile.
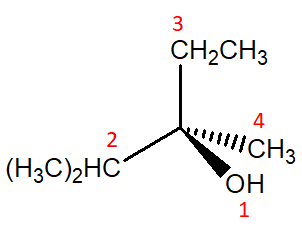
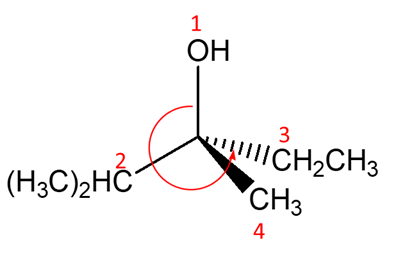
A questo punto, dobbiamo verificare che il sostituente a priorità minore si trovi lontano dall’osservatore. Dato che questo è il caso, tracciamo una freccia nella direzione di priorità crescente 1–>2–>3 e vediamo il senso di rotazione della freccia (orario–>R, antiorario–>S)
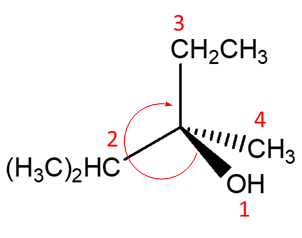
Nel caso specifico la rotazione è oraria, quindi la configurazione assoluta del carbonio chirale sarà R.
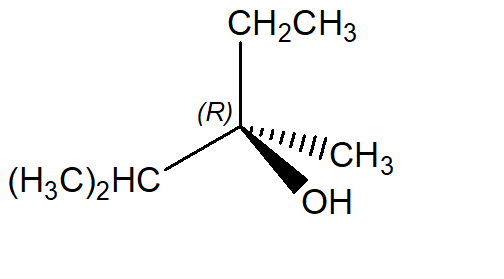
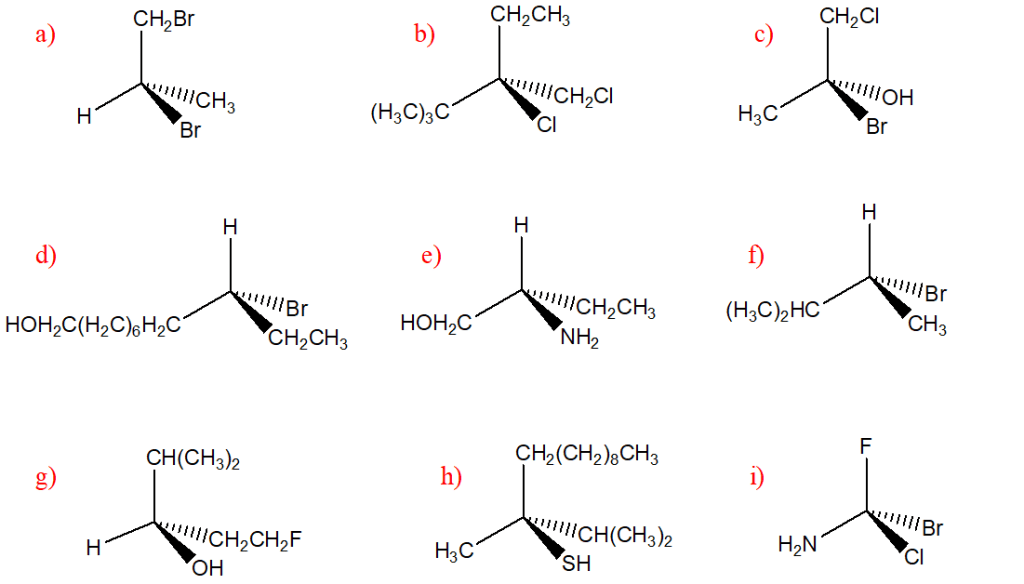
Esercizi da svolgere:
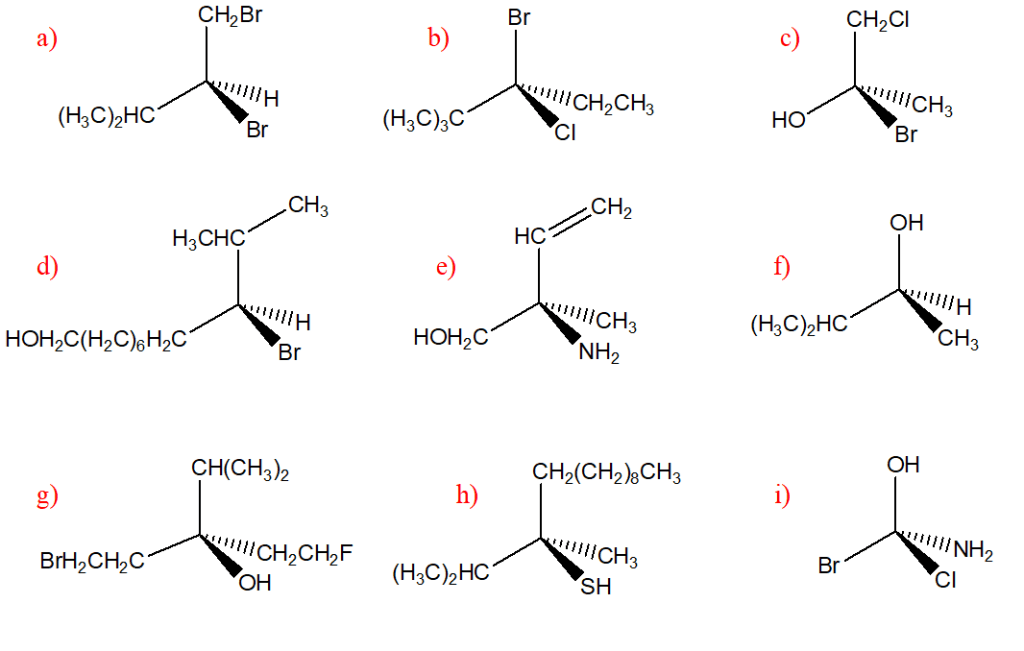
SECONDO SET: gruppo a priorità minore verso l’osservatore
Esercizio guidato

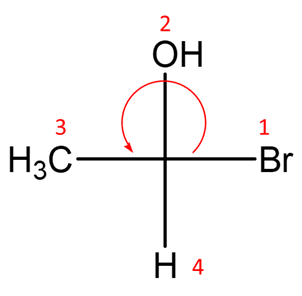
In questo caso, vediamo che il gruppo a priorità minore si trova verso l’osservatore. Praticamente, stiamo guardando la molecola dal lato diametralmente opposto rispetto a quello prescritto dal sistema di Cahn-Ingold-Prelog. In questo caso, rotazione oraria corrisponderà all’enantiomero S e antioraria all’enantiomero R. Per capire meglio questo concetto, provare a lavorare con i modellini con un collega: uno osserverà la molecola secondo la prospettiva giusta (sostituente a priorità minore lontano dall’osservatore), l’altro gli starà di fronte e quindi guarderà la molecola come illustrato sopra (col sostituente a priorità minore verso l’osservatore). A questo punto definite la rotazione e vedrete che se il primo osservatore determina una rotazione oraria, il secondo avrà una rotazione antioraria (e viceversa).
Ora, nel caso specifico, visto che in questo caso stiamo osservando la molecola dal lato diametralmente opposto a quello richiesto, dopo aver tracciato una freccia nella direzione di priorità crescente 1–>2–>3, osserviamo che essa avrà direzione antioraria.
Possiamo quindi dedurre che il nostro composto ha configurazione assoluta R.

Esercizi da svolgere:

TERZO SET: gruppo a priorità minore sul piano
Esercizio guidato
Se il sostituente a priorità minore si trova sul piano, dobbiamo necessariamente effettuare uno scambio per portarlo sul cuneo tratteggiato, dato che non stiamo osservando la molecola nè dal lato giusto, nè dal lato opposto.

Attenzione: in questo modo ho ottenuto l’enantiomero del composto di cui voglio determinare la configurazione assoluta (anche questo è facilmente dimostrabile utilizzando i modellini). Quindi, detemino il senso di rotazione della freccia e di conseguenza la configurazione assoluta dell’enantiomero.

Nel caso specifico, sarà S. A questo punto conosco anche la configurazione assoluta del composto di partenza, che sarà quindi R.

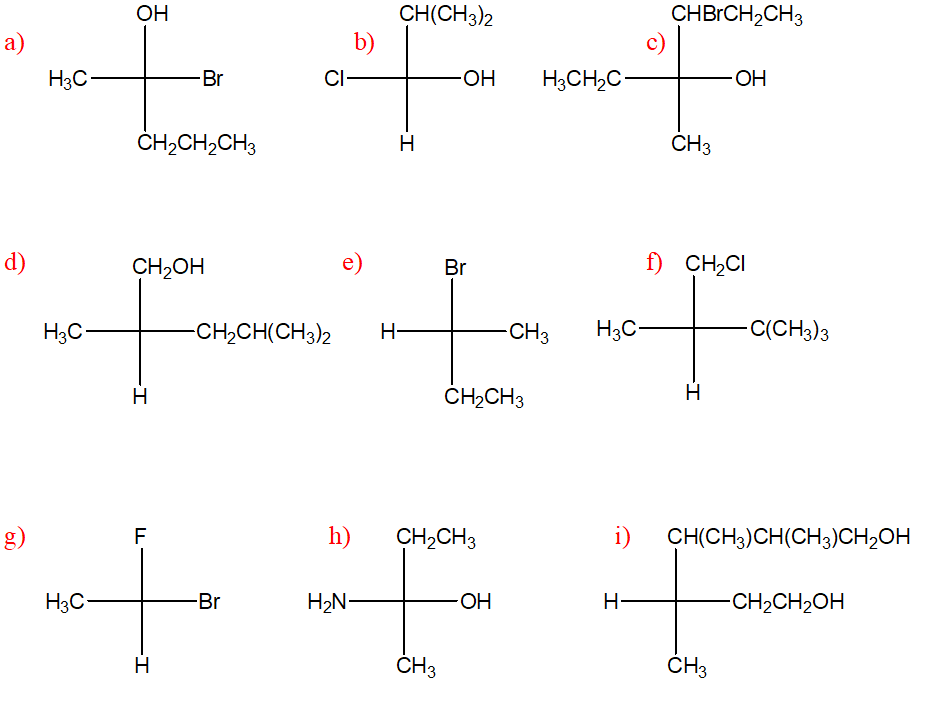
Esercizi da svolgere:
QUARTO SET: proiezioni di Fischer
Esercizio guidato
Nel caso della proiezione di Fischer, non ci sono gruppi sul piano (vedere immagine sotto ed utilizzare i modellini per capire da dove stiamo osservando il carbonio e i suoi legami). I gruppi sui legami verticali sono lontano dall’osservatore, quelli sui legami orizzontali verso l’osservatore.

In questo caso bisogna quindi
1) attribuire le priorità relative sempre seguendo le stesse regole
2) tracciare una freccia nella direzione di priorità crescente 1–>2–>3
3) determinare il senso di rotazione della freccia
4) osservare dove si trova il sostituente a priorità minore. Se su legami verticali, allora rotazione oraria–>R e antioraria–>S. Se invece è su uno dei legami orizzontali, la direzione della freccia darà una risposta opposta a quella corretta.
In questo caso, la direzione è antioraria e il sostituente a priorità minore è sulla linea verticale, quindi la configurazione assoluta sarà S.

Nell’esempio seguente, invece, l’atomo a priorità minore si trova su un legame orizzontale.

In questo caso, la direzione della freccia è oraria, ma poichè il sostituente a priorità minore si trova sulla linea orizzontale, la configurazione assoluta sarà S.

Esercizi da svolgere:
QUINTO SET: strutture a segmenti
Esercizio svolto
Su una struttura a segmenti, il cuneo pieno indica un sostituente rivolto verso l’osservatore, il cuneo tratteggiato un sostituente lontano dall’osservatore. NB: l’idrogeno è spesso sottinteso.

Si individua il carbonio chirale, qui indicato dall’asterisco e si applicano le regole già viste per determinare le priorità relative degli atomi o dei gruppi legati. Si vede poi il verso della freccia nella direzione di priorità crescente 1–>2–>3. Fatto questo, di controlla se il sostituente a priorità minore è lontano dall’osservatore. Se è così, come in questo caso, la rotazione oraria, corrisponde alla configurazione assoluta R.
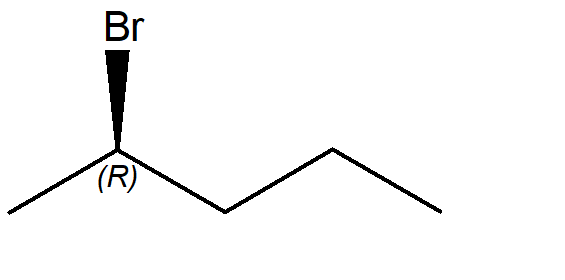
Se, invece, il sostituente a priorità minore è rivolto verso l’osservatore…
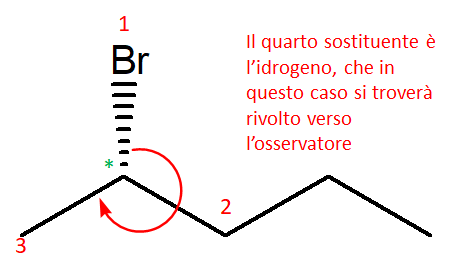
…la direzione oraria della freccia corrisponde alla configurazione assoluta S.

Se il verso della freccia fosse stato antiorario, allora: sostituente a priorità minore lontano dall’osservatore–>S, verso l’osservatore–>R (NB: nell’esempio mostrato, il sostituente a priorità minore è sempre l’idrogeno, che è sottinteso…ma poichè abbiamo già l’informazione su come sono orientati 3 dei sostituenti, sappiamo anche già come è orientato quello sottinteso).
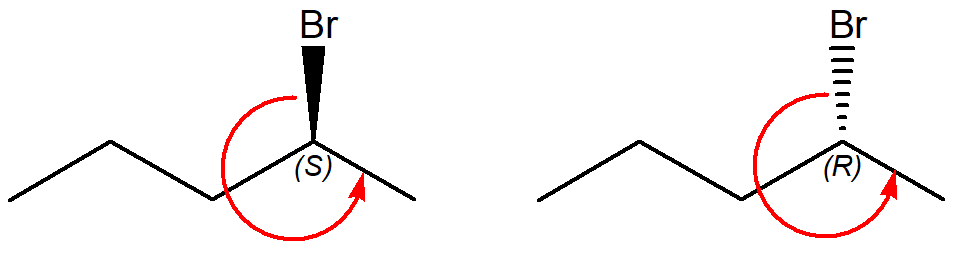
In presenza di più carboni chirali, si attribuisce la configurazione assoluta a ciascuno di essi in maniera indipendente.
Lo stesso approccio si applica anche ai composti ciclici.
Esercizi da svolgere

NB: prima di affrontare gli esercizi è essenziale studiare la teoria!
ALTRI ESERCIZI
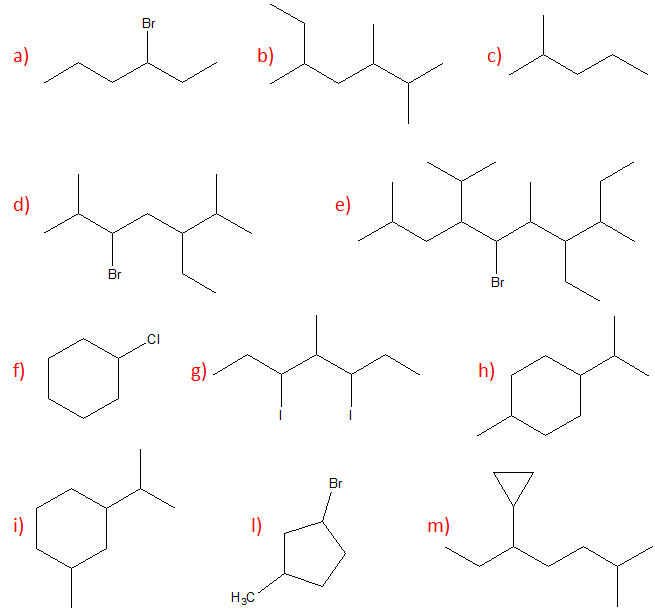
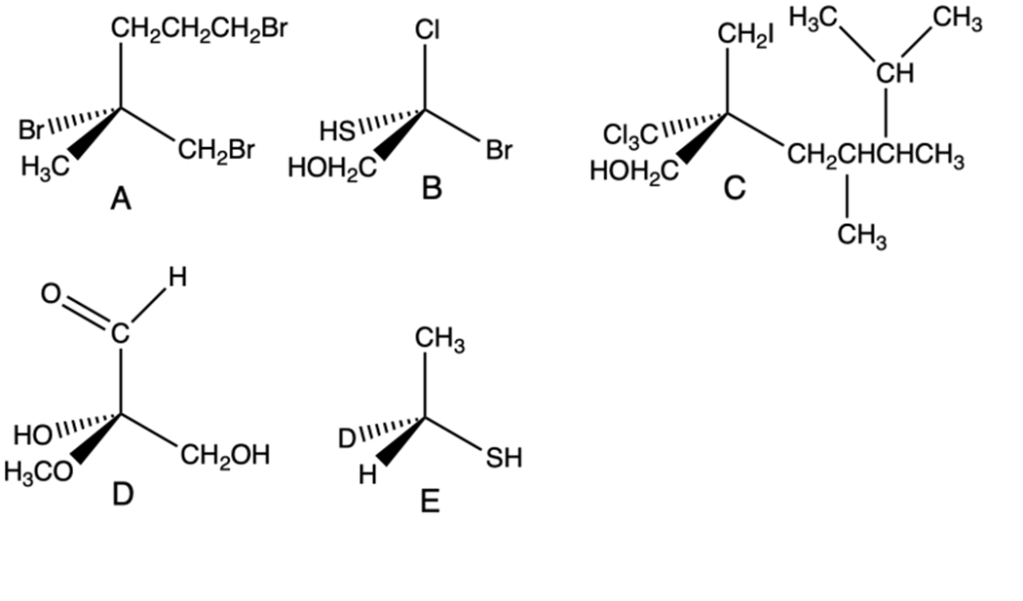
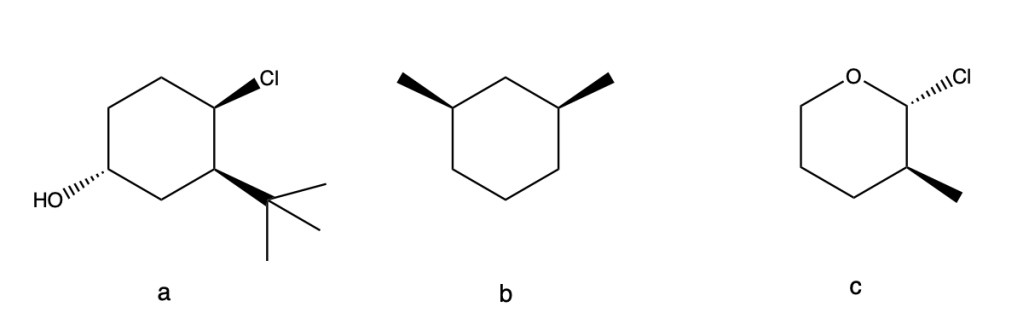
1) Assegnare la configurazione assoluta (R/S) ai carboni chirali delle seguenti molecole.

2) Rappresentare i seguenti composti come con: I) formule prospettiche, II) strutture a segmenti; III) proiezioni di Fischer:
a) (2S)-2-bromobutano
b) (3R)-3-cloro-2-metilpentano
c) (2S,3R)-3-cloro-2-pentanolo
d) (3R)-3-etil-2-metilesano
e) (2S,3S)-3-etil-4-metilentan-2-olo
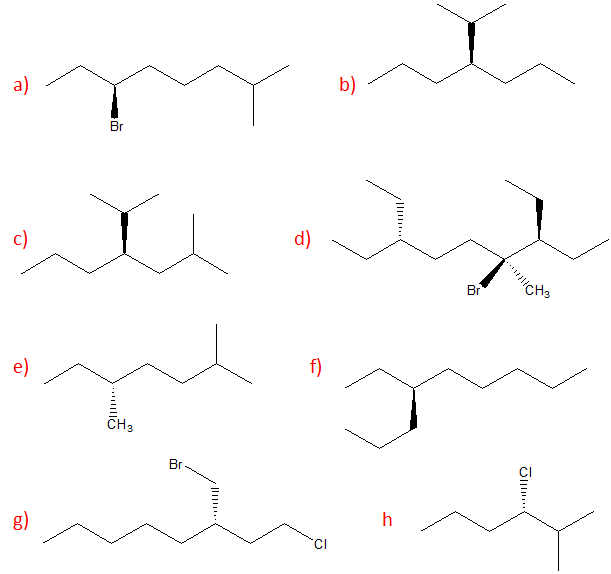
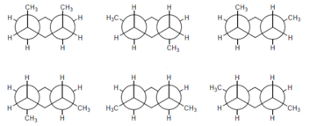
3) Individuare, tra le seguenti strutture, l’enantiomero del (2R)-2-bromo-1-esanolo

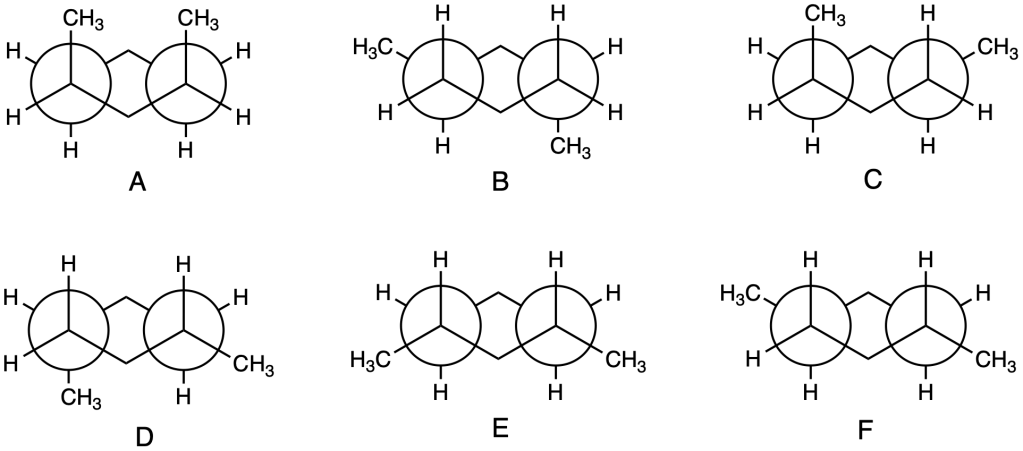
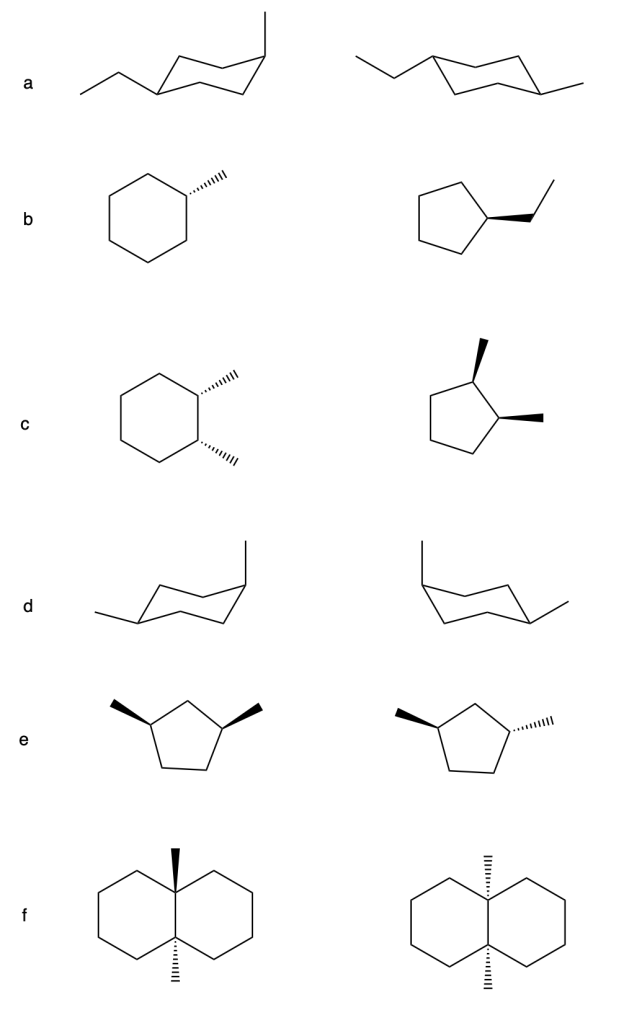
4) Dire quale tra le strutture a-d è un’altra rappresentazione del seguente composto:

5) Scrivi i quattro composti (inclusi gli enantiomeri) di formula molecolare C5H11Br che abbiano almeno un carbonio chirale. Attribuisci il nome, comprensivo di stereochimica, a ciascuno di essi.















You must be logged in to post a comment.