Nomenclatura: Alcoli, Eteri, AMmine


Università degli Studi della Campania "Luigi Vanvitelli"



Ancora esercizi su nomenclatura di alcani e cicloalcani

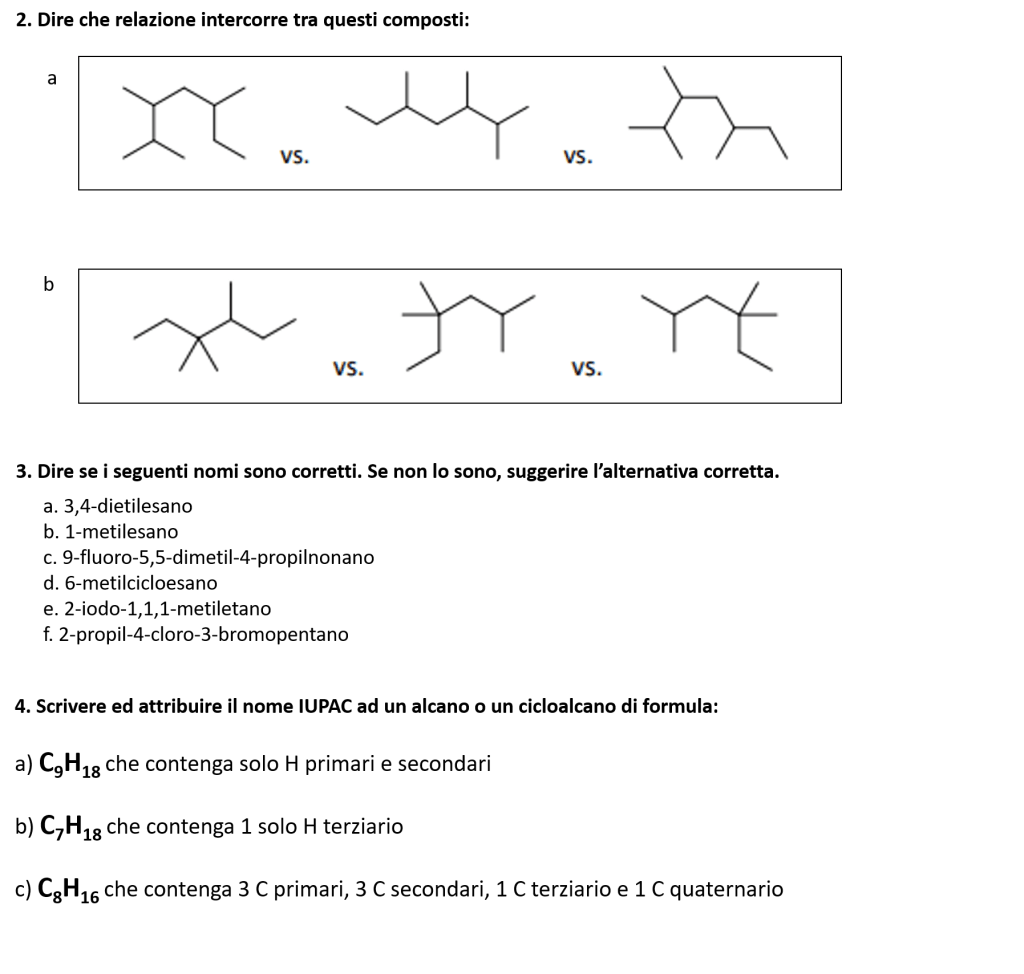
È inoltre possibile anche divertirsi con questi esercizi interattivi: 
ATTENZIONE: Esercizio 4 b) la formula bruta non è C7H18, ma C7H16!

Regolamento:
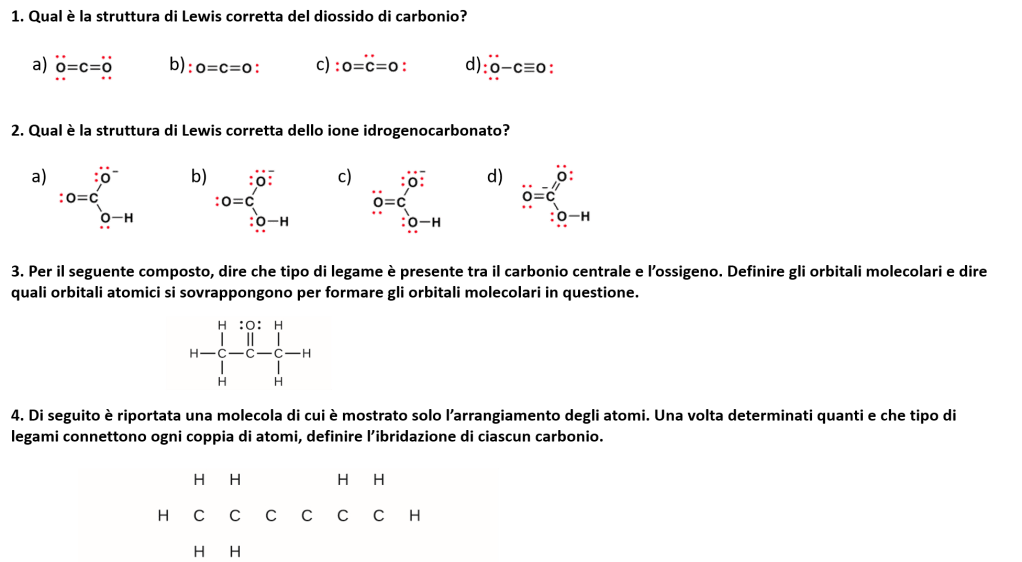
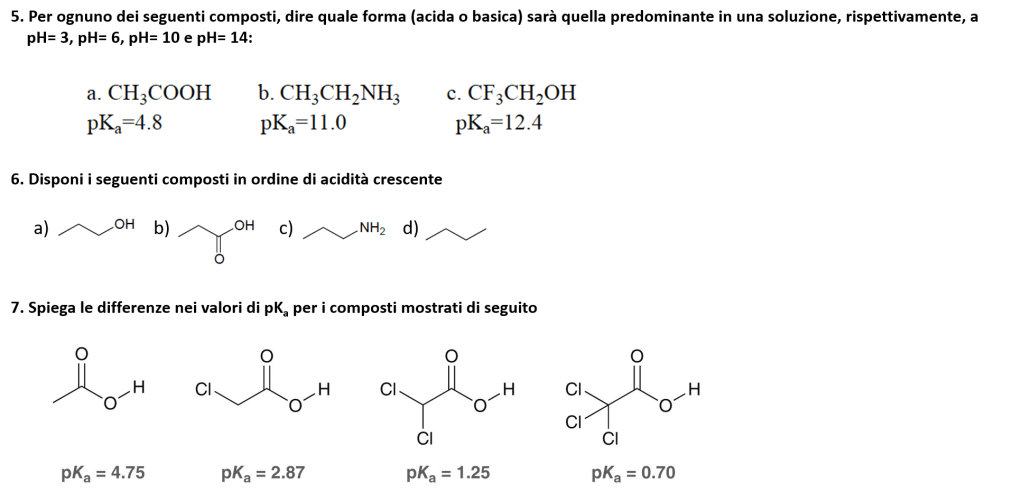

È il momento di esercitarsi su acidi e basi in chimica organica.
Riuscite a risolvere i seguenti quesiti?
NB: È possibile usare la sezione commenti per rispondere, porre domande e discutere!
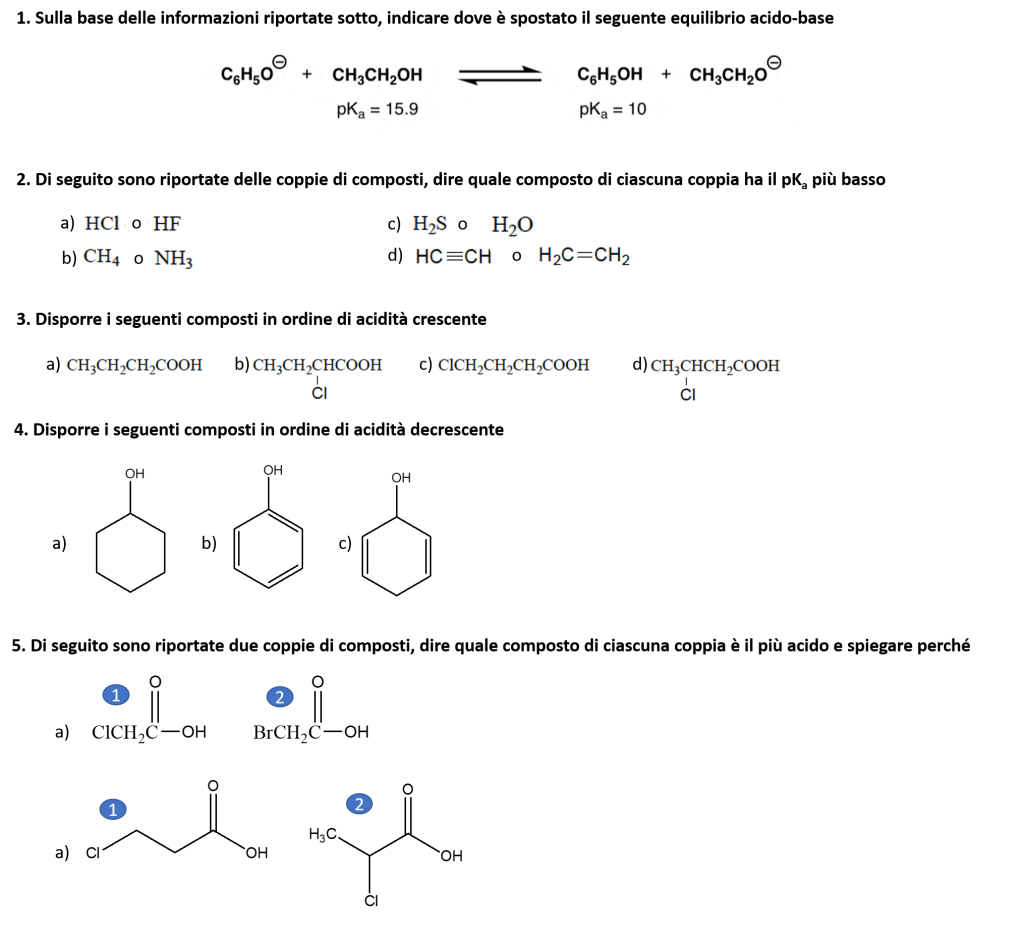


Regolamento:
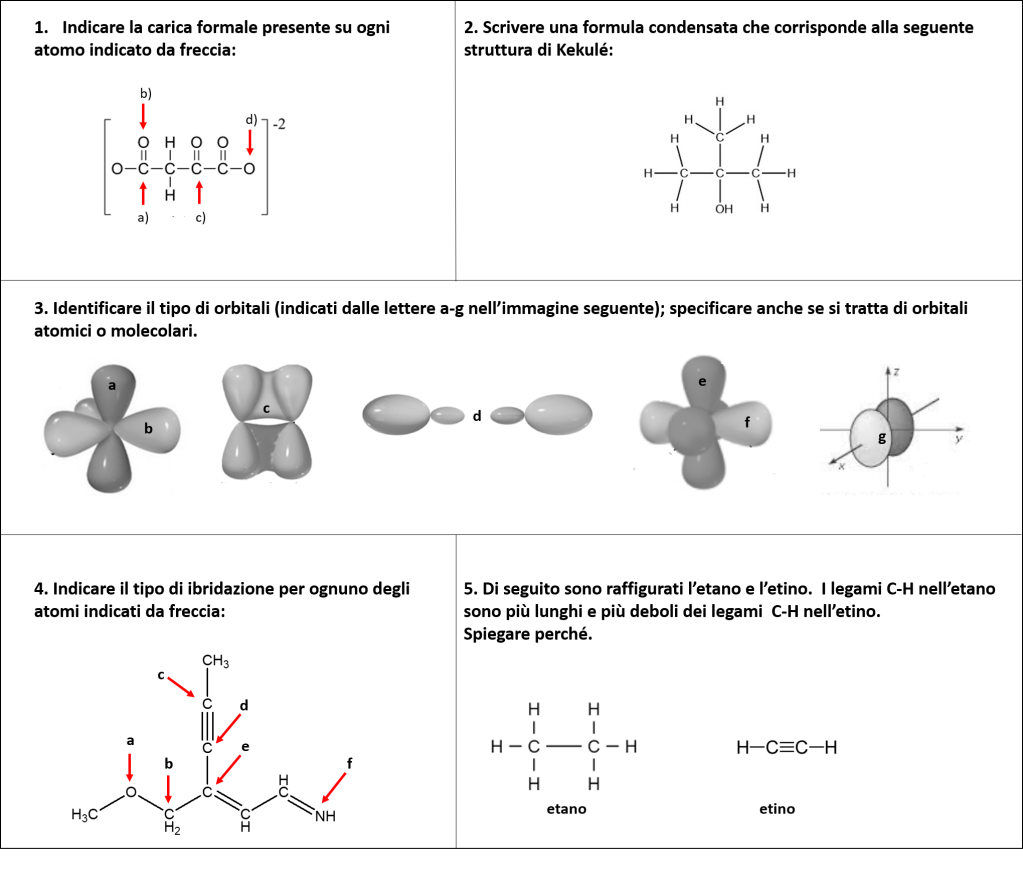

“Scaldiamo i motori” in vista della Weekend Organic Chemistry Challenge!
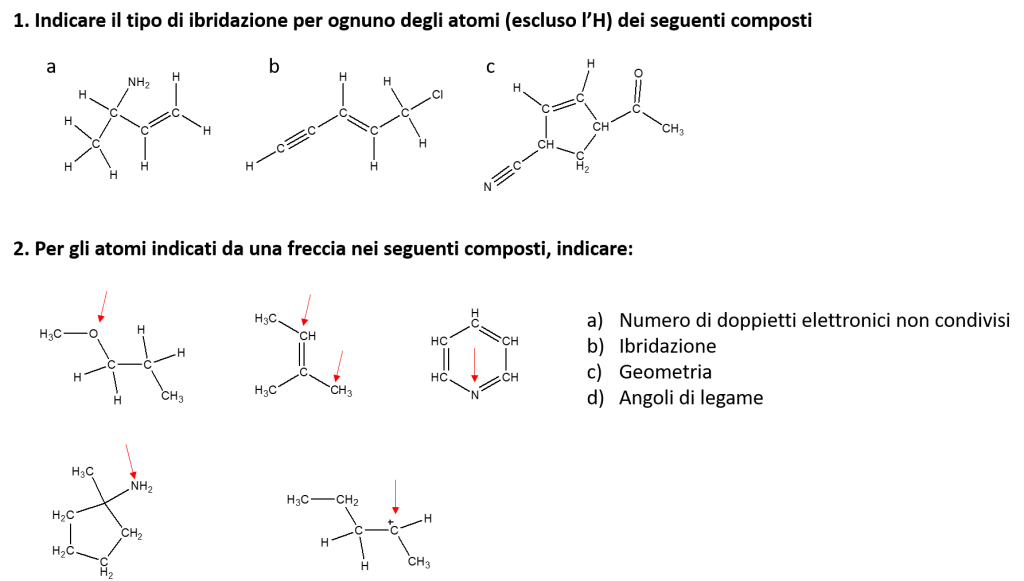
NB: è possibile discutere degli esercizi nell’area commenti!

Una serie di video per visualizzare e capire l’ibridazione del carbonio e la formazione dei legami nei composti organici!
Per chiudere, un apprroccio tecnologicamente meno avanzato, ma sicuramente più divertente…

Come formulare la struttura di Lewis di una specie poliatomica
Fase 1: Contiamo il numero totale degli elettroni di valenza degli atomi che compongono la specie poliatomica. Nel caso di ioni, aggiungere 1 per ogni carica negativa e sottrarre 1 per ogni carica positiva.
Dividendo il numero totale degli elettroni di valenza per due otteniamo il numero delle coppie di elettroni.
Fase 2: Scriviamo i simboli chimici mostrandone la disposizione.
Come scegliere l’atomo centrale? L’atomo centrale è quello dell’elemento dotato della minore energia di ionizzazione. Nelle formule chimiche semplici l’atomo centrale si trova spesso scritto per primo. L’H è sempre un atomo terminale. Se il composto in esame è un ossiacido, gli atomi di H sono legati a quelli dell’O.
Disporre gli atomi simmetricamente intorno a quello centrale.
Fase 3: Collochiamo una coppia di elettroni tra gli atomi di ciascuna coppia.
Fase 4: Completiamo l’ottetto (il doppietto nel caso dell’H) di ciascun atomo collocando tutte le coppie residue intorno agli atomi. Se le coppie di elettroni non sono sufficienti per formare l’ottetto di tutti gli atomi, riordiniamo gli elettroni per formare doppi o tripli legami
Calcolo della carica formale
Carica formale= V- (L+1/2 S)
dove
V= numero di elettroni di valenza
L=numero di elettroni presenti come coppie solitarie
S= numero di elettroni condivisi
Fonte: Principi di Chimica, Atkins e Jones
NB: per una versione più completa e per vari esempi consultare i testi di riferimento sia per la chimica generale sia per la chimica organica.
Di seguito delle risorse online per esercitarci:
Construct a Lewis Structure: scegliendo un composto dal menù a sinistra è possibile esercitarsi a completare le strutture di Lewis. In basso a destra c’è una tabella che ci aiuta col conteggio degli elettroni.
Lewis structure tutorials: esercitiamoci a formulare le strutture di Lewis delle specie poliatomiche in tabella. Cliccando su ogni singola specie è possibile guardare un video esplicativo.
Lewis dot structures: una serie di esercizi. Cliccando su “answers” sarà possibile visualizzare le risposte.



Il corso di Chimica Organica avrà inizio lunedì 12/10/2020 alle 10:40.
Sarà possibile aggiungersi all’aula virtuale Teams utilizzando il seguente codice: 0ylhqe6
You must be logged in to post a comment.