ACIDI E BASI

Esercizio n. 1
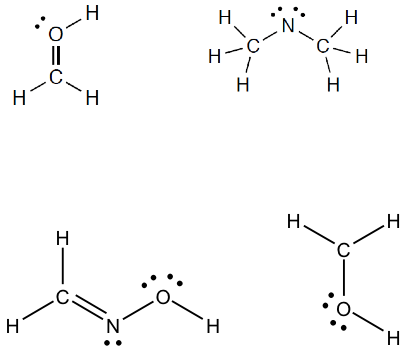
Per ciascuna coppia acido-base coniugati, identificate la prima specie come acido o base e la seconda specie come base o acido coniugato. Inoltre, disegnare per ogni specie le strutture di Lewis, mostrando tutti gli elettroni di valenza e le cariche formali.
(a) HCOOH / HCOO–
(b) NH4+ / NH3
(c) CH3CH2O– / CH3CH2OH
(d) HCO3– / CO32-
(e) H2PO4– / HPO42-
(f) CH3CH3 / CH3CH2–
(g) CH3S– / CH3SH
Esercizio n. 2
Completare le seguenti reazioni di trasferimento protonico utilizzando le frecce curve per mostrare il flusso di elettroni in ogni reazione. Inoltre, indicare le strutture di Lewis per tutti i composti di partenza e per tutti i prodotti. Definire l’acido di partenza e la sua base coniugata, la base di partenza e il sui acido coniugato.
(a) NH3 + HCl —>
(b) CH3CH2O- + HCl —>
(c) HCO3– + OH– —>
(d) CH3COO– + NH4+ —>
Esercizio n. 3
Per ogni reazione di trasferimento protonico completare l’equazione ionica impiegando le frecce curve per indicare il flusso degli elettroni. Indicare l’acido di partenda e la sua base coniugata nonchè la base di partenza e il suo acido coniugato
(a) NH4+ + OH– —>
(b) CH3COO- + CH3NH3+ —>
(c) CH3CH2O– + NH4+ —>
d) CH3NH3+ + OH– —>
Esercizio n. 4
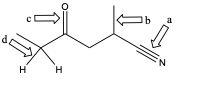
Nell’acido acetico, CH3COOH, l’idrogeno dell’OH è più acido degli idrogeni del CH3. Spiegare il perchè.
Esercizio n. 5
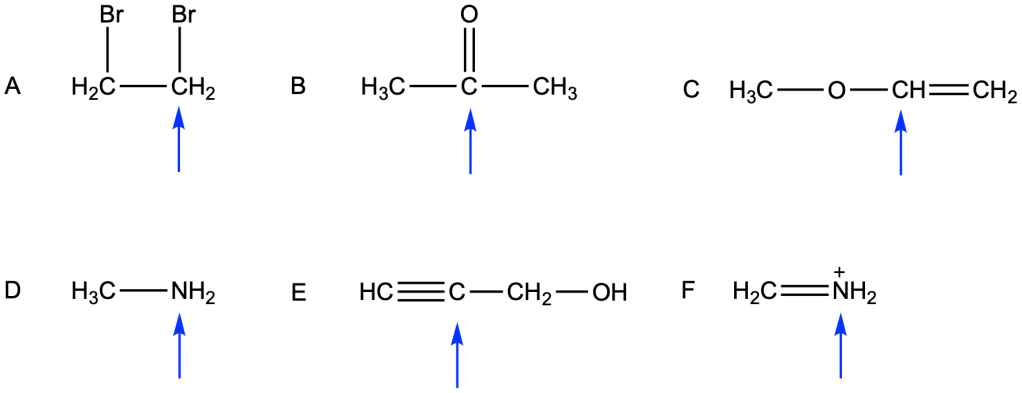
Ciascuna delle seguenti molecole o ioni può funzionare da base. Scrivere la formula di struttura dell’acido coniugato che si forma dalla reazione ddegli stessi con HCl.
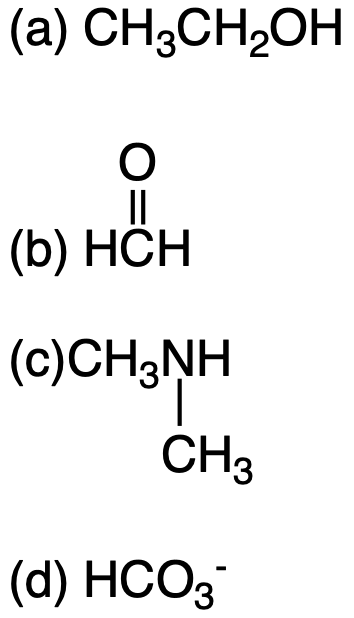
Esercizio n. 6
Disporre i composti seguenti in ordine crescente di forza acida:

Esercizio n. 7
Disporre i composti seguenti in ordine crescente di forza basica:
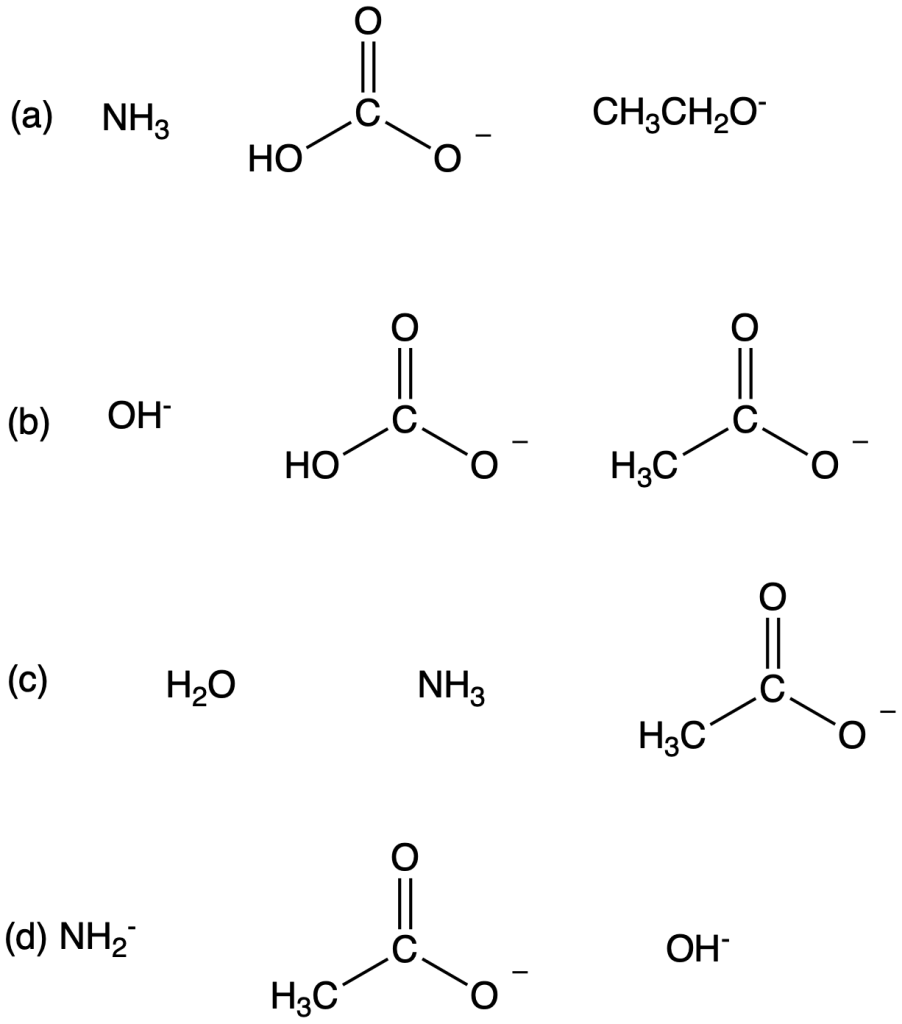
Esercizio n. 8
L’acido acetico è un acido organico debole, pKa 4,76. Scrivere l’equazione della reazione di equilibrio dell’acido acetico con ognuna delle seguenti basi. Indicare dov’è spostato l’equilibrio
(a) NaHCO3
(b) NH3
(c) H2O
(d) NaOH
Esercizio n. 9
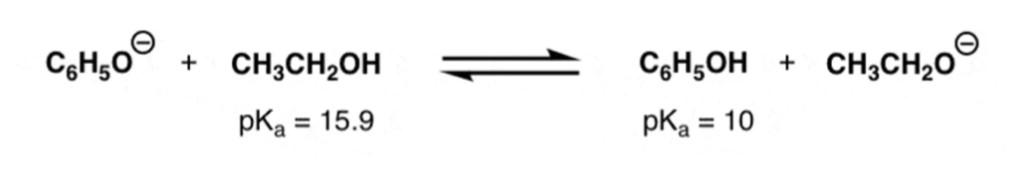
L’acio benzoico, C6C5COOH (pKa 4,19), è solo poco solubile in acqua, ma il suo sale sodico, C6C5COO–Na+, è piuttosto solubile in acqua. Potrà l’acido benzoico sciogliersi in:
(a) NaOH acquoso
(b) NaHCO3 acquoso
(c) Na2CO3 acquoso


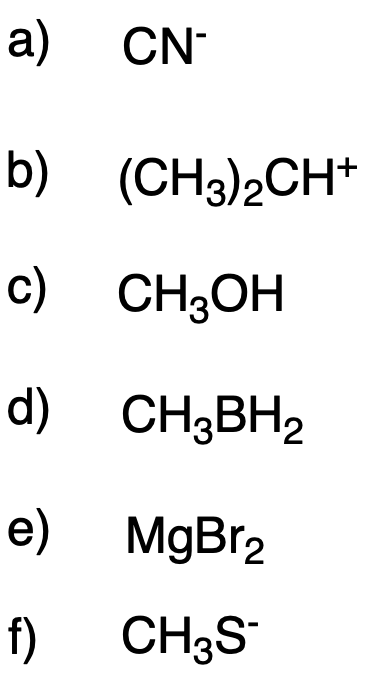

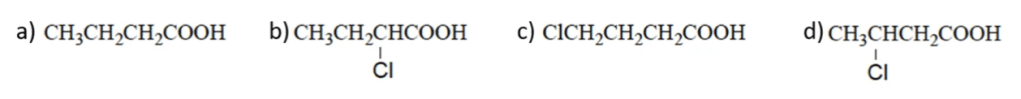
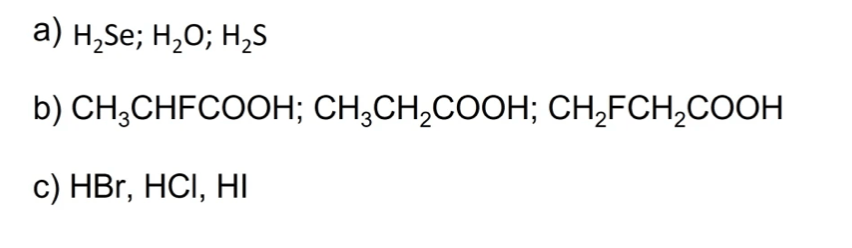
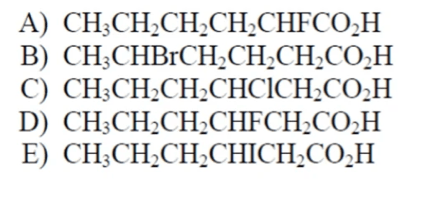














You must be logged in to post a comment.