Concetti importanti 1: Acidi e basi

TUTORIAL: USO DELLE FRECCE
FRECCE CURVE:
- Le frecce rappresentano il movimento simultaneo di due elettroni
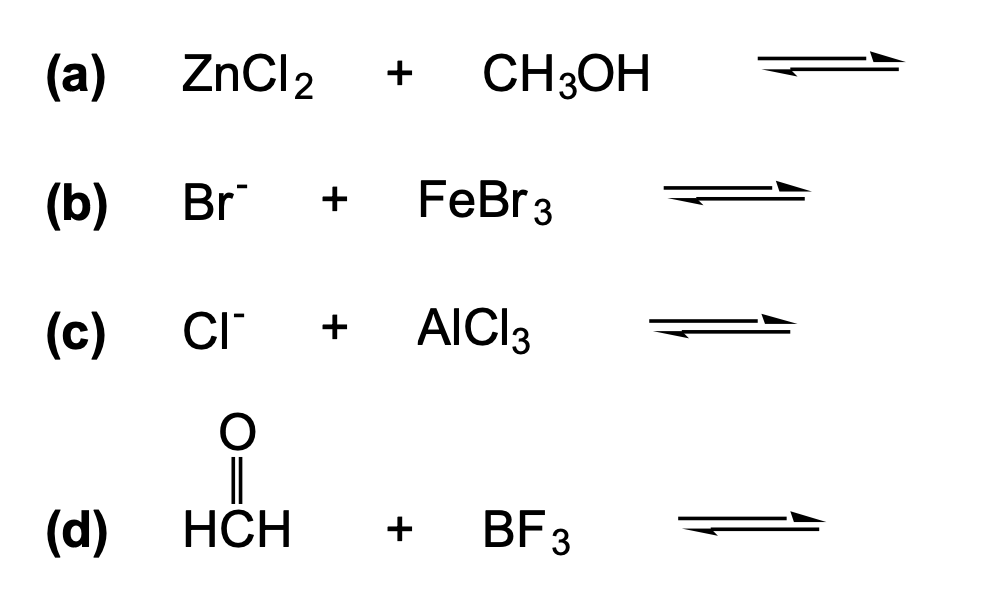
- La coda della freccia è posizionata in corrispondenza degli elettroni nel reagente. Ci sono due fonti di elettroni: (a) un atomo che possiede una coppia solitaria; (b) una coppia di elettroni di legame.
- Gli ioni spettatori vanno ignorati (ioni metallici)
- Disegnare gli idrogeni sugli atomi coinvolti nei legami che cambiano
- Disegnare le coppie solitarie sugli atomi coinvolti nei legami che cambiano
TUTORIAL: ACIDI E BASI
ACIDI E BASI:
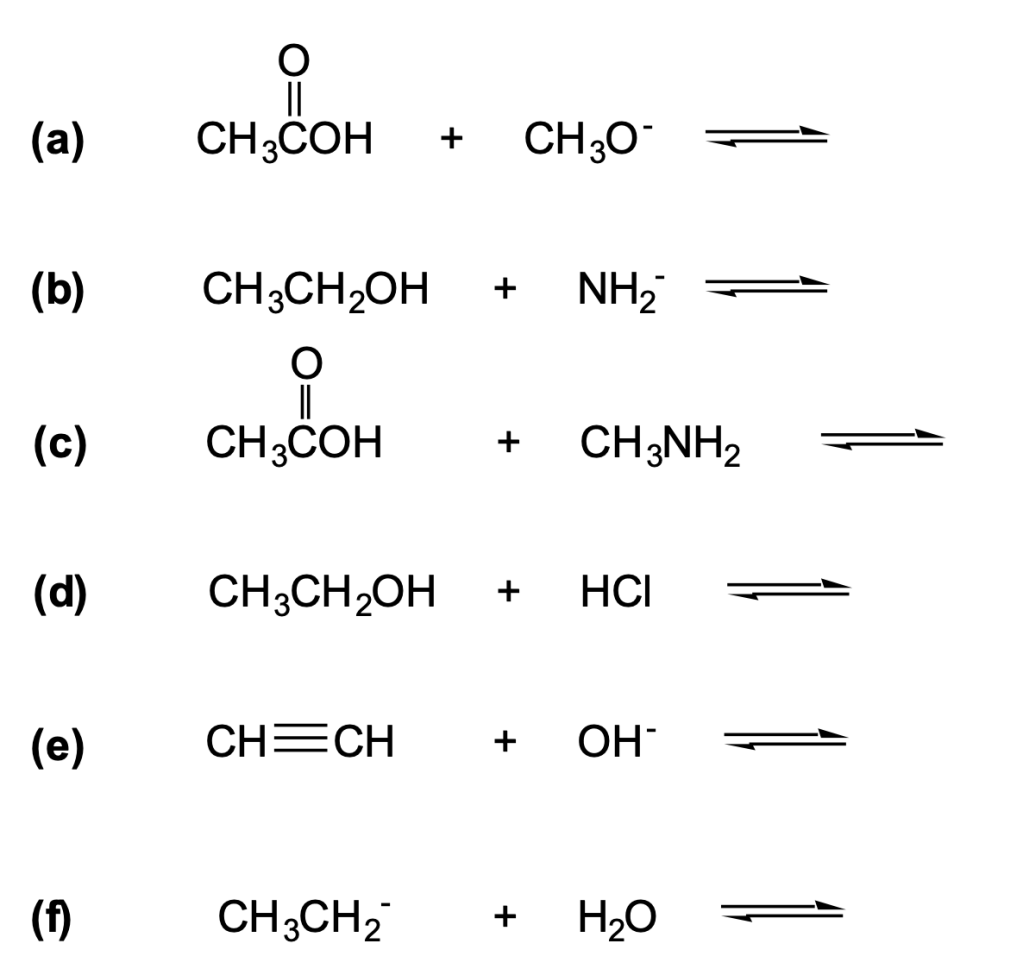
- Un acido è una specie che può perdere un protone (Bronsted-Lowry) trasformandosi così nella sua base coniugata. Quando il protone si allontana dall’acido, la base coniiugata trattiene la coppia di elettroni che legava il protone: la freccia deve partire dal legame tra l’atomo e il protone e deve arrivare sull’atomo.

- Una base è una specie che può ricevere un protone formando così il suo acido coniugato
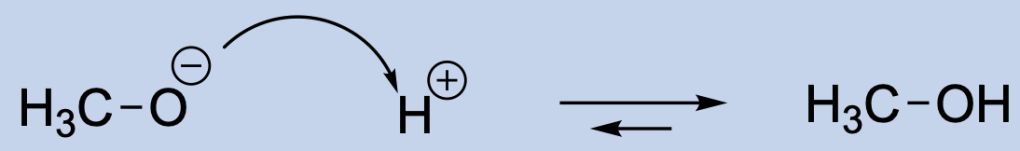
- Un acido non può perdere un protone senza la presenza di una base che lo accetta: un acido reagisce sempre con una base

- Spesso le due specie (acido e base) che reagiscono possiedono entrambe degli idrogeni acidi e delle coppie solitarie: questo significa che entrambe le specie possono comportarsi sia da acido che da base. Per capire chi perde il protone e chi lo acquista, bisogna confrontare i valori di pKa: L’acido che ha il valore di pKa più basso (acido più forte) è la specie che agisce da acido, perdendo un protone.
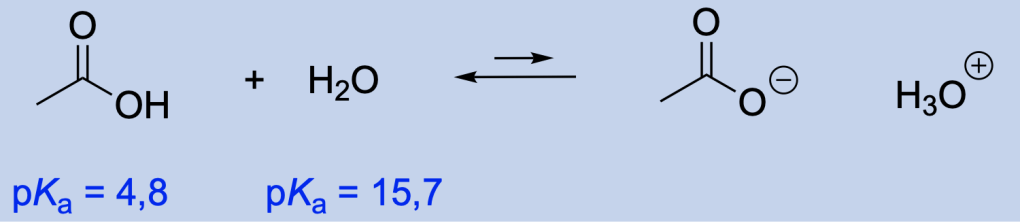
- L’equilibrio favorisca la formazione dell’acido più debole da quello più forte
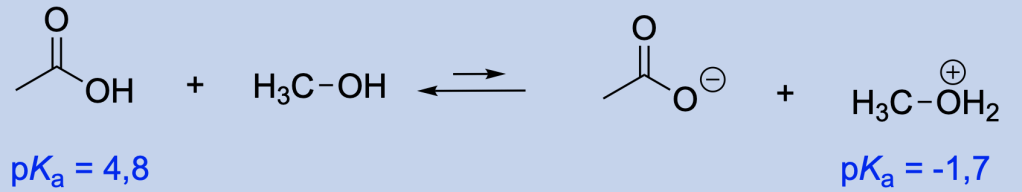
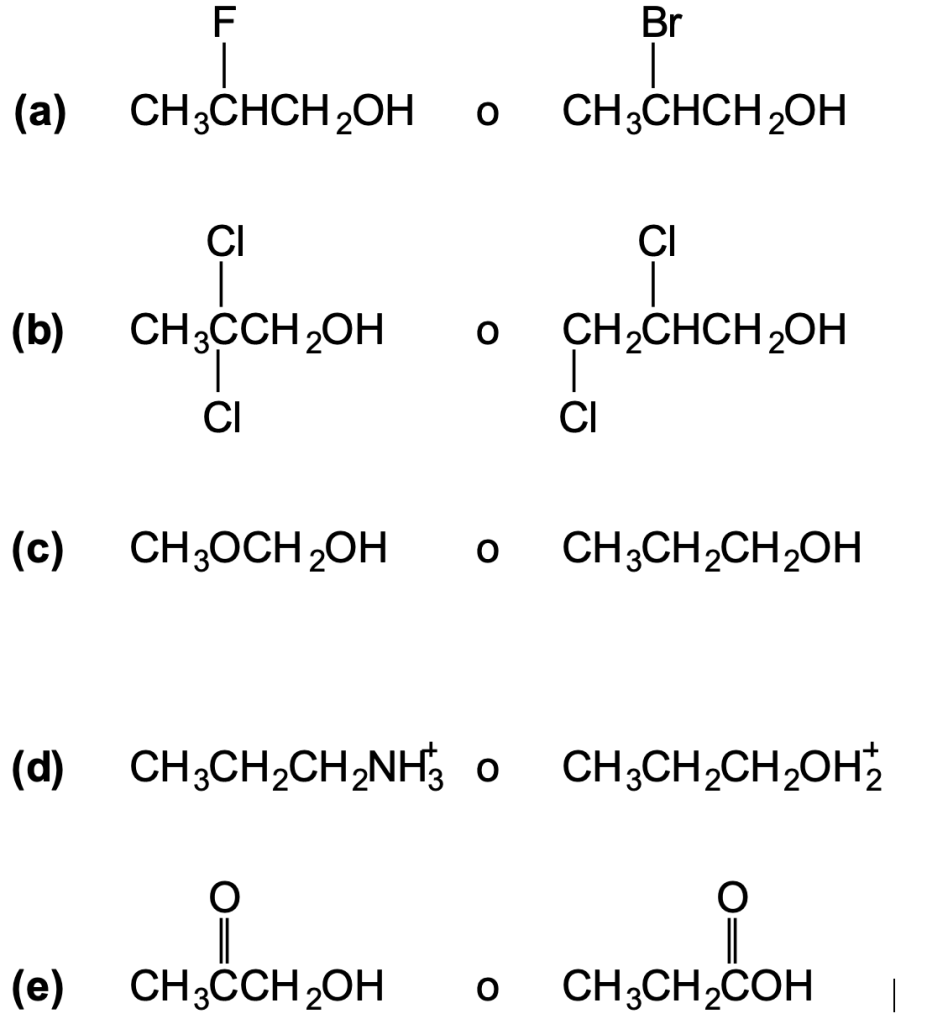
- Quando gli acidi hanno protoni legati ad atomi di dimensioni simili, l’acido più forte è costituito da quello con il protone legato all’atomo più elettornegativo.

- L’elettronegatività di un atomo dipende dalla sua ibridazione; l’acido più forte è quello il cui protone è legato all’atomo più elettronegativo
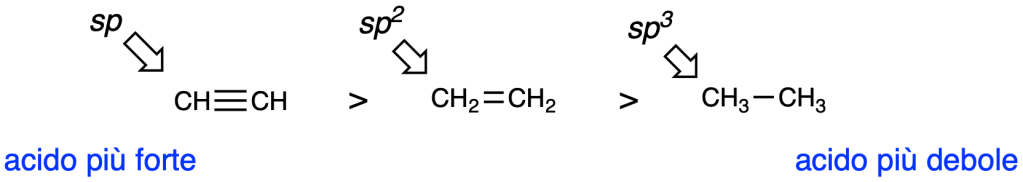
- Quando compariamo due acidi con i protoni legati ad atomi di differenti dimensioni, l’acido più fote risulterà quello nikl cui protone è legato all’atomo più grande

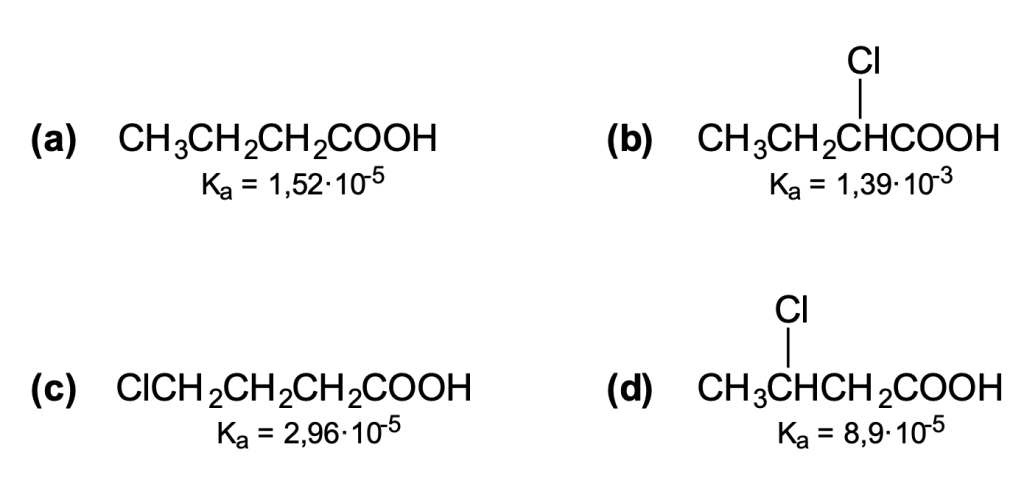
- La sostituzione di un idrogeno con un sostituente elettronegativo, che attira versi di sé gli elettroni di legame, aumenta la forza dell’acido.

















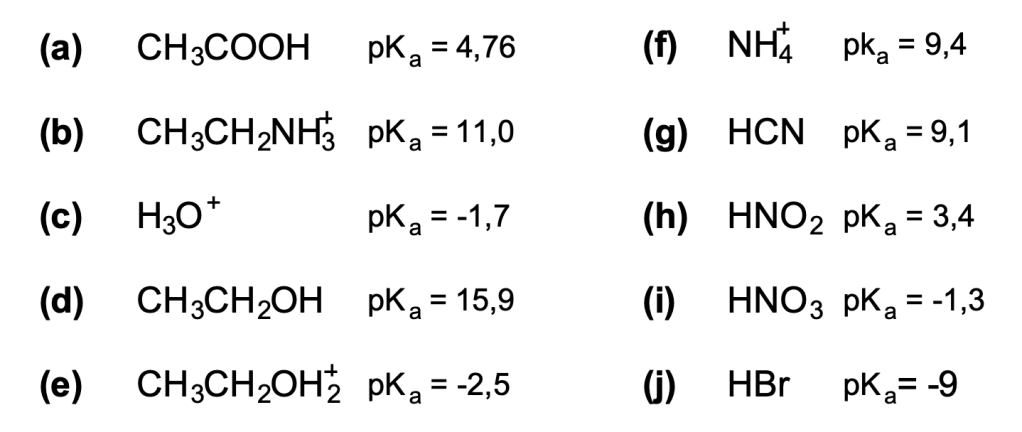
You must be logged in to post a comment.