Alleniamoci per la quarta prova intercorso

Esercizio n. 1
Indicare i prodotti di eliminazione delle seguenti reazioni. Se i prodotti possono esistere come stereoisomeri specificare quali di essi si ottengono.
- (R)-2-bromobutano + HO–
- (R)-2-bromobutano + H2O
- trans-1-cloro-2-metilcicloesano + HO–
- trans-1-cloro-2-metilcicloesano + H2O
- 3-bromo-3-metilpentano+ HO–
- 3-bromo-3-metilpentano + H2O
- (2S,3S)-2-cloro-3-metilpentano + CH3O–
- (2S,3R)-2-cloro-3-metilpentano + CH3O–
- (2R,3S)-2-cloro-3-metilpentano + CH3O–
- (2R,3R)-2-cloro-3-metilpentano + CH3O–
- 3-cloro-3-etil-2,2,-dimetilpentano + CH3O–
Esercizio n. 2
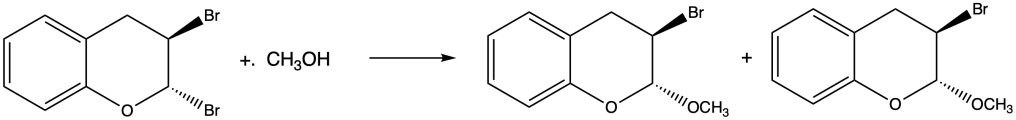
Dalla seguente reazione si ottengono tre prodotti di sostituzione e tre prodotti di eliminazione. Spiegare la formazione di ciascuno di essi.
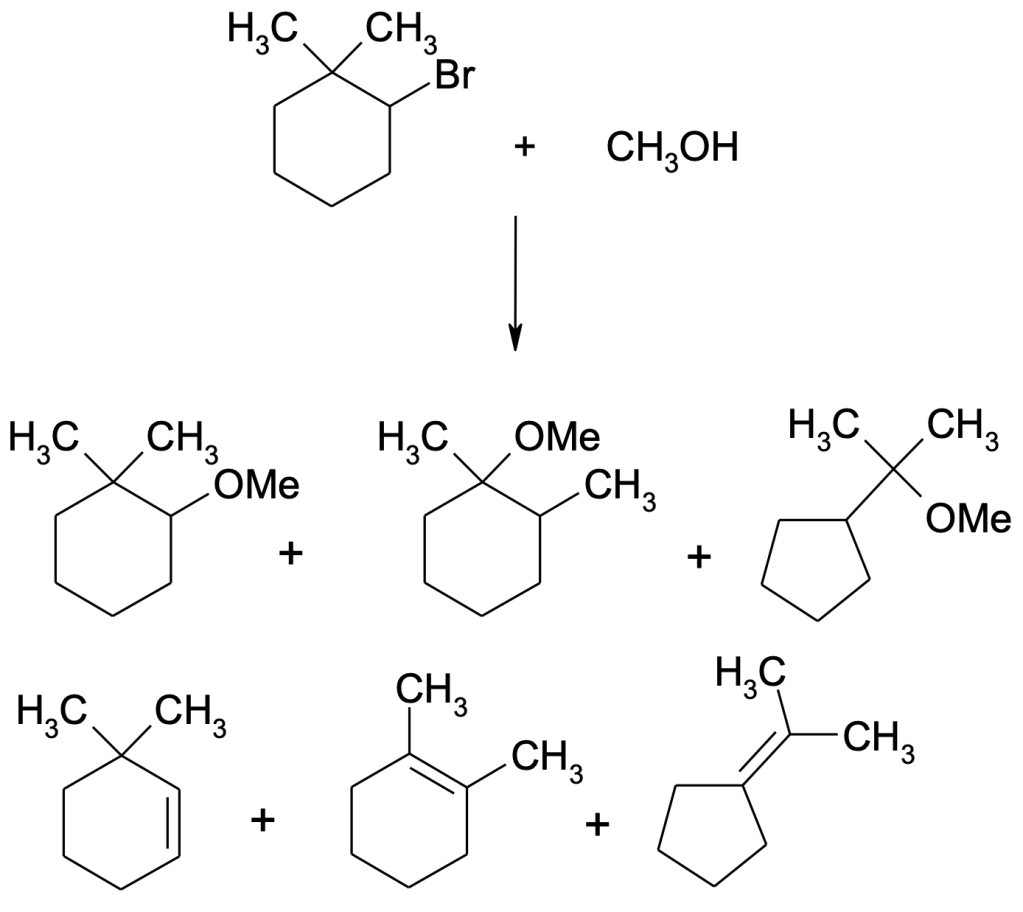
Esercizio n. 3
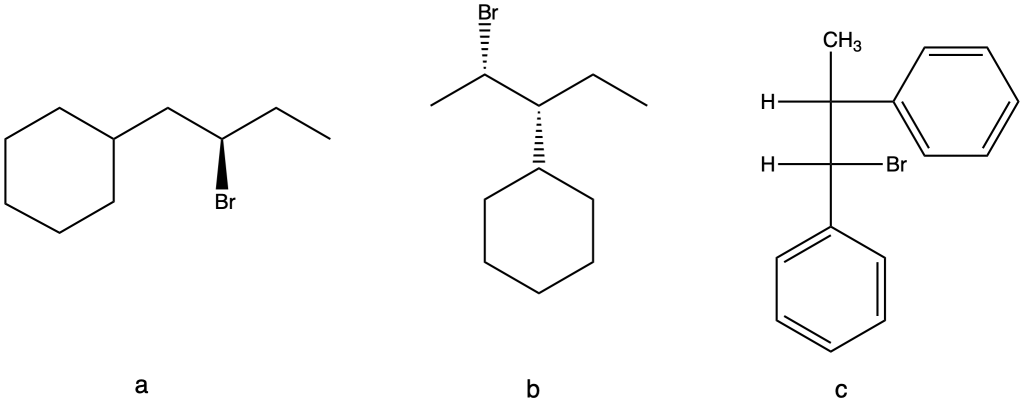
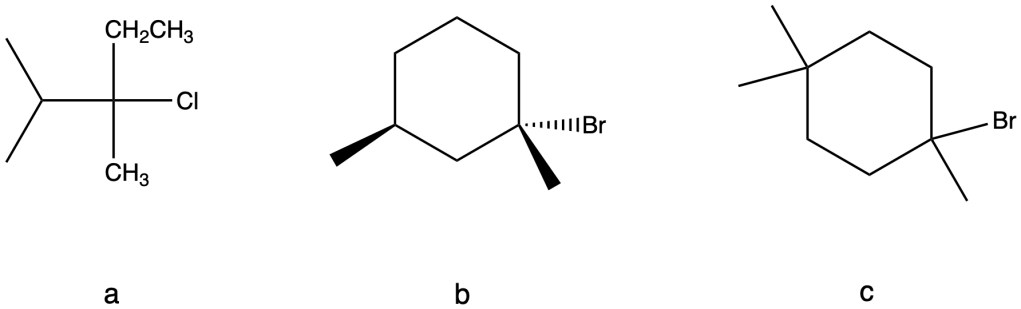
Scrivi le formule di struttura degli alcheni che si formano per trattamento di ciascun alogenuro alchilico con etossido di sodio in etanolo. Assumi che tutte le reazioni avvengano con un meccanismo E2

Esercizio n. 4
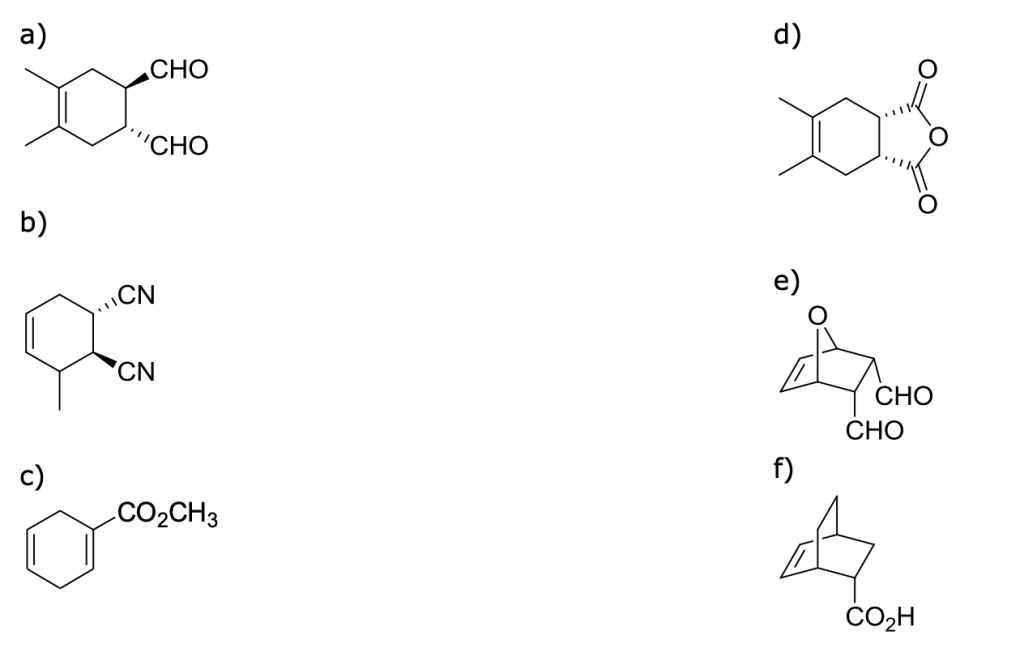
Come si può sintetizzare i seguenti composti a partire da un alogenuro alchilico ed un nucleofilo?
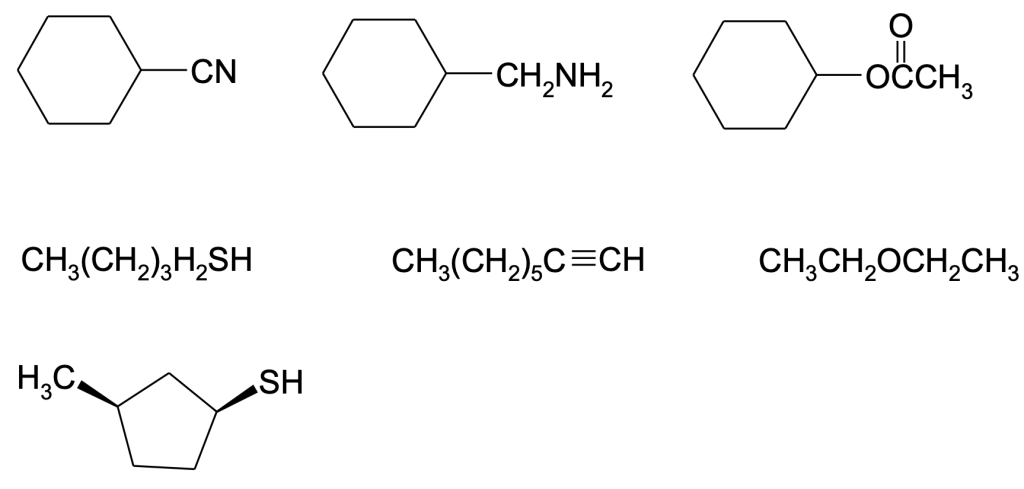
Esercizio n. 5
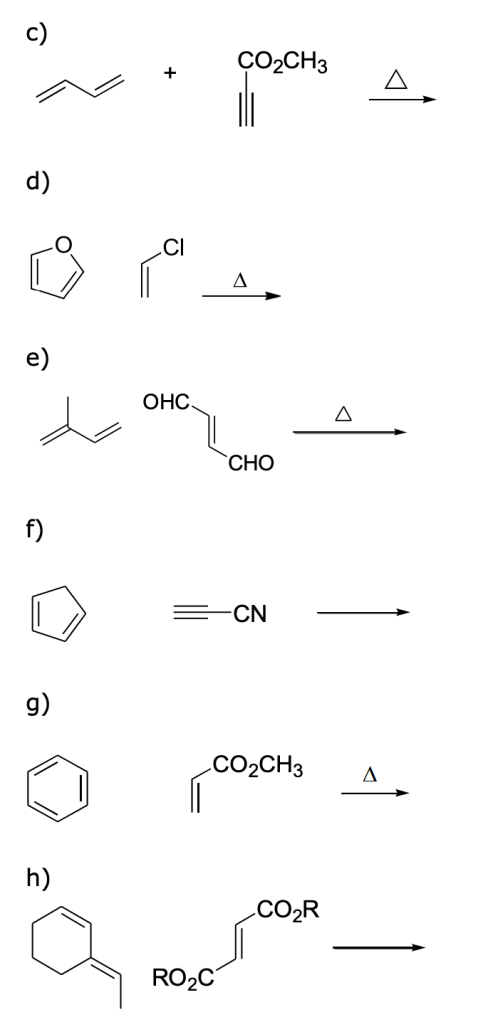
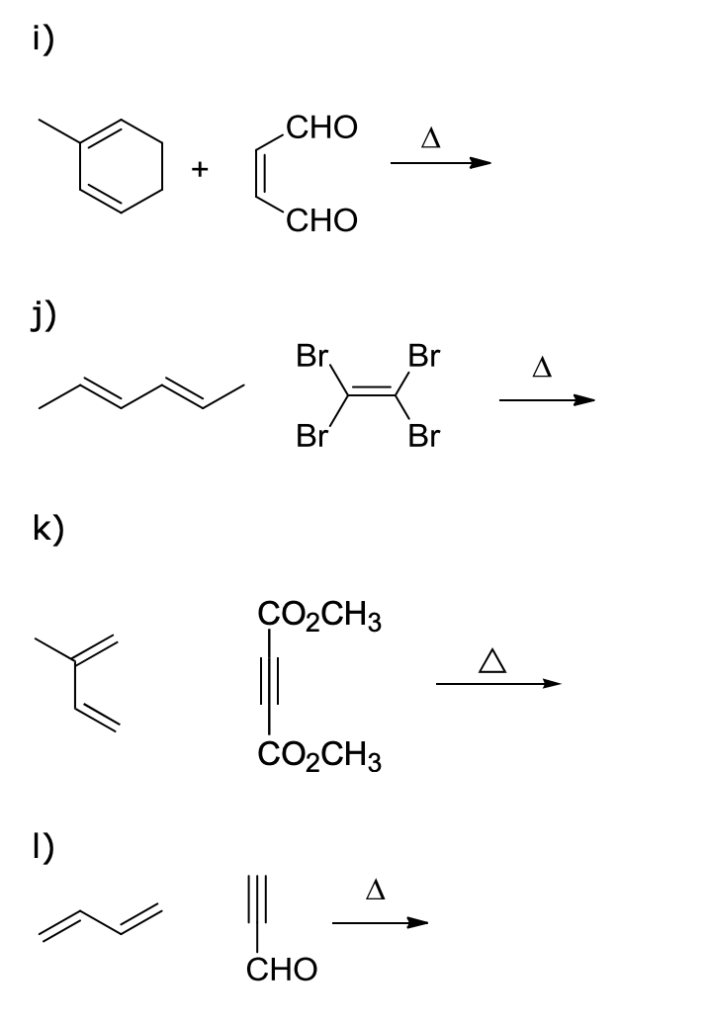
Scrivi la formula di struttura del prodotto organico principale per ognuna delle reazioni e specifica il meccanismo più probabile per la sua formazione

Esercizio n. 6
Quando il cis-4-clorocicloesanolo viene trattato con idrossido di sodio in etanolo, si ottiene solo il prodotto di sostituzione trans-1,4-cicloesandiolo (1). Nelle stesse condizioni di reazione il trans-4-clorocicloesanolo si trasforma nel 3-cicloesenolo (2) e nell’etere biciclico (3).
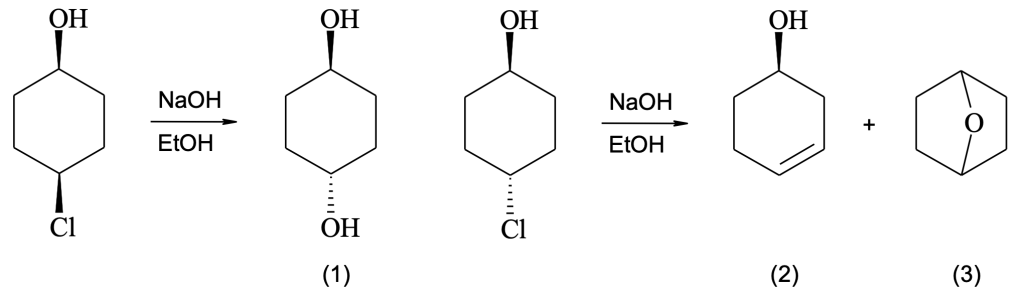
- proponi un meccanismo per la formazione del prodotto (1) e spiega le ragioni della sua configurazione.
- Proponi un meccanismo per la formazione del prodotto (2).
- Spiega la ragione per cui l’etere biciclico (3) si forma dall’isomero trans ma non da quello cis.



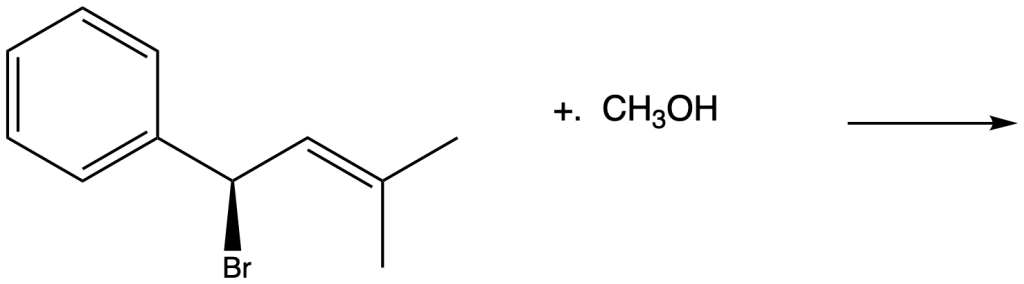


















You must be logged in to post a comment.