SET DI DOMANDE N. 2

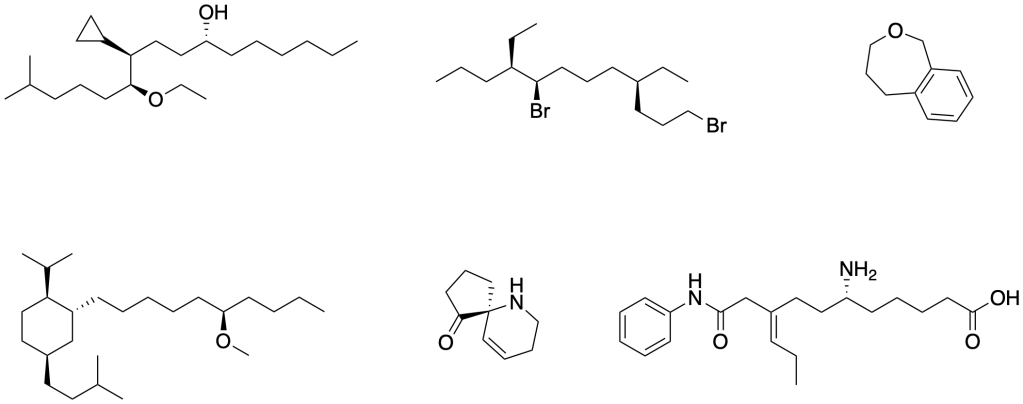
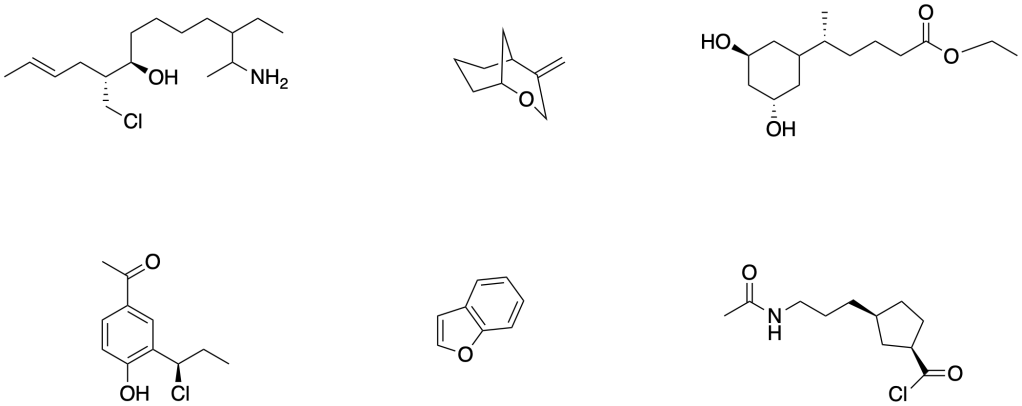
Assegnare il nome IUPAC al seguente composto:

- Scrivere il nome del composto individuando la struttura principale ed assegnando i corretti prefissi a tutti gli altri sulla catena principale.
- Assegnare la configurazione assoluta a tutti i centri stereogenici, spiegando le regole CIP e come sono state applicate
Utilizzando un approccio retrosintetico, progettare la sintesi dell’acido butanoico a partire dall’etilene
Rappresenta i conformeri del (1R,2R,4S)-1-etil-2,4-dimetilcicloesano; usare le proiezioni di Newmann per spiegare le interazioni steriche tra i gruppi alchilici nelle due conformazioni.
Illustrare il meccanismo di reazione della sintesi del 2,4-difenil-3-osso-butanoato di etile a partire da iodobenzene e ossido di etilene
Utilizzando la sintesi in fase solida di Merrifield, sintetizzare il dipeptide aspartilleucina. il gruppo R dell’aspartato è idrossicarbonilmetile; quello della leucina è isobutile.
Imidazolo, tiazolo e ossazolo sono tre composti eterociclici aromatici. Spoiegare perché sono aromatici; in quali orbitali si trovano gli elettroni delle coppie solitarie degli eteroatomi. Qual è il composto più aromatico?






















You must be logged in to post a comment.