Esercizi III e IV Prova intercorso
Gli esercizi della III e IV prova intercorso possono essere consultati qui: https://chimicaorganicadistabif.com/2025/01/07/prova-di-recupero-esercitazione-iv/
Università degli Studi della Campania "Luigi Vanvitelli"
Gli esercizi della III e IV prova intercorso possono essere consultati qui: https://chimicaorganicadistabif.com/2025/01/07/prova-di-recupero-esercitazione-iv/

Gli studenti regolarmente prenotati per la prova di recupero e coloro che sono prenotati per l’esame orale entro il 5/02 hanno ricevuto, via mail (indirizzo email istituzionale), dei link per i questionari da compilare nel caso siano interessati agli incontri in oggetto.
Entrambi i form si chiuderanno sabato 11 Gennaio

I set di esercizi che seguono riportano gli esercizi della terza e quarta prova intercorso.
Per questi set di esercizi è prevista la pubblicazione degli esercizi svolti (pubblicazione che avverrà nel prossimo fine settimana). Questo post è dunque di interesse anche per coloro che hanno superato le prove intercorso.
TERZA PROVA
1. A) Il 2-metil-2-butene reagirà con Br2 in acqua per dare un’aloidrina (ignorare la stereochimica). La reazione ha Keq>1. Mostrare il meccanismo di reazione, inclusi gli stati di transizione. Poi, disegnare il diagramma energetico della reazione. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, intermedio, variazione dell’energia libera di Gibbs, energia di attivazione di ciascuno stadio della reazione.
B) Il 2-metil-2-butene reagirà con Cl2 in acqua per dare un’aloidrina (ignorare la stereochimica). La reazione ha Keq>1. Mostrare il meccanismo di reazione, inclusi gli stati di transizione. Poi, disegnare il diagramma energetico della reazione. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, intermedio, variazione dell’energia libera di Gibbs, energia di attivazione di ciascuno stadio della reazione.
2. Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto utilizzando una reazione di idroborazione/ossidazione. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
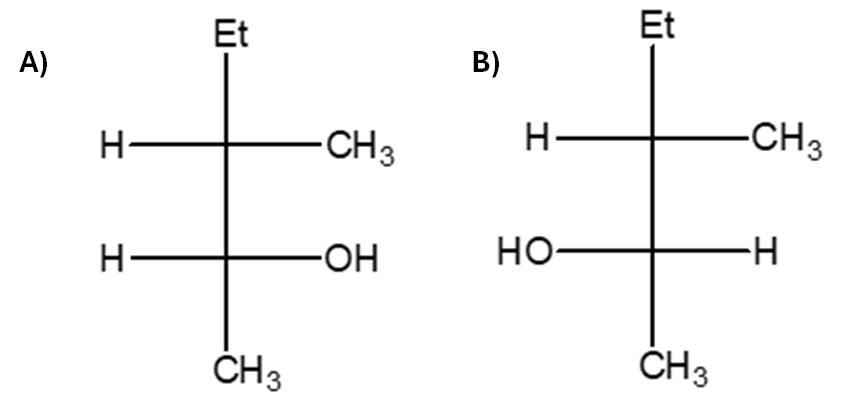
3. Disponi i seguenti composti in ordine di calore di idrogenazione crescente, motivando la scelta
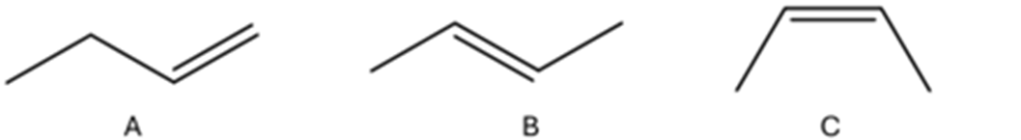
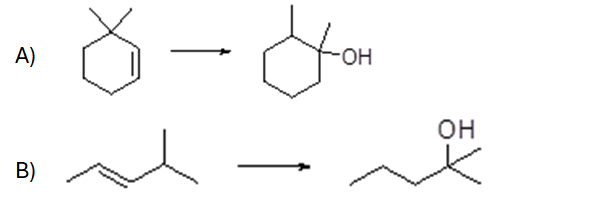
4. Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica, quando opportuno
A)
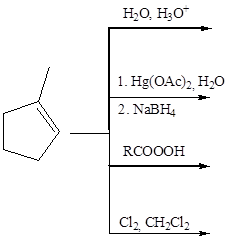
B)
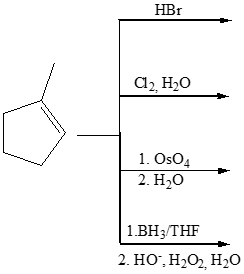
5. Mostrare le condizioni di reazione e il meccanismo della seguente trasformazione (ignorare la stereochimica)
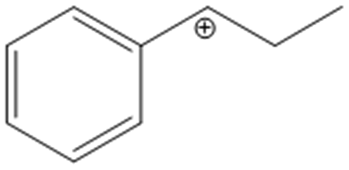
6. A) Scrivere tutte le strutture limite di risonanza del seguente carbocatione
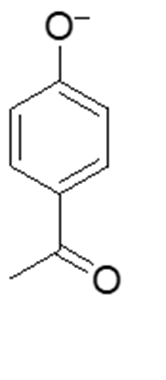
B) Mostrare come il seguente anione è stabilizzato per risonanza
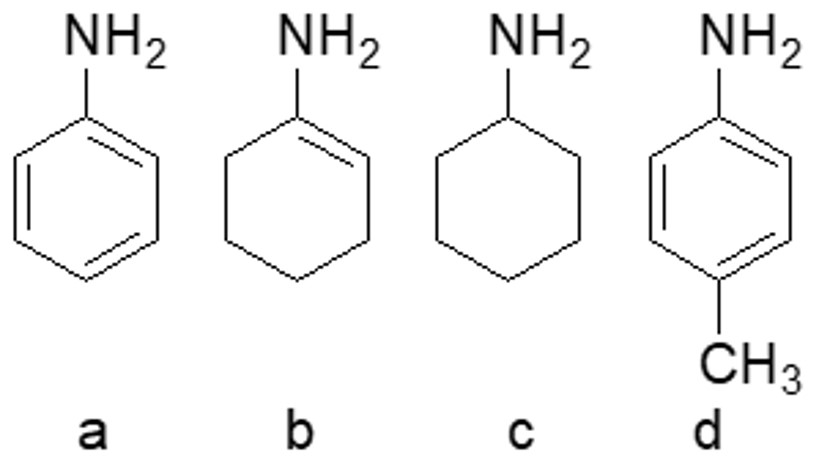
7. A) Disporre i seguenti composti in ordine di basicità crescente e motivare la risposta data
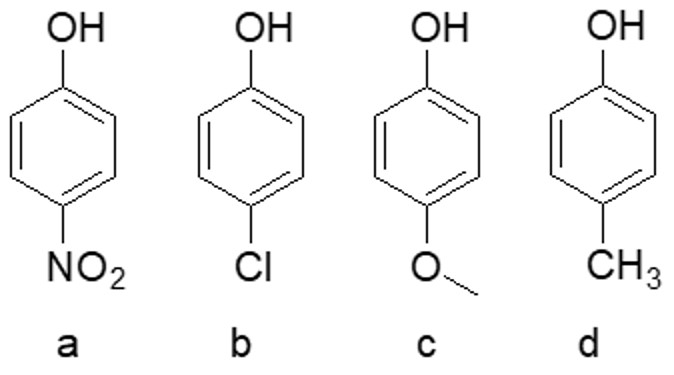
A) Disporre i seguenti composti in ordine di acidità crescente e motivare la risposta data
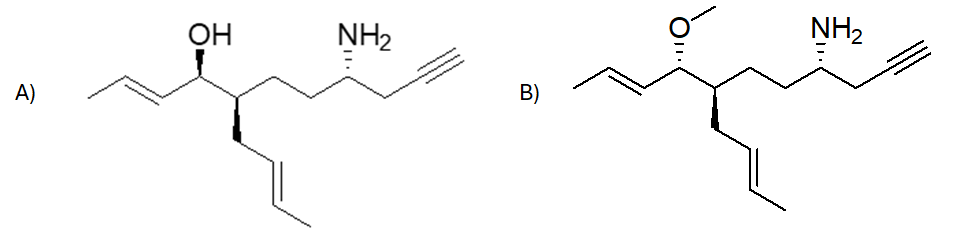
8. Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto
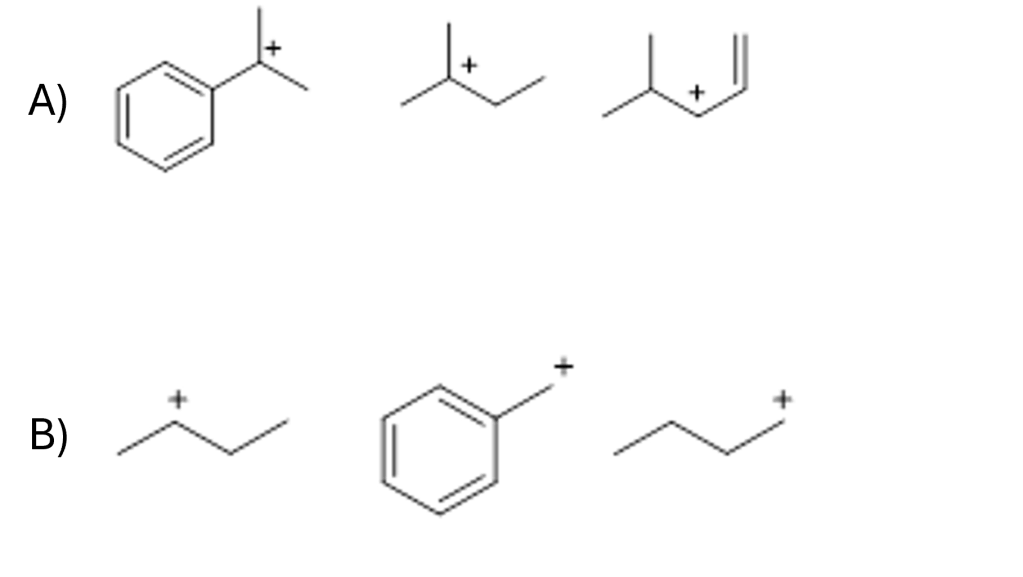
9. Cerchiare il carbocatione più stabile tra i seguenti
QUARTA PROVA
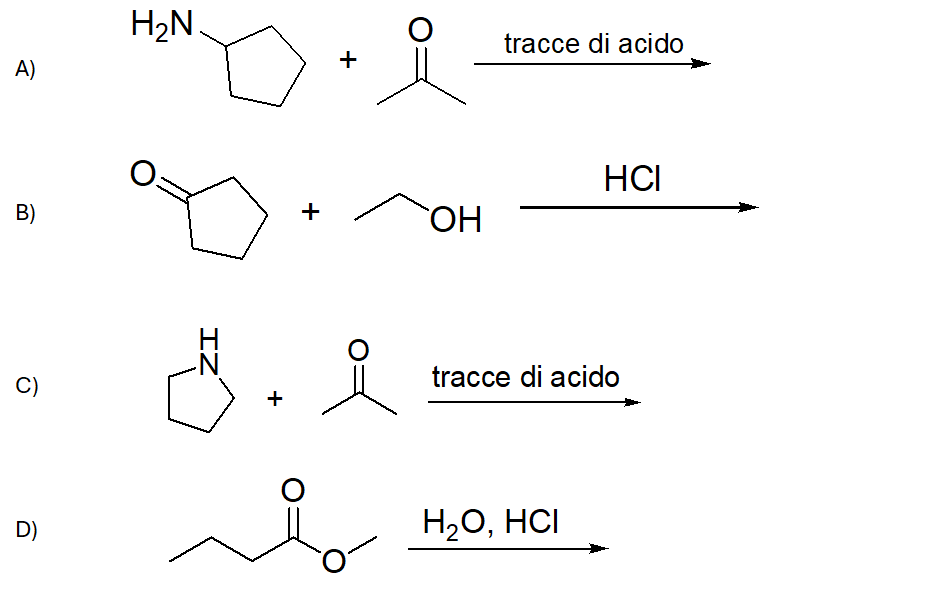
1. Mostrare il meccanismo e i prodotti della seguente reazione:
2. Scrivere i prodotti principali delle seguenti reazioni (se avvengono), indicando la stereochimica quando opportuno. Se la reazione non avviene, scrivere “nessuna reazione”
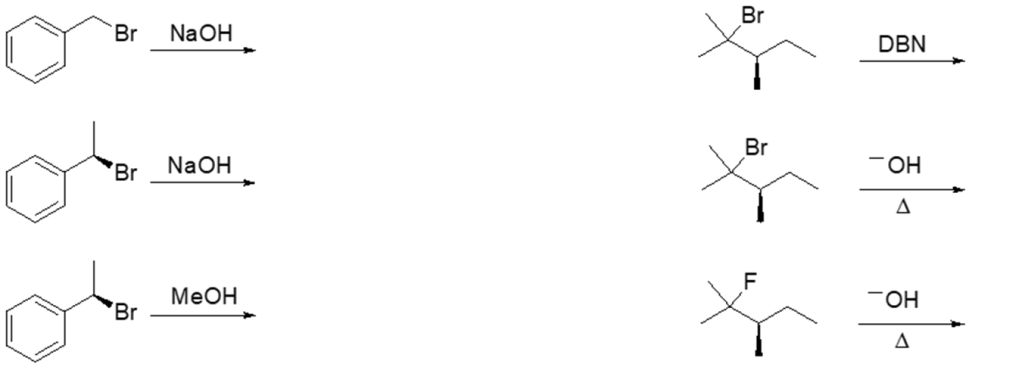
3. Mostrare il meccanismo di apertura del seguente epossido a) con metanolo in ambiente acido; b) con ione metossido. Mostrare la stereochimica dei prodotti. Attribuire il nome IUPAC all’epossido e ai prodotti formati.
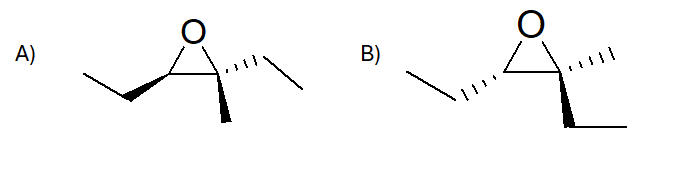
Mostrare il meccanismo di apertura del seguente epossido a) con etanolo in ambiente acido; b) con ione etossido. Mostrare la stereochimica dei prodotti. Attribuire il nome IUPAC all’epossido e ai prodotti formati.
4. A) Spiegate perché il trattamento con base del (1R,2R)-1-bromo-2-metilcicloesano genera il 3-metilcicloes-1-ene, un prodotto di eliminazione non Zeitzev
B) Spiegate perché il trattamento con base del (1S,2S)-1-bromo-2-metilcicloesano genera il 3-metilcicloes-1-ene, un prodotto di eliminazione non Zeitzev
5. Ordina i seguenti composti per reattività crescente in A) un’eliminazione E2; B) una reazione SN2
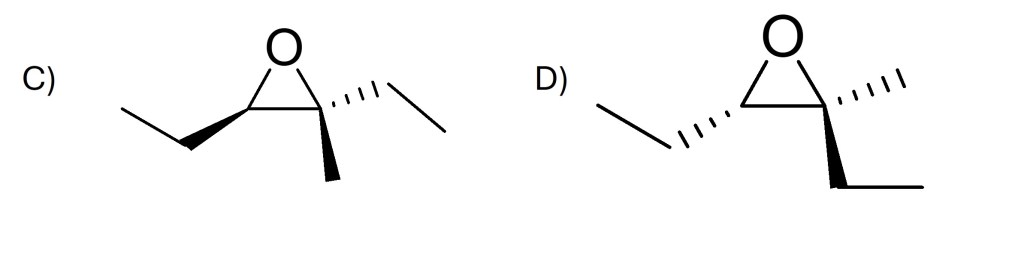
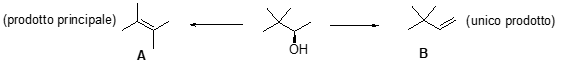
6. Proporre le condizioni e il meccanismo per la formazione degli alcheni A e B
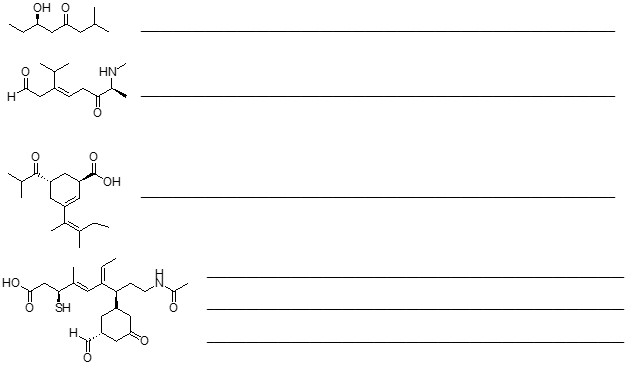
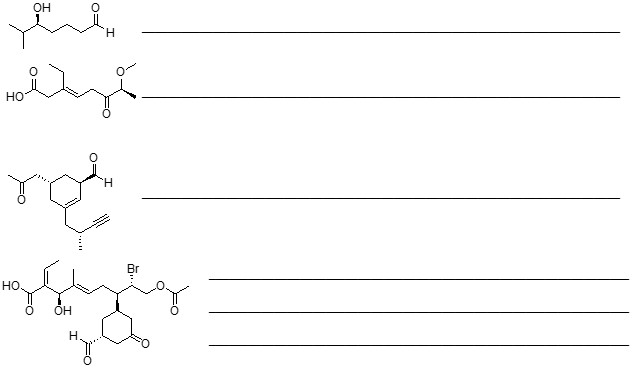
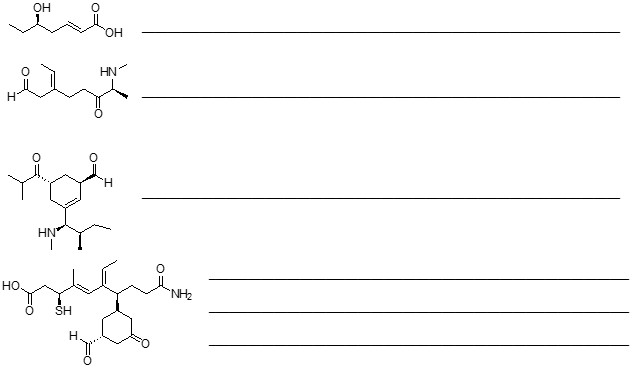
7. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
A)
B)
C)
D)

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 9/01 | 10:00 | VISIONE PROVA | Ufficio Prof. Scognamiglio | Studenti il cui cognome cominci con le lettere comprese tra A e F* |
| 10:30 | VISIONE PROVA | Ufficio Prof. Scognamiglio | Studenti il cui cognome cominci con le lettere comprese tra G e M* | |
| 11:00 | VISIONE PROVA | Ufficio Prof. Scognamiglio | Studenti il cui cognome cominci con le lettere comprese tra N e Z* |
*NB: l’appuntamento è valido SOLO per gli studenti che si sono regolarmente prenotati utilizzando l’apposito form (https://chimicaorganicadistabif.com/2025/01/05/ricevimento-di-gruppo-del-9-gennaio-e-reminder-prenotazioni/). La prenotazione è possibile fino alla giornata di domani.
Non sarà invece prevista l’esercitazione/ricevimento di gruppo, dato che solo 1 persona ha risposto al form dedicato. Lo studente in questione potrà prenotarsi per il ricevimento per chiarire i dubbi esposti.
Nel corso della settimana, gli studenti prenotati per le prove di recupero riceveranno una mail con un link con un questionario cui dovranno rispondere in vista delle esercitazioni di recupero.
Gli studenti prenotati per l’esame orale entro il 5 Febbraio riceveranno invece un link con un questionario in preparazione all’incontro pre esame orale del 15 gennaio.
Le comunicazioni saranno inviate alle email istituzionali (studenti.unicampania.it)
Anche in questi casi, in assenza di un numero sufficiente di risposte, le esercitazioni/incontri non si terranno.
I questionari saranno utilizzati per definire il programma degli incontri che saranno, però, aperti a tutti, non solo a coloro che compileranno i questionari.

LA PROVA SI TERRA’ IL GIORNO 27 GENNAIO 2025 ALLE ORE 15:00
Le prenotazioni potranno esserer fatte, a partire dalle ore 17 del 6 gennaio fino alle ore 18 del 25 gennaio, al seguente link


Di seguito sono riportati i risultati della prima prova intercorso.
Gli studenti identificati con il colore verde hanno superato la prova con sufficienza (verde scuro voti più alti) e sono ammessi a sostenere le prove intercorso del secondo semestre. I risultati della quarta prova sono indicati nella seconda colonna; nella prima colonna, la media delle quattro prove.
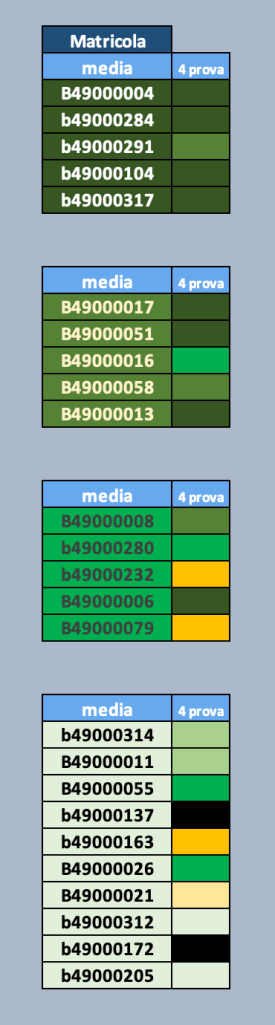
Gli studenti identificati dai colori giallo e arancione hanno superato con riserva. Anche gli studenti che hanno superato con riserva sono ammessi a sostenere le prove intercorso del secondo semestre. I risultati della quarta prova sono indicati nella seconda colonna; nella prima. colonna, la media delle tre prove.

Per gli studenti indicati dai colori rosso, di seguito riportati, la prova si intende non superata.

Tutti gli studenti frequentanti, che non hanno superato le prove intercorso, hanno la possibilità di prenotarsi per sostenere una prova intercorso di recupero su tutti gli argomenti trattati nel primo semestre.
LA PROVA SI TERRA’ IL GIORNO 27 GENNAIO 2025 ALLE ORE 15:00
Le prenotazioni potranno esserer fatte, a partire dalle ore 17 del 6 gennaio fino alle ore 18 del 25 gennaio, al seguente link


Come già sapete, da calendario è previsto un ricevimento di gruppo per il 9 gennaio 2025.
In quella sede, sarà possibile:
Vi ricordo, inoltre, le seguenti scadenze:

Nel testo di riferimento (il Bruice) alcuni meccanismi non sono esplicitati (o in alcuni casi non lo sono per esteso), data la somiglianza con altri meccanismi (o per il fatto che si tratta di meccanismi già spiegati altrove).
Qui troverete un elenco di questi meccanismi con indicazioni su dove trovarli o con spiegazioni relative alla loro estrapolazione da meccanismi già presenti sul libro:
Sintesi di Gabriel: Dopo aver sintetizzato l’immide N-sostituita, questa deve essere idrolizzata. Ci sono diversi metodi per ottenere questa idrolisi, quello indicato sul testo è l’idrolisi in ambiente acido. Il meccanismo ricorda quello dell’idrolisi di un’ammide catalizzata da acidi (la cui spiegazione potete utilizzare a supporto della comprensione del meccanismo qui riportato; NB: per visualizzare i commenti ai singoli passaggi, è necessario scaricare il file pdf).
Transesterificazione catalizzata da acidi: meccanismo identico all’idrolisi dell’estere catalizzata da acidi. Il meccanismo per esteso è presente nel file delle correzioni degli esercizi su Reazioni di sostituzione nucleofila acilica (Ex 1a). Per la spiegazione relativa ad ogni passaggio, far riferimento al meccanismo di idrolisi dell’estere catalizzata da acidi.
Transesterificazione favorita da base: meccanismo identico all’idrolisi dell’estere favorita da ione idrossido. Il meccanismo per esteso è presente nel file delle correzioni degli esercizi su Reazioni di sostituzione nucleofila acilica (Ex 1e). Per la spiegazione relativa ad ogni passaggio, far riferimento al meccanismo di idrolisi dell’estere favorita da ioni idrossido.
Esterificazione di Fischer: il meccanismo è l’esatto contrario del meccanismo di idrolisi dell’estere catalizzata da acidi. Esso è presente nel file delle correzioni degli esercizi su Reazioni di sostituzione nucleofila acilica (Ex 4c). Per la spiegazione relativa ad ogni passaggio, far riferimento al meccanismo di idrolisi dell’estere catalizzata da acidi (ovviamente tenendo conto che si tratta del meccanismo inverso).
Idrolisi di un nitrile catalizzata da acidi: il meccanismo è riportato sul libro, ma ad un certo punto, dopo la formazione dell’ammide protonata, si fa riferimento ad “alcuni stadi”. Questi stadi non sono altro che quelli descritti nel meccanismo di idrolisi di un’ammide catalizzata da acidi (pag. 712, a partire dal secondo passaggio).
Reazioni delle anidridi con acqua (idrolisi) e ammine: scaricare il file qui
Idrolisi immina: il meccanismo corrisponde alla reazione inversa rispetto alla sintesi dell’immina (ma fare attenzione alla irreversibilità dell’idrolisi, a causa delle condizioni di reazione–> vedi spiegazione a pag. 762) ed è esplicitato nel file relativo agli esercizi svolti del post relativo alle Biomolecole (Ex 6, ultima fase della sintesi di Kiliani-Fischer; nel consultare il file, prestare attenzione anche ai commenti, dato che nella figura c’è un errore relativo alla freccia dell’ultimo passaggio, che viene chiarito proprio nei commenti).
Idrolisi emammine: scaricare il file qui. Valgono le stesse considerazioni fatte per l’idrolisi dell’immina.
Idrolisi acetale: il meccanismo corrisponde alla reazione inversa rispetto alla sintesi dell’acetale ed è esplicitato sul libro nella “strategia per la risoluzione dei problemi” a pag. 771.
Meccanismo di ciclizzazione degli zuccheri: riportato nel file relativo alla correzione degli esercizi sulle Biomolecole (Ex 2).
Sintesi di Kiliani-Fischer: Si tratta di reazioni già note, in ogni caso i meccanismi per esteso sono riportati nel file relativo alla correzione degli esercizi sulle Biomolecole (Ex 6). Per le spiegazioni è possibile far riferimento ai paragrafi del libro in cui sono spiegati i singoli meccanismi.
Sintesi dei peptidi: Pur essendo i meccanismi coinvolti riportati sul libro, come chiarito a lezione, alcuni passaggi sono sottintesi. Un meccanismo più dettagliato è riportato nel file relativo alla correzione degli esercizi sulle Biomolecole (Ex 13). Da integrare con le spiegazioni presenti sul testo. Per l’ultimo passaggio (idrolisi con acido trifluoroacetico) non è richiesto il meccanismo.
Per finire, qui troverete la slide relativa allo ione tropilio (catione aromatico).
Utilizzando questo form è possibile segnalare eventuali meccanismi per cui non si ha ancora a disposizione materiale sufficiente. NB: Consultare attentamente il libro e il materiale caricato sul blog (incluse le correzioni degli esercizi) PRIMA dell’eventuale compilazione del form, che si chiuderà il 14/01.

Esercitazione destinata agli studenti che dovranno sostenere la seconda prova di recupero.
Suggerimento: per poter usare questi esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore.
Altri set di esercizi saranno pubblicati successivamente.
PRIMO SET
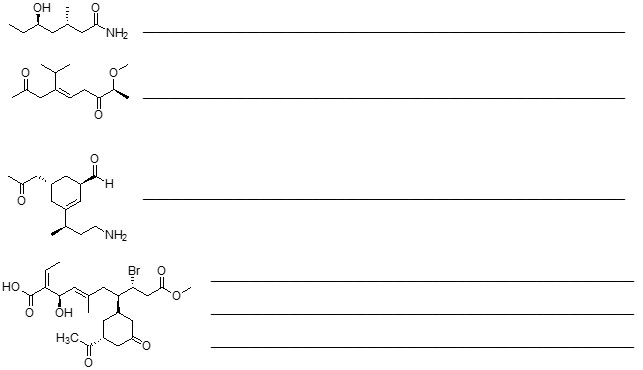
1. Attribuire il nome IUPAC, comprensivo di stereochimica (se indicata), ai seguenti composti
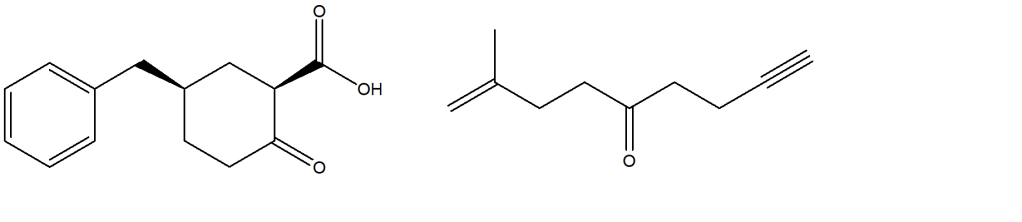
2) Mostrare una strategia per ottenere la seguente trasformazione. Mostrare anche i meccanismi di reazione

3) Scrivere i prodotti principali delle seguenti reazioni (indicare la stereochimica quando opportuno)

4) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione di idrolisi del butanoato di etile
5) Indicare le condizioni di reazione ottimali per ottenere le seguenti trasformazioni:

6) Disporre i seguenti composti in ordine di acidità decrescente, motivando la risposta

7) Mostrare le condizioni, il meccanismo e i prodotti della seguente reazione:
SECONDO SET
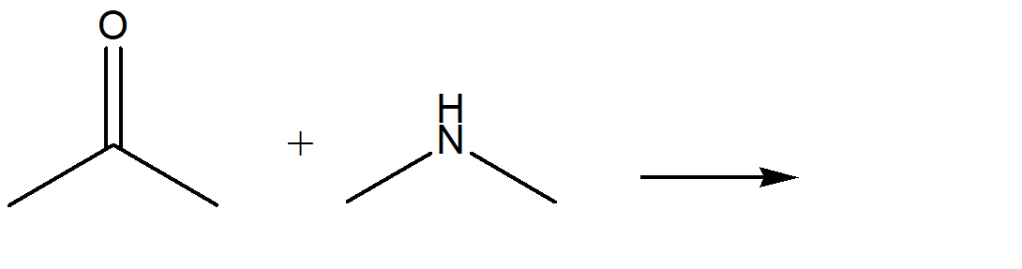
1) Mostrare le condizioni, il meccanismo e i prodotti della seguente reazione:

2) Fornire un meccanismo plausibile per la seguente trasformazione (indicare le condizioni di reazione e mostrare il meccanismo)

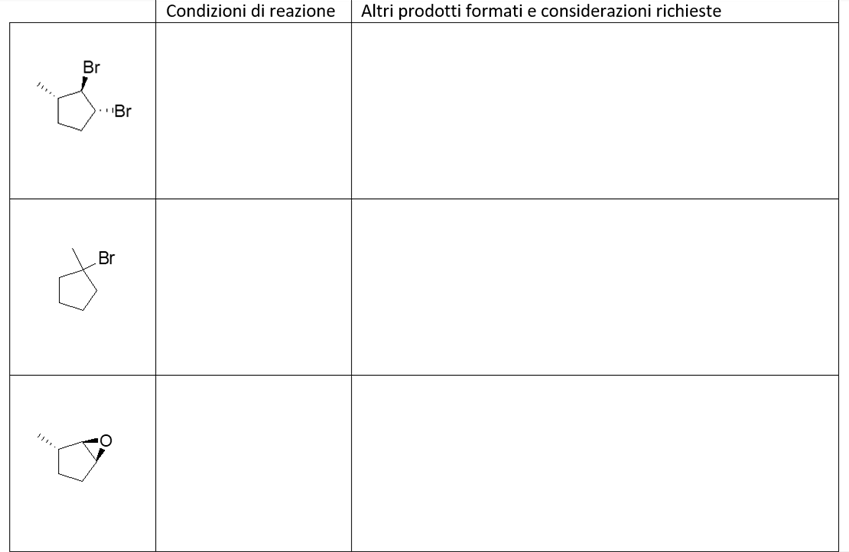
3) Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal (S)-3-metilciclopentene. Se quello ottenuto non è l’unico prodotto di reazione, indicare gli ulteriori altri prodotti formati, dire in che relazione sono col prodotto riportato e indicare se si formano o meno in quantità equimolari rispetto a quest’ultimo. NB: se non si formano ulteriori prodotti, scrivere “nessuno” nella casella dedicata.
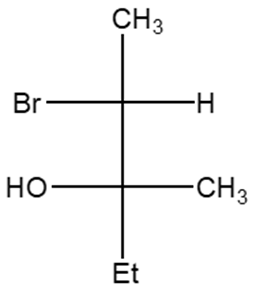
4) Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
5) Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica, quando opportuno.

6) Spiegare perchè nella seguente reazione non so ottiene alcun prodotto di eliminazione

7) Mostrare il meccanismo di apertura del seguente epossido a) con metanolo in ambiente acido; b) con lo ione acetiluro ottenuto trattando l’etino con NaNH2. Mostrare la stereochimica dei prodotti. Attribuire il nome IUPAC all’epossido e ai prodotti formati.

8) Il prodotto di eliminazione E2 di (1R,2S)-1-bromo-2-isopropilcicloesano sarà diverso dal prodotto di eliminazione di (1S,3S)-1-bromo-2-isopropilcicloesano. Spiegare sinteticamente perché
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2) Scrivere e attribuire il nome IUPAC al composto di formula C6H12 che possiede solo idrogeni primari e terziari
3) Disegnare il conformero a minore energia del cis-1-terz-butil-4-etilcicloesano e del trans-1- terz-butil-4-etilcicloesano. Poi, confrontare tra loro i due isomeri geometrici. Quale dei due sarà quello più stabile? Perché?
4) Stabilire le configurazioni assolute dei carboni chirali e dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/stesso composto/isomeri costituzionali/altro).
5) Disporre i seguenti composti in ordine di basicità decrescente (dal più basico al meno basico) e spiegare sinteticamente il perché:

6) Disporre i seguenti composti in ordine di acidità decrescente e motivare la risposta data

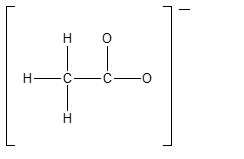
7) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di carbonio e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza
8) Analizzare il diagramma di energia libera/coordinata di reazione dell’addizione di HBr al 1-butene e rispondere ai seguenti quesiti.

a) Cosa possiamo dire circa la Keq della reazione?
b) Cosa possiamo dire circa il ΔG° della reazione?
c) Di quanti stadi si compone la reazione?
d) Qual è lo stadio cineticamente determinante?
e) Indicare sul grafico l’energia di attivazione relativa allo stadio veloce.
f) Cosa sono, rispettivamente B, C e D?
g) Disegnare la struttura di C e D
h) Spiegare perché la reazione è regioselettiva
9) Mostrare la strategia di sintesi e il meccanismo che permette di ottenere il 2-cicloesen-1-one mediante una reazione di condensazione aldolica
SECONDO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
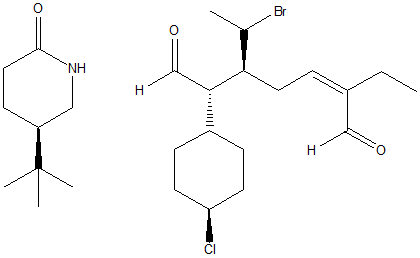
2. Disegnare il 1-sec-butil-4-etil-2-metilciclopentano
3. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

4) Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

5) Cerchiare l’acido più debole e motivare sinteticamente la scelta.
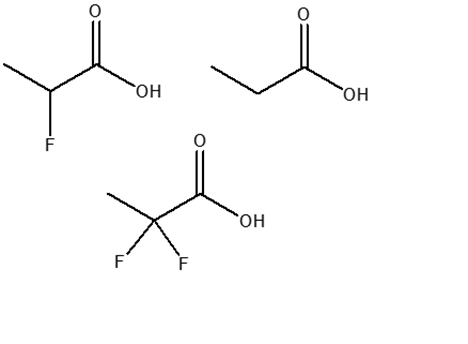
6) Mettere i seguenti composti in ordine di acidità crescente e motivare la scelta:
a) CH3CH2CH2SH b) CH3CH2CH2NH2 c) CH3CH2CH2OH d) CH3CH2CH2CH3
7) Qual è il numero massimo di stereoisomeri per il seguente composto?

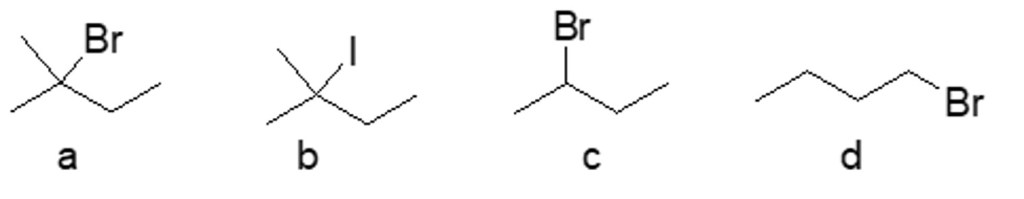
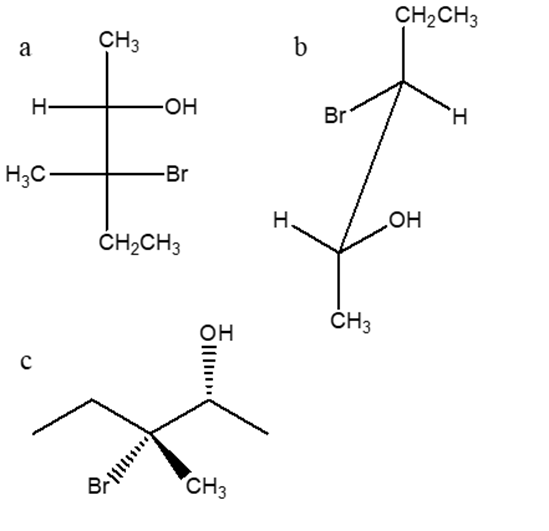
8) Dire quale tra le strutture a-d è l’enantiomero del seguente composto:

9) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione del ciclopentanone con etanammina
10) Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica, quando opportuno.
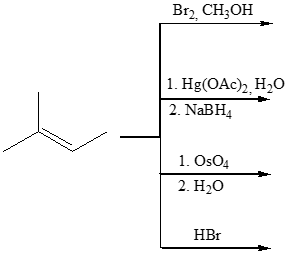
11. Classifica i seguenti composti o ioni come aromatici, antiaromatici o non aromatici:
TERZO SET
1a. Rispondi alle domande sulla seguente molecola:

a) Quante coppie solitarie sono presenti sul cloro e quali orbitali occupano? ____________________
b) Quanti carboni ibridati sp sono presenti? ________________________________________
c) Indicare con una freccia sulla figura il legame singolo carbonio-carbonio più corto
1b. Nella molecola dell’esercizio 1a, sono presenti diversi legami multipli. Fornire una descrizione dettagliata dei legami formati dai due carboni impegnati nel triplo legame (informazioni necessarie: atomi con cui formano i legami; orbitali molecolari formati; orbitali atomici/ibridi coinvolti)
2. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
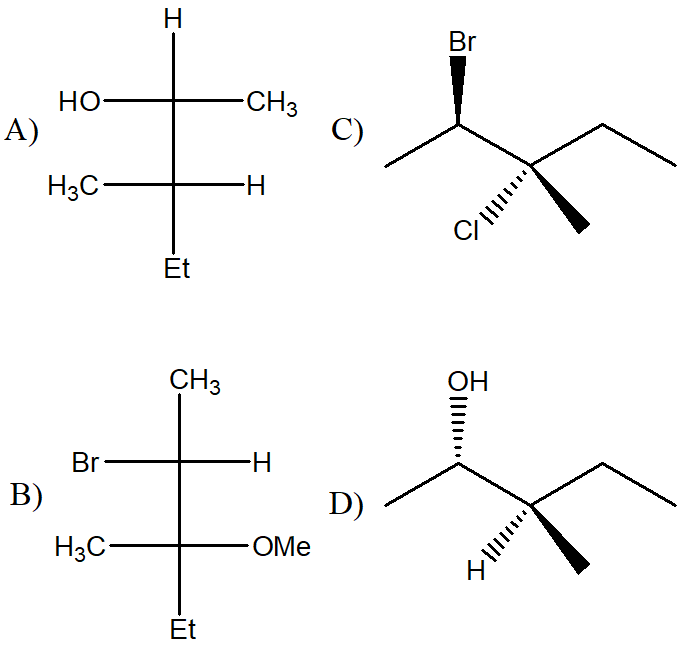

3. Dire se le strutture riportate a destra sono isomeri conformazionali, isomeri geometrici, isomeri ottici, isomeri costituzionali, o lo strutture identiche rispetto alla seguente struttura a segmenti:

4) Scrivi il (2R,3S)-2-bromo-3,4-dimetilpentano in proiezione di Fischer.
Scrivi, poi, la proiezione di Newman lungo il legame C2-C3 del conformero a minore energia.
5) a. Individuare gli idrogeni più acidi in ciascuno dei seguenti composti. b. ordinare i seguenti composti in ordine di acidità crescente
a) 3-ossobutanoato di metile
b) acetone (=propanone)
c) 2,4-pentandione
d) etanoato di metile
6) Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal (S)-3-metilciclopentene. Se quello ottenuto non è l’unico prodotto di reazione, indicare gli ulteriori altri prodotti formati, dire in che relazione sono col prodotto riportato e indicare se si formano o meno in quantità equimolari rispetto a quest’ultimo. NB: se non si formano ulteriori prodotti, scrivere “nessuno” nella casella dedicata.

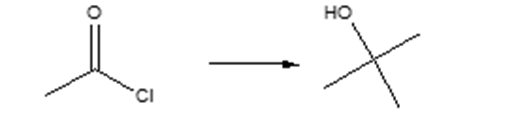
7) Indicare le condizioni di reazione ottimali per ottenere la seguente trasformazione e mostrare il meccanismo di reazione:
8) Scrivere la struttura di un trigliceride semplice in cui il glicerolo (1,2,3-propantriolo) è esterificato con un acido grasso a 18 atomi di carbonio
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate
You must be logged in to post a comment.