Soluzioni esercizi III e IV prova

Sono state pubblicate le soluzioni del seguente set di esercizi (vedere commenti del post in questione)
Università degli Studi della Campania "Luigi Vanvitelli"

Sono state pubblicate le soluzioni del seguente set di esercizi (vedere commenti del post in questione)

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 23/01 | 10:00 | ESERCITAZIONE DI RECUPERO | L |
L’esercitazione sarà incentrata soprattutto sugli esercizi di NOMENCLATURA, a cui saranno affiancanti esercizi misti, atti a coprire sopratutto reazioni di alcoli, eteri, epossidi e composti carbonilici
LA PARTECIPAZIONE ALLE ESERCITAZIONI DI RECUPERO E è APERTA A TUTTI GLI STUDENTI (inclusi gli studenti che non hanno seguito il corso e/o devono fare la prova intera).

L’ultima esercitazione di recupero si terrà, come da calendario, giovedì 23 gennaio.
Il seguente form può essere utilizzato per esprimere i propri dubbi: https://forms.office.com/e/2sf2i2Actq. Prima di compilarlo, leggere le seguenti istruzioni:

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomenti, ma potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti. In fondo alla lista, troverete anche un’indicazione del livello di difficoltà delle domande.

Grado di difficoltà delle domande:
Alto (richiedono più passaggi e/o notevole padronanza della disciplina): 27, 29
Medio (domande che vanno al di là della mera esposizione/applicazione di concetti teorici): 14, 22, 26, 28
Basso (domande che riguardano l’esposizione di concetti teorici, la dimostrazione di semplici meccanismi di reazione, l’applicazione diretta di concetti teorici di base): tutte le domande non incluse nelle due liste precedenti.

PRIMO SET
1. La reazione del 2-metilpropene con metanolo in presenza di acido solforico porta alla formazione del 2-metossi-2-metilpropano (=terz-butil metil etere). Proporre un meccanismo per la formazione dell’etere.
2. Mostrare i prodotti delle seguenti reazioni. Nel caso, indicare il/i prodotti principali. Indicare la stereochimica e attribuire il nome IUPAC a tutti i prodotti.
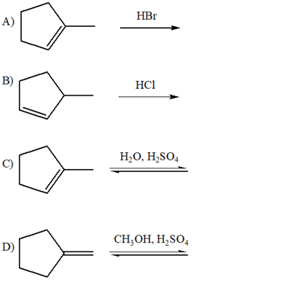
3. Indicare le condizioni ottimali per le seguenti reazioni:
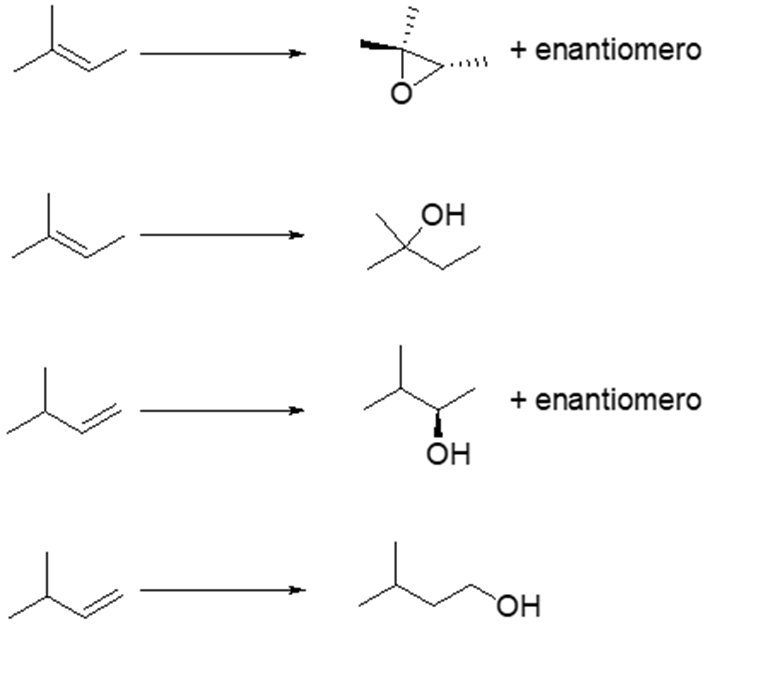
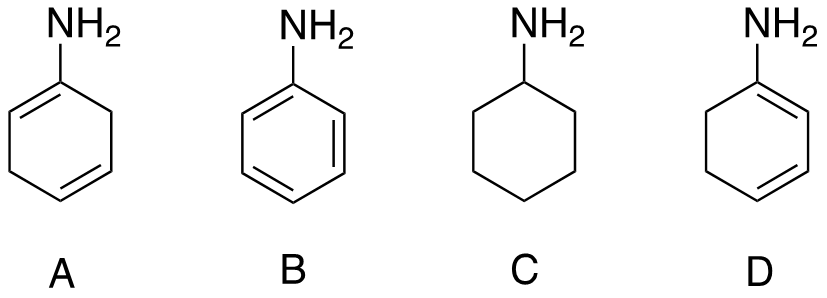
4. Disporre i seguenti composti in ordine di acidità crescente e motivare la risposta data

5. Dire quale composto delle seguenti coppie reagisce più velocemente in una reazione di eliminazione E2 e spiegare perchè:
(1R,3S)-1-bromo-3-isopropilcicloesano o (1R,3R)-1-bromo-3-isopropilcicloesano
6. Spiegare come i seguenti cambiamenti influenzino la velocità di reazione del 2-bromo-2-metilpentano con metanolo
a) l’alogenuro alchilico è cambiato con 2-cloro-2-metilpentano
b) l’alogenuro alchilico è cambiato con 2-cloro-3-metilpentano.
7. Proporre un meccanismo per la seguente trasformazione:
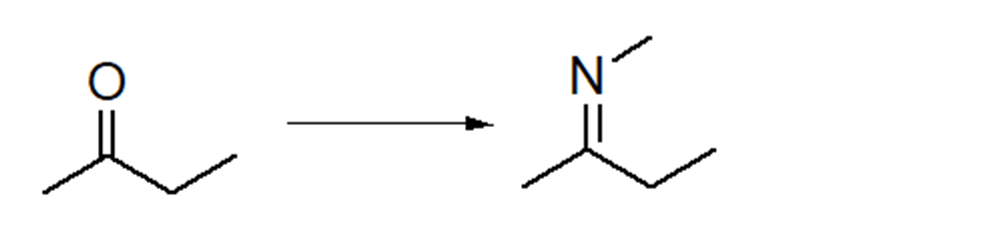
8. Scrivere i prodotti delle seguenti reazioni:

9. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti
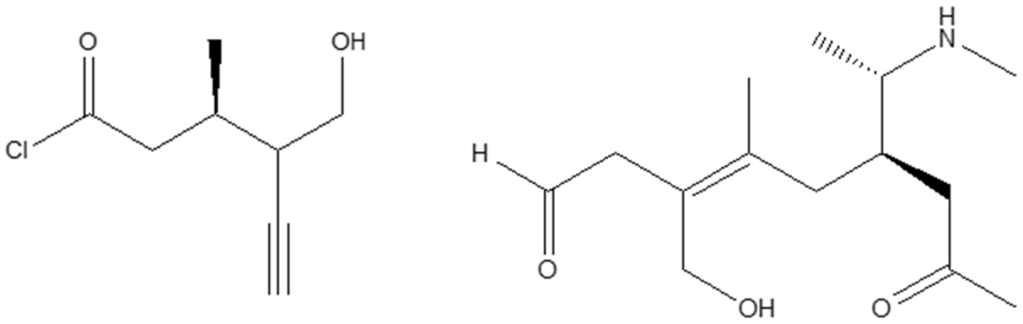
SECONDO SET
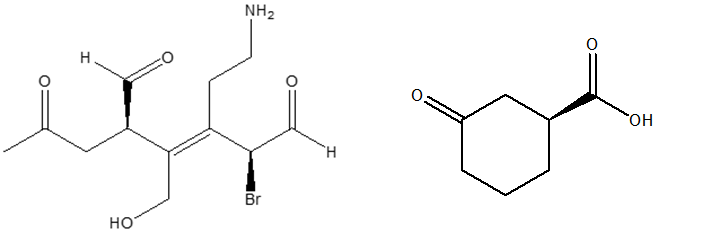
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
2. Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Indicare la stereochimica quando opportuno.

3. Mostrare le condizioni di reazione, il meccanismo e indicare i prodotti delle seguenti reazioni. Classificare i prodotti come immine o enammine
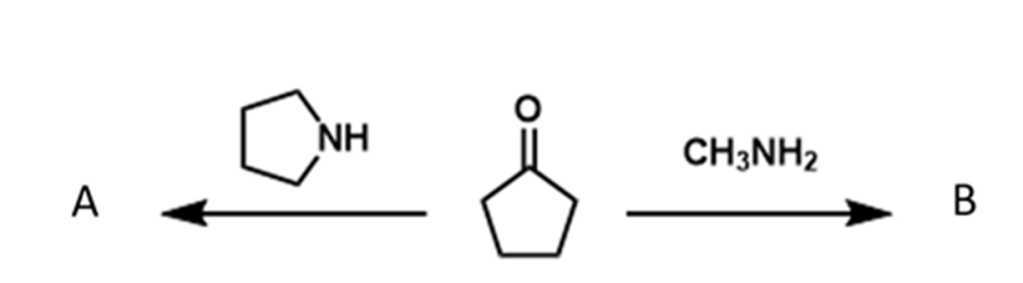
4. Mettere i seguenti composti in ordine di reattività crescente in una reazione E2 e motivare la scelta: 4-bromocicloes-1-ene, 5-bromo-1,3-cicloesadiene, 3-bromocicloes-1-ene
5. Quale/i dei seguenti alcheni darà l’1-bromo-1,2-dimetilciclopentano come prodotto principale della reazione con HBr?
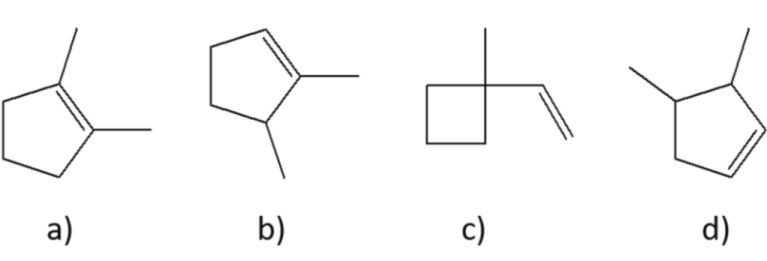
6. Analizzare il seguente diagramma di energia libera/coordinata di reazione e rispondere ai seguenti quesiti.

a) Calcolare il ΔG° approssimativo per la reazione
b) Calcolare l’energia di attivazione per ciascuno stadio della reazione
c) cosa rappresenta B?
d) i prodotti sono più o meno stabili dei reagenti?
e) Il primo stadio della reazione è endoergonico o esoergonico?
7. Metti i seguenti carbocationi in ordine di stabilità crescente:
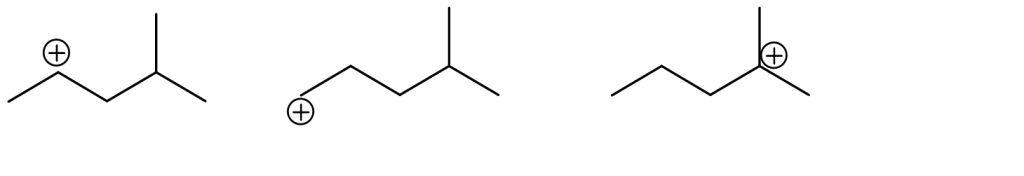
8. Disporre i seguenti composti in ordine di acidità crescente e spiegare sinteticamente il perché:
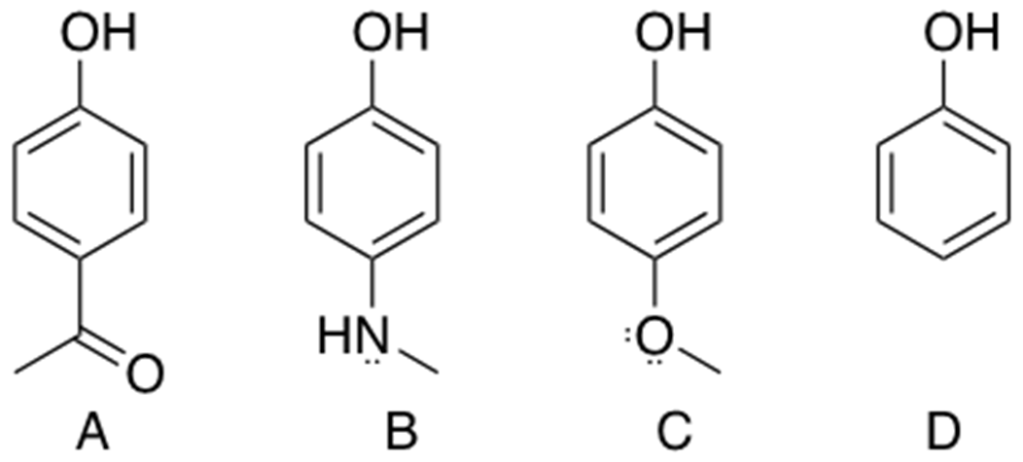
TERZO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
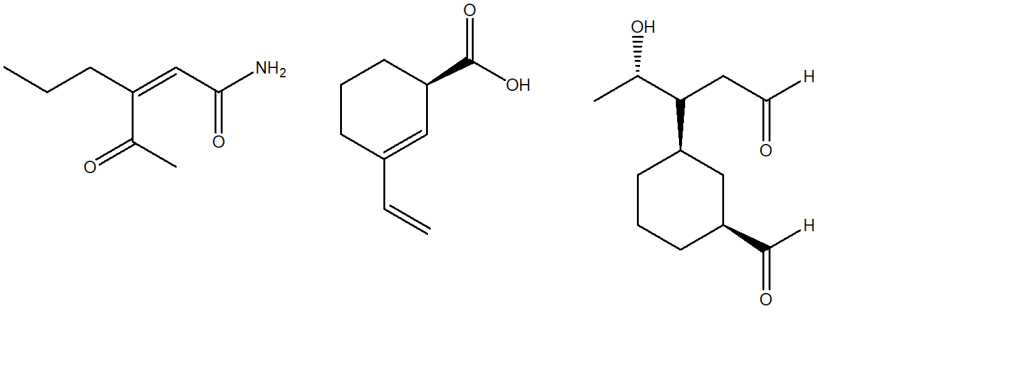
2. Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal (S)-3-metilciclopentene.

3. Completare il seguente schema:
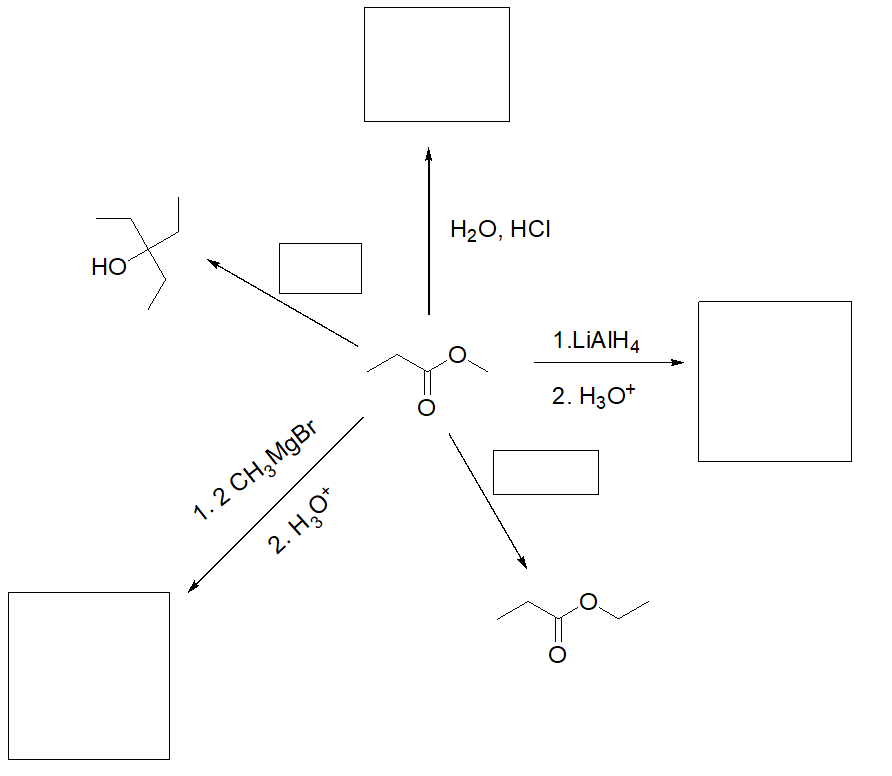
4. Scrivere i prodotti principali delle seguenti reazioni.
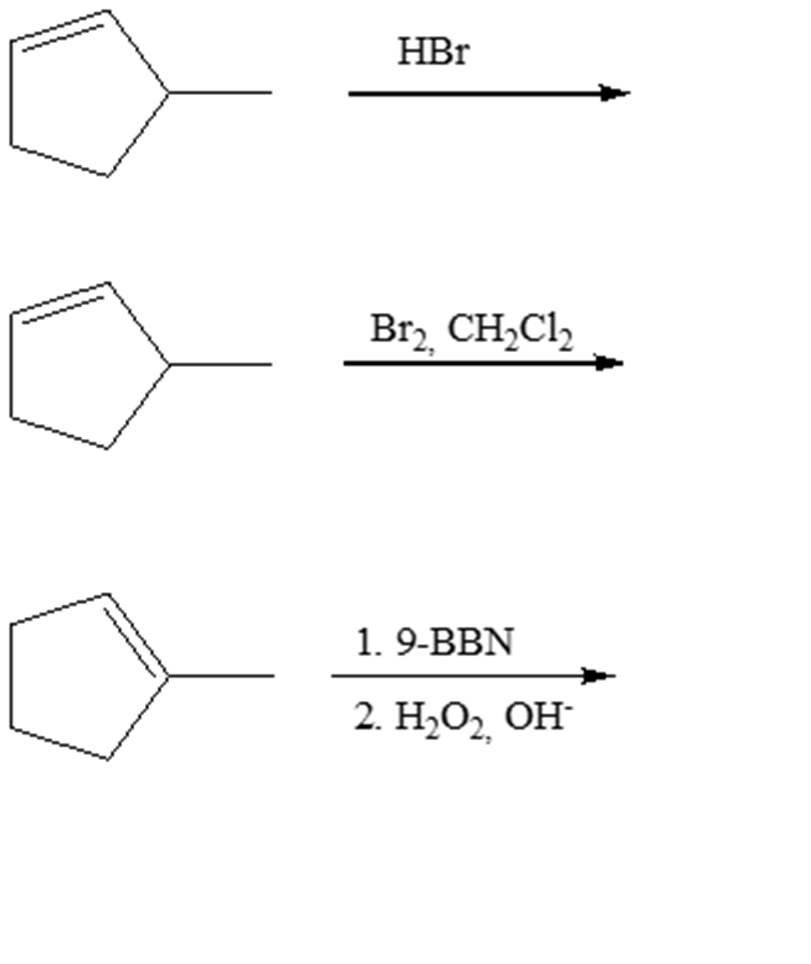
5. Proporre una strategia di sintesi del seguente composto a partire dall’opportuno alogenuro alchilico: (1R, 3S)-3-metilcicloesan-1-olo
6. Scrivere il meccanismo che porta alla formazione del prodotto principale di disidratazione del (1R,3S)-3-metilcicloesan-1-olo
7. Indicare le condizioni di reazione ottimali per ottenere le seguenti trasformazioni:

8. Mostrare il meccanismo e i prodotti della reazione del ciclopentanone con etanolo in ambiente acido.
9. Ordina i seguenti composti per reattività crescente in una reazione E2, giustificando la scelta

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
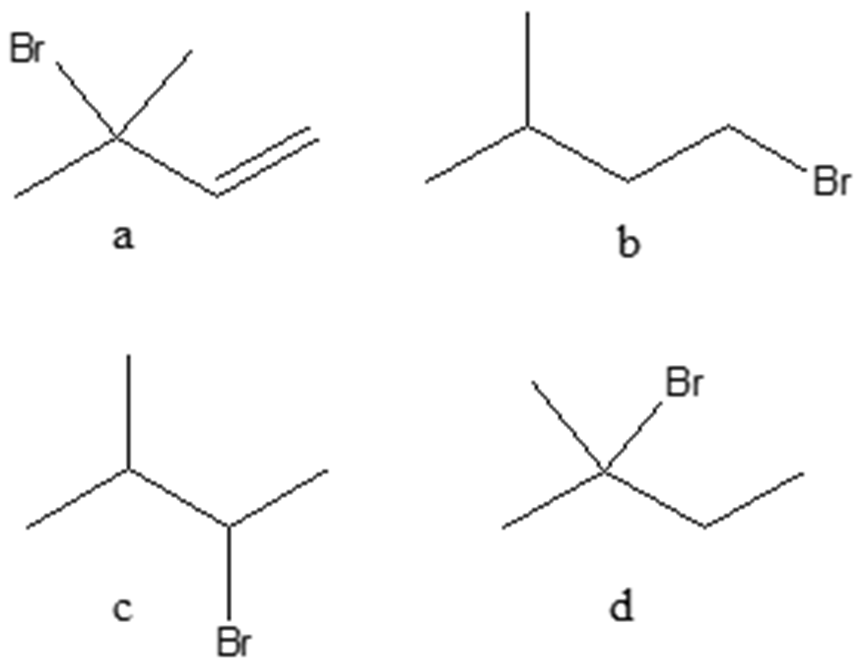
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2. Disegnare la struttura di Lewis della seguente molecola: CH3CHO. Calcola le cariche formali per tutti gli atomi diversi dall’idrogeno
3. Qual è il più corto tra i legami indicati dalle frecce nella seguente molecola?
a) Cerchiare la lettera corrispondente.
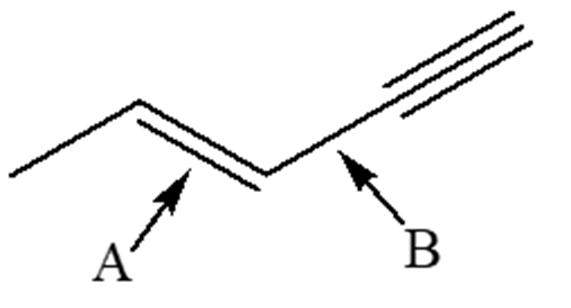
b) In riferimento al legame A, dire:
I) quali orbitali molecolari sono presenti
II) quali orbitali atomici o ibridi sono coinvolti nella formazione del legame
4. Il composto mostrato di seguito è l’acido nicotinico
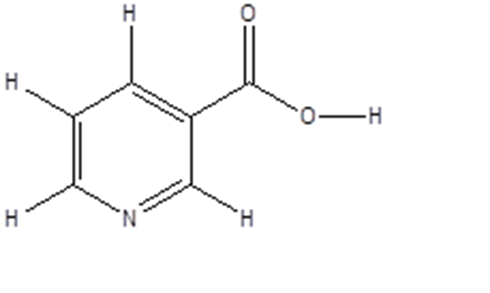
a) indicare con una freccia l’idrogeno più acido;
b) dire quale orbitale occupa la coppia solitaria dell’atomo di azoto
5. Disporre i seguenti composti in ordine di punto di ebollizione crescente. Indicare l’ordine inserendo i numeri nei riquadri sotto le strutture: 1= quello col punto di ebollizione più basso, 5= quello col punto di ebollizione più alto

6. Per l’1,4-dimetilcicloesano esistono due isomeri configurazionali (I e II); per l’1,2-dimetilcicloesano esistono tre isomeri configurazionali (I, II, III). Completare la seguente tabella.

7. Attribuire la configurazione assoluta al seguente carbonio chirale:
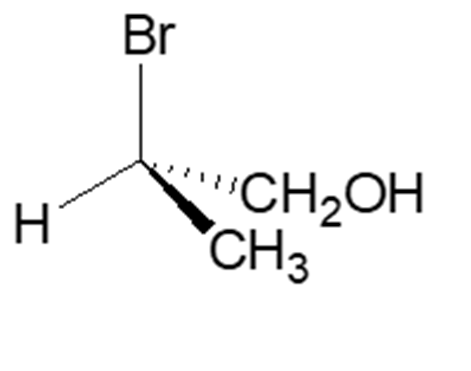
8. Dire quale dei seguenti composti non è otticamente attivo (è possibile scegliere più opzioni):

9. Il 2-metil-2-butene reagirà con Br2 in acqua per dare un’aloidrina (ignorare la stereochimica). La reazione ha Keq>1. Mostrare il meccanismo di reazione, inclusi gli stati di transizione. Poi, disegnare il diagramma energetico della reazione. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, intermedio, variazione dell’energia libera di Gibbs, energia di attivazione di ciascuno stadio della reazione.
10. Scrivere i prodotti principali delle seguenti reazioni (se avvengono), indicando la stereochimica quando opportuno. Se la reazione non avviene, scrivere “nessuna reazione”
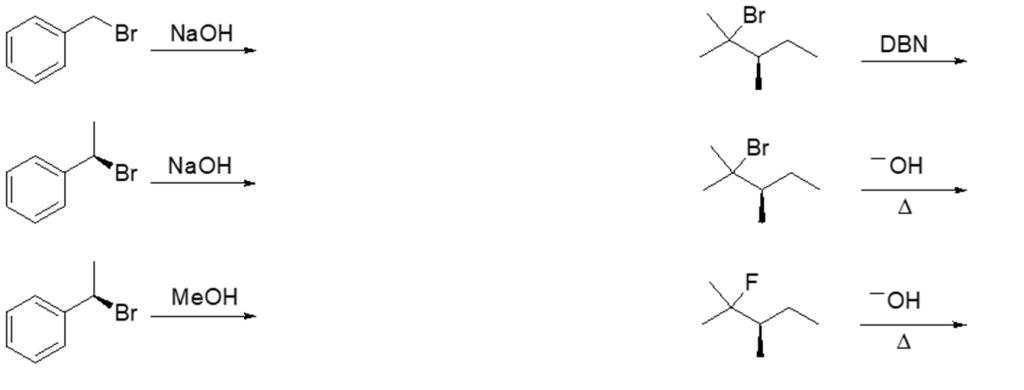
SECONDO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto:
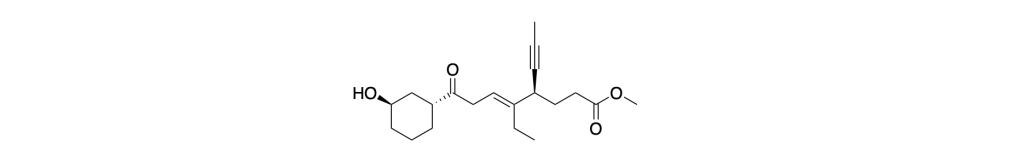
2. Disporre i seguenti composti in ordine di acidità crescente (dal meno acido al più acido) e spiegare sinteticamente il perché
a) CH3CH2SH
b) CH3CH2NH2
c) CH3CH2OH
d) CH3CH2CH3
3. In riferimento ai composti dell’esercizio 2, rispondere alle seguenti domande:
a) quale di esso sarà caratterizzaro dal valore di pKa più elevato?
b) quale dal valore di Ka più elevato?
4. Scrivere la struttura a segmenti del seguente composto e dire se il nome IUPAC è corretto; se non lo è, scrivere il nome corretto: 2-ciclopropilesano
5. Disegnare e scrivere il nome IUPAC di un composto di formula C9H18 che contenga solo idrogeni primari
6. Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (isomeri conformazionali/enantiomeri/diastereoisomeri/stesso composto/altro):


7. Prendendo in considerazione il legame C3-C4 del 2-metilpentano, scrivere la proiezione di Newman del conformero meno stabile in assoluto e la struttura a cavalletto del conformero più stabile in assoluto
8. Disporre i seguenti composti in ordine di basicità crescente e motivare la risposta data

9. Mostrare il meccanismo di apertura del seguente epossido a) con metanolo in ambiente acido; b) con ione metossido. Mostrare la stereochimica dei prodotti. Attribuire il nome IUPAC all’epossido e ai prodotti formati.

10. Spiegate perché il trattamento con base del (1R,2R)-1-bromo-2-metilcicloesano genera il 3-metilcicloes-1-ene, un prodotto di eliminazione non Zeitzev
11. Scrivere iol D-glucosio e mostrare il meccanismo di riarrangiamento enediolico e quello di epimerizzazione.
12. Scrivere un L-amminoacido generico in proiezione di Fischer.
TERZO SET
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2. Disponi i seguenti composti in ordine di basicità crescente (dal meno basico al più basico), motivando sinteticamente la scelta
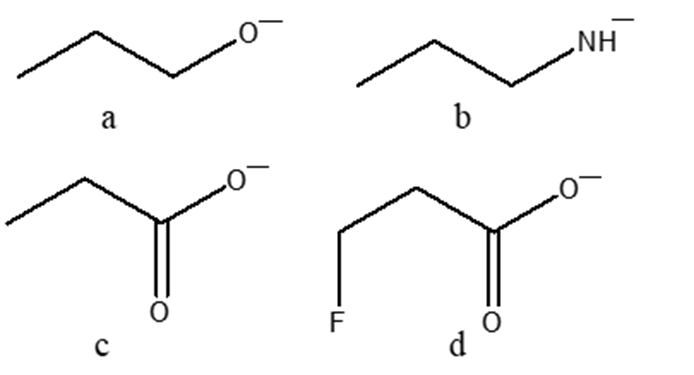
3. L’acido acetico ha pKa=4.8.
a) Quale sarà la forma predominante in una soluzione a pH 2.8? Disegnarne la formula di Kekulé nel riquadro sotto.
b) In quale rapporto saranno la forma acida e la forma basica a questo valore di pH?
4. Scrivere il seguente composto in proiezione di Newman secondo i legami C1-C6 e C3-C4: (1R,3S,4R)-4-isopropil-3-metilcicloesan-1-olo. Poi, effettuare l’inversione d’anello e dire qual è il conformero più stabile
5. In riferimento alla conformazione più stabile del composto dell’esercizio 4, descrivere le interazioni 1,3-diassiali (se presenti) e altre interazioni gauche (se presenti). NB: è sufficiente indicare i gruppi tra cui si instaurano tali interazioni (es.: tra il sostituente X in assiale e…).
6. Calcolare il numero massimo di stereoisomeri possibili per la seguente struttura. Scriverne uno a scelta e assegnargli il nome IUPAC completo di stereochimica

7. Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto utilizzando una reazione di idroborazione/ossidazione. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
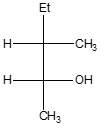
8. Mostrare il meccanismo e i prodotti della seguente reazione:
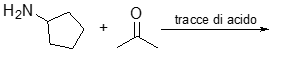
9. Scrivere un legame peptidico tra due amminoacidi (usare R per indicare le catene laterali degli amminoacidi). Dimostrare che tale legame ha parziale carattere di doppio legame.
10. Scrivere la proiezione di Fischer dell’L-alanina (R=-CH3) e determinare la configurazione assoluta del carbonio chirale

Le domande che seguono possono essere utili per capire se ci sono alcune parti del programma su cui ci sono ancora dei dubbi. Attenzione: le domande non sono certamente esaustive dato che non coprono tutti gli argomenti, ma potete utilizzarle per fare un controllo della vostra preparazione su alcuni argomenti. Se avete difficoltà a rispondere ad alcuni quesiti, è probabilmente il caso di approfondire quegli argomenti. In fondo alla lista, troverete anche un’indicazione del livello di difficoltà delle domande.

2. Che succede se mettiamo il composto raffigurato in alto in presenza di ione metossido?
3. Nel composto 1 c’è un anello aromatico, in particolare un benzene sostituito. Immaginiamo di avere il nitrobenzene. Il gruppo nitro è un gruppo fortemente disattivante. Dimostare quest’affermazione.
4. In che modo il gruppo nitro orienta eventuali altri sostituenti.
5. Che effetto ha il gruppo nitro sull’acidità del fenolo? Prendere in considerazione il fenolo sostituito col gruppo nitro in diverse posizioni (orto/meta/para).
6. Definire l’ibridazione di tutti gli atomi di ossigeno della molecola in 1.
7. In che modo possiamo predire le proprietà fisiche dei composti organici? Fornire degli esempi pratici.
8. Spiegare in che modo la geometria molecolare influenza il momento dipolare di una molecola.
9. Per una stessa molecola, conformeri diversi possono essere caratterizzati da momenti dipolari diversi. Spiegare questa affermazione e fornire degli esempi concreti.
10. Il composto 1,4-diclorobenzene non ha momento dipolare. Momento dipolare che è invece presente nel cis-1,4-diclorocicloesano. Spiegare perchè.
11. Per l’1,4-diclorocicloesano esistono due isomeri geometrici. Per ciascuno degli isomeri geometrici, disegnare i conformeri a sedia e individuare il conformero più stabile, spiegando il perchè.
12. Confrontando tra loro gli alogeni per quel che concerne l’influenza sulla costante di equilibrio per i cicloesani monosostituiti (Tabella 3.9 del Bruice), si osserva un trend interessante. Quale? Fornire una spiegazione plausibile per i dati sperimentali.
13. Come sintetizzeresti il terz-butossicicloesano mediante sintesi di Williamson? Dopo aver scelto la strategia sintetica migliore, valutare l’effettiva efficacia della sintesi proposta ed eventualmente proporre metodi alternativi.
14. Confronta lo ione terz-butossido e lo ione metossido dal punto di vista della basicità e dal punto di vista della nucleofilicità. Definisci, inoltre, in maniera chiara i due concetti (basicità e nucleofilicità).
15. Fai degli esempi di acidi organici e di basi organiche.
16. Parla degli effetti della struttura sull’acidità.
17. In che modo possiamo utilizzare l’equazione di Henderson-Hasselbalch per capire se un composto ionizzabile si troverà in soluzione nella sua forma acida o nella sua forma basica?
18. Parlare dell’acidità degli idrogeni in alfa ad un gruppo carbonilico. Confrontare tra loro i diversi composti carbonilici definendo anche una scala di acidità per gli idrogeni legati al carbonio alfa.
19. A proposito di composti carbonilici, confronta tra loro i meccanismi di sostituzione nucleofila acilica e quelli di addizione nucleofila.
20. Se alcuni tra i composti carbonilici vanno incontro a reazioni di addizione nucleofila, gli alcheni vanno incontro a reazioni di addizione elettrofila. Fare degli esempi di addizione elettrofila agli alcheni, mostrando i meccanismi.
21. A differenza degli alcheni, il benzene va incontro a reazioni di sostituzione elettrofila. Spiegare perchè.
22. Gli alcheni possono essere sintetizzati a partire dagli alogenuri alchilici. In che modo? Quale sarà l’alchene principale ottenuto a partire da (2S,3R)-2-cloro-3-metilpentano? E a partire da (2S,3R)-2-fluoro-3-metilpentano?
23. La regola di Zeitzev non è sempre utile per identificare il prodotto principale di una reazione di eliminazione. Spiegare il perchè e fare degli esempi concreti.
24. Scrivere un monosaccaride che sia un aldopentoso e che abbia tutti i carboni chirali con configurazione S. Questo zucchero appartiene alla serie D o alla serie L?
25. A partire dallo zucchero in 24 mostrare il meccanismo di epimerizzazione e di riarrangiamento enediolico.
26. Cosa sono due epimeri?
27. Scrivere un legame peptidico.
28. Che tipo di legame è il legame peptidico? Che caratteristiche ha?
29. Immagina di voler sintetizzare un dipeptide, ma la sintesi coinvolge amminoacidi che hanno gruppi reattivi in catena laterale. Cosa faresti per evitare che questi reagiscano? (NB: la domanda è generica, non riguarda un gruppo in particolare)
30. Mostrare una strategia per la sintesi del 2-metil-1-propil-1-cicloesanolo a partire da 1-cloro-2-metilcicloesano (sono necessari più passaggi). Mostrare i meccanismi delle reazioni qualora siano tra quelli oggetto del programma.
Grado di difficoltà delle domande:
Alto (richiedono più passaggi e/o notevole padronanza della disciplina): 2, 5, 12, 13, 23, 29
Medio (domande che vanno al di là della mera esposizione/applicazione di concetti teorici): 30
Basso (domande che riguardano l’esposizione di concetti teorici, la dimostrazione di semplici meccanismi di reazione, l’applicazione diretta di concetti teorici di base): tutte le domande non incluse nelle due liste precedenti.

| Giorno | Ora | Evento | Aula | Note |
|---|---|---|---|---|
| 14/01 | 10:00 | ESERCITAZIONE DI RECUPERO | L | |
| 15/01 | 10:00 | INCONTRO PRE-ESAME ORALE | L | |
| 16/01 | 10:00 | ESERCITAZIONE DI RECUPERO | D1 |
PROGRAMMI DELLE ESERCITAZIONI DI RECUPERO
14/01: reazioni degli alcheni e reazioni di sostituzione ed eliminazione
16/01: reazioni dei composti carbonilici (oggetto della prova)
NB: la nomenclatura sarà oggetto din un’esercitazione successiva
PROGRAMMA DELL’INCONTRO PRE-ESAME ORALE
Si ricorda che gli studenti prenotati per i primi appelli (fino alla data del 5/02) possono suggerire gli argomenti utilizzando il link ricevuto. Il form si chiuderà domani. Gli argomenti indicati, se non inclusi tra quelli elencati in alto, saranno aggiunti al programma.
LA PARTECIPAZIONE ALLE ESERCITAZIONI DI RECUPERO E ALL’INCONTRO PRE-ESAME ORALE è APERTA A TUTTI GLI STUDENTI (inclusi gli studenti che non hanno seguito il corso e/o devono fare la prova intera).

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2) Disporre i seguenti composti in ordine di solubilità crescente in acqua. Indicare l’ordine inserendo i numeri nei riquadri sotto le strutture: 1= il meno solubile, 4= il più solubile

3) Calcolare il numero massimo di stereoisomeri possibili per la seguente struttura. Scriverne uno a scelta e determinare la configurazione assoluta dei carboni chirali

4) In basso è riportata la struttura del dolcificante aspartame:

I) Oltre al fenile, sono presenti altri 4 gruppi funzionali: cerchiare ogni gruppo funzionale ed identificarlo come nell’esempio in alto
II) Individuare i carboni chirali ed assegnare a ciascuno di essi la configurazione assoluta.
III) Indicare l’ibridazione dei due atomi di azoto
IV) Dire quale dei due atomi di azoto è più basico e perché
5) Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (enantiomeri/diastereoisomeri/stesso composto/altro):
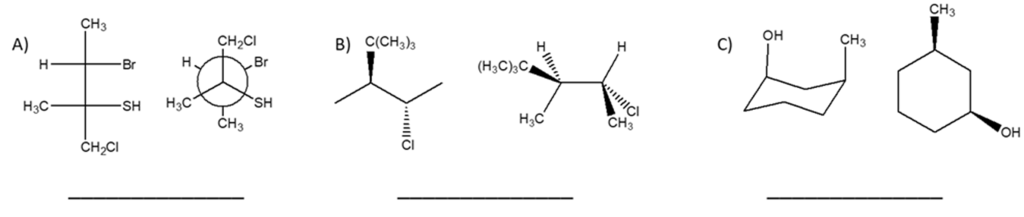
6) Dire se le strutture riportate a destra sono isomeri conformazionali, isomeri geometrici, isomeri ottici, isomeri costituzionali, o lo strutture identiche rispetto alla seguente struttura a segmenti:

7)Mostrare come il seguente anione è stabilizzato per risonanza

8) Mostrare le condizioni di reazione e il meccanismo della seguente trasformazione (ignorare la stereochimica).

9) Mostrare il meccanismo e i prodotti della seguente reazione:

10)Indicare le condizioni di reazione per ottenere la seguente trasformazione e dire se i due composti raffigurati sono otticamente attivi
SECONDO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

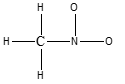
2) Completare la seguente struttura di Lewis e calcolare la carica formale per tutti gli atomi diversi all’idrogeno:
3) Quali sono la geometria, l’angolo di legame e l’ibridazione previste per il catione metile?
4) Dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/ isomeri geometrici/isomeri conformazionali/ stesso composto/isomeri costituzionali/altro)

5) Disporre i seguenti composti in ordine di basicità decrescente e spiegare sinteticamente il perché:
6) Scrivere i prodotti principali delle seguenti reazioni.


7) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione del ciclopentanone con dimetilammina.
8) L’acido L-aspartico è un amminoacido con R= -CH2COOH.
I valori di pKa dei gruppi ionizzabili sono i seguenti:
pKa α-COOH = 2.09
pKa α-NH3+ = 9.82
pKa COOH in catena laterale = 3.86
a) Scrivere l’amminoacido in proiezione di Fischer al punto isoelettrico
b) Determinare la configurazione assoluta del carbonio chirale
c) Calcolare il punto isoelettrico
d) Scrivere la struttura dell’amminoacido a pH>10 e a pH
TERZO SET
1. Attribuire il nome sistematico IUPAC, comprensivo di stereochimica, alle seguenti molecole:

2. Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (isomeri conformazionali/enantiomeri/diastereoisomeri/stesso composto/altro):

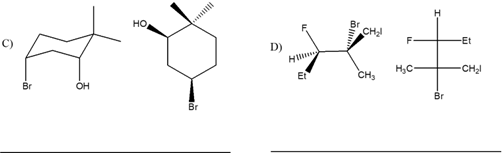
3. Prendendo in considerazione il legame C3-C4 del 2-metilpentano, scrivere la proiezione di Newman del conformero più stabile in assoluto e la struttura a cavalletto del conformero meno stabile in assoluto
4. Scrivere i prodotti principali delle seguenti reazioni. Indicare anche il meccanismo con cui avvengono. Indicare la stereochimica, quando opportuno.
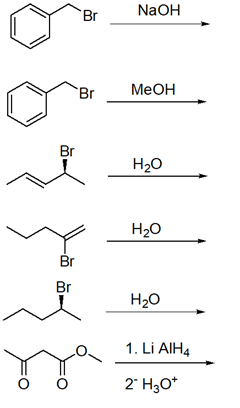
5. Ordina i seguenti composti per reattività crescente in una reazione E2

6. Mostra il meccanismo e i prodotti della seguente reazione:

7. Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Indicare la stereochimica quando opportuno.

8. Scrivi il dipeptide Ala-Gly sapendo che le catene laterali dei due amminoacidi sono -CH3 e -H, rispettivamente

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
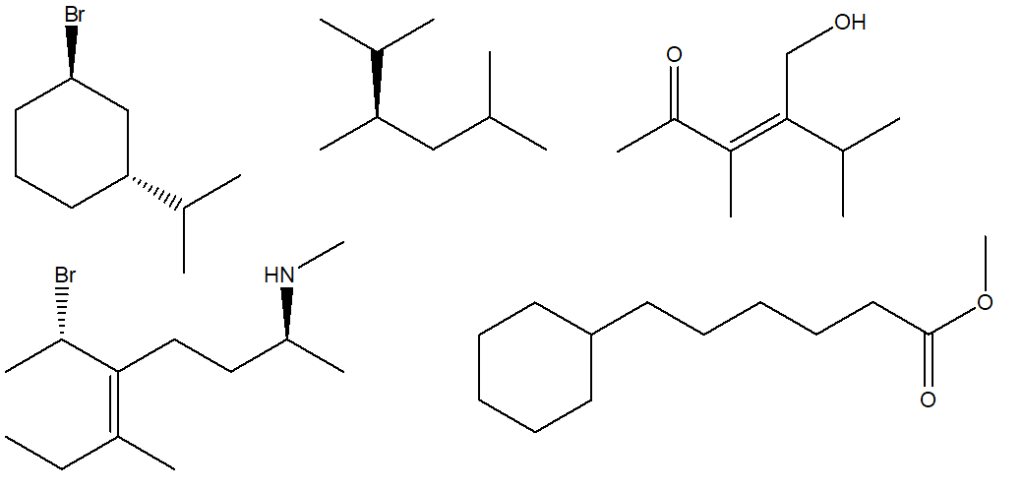
2) Per lo ione fosfato (PO43-) è possibile scrivere diverse strutture di risonanza. Scrivere la struttura di Lewis che rappresenta una delle strutture che contribuisce maggiormente all’ibrido di risonanza. Calcolare le cariche formali per tutti gli atomi.
3) Per ciascuno dei seguenti composti, scrivi la forma predominante a pH 3; 6; 10; 14
CH3CH2OH (pKa= 15,9)
CH3COOH (pKa= 4,8)
CH3CH2NH3+ (pKa= 11,0)
4) Quella qui riportata è la struttura della vitamina C

a) Individuare il legame singolo C-C più corto.
b) dire quali orbitali molecolari danno luogo al doppio legame C=O e quali orbitali atomici/ibridi sono usati per formare tali orbitali molecolari.
c) individuare gli atomi di carbonio ibridati sp2
6) Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (enantiomeri/diastereoisomeri/stesso composto/altro):
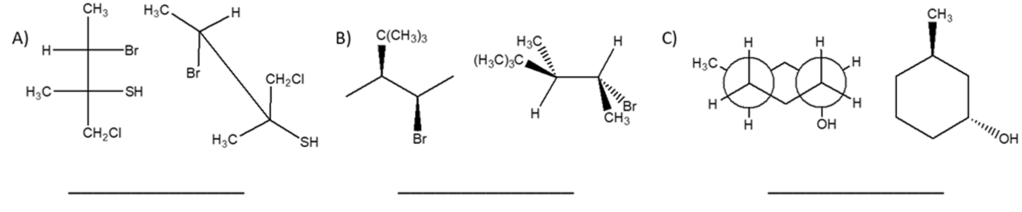
7) Rispondere alle domande A-D relative ai seguenti composti:

8) Quale alchene sarà il seguente composto come prodotto di una reazione di ozonolisi seguita da trattamento con dimetilsolfuro?

9) Proponi un meccanismo per ciascuna delle seguenti reazioni:

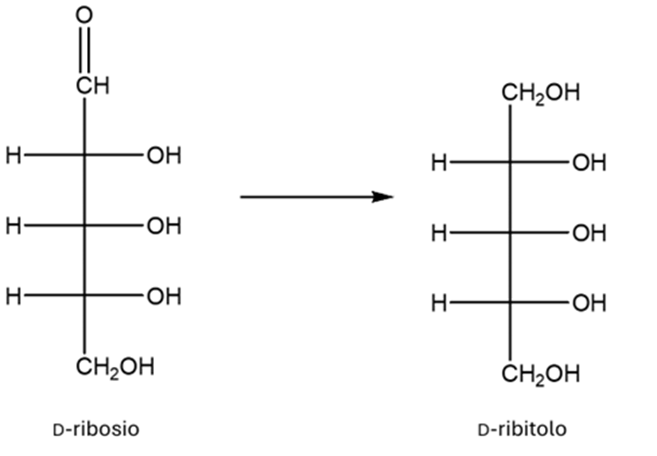
10) Scrivere:
a) D-mannosio (il mannosio è l’epimero in 2 del glucosio)
b) L-galattosio (il galattosio è l’epimero in 4 del glucosio)
c) L-idosio (l’idosio è un diastereoisomero del glucosio, che ne differisce per la configurazione al C-2, C-3 e C-4)
d) il D-fruttosio (il fruttosio è un chetoso che presenta, ai carboni chirali che restano tali, le stesse configurazioni assolute del glucosio)ile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza
SECONDO SET
1) Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
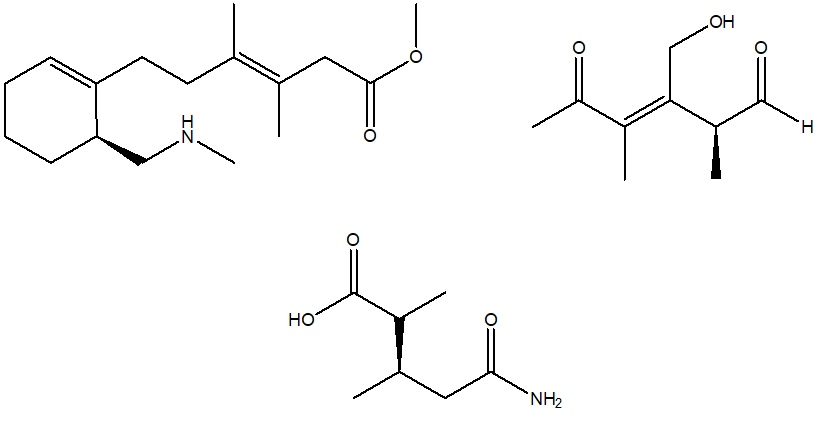
2) Disegnare l’acido (1S,3S)-3-benzilcicloesancarbossilico
3) Proporre formule di struttura per le molecole aventi le seguenti caratteristiche:
a) due atomi di carbonio ibridati sp2 e due atomi di carbonio ibridati sp3
b) quattro atomi di carbonio tutti ibridati sp2
c) due atomi di carbonio ibridati sp, e due atomi di carbonio ibridati sp2
4) Gli orbitali molecolari di antilegame sono prodotti da:
a) interazione costruttiva (in fase) degli orbitali atomici
b) interazione distruttiva (fasi opposte) degli orbitali atomici
c) la sovrapposizione degli orbitali atomici di due ioni negativi
d) tutte le precedenti
e) nessuna delle precedenti
5) Ordina i seguenti composti per acidità crescente e motivare la scelta
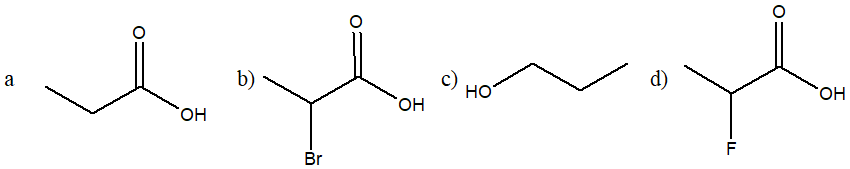
6) Disporre i seguenti composti in ordine di basicità decrescente (dal più basico al meno basico) e spiegare sinteticamente il perché
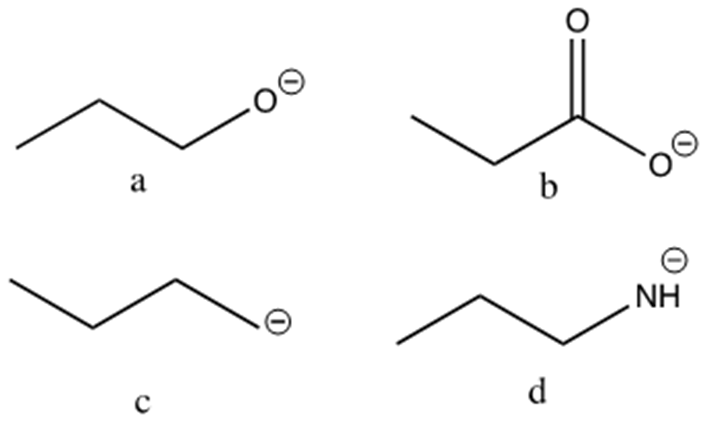
7) a. Individuare gli idrogeni più acidi in ciascuno dei seguenti composti. b. ordinare i seguenti composti in ordine di acidità crescente
a) 3-ossobutanoato di metile
b) acetone (=propanone)
c) 2,4-pentandione
d) etanoato di metile
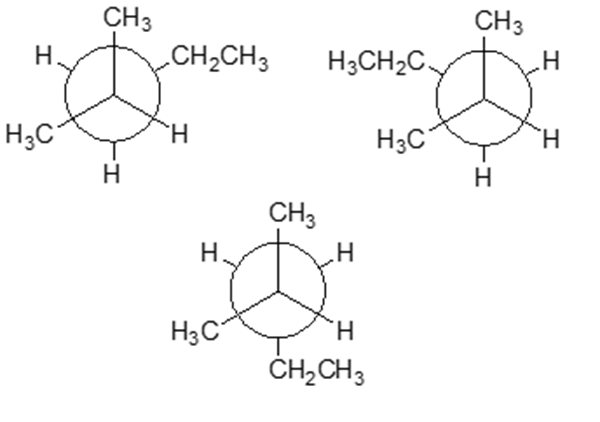
8) Cerchiare quella che, tra le seguenti, è la conformazione più stabile del 2-metilpentano e spiegare quali sono i fattori che la rendono tale:
9) Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (enantiomeri/diastereoisomeri/stesso composto/altro):

10) Scrivere il meccanismo e i prodotti delle seguenti reazioni

11. Fai un esempio di ione aromatico
TERZO SET
1 Rispondi alle domande sulla seguente molecola:
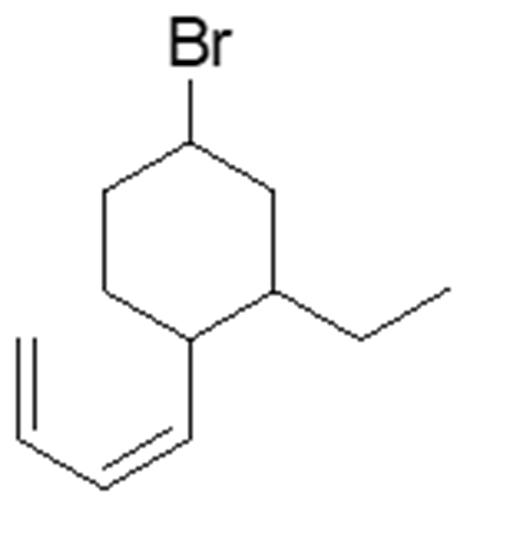
a) Quante coppie solitarie sono presenti sul bromo e quali orbitali occupano? ___________________
b) Quanti carboni ibridati sp3 sono presenti? ________________________________________
c) Indicare con una freccia sulla figura il legame singolo carbonio-carbonio più corto.
2) Quali sono la geometria, l’angolo di legame e l’ibridazione previste per il radicale metile?
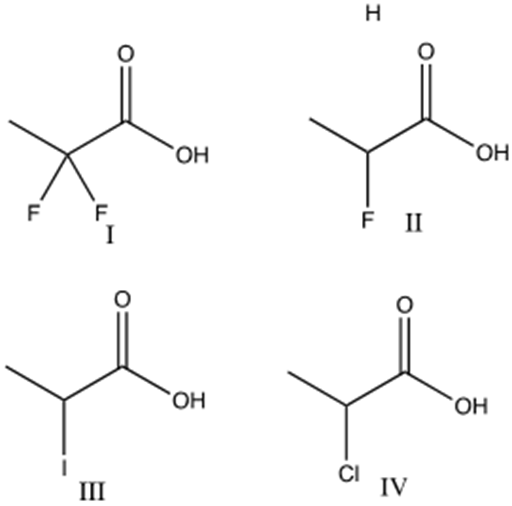
3) Disporre i seguenti composti in ordine di acidità decrescente (dal più acido al meno acido) e spiegare sinteticamente il perché:
4) Disegnare il composto di formula molecolare C5H9Br che contenga 2 carboni chirali. Disegnare e attribuire il nome IUPAC a tutti i possibili stereoisomeri.
5) Attribuire la configurazione assoluta a tutti i carboni chirali e individuare la relazione stereochimica esistente tra le seguenti strutture:

6) Disegnare un diagramma di energia potenziale per la rotazione di 360° del legame C2-C3 del 2-metilbutano, partendo da uno dei conformeri più stabili e disegnando tutte le conformazioni corrispondenti ai massimi e ai minimi di energia.
7) Disponi i seguenti composti in ordine di calore di idrogenazione decrescente

8) Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
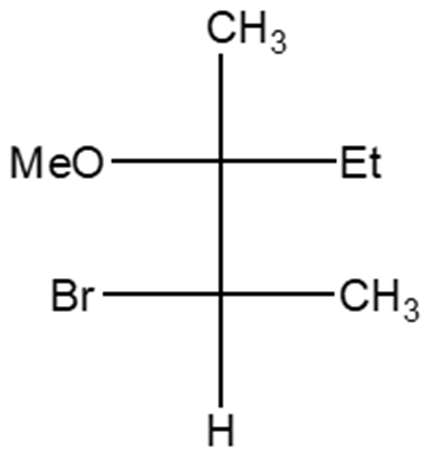
9) Mostrare i prodotti ottenuti a partire dai seguenti composti posti in presenza di tracce di acido
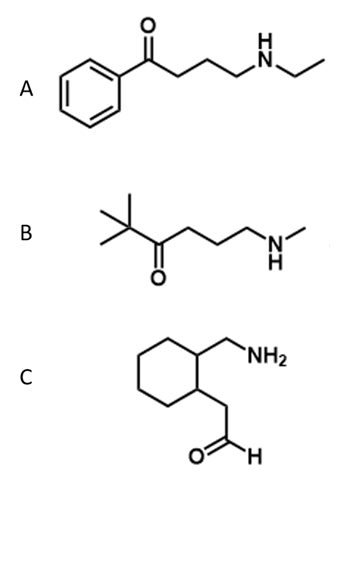
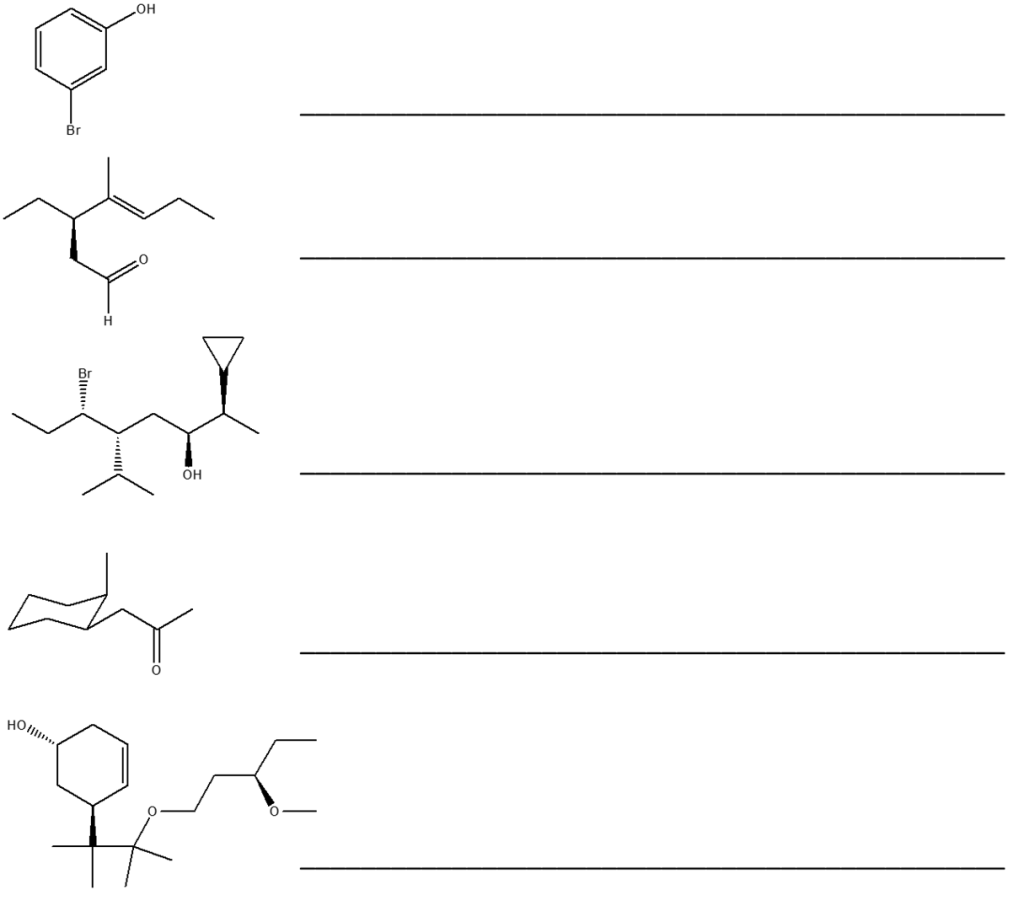
10) Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate
You must be logged in to post a comment.