Reazioni di sostituzione nucleofila acilica e di addizione nucleofila ai composti carbonilici

PRIMA DI SVOLGERE QUESTI ESERCIZI è NECESSARIO STUDIARE I CAP. 15 e 16 (in parte) del Bruice, Inoltre, molti degli esercizi di questo post richiedono conoscenze pregresse
1) Indicare i prodotti della reazione dell’acetone (=propanone) e dell’acetato di etile con i seguenti composti (se la reazione avviene). Indicare le opportune condizioni di reazione e mostrare il meccanismo.
a) metanammina
b) dimetilammina
c) metanolo
d) bromuro di etilmagnesio
e) NaBH4
1) Come si potrebbero sintetizzare i seguenti composti mediante una reazione tra un aldeide o un chetone e un reattivo di Grignard?
a) 2-pentanolo
b) 1-butanolo
c) 1-fenilcicloesan-1-olo
Mostrare i meccanismi di reazione
3) Indicare il reattivo di Grignard e il composto carbonilico opportuni per ottenere i seguenti alcoli. Quando sono possibili più strategie, mostrarle tutte. Mostrare il meccanismo e indicare la stereochimica dei prodotti, se opportuno.
a) 1-esanolo
b) 2-esanolo
c) 1-cicloesil-1-pentanolo
d) 1-etilcicloesan-1-olo
e) 2-ciclopentil-2-propanolo
4) Il carbonio carbonilico del propanale viene attaccato dallo ione cianuro. Quale saranno gli orbitali HOMO e LUMO coinvolti nella reazione?
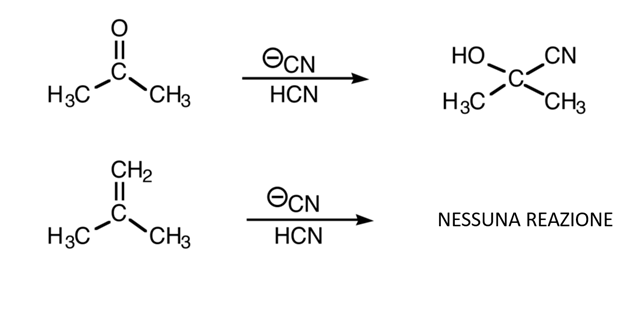
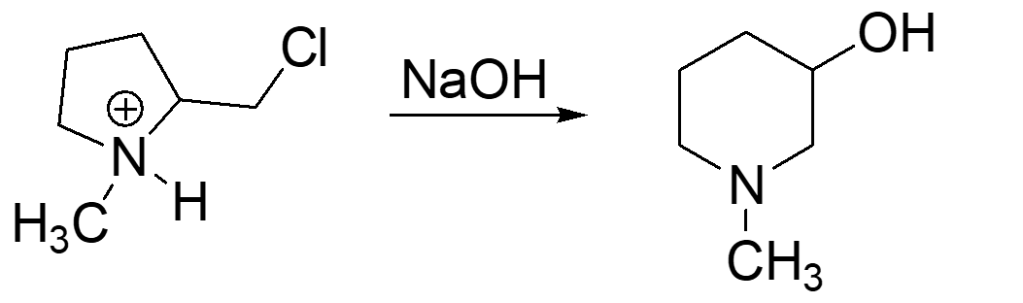
5) Spiegare perchè delle due reazioni mostrate in basso la prima avviene velocemente e la seconda non avviene
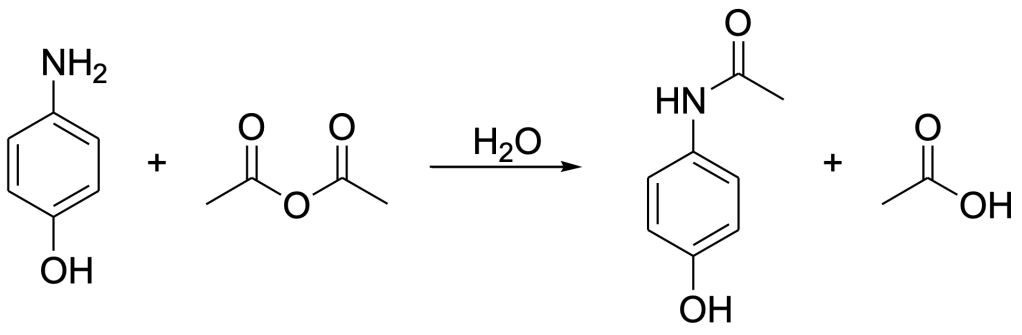
6) Il paracetamolo, N-(4-idrossifenil)acetammide, è un farmaco ad azione analgesica ed antipiretica molto utilizzato. Tachipirina ed Efferalgan sono i nomi commerciali più conosciuti dei farmaci che lo contengono. il paracetamolo può essere preparato per acetilazione selettiva del gruppo amminico del 4-amminofenolo con anidride acetica in H2O (vedi figura). Proporre il meccanismo di reazione utilizzato nella sintesi del paracetamolo a partire dal 4-amminofenolo.
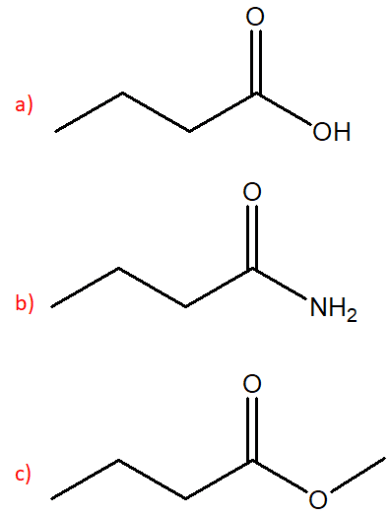
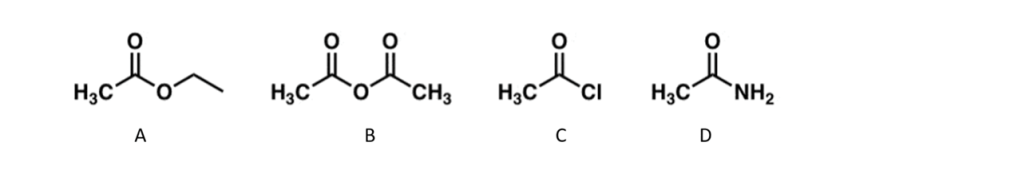
7) Completare il seguente schema:

8) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Indicare la stereochimica quando opportuno.

9) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Evidenziare la stereochimica quando opportuno.

10) Partendo da acido acetico (=acido etanoico) indicare le condizioni e il meccanismo di reazione (quando possibile) per ottenere i seguenti composti (in alcuni casi potrebbero essere necessari più passaggi, che prevedono anche reazioni già studiate):
a) cloruro di acetile
b) anidride acetica
c) acetato di etile
d) N-metilacetammide
e) etanolo
f) 2-metil-2-propanolo
g) 2-metil-1-propanolo
h) etanale












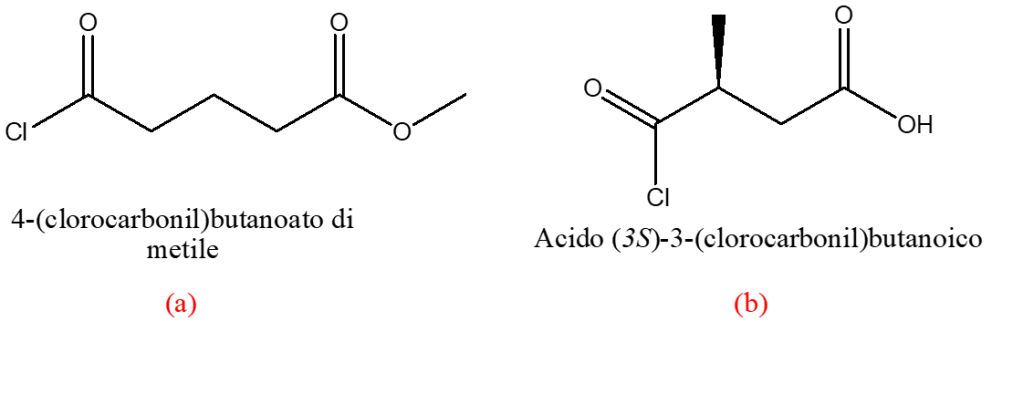


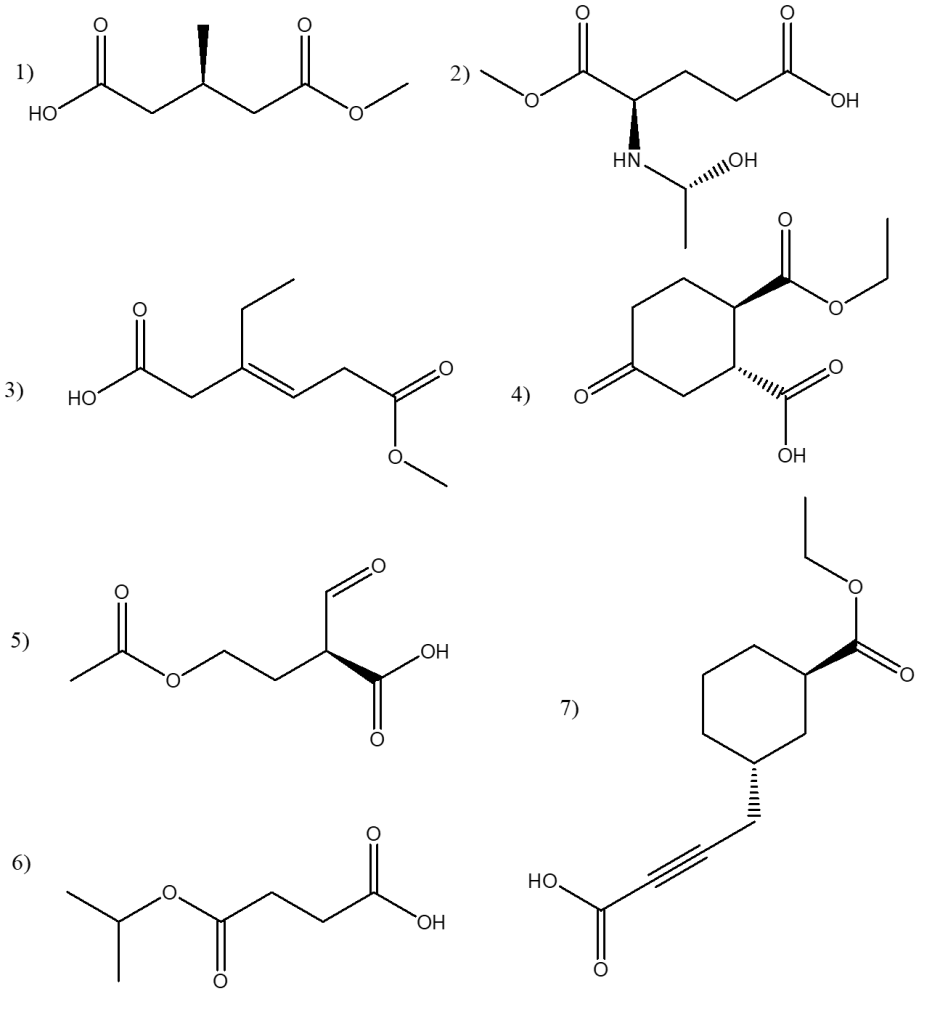
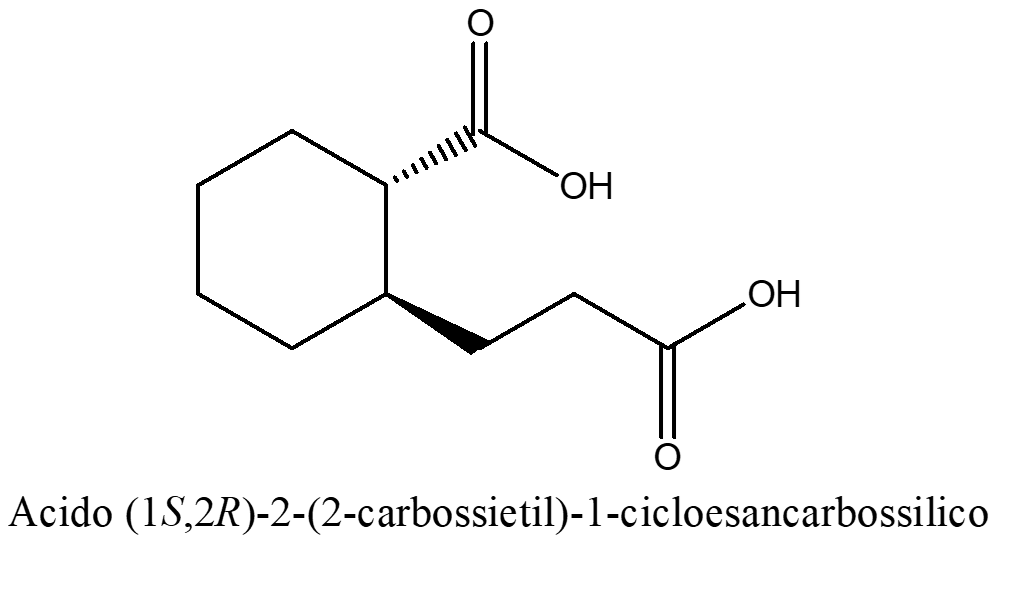
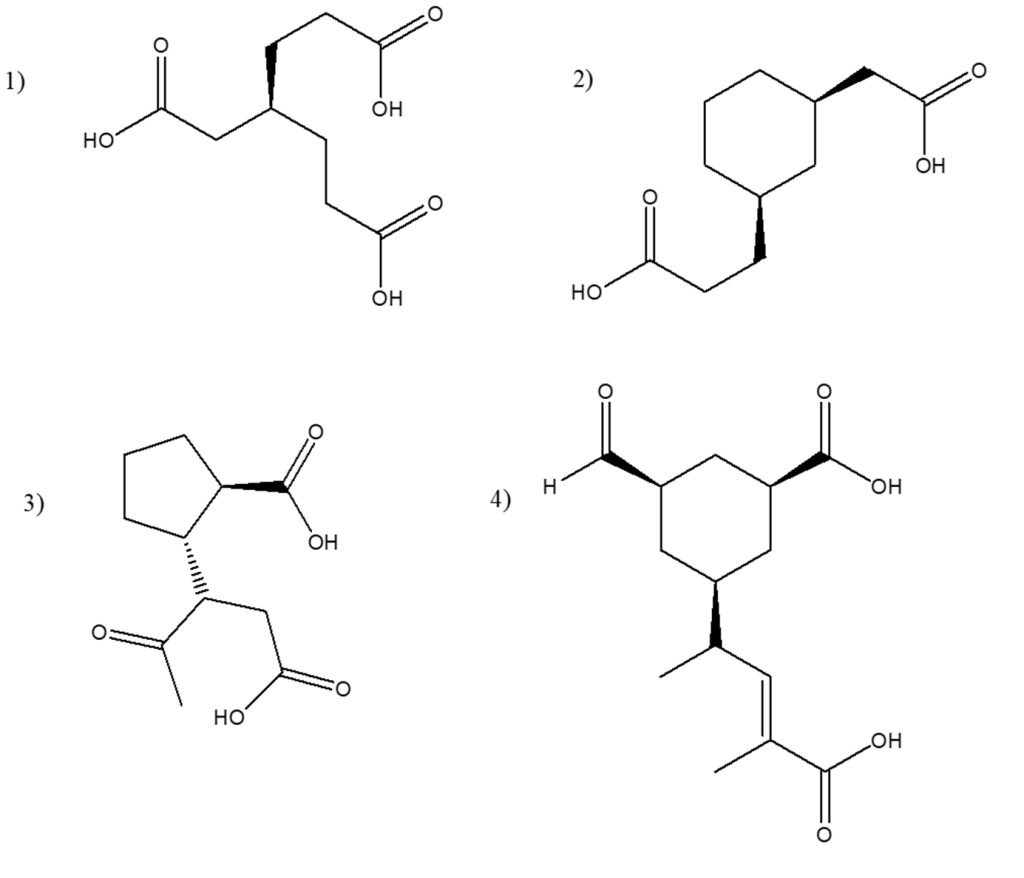

















You must be logged in to post a comment.