Esercitazione di recupero sulla stereochimica

Università degli Studi della Campania "Luigi Vanvitelli"


Prima di svolgere questi esercizi, oltre a studiare le reazioni di idroborazione-ossidazione e di addizione di alogeni (inclusi gli aspetti relativi alla stereochimica) dal libro e dagli appunti, potrebbe essere utile consultare il materiale didattico condiviso.
1) Scrivere il meccanismo e i prodotti della reazione di idroborazione-ossidazione dei composti dell’esercizio 1 del post precedente (SEGUIRE IL LINK). Indicare anche la stereochimica dei prodotti e assegnare il nome IUPAC a ciascuno di essi.
2) Scrivere il meccanismo e i prodotti della reazione dei composti dell’esercizio 1 del post precedente con Br2 in diclorometano (il diclorometano è il solvente). Indicare anche la stereochimica dei prodotti e assegnare il nome IUPAC a ciascuno di essi.
3) Scrivere il meccanismo e i prodotti della reazione dei composti dell’esercizio 1 del post precedente con Br2 in acqua (l’acqua è il solvente, ma fornisce anche un nucleofilo competitivo). Indicare anche la stereochimica dei prodotti e assegnare il nome IUPAC a ciascuno di essi.
4) Scrivere il/i prodotto/i di idrogenazione catalitica per le seguenti molecole (indicare la stereochimica) :
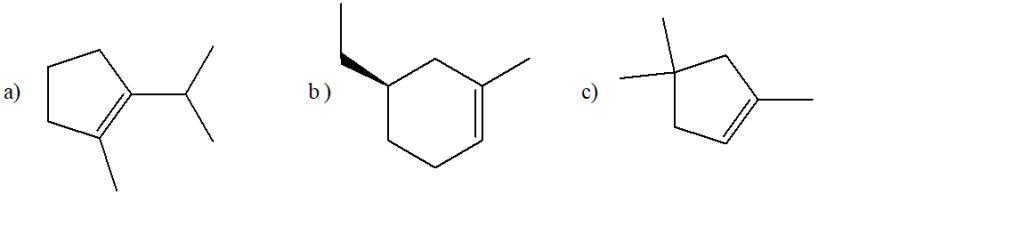

5) Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
Consultare i consigli sull’analisi retrosintetica presenti nel materiale didattico sul blog prima di svolgere l’esercizio.

6) Quale/i delle seguenti reazioni darà come prodotto un composto meso?

7) Come sintetizzeresti i seguenti alcoli a partire da un alchene? Indicare i reagenti necessari, le condizioni di reazione e la stereochimica di tutti i prodotti. Mostrare il meccanismo di reazione.

8) Sintetizzare il seguente composto utilizzando 1-butene come unica fonte di atomi di carbonio.
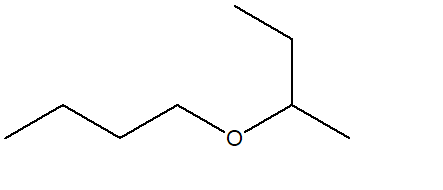

Quando è necessario prevedere il meccanismo e il/i prodotti principali di una reazione dobbiamo porre attenzione, dove appropriato, alla regioselettività, stereoselettività e stereospecificità della reazione stessa. È dunque chiaro che lo studio preliminare dei meccanismi di reazione è essenziale. Nel rivedere tali meccanismi, provare a razionalizzare ogni passaggio in termini di reazione del nucleofilo con l’elettrofilo.
Nel descrivere il meccanismo di reazione, è importante fare un uso corretto delle frecce ricurve, per mostrare il movimento degli elettroni, e delle frecce adatte ad indicare il passaggio da uno stadio all’altro della reazione. Prestare, inoltre, attenzione alla presenza di eventuali atomi carichi positivamente o negativamente.
Per reazioni che prevedono la formazione di un intermedio carbocationico, fare sempre attenzione alla possibilità di trasposizioni che possano portare alla formazione di un carbocatione più stabile.
Seguire l’aspetto stereochimico delle reazioni
Per le reazioni stereospecifiche* (e, di conseguenza, stereoselettive), è necessario seguire la stereochimica della reazione utilizzando le opportune rappresentazioni grafiche (per i composti a catena aperta, usare strutture a cavalletto o formule prospettiche).
Di seguito, due esempi.
Nel primo, facciamo reagire il (2E)-3-metil-2-pentene con Br2 in H2O. Mostriamo la stereochimica della reazione utilizzando le formule prospettiche.
Ricordiamo che il doppio legame è planare (i due carboni sp2 e gli atomi ad essi direttamente legati giacciono tutti in un piano); nell’immagine che segue, troverete i sostituenti legati ai carboni sp2 su cuneo pieno o su cuneo tratteggiato. Questo indica che stiamo immaginando che il piano su cui si trovano tutti i legami dei due carboni ibridati sp2 non è quello sello schermo (o del foglio), ma quello ad esso perpendicolare.
Gli elettroni π (pi-greco) potranno dare l’attacco all’elettrofilo sia al di sopra sia al di sotto del piano. Nell’immagine seguente è mostrato l’attacco verso l’alto. Si formerà quindi lo ione bromonio ciclico che subirà l’attacco del nucleofilo sul carbonio più sostituito. Questo attacco avviene in anti. Si formerà, quindi, un unico stereoisomero. (NB: per una descrizione dettagliata del meccanismo si rimanda al libro).

Da questa reazione stereospecifica (e quindi anche stereoselettiva) otterremo anche l’enantiomero del prodotto appena formato. Questo deriva dalla formazione dello ione bromonio sulla faccia inferiore del piano definito dai due carboni sp2.

NB: il prodotto ottenuto a seguito dell’attacco dell’acqua su questo ione bromonio avrà configurazione (2S,3R)
È possibile mostrare la stereochimica della reazione anche utilizzando le rappresentazioni a cavalletto.
A titolo di esempio, facciamo avvenire la reazione sull’alchene (2Z)-3-metil-2-pentene (ci aspettiamo, dunque, la formazione di due composti che saranno tra loro enantiomeri, e saranno diastereoisomeri dei prodotti della reazione precedente).
Per usare le strutture a cavalletto, riportiamo il doppio legame come mostrato di seguito (attenzione a rispettare la geometria del doppio legame!). Anche in questo caso, per attacco da parte degli elettroni π all’elettrofilo da sopra o da sotto al piano di formano due ioni bromonio. Qui è mostrato l’attacco verso il basso che porterà alla sintesi dello stereoisomero mostrato.

Per definire la stereochimica è consigliabile riportare la struttura su una proiezione di Fischer (ricordandosi di eclissarla prima di farlo).
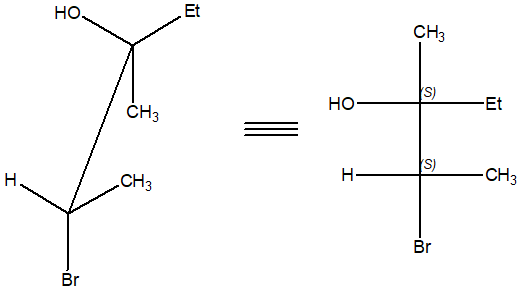
A seguito della formazione dell’altro ione bromonio (che deriva dall’attacco al di sopra del piano), si otterrà l’enantiomero del composto qui ottenuto.
NB: avendo familiarità con le varie rappresentazioni delle molecole organiche, è possibile passare agevolmente dall’una all’altra. A questo punto potremmo, ad esempio, scrivere questo composto usando una struttura a segmenti.
La tabella 6.1 del libro può essere utile per verificare se la stereochimica della reazione è stata determinata correttamente
*Tutte le reazioni stereospecifiche sono anche stereoselettive (mentre non è sempre vero il contrario)
Analisi retrosintetica
Se per le reazioni stereospecifiche è necessario effettuare un’analisi retrosintetica (analisi necessaria per capire quale è l’alchene di partenza), è essenziale tener conto proprio della stereochimica con cui procede la reazione. È quindi fondamentale capire da quale alchene partire: per farlo, bisogna aver ben chiaro se la reazione prevede una stereochimica sin o anti.
Vediamo che succede se la reazione procede con stereochimica anti
ES.1: Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.

Si tratta di una reazione di un alchene (3-metil-2-pentene) con bromo in metanolo. Poichè questa è una reazione stereospecifica, è ESSENZIALE capire da quale isomero (E o Z) dell’alchene bisogna partire per ottenere il prodotto desiderato. Dal momento che questa reazione è anche stereoselettiva, determiniamo le configurazioni assolute dei carboni chirali, sapendo che in questo caso otterremo anche l’enantiomero.

Per capire da quale alchene dobbiamo partire, trasformiamo questa proiezione di Fischer in una rappresentazione a cavalletto, sapendo che i sostituenti sulla linea verticale si trovano lontani dall’osservatore, mentre quelli sulla linea orizzontale sono rivolti verso l’osservatore:
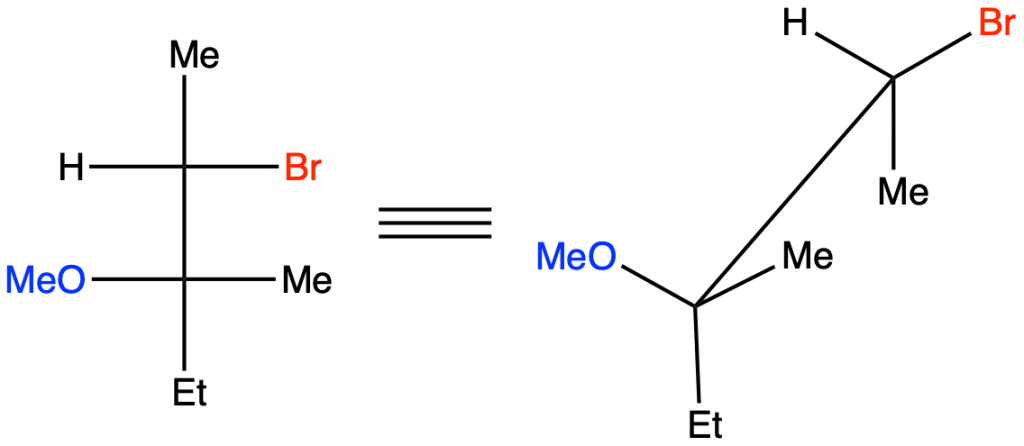
L’addizione di bromo in metanolo procede con stereochimica anti; questo significa che Br e OMe devono trovarsi da parte opposta. Ruotiamo dunque la rappresentazione a cavalletto lungo il legame C2-C3 in modo da evidenziare quanto appena detto (dobbiamo ottenere il conformero sfalsato qui mostrato):

L’alchene di partenza è dunque (2Z)-3-metil-2-pentene (se la struttura a cavalletto è orientata come sopra mostrato e i sostituenti sono correttamente posizionati, basta a questo punto “eliminare” i due sostituenti e “aggiungere” il doppio legame come mostrato in figura).
Il seguente video può essere utile per visualizzare l’attacco in anti:
Vediamo che succede se la reazione procede con stereochimica sin
ES. 2: Da quale 2,3,4-trimetil-3-esene è possibile ottenere il seguente prodotto di idrogenazione catalitica?
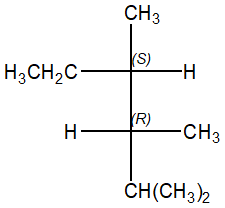
L’idrogenazione catalitica porta all’addizione di un idrogeno a ciascun carbonio sp2 e procede con stereochimica sin.
La reazione è stereospecifica. Per capire da quale alchene dobbiamo partire, trasformiamo la proiezione di Fischer in una rappresentazione a cavalletto

L’addizione avviene con stereochimica sin; questo significa che i due H devono trovarsi dallo stesso lato. Ruotiamo dunque la rappresentazione a cavalletto lungo il legame C3-C4 in modo da evidenziare quanto appena detto (dobbiamo ottenere il conformero eclissato qui mostrato):
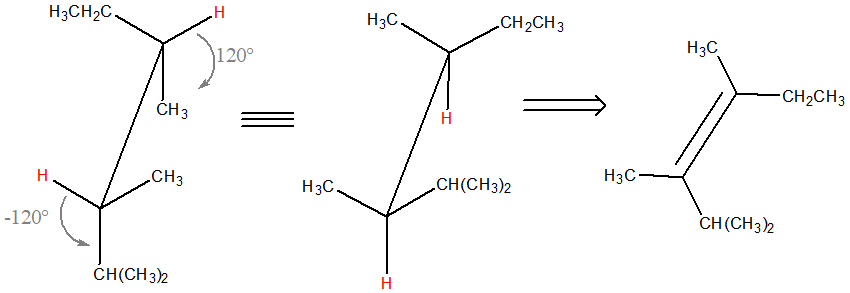
L’alchene di partenza è dunque (3Z)-2,3,4-trimetil-3-esene (se la struttura a cavalletto è orientata come sopra e i sostituenti sono correttamente posizionati, per definire l’alchene di partenza, basta a questo punto “eliminare” i due atomi di idrogeno e “aggiungere” il doppio legame come mostrato in figura). Da questo alchene, per idrogenazione catalitica, otterremo anche l’enantiomero del composto iniziale.
NB: in molti esercizi, una volta individuato l’alchene di partenza, viene poi richiesto di mostrare anche il meccanismo che porta alla formazione dei prodotti oppure viene chiesto di indicare eventuali altri prodotti (LEGGERE SEMPRE BENE LA TRACCIA).
Schemi riassuntivi e materiale didattico integrativo
Qui è possibile scaricare una tabella riassuntiva delle reazioni degli alcheni che può integrare lo schema che trovate sul libro alla fine del capitolo dedicato proprio a queste reazioni.
NB: per gli aspetti regiochimici delle reazioni per cui le informazioni non sono presenti nella tabella, far riferimento al testo e agli appunti delle lezioni (in quanto l’argomento richiede una trattazione più dettagliata; ad es.: la reazione che porta alla sintesi di aloidrine dà una regioselettività Markovnikov che è possibile capire analizzando il meccanismo della reazione).
Al link seguente è possibile scaricare un secondo schema riassuntivo sulle reazioni degli alcheni studiate. Sono inoltre riportati, nello stesso file, alcuni approfondimenti relativi sia alle trasposizioni, sia agli orbitali coinvolti in alcune delle reazioni in questione:
Infine, qui è possibile scaricare materiale relativo alla reazione di ossimercuriazione-riduzione.
Nel corso della reazione, si forma uno ione mercurinio a ponte come intermedio, che viene, a sua volta, attaccato dall’acqua. Questo stadio avviene con stereoselettività anti. In un secondo stadio, viene aggiunto NaBH4, ottenendo così il prodotto di riduzione. Questo passaggio rimescola la stereochimica, per cui il processo complessivo è un misto di addizione sin e anti.

Mercoledì 20 Novembre dalle 16:00 alle 18:00 si terrà un’esercitazione di recupero sulla stereochimica.

Nota: gli esercizi che seguono sono quelli della prova scritta di Luglio 2024
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2) Completare la seguente struttura di Lewis e calcolare la carica formale per tutti gli atomi diversi all’idrogeno:
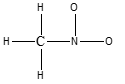
3) Quali sono la geometria, l’angolo di legame e l’ibridazione previste per il catione metile?
4) Dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/ isomeri geometrici/isomeri conformazionali/ stesso composto/isomeri costituzionali/altro)

5) Disporre i seguenti composti in ordine di basicità decrescente e spiegare sinteticamente il perché:
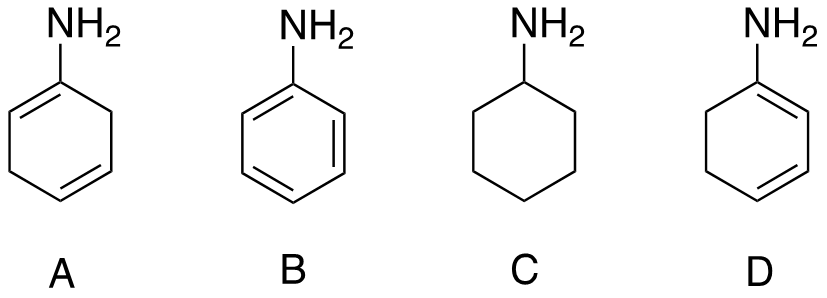
6) Scrivere i prodotti principali delle seguenti reazioni.


7) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione del ciclopentanone con dimetilammina.
8) L’acido L-aspartico è un amminoacido con R= -CH2COOH.
I valori di pKa dei gruppi ionizzabili sono i seguenti:
pKa α-COOH = 2.09
pKa α-NH3+ = 9.82
pKa COOH in catena laterale = 3.86
a) Scrivere l’amminoacido in proiezione di Fischer al punto isoelettrico
b) Determinare la configurazione assoluta del carbonio chirale
c) Calcolare il punto isoelettrico
d) Scrivere la struttura dell’amminoacido a pH>10 e a pH <1

Regolamento:
Prendendo in considerazione le reazioni di addizione elettrofila al doppio legame, per i composti mostrati in basso è stato osservato il seguente ordine di reattività:
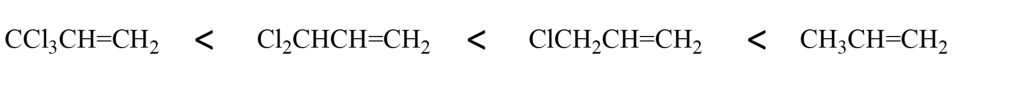
Fornire una spiegazione plausibile utilizzando non più di 20 parole

NB: PRIMA di AFFRONTARE GLI ESERCIZI DI QUESTO POST è NECESSARIO AVER STUDIATO E COMPRESO AL FONDO LA PARTE RELATIVA AGLI ASPETTI TERMODINAMICI E CINETICI DELLE REAZIONI, OLTRE AI MECCANISMI DI ADDIZIONE DI HX, ACQUA E ALCOL AD UN ALCHENE (INCLUSI GLI ASPETTI STEREOCHIMICI)
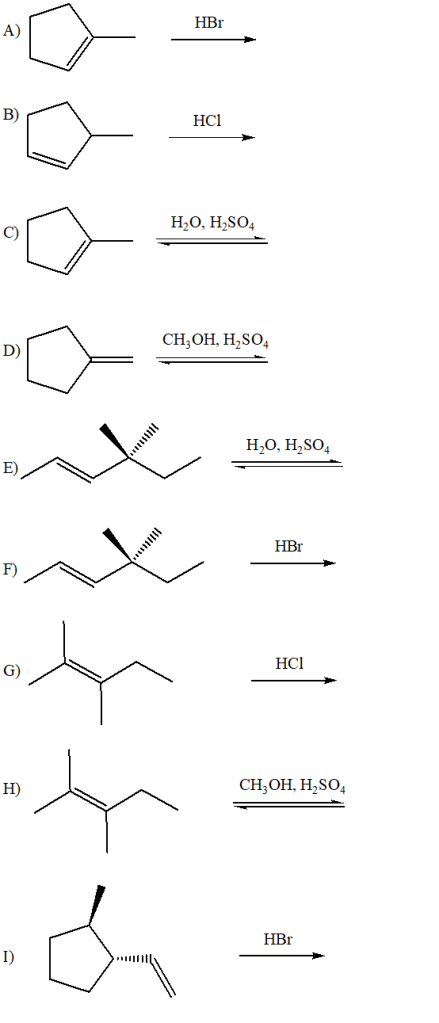
1) Scrivere il meccanismo e il/i prodotto/i (indicando qual è il principale, quando necessario) della reazione dei seguenti composti con HCl. Indicare anche la stereochimica dei prodotti e assegnare il nome IUPAC a ciascuno di essi.
a) 2-metil-2-pentene
b) 2-metil-1-pentene
c) (2E)-4-metil-2-pentene
d) 4-metil-1-pentene
e) (4R)-4-metil-1-esene
f) 4-etil-2-esene
g) (2Z)-4,4-dimetil-2-pentene
h) (2E)-4,4-dimetil-2-pentene
i) 1-metil-1-cicloesene
l) (6S)-1,6-dimetil-1-cicloesene
2) Proporre una strategia per la sintesi dei seguenti alogenuri alchilici partendo da un alchene. Quando sono possibili più opzioni, scegliere quella che darà il composto desiderato come prodotto principale o come unico prodotto e argomentare la scelta. Infine, per ogni reazione, indicare la stereochimica dei prodotti.
a) 2-cloropentano
b) 2-bromo-2-metilbutano
c) 2-cloro-2,3-dimetilbutano
d) 2-cloro-2,3-dimetilpentano
3) Per le reazioni dell’1-butene e del 2-butene con I) acido bromidrico e II) con acqua in ambiente acido:
1) mostrare i meccanismi;
2) disegnare, per ciascuna reazione, un grafico della variazione dell’energia libera rispetto alla coordinata di reazione in cui vengono indicate le strutture dei reagenti, degli stati di transizione, degli intermedi e dei prodotti;
3) se i carbocationi che si formano sono caratterizzati da stabilità differente, dire quali fattori stabilizzano i carbocationi più stabili
4) indicare se le reazioni sono o meno regioselettive (e quando possibile indicare anche il grado di regioselettività).
4) Determinare l’ordine di reattività in una reazione di addizione di acido alogenidrico per i seguenti alcheni: 2-metilpropene; (2Z)-2-butene; (2E)-2-butene. Motivare la risposta.
5) I seguenti meccanismi di reazione sono caratterizzati da un certo numero di errori gravissimi. Individuarli e correggerli.

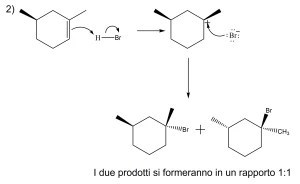
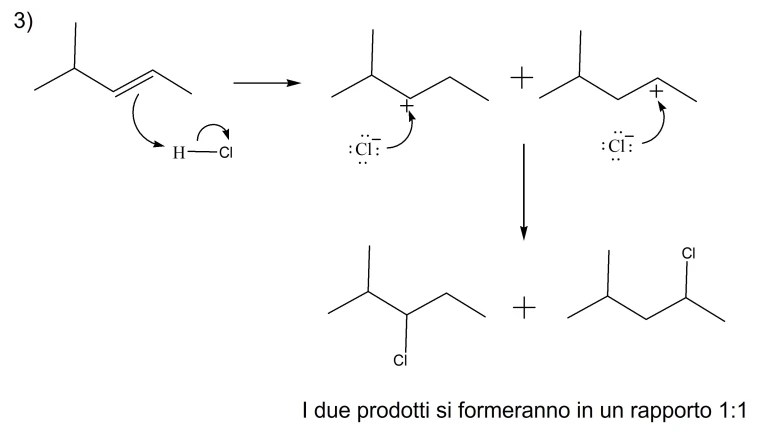
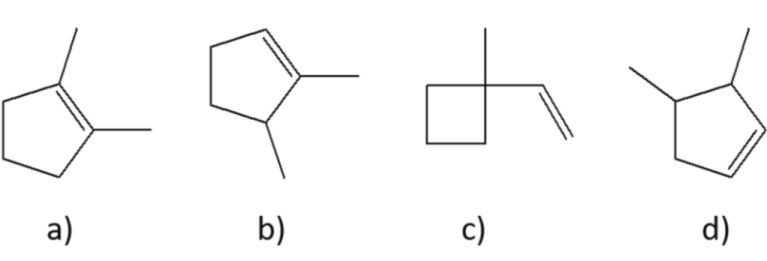
6) Quale/i dei seguenti alcheni darà l’1-bromo-1,2-dimetilciclopentano come prodotto principale della reazione con HBr?
7) La coordinata di reazione qui sotto mostra il profilo energetico della reazione di 3 alcheni diversi con HBr. Identificare alla reazione di quale alchene si riferisce ciascuna curva:

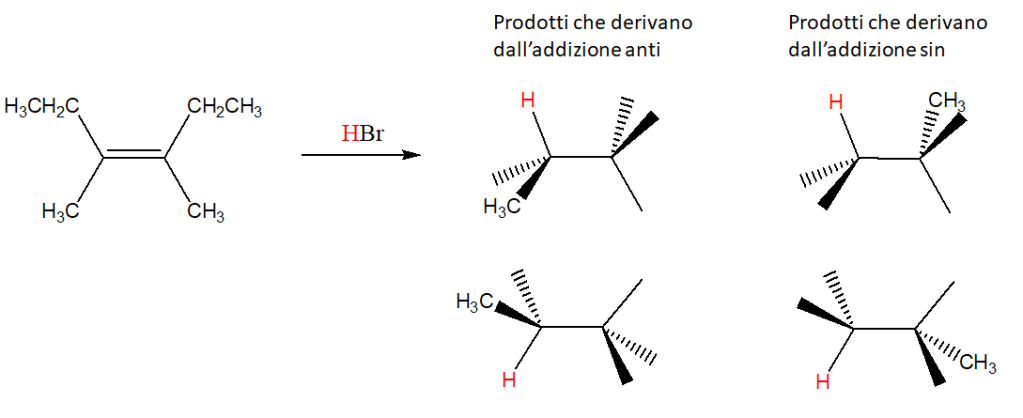
8) Completare i prodotti della seguente reazione, prendendo in considerazione quella che è la posizione relativa dei sostituenti già indicati (attenzione: tutte le strutture dei prodotti sono qui riportate come conformazioni eclissate, anche quelle che derivano dall’addizione sin).
9) Disegnare la formula di struttura dell’alchene di formula molecolare C8H14 che, per reazione con HBr, dà come prodotto principale 1-bromo-1-isopropilciclopentano.
10) Scrivere il meccanismo e il/i prodotto/i principale/i della reazione di idratazione acido-catalizzata dei composti dell’esercizio 1. Indicare anche la stereochimica e assegnare il nome IUPAC a ciascuno dei prodotti.
11.A) Di seguito è mostrato il diagramma energetico della reazione di idratazione acido-catalizzata del 2-butene:
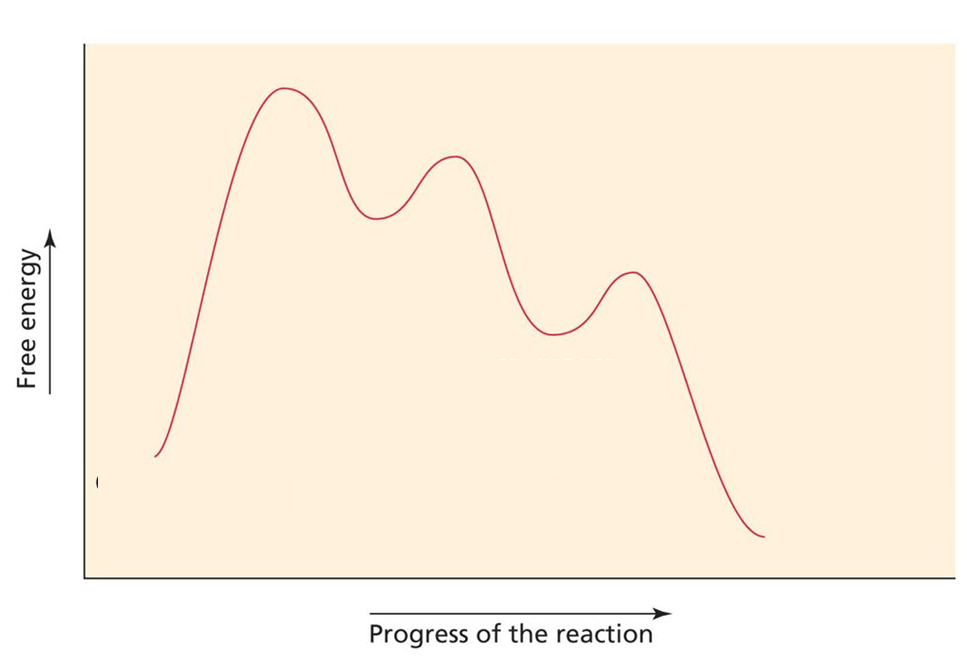
a) Cosa possiamo dire circa il ΔG° della reazione?
b) Cosa possiamo dire circa la Keq della reazione?
c) Di quanti stadi si compone la reazione?
d) Qual è lo stadio cineticamente determinante?
e) Indicare sul grafico l’energia di attivazione relativa a ciascuno stadio
f) Disegnare lo stato di transizione dello stadio cineticamente determinante.
g) Quanti intermedi si formano nel corso della reazione? Disegnarne la/le struttura/e.
11.B) Disegnare il diagramma energetico della reazione del 2-metil-2-butene con HCl e giustificare la regioselettività della reazione.
12) Proporre un metodo per sintetizzare l’1,2-dimetilcicloesanolo a partire dal 3,3-dimetilcicloes-1-ene.
13) Spiegare perchè il prodotto della reazione di idratazione acido-catalizzata del (4R)-4-metil-1-esene ruota il piano della luce polarizzata.
14) La reazione del 2-metilpropene con metanolo in presenza di acido solforico porta alla formazione del 2-metossi-2-metilpropano (=terz-butil metil etere). Proporre un meccanismo per la formazione dell’etere.
15) Spiegare perché è impossibile sintetizzare il seguente etere utilizzando la reazione tra un alchene e un alcol:

16) Mostrare il meccanismo e i prodotti delle seguenti reazioni. Nel caso, indicare il/i prodotti principali. Indicare la stereochimica e attribuire il nome IUPAC a tutti i prodotti.
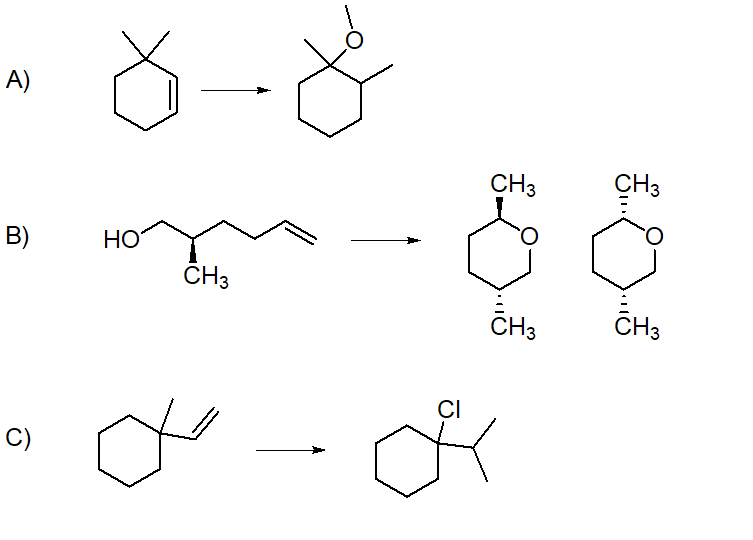
17) Proporre un meccanismo per le seguenti trasformazioni

18) Indicare le condizioni di reazione e proporre un meccanismo per le seguenti trasformazioni
19) Metti i seguenti carbocationi in ordine di stabilità crescente, motivando la scelta:

20) Mostrare il meccanismo della seguente trasformazione:



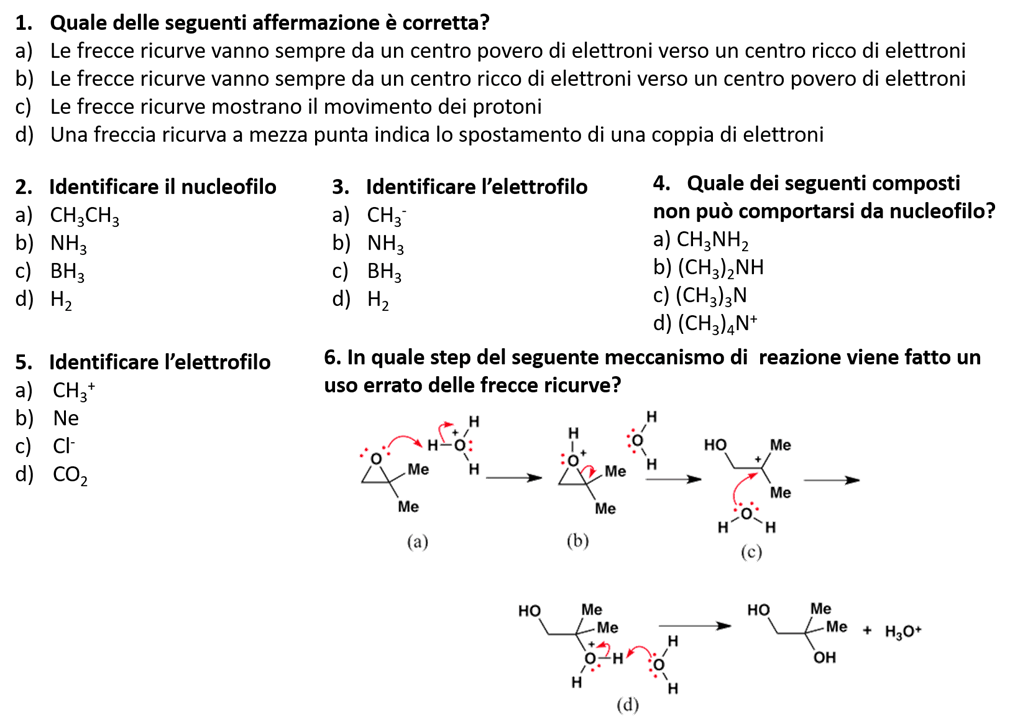
7) Dire quali delle seguenti specie chimiche tenderanno a reagire come nucleofili e quali come elettrofili
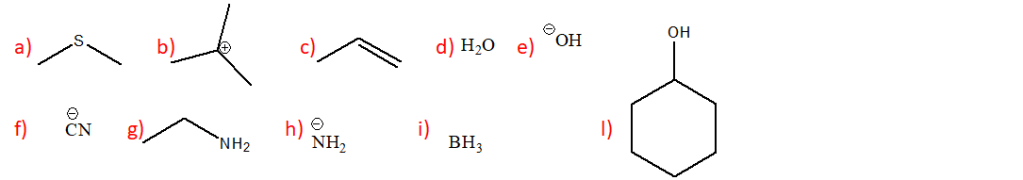
8) Sulla base del movimento degli elettroni mostrato dalle frecce ricurve nelle seguenti reazioni, disegnare i prodotti

9) Queste due reazioni formano i prodotti mostrati, ma non attraverso i meccanismi disegnati! Per ciascun meccanismo, spiegare perchè è errato e disegnarne uno corretto

10) Quale delle seguenti affermazioni è falsa:
a) se una reazione è spontanea, può avvenire velocemente
b) una reazione lenta può essere spontanea
c) se una reazione è spontanea, può avvenire lentamente
d) una reazione spontanea deve avere energia di attivazione bassa
11) Disegnare il diagramma energetico di una reazione monostadio con Keq<1. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, variazione dell’energia libera di Gibbs, energia di attivazione. Il ΔG° è positivo o negativo?
12) Disegnare il diagramma energetico di una reazione a due stadi con Keq>1. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, intermedio, variazione dell’energia libera di Gibbs, energia di attivazione. Il ΔG° è positivo o negativo?
13) Disegnare il diagramma energetico di una reazione esoergonica a due stadi, il cui secondo stadio sia più veloce del primo.
14) Data la seguente legge cinetica per una reazione:
velocità= k [A]1[B]2
determinare: a) l’ordine della reazione rispetto ad A; b) l’ordine della reazione rispetto a B; c) l’ordine complessivo per la reazione.
Rispondere, inoltre, alle seguenti domande: d) Che succede alla velocità della reazione raddoppiando la concentrazione di A? e) E raddoppiando la concentrazione di B?
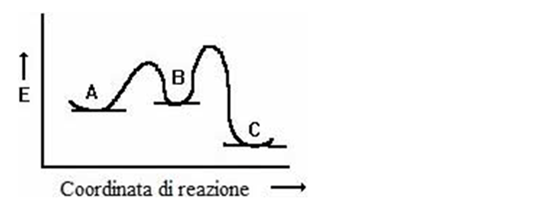
15) Individuare, nel grafico riportato, I) l’energia di attivazione per la reazione A–>B ,II) l’energia di attivazione per la reazione B–>A

16) Basandosi sul seguente diagramma energetico, il composto________si formerà più velocemente a partire da B. Il composto più stabile è_____perchè_____________________________________________________________.
17) Di seguito è mostrato il diagramma energetico di una reazione.
a) individuare lo stato di transizione;
b) dire se la reazione è esoergonica o endoergonica;
c) cosa possiamo dire circa la costante di equilibrio di questa reazione?
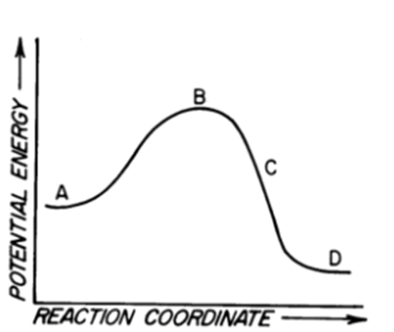
18) Rispondere alle seguenti domande sul diagramma energetico mostrato in basso
a) di quanti stadi si compone la reazione?
b) quanti e quali intermedi si formano?
c) quanti e quali stati di transizione?
d) qual è lo stadio cineticamente determinante?
e) si tratta di una reazione esoergonica o endoergonica?
f) quale sarebbe l’effetto dell’aggiunta di un catalizzatore?

19) Disegnare il diagramma energetico della reazione del 3-metil-1-butene con HBr. Mostrare le strutture dello stato di transizione e degli intermedi di reazione
20) Quale delle seguenti opzioni descrive correttamente la seguente reazione?

21) In un tipico diagramma di reazione, a cosa corrisponde l’asse delle ascisse?
a) variazione di energia libera
b) coordinata di reazione
c) temperatura
d) variazione di entalpia
e) variazione di entropia
22) Quale tra le seguenti è la relazione corretta che intercorre tra la variazione di energia libera di Gibbs e la costante di equilibrio di una reazione chimica?

23) Si definisce stato di transizione di una reazione:
a) una delle strutture di risonanza dei reagenti
b) la struttura a più bassa energia associata ad un certo stadio della reazione
c) un carbocatione
d) la struttura intermedia tra reagenti e prodotti, isolabile e relativamente stabile
e) la struttura a più alta energia associata ad un certo stadio della reazione.
24) Quale delle seguenti coordinate di reazione è relativa ad una reazione esoergonica che procede con la formazione di un intermedio?

25) Assumendo condizioni standard e in riferimento alla seguente coordinata di reazione, quale delle seguenti affermazioni è sicuramente vera?

26) Data la seguente coordinata di reazione, la freccia rossa indica:

27) Osservando il seguente diagramma di coordinata per la reazione che da A porta a D, rispondere alle seguenti domande
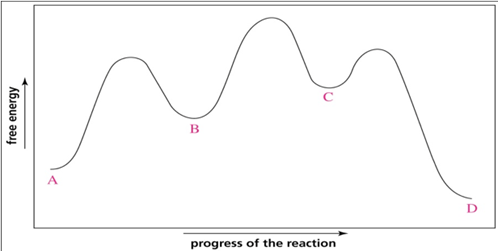
a) quanti intermedi ci sono nella reazione?
b) quanti stati di transizione ci sono?
c) qual è lo stadio più veloce nella reazione?
d) chi è più stabile A o D?
e) qual è il reagente nello stadio determinante la velocità?
f) il primo stadio della reazione è esoergonico o endoergonico?
g) la reazione, nel complesso, è esoergonica o endoergonica?
28) Molte reazioni sono più veloci ad alte che a basse temperature. Questo è in accordo con:
(I) Un aumento della energia di attivazione all’aumentare della temperatura
(II) Un aumento della costante cinetica all’aumentare della temperatura
(III) Un aumento della frequenza di collisioni efficaci all’aumentare della temperature.
a)Solo I
b)Solo II
c)Solo III
d)Solo I e II
e)Solo II e III
29) Analizzare il diagramma di energia libera/coordinata di reazione dell’addizione di HBr al 2-metilpropene e rispondere ai seguenti quesiti.

a) Cosa possiamo dire circa la Keq della reazione?
b) Cosa possiamo dire circa il ΔG° della reazione?
c) Di quanti stadi si compone la reazione?
d) Qual è lo stadio cineticamente determinante?
e) Indicare sul grafico l’energia di attivazione relativa allo stadio cineticamente determinante.
f) Cosa sono, rispettivamente, B, C e D?
30) Disponi i seguenti composti in ordine di calore di idrogenazione decrescente


Il ricevimento di oggi si terrà alle 16:00 in aula B.
Gli esami di venerdì 15 si terranno alle 16 in aula B1. Gli studenti che hanno prenotato il ricevimento dalle 16 in poi dovranno recarsi nella stessa aula per poter prendere visione della prova.
Per quanto riguarda le esercitazioni di recupero, si fa presente che saranno prese in considerazione solo le prenotazioni degli studenti che seguono il corso regolarmente (fermo restando la possibilità di tutti di partecipare). https://chimicaorganicadistabif.com/2024/11/11/questionario-in-preparazione-allesercitazione-2/
You must be logged in to post a comment.