Risultati ultima prova di Chimica Organica

Di seguito sono riportati i risultati dell’ultima prova.
A breve saranno pubblicati i voti medi con le ammissioni alla prova orale


Università degli Studi della Campania "Luigi Vanvitelli"

Di seguito sono riportati i risultati dell’ultima prova.
A breve saranno pubblicati i voti medi con le ammissioni alla prova orale



Regolamento:
CHALLENGE
Alcuni tipi di esteri, come il dietil succinato, condensano con aldeidi e chetoni in presenza di basi come EtONa, NaH o t-BuOK. Questa reazione è chiamata condensazione di Stobbe.
Quando si fa reagire il cicloesanone con butillitio si ottiene il corrispondente enolato di litio. Questo enolato, cicloes-1-en-1-olato di litio, reagisce con 2 equivalenti di prop-2-enoato di etile per formare, in seguito a diversi stadi, l’estere dietilico dell’acido 1-idrossibiciclo-[4.4.0]decan-2,4-dicarbossilico. Dopo la condensazione del cicloes-1-en-1-olato di litio con il primo equivalente di prop-2-enoato di etile, la reazione è condotta in presenza di etossido di sodio (condensazione di Stobbe).
Proporre il meccanismo della reazione.
La challenge scadrà alle 19:30 del 5 maggio


L’ultima esercitazione di Chimica Organica si terrà in due turni nei giorni 7 (I TURNO) e 14 maggio (II TURNO) alle ore 14:30.

La lezione teorica si terrà lunedì 6 maggio alle ore 13,30.

RISPOSTA n. 1
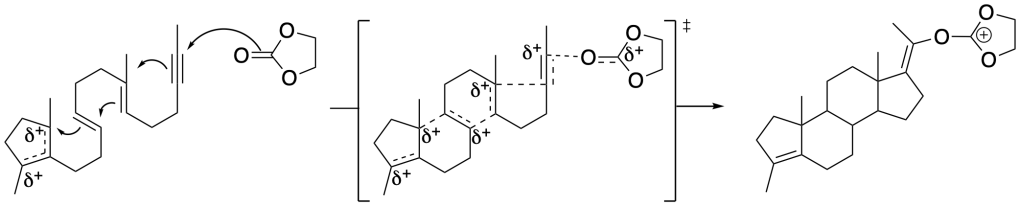
L’alcol terziario in seguito alla protonazione con TFA (acido forte), perde acuq e porta alla formazione di un carbocatione allilico.

Carbocatione allilico:

in seguito all’attacco dell’1,3-diossolan-2-one, questo intermedio va incontro ad una serie di ciclizzazioni concertate che portano alla formazione dell’intermedio B
RISPOSTA n. 2
Il composto C viene trattato con ozono in modo da ottenere un dichetone:

Il dichetone, trattato con NaOH dà luogo ad una reazione aldolica intramolecolare:
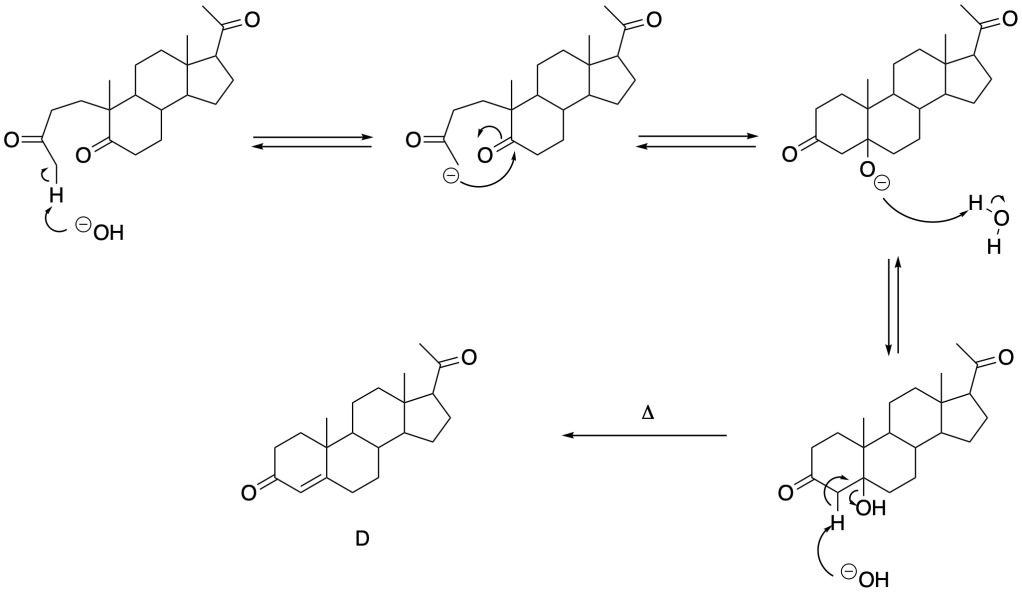
CONGRATULAZIONI ALLA VINCITRICE DELLA CHALLENGE


Regolamento:
CHALLENGE
La procedura standard per sintetizzare un determinato composto è quella di avvicinarsi alla struttura della molecola target per stadi, formando i vari legami per mezzo di reazioni specifiche. In generale, il prodotto di ogni reazione viene isolato e purificato prima della reazione successiv. Uno dei metodi con cui la natura evita questa noiosa pratica, basata sull’isolamento e la purificazione, è quello di usare una reazione domino ,ossia una reazione in cui ogni stadio porta a condizioni favorevoli affinché si verifichi lo stadio successivo. Un esempio importante di reazione domino sviluppata in laboratorio è quella della sintesi del progesterone (un ormone femminile); si tratta di una elegante via sintetica progettata da W. S. Johnson. Inizialmente, Johnson preparò l’alcol terziario monociclico A. Quindi attraverso una reazione domino promossa da acidi, lo trasformò nel composto B che, successivamente, convertì il progesterone (D).

Un aspetto interessante di questa sintesi è che il composto A, contenente un solo stereocentro, dà il composto B, contenente cinque stereocentri, ciascuno con la stessa configurazione di quelli presenti nel progesterone naturale.
DOMANDA 1:
Assumere che la reazione domino dello stadio 1 cominci con la protonazione del gruppo alcolico terziario nel composto A, seguita dalla perdita di acqua per dare un carbocatione terziario. Mostrare in che modo la serie di reazioni iniziate dalla formazione di questo carbocatione può generare il composto B.
Negli stadi 3 e 4 l’anello A del composto subisce un riarrangiamento in seguito a due reazioni successive.
DOMANDA 2
Indicare i reagenti per ciascuno stadio; scrivere la struttura dell’intermedio del primo stadio e proporre un meccanismo per la sua trasformazione in progesterone nello stadio 4.

La challenge scadrà alle 22 del 27 aprile

Di seguito sono riportati i risultati della sesta prova intercorso (come media delle sei prove).
Tutti gli studenti identificati con il colore verde hanno ottenuto la sufficienza (verde scuro voti più alti) e sono ammessi a sostenere le prove intercorso del secondo semestre.
Gli studenti identificati dai colori giallo e arancione hanno superato con riserva. Anche gli studenti che hanno superato con riserva sono ammessi a sostenere l’e prove intercorso del secondo semestre l’ultima prova.


La dispensa della seconda esercitazione del secondo semestre è scaricabile al seguente link.
Nella lezione di domani 15 aprile ci sarà la lezione teorica, obbligatoria per accedere al laboratlrio didattico.

Esercizio n. 1
Assegnare il nome IUPAC completo di stereochimica ai seguenti composti:
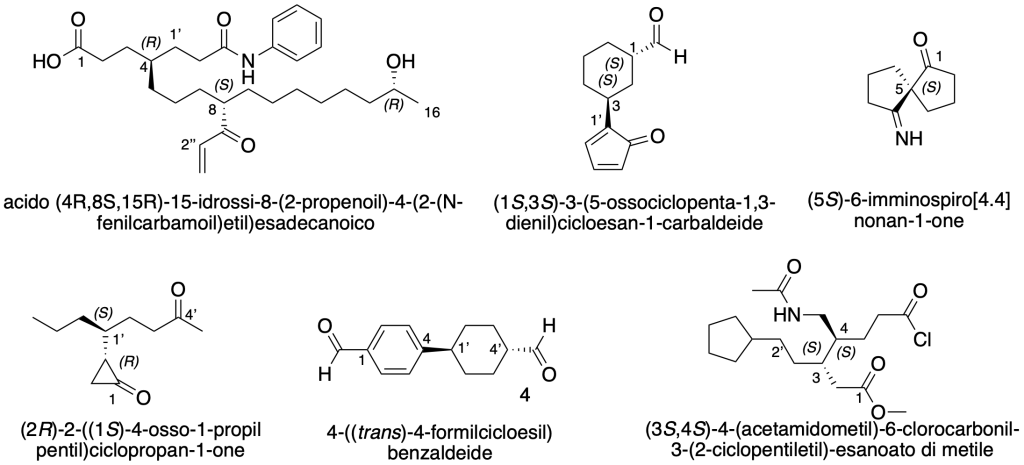
Esercizio n. 2
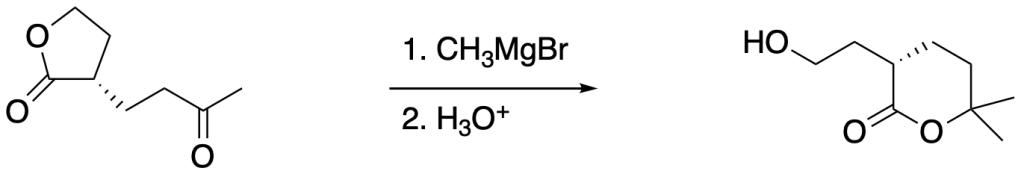
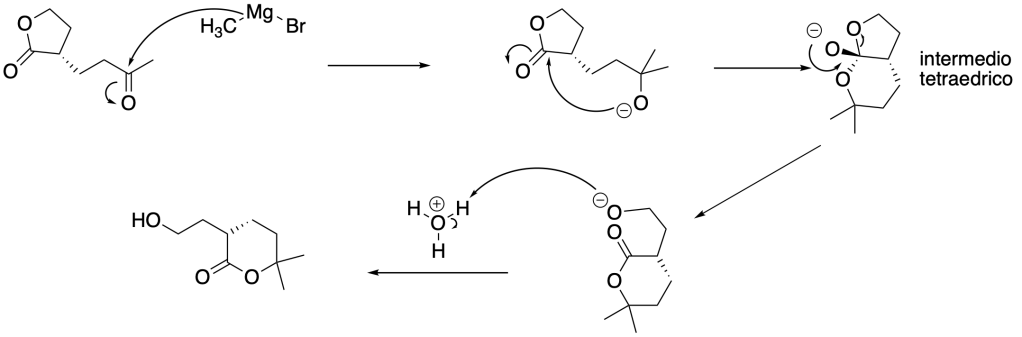
Proporre un meccanismo per la seguente reazione:
meccanismo:
Esercizio n. 3
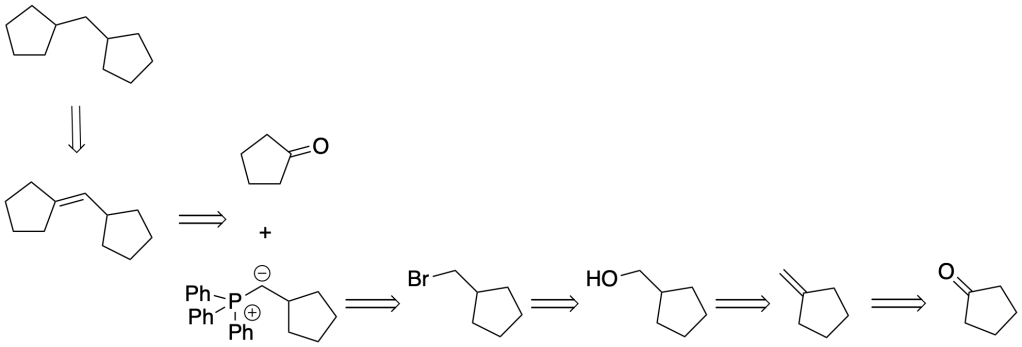
Proporre un meccanismo per la seguente trasformazione. E’ possibile usare il ciclopentanone e qualsiasi composto inorganico, compresi agenti ossidanti o riducenti.

Analisi retrosintetica:
Schema di sintesi:
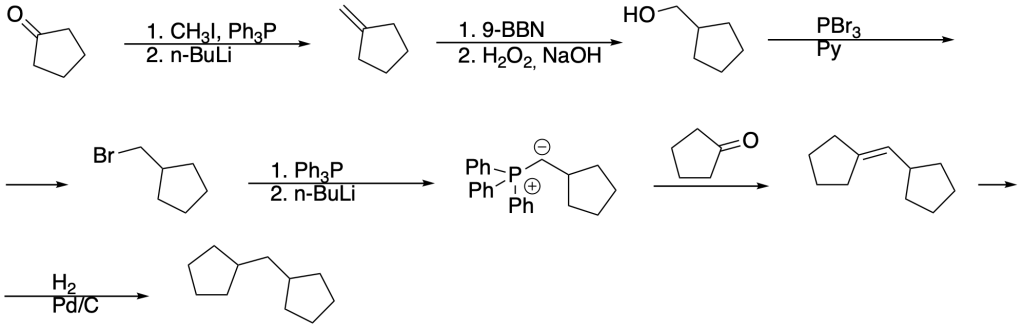
Esercizio n. 4
La sintesi di Kiliani-Fischer, a partire dall’aldopentoso D-ribosio, produce una miscela di D-allosio e D-altrosio. Il 2,6-dideossi-D-altrosio, noto anche come D-digitossosio, è un monosaccaride ottenuto per idrolisi della digitossina, un prodotto naturale estratto dalla digitale (Digitalis purpurea). La digitossina trova largo impiego in cardiologia poichè riduce la velocità delle pulsazioni, regolarizza il ritmo e rinforza il battito cardiaco. Disegnare la proiezione di Fischer del 2,6-dideossi-D-altrosio. Disegnare la struttura del beta-L-digitossopiranosio nella conformazione a sedia più stabile.
proiezione di Fischer del 2,6-dideossi-D-altrosio:
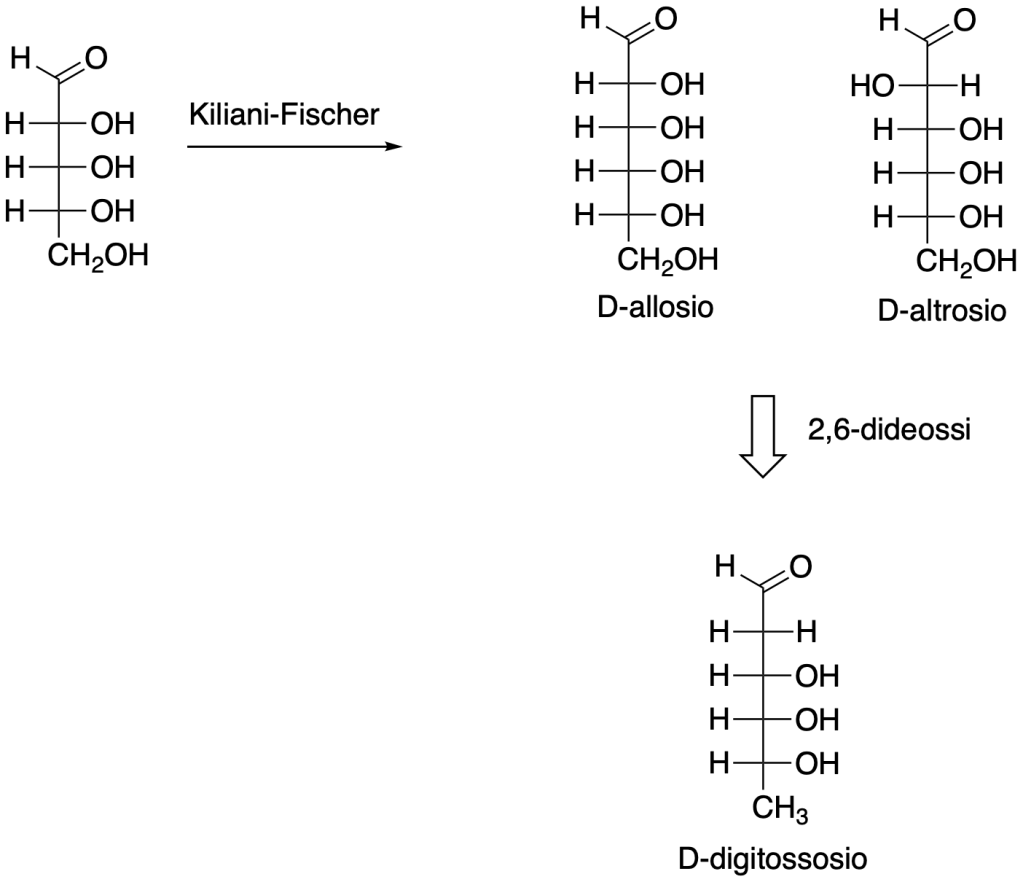
struttura del beta-L-digitossopiranosio
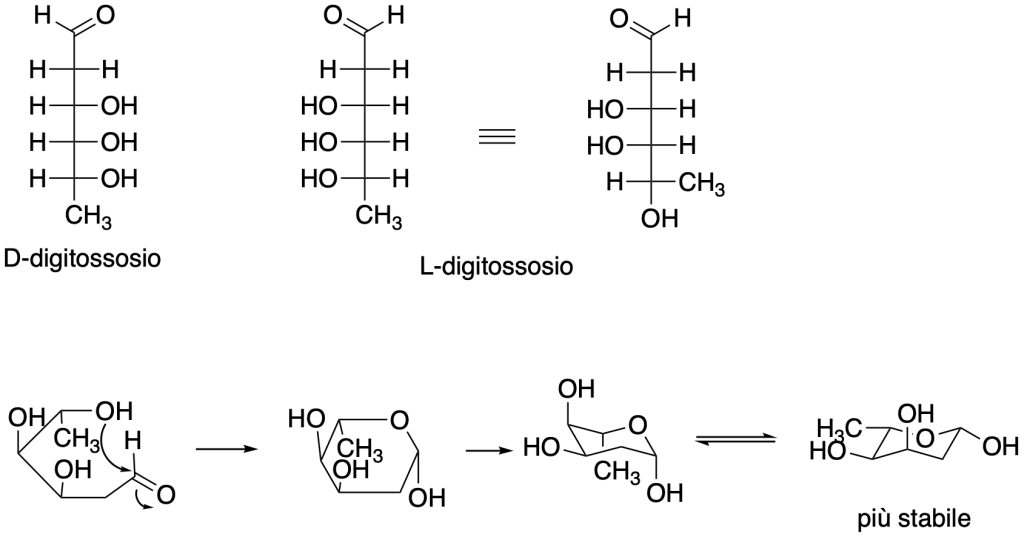
Esercizio n. 5
Proporre una sintesi efficiente della 4-idrossi-4-metilcicloesan-1-carbaldeide a partire da 4-idrossicicloesan-1-carbaldeide. Partendo dallo stesso reagente, proporre la sintesi dell’1-ciclesil-1-etanone
Sintesi della 4-idrossi-4-metilcicloesan-1-carbaldeide

Analisi retrosintetica
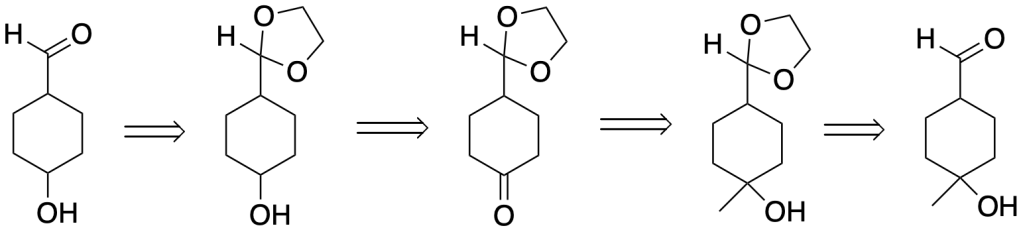
Schema di sintesi
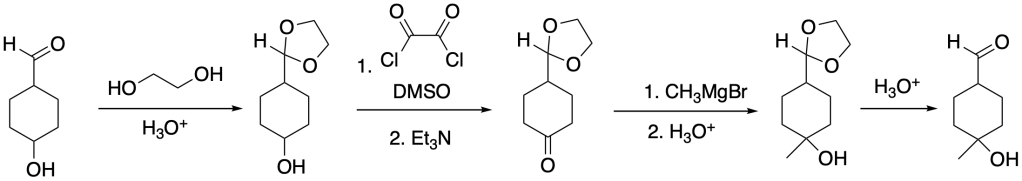
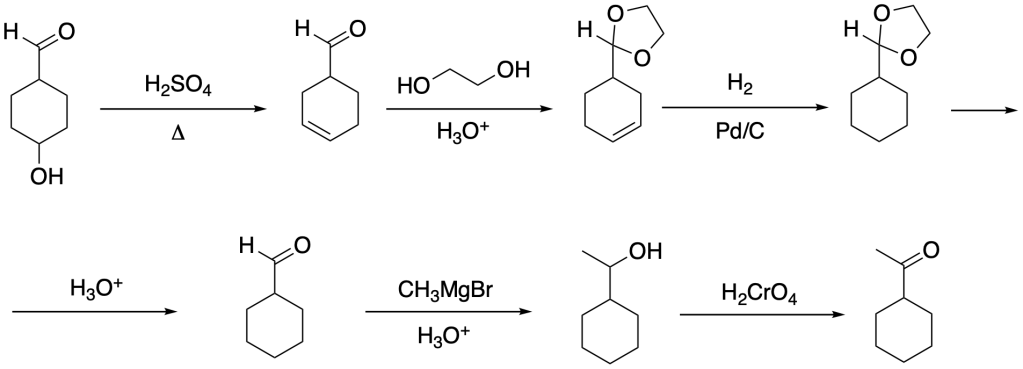
Sintesi dell’1-ciclesil-1-etanone

Analisi retrosintetica
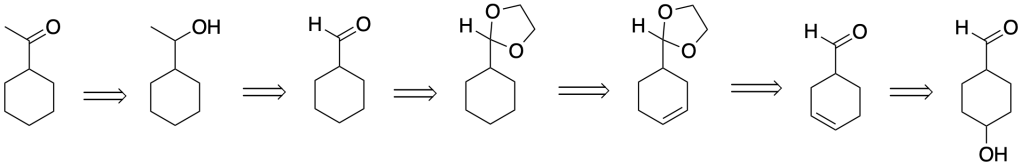
Sciema di sintesi

PER IMPEGNI ISTITUZIONALI DEI DOCENTI, LE LEZIONI DELLA SETTIMANA 18-21 MARZO 2024 SUBIRANNO LE SEGUENTI MODIFICHE:
| LUNEDI’ | MARTEDI’ | MERCOLEDI’ | GIOVEDI’ | |
| 9-10 | Chim. anal Anal 1 | Patologia | Patologia | |
| 10-11 | Chim. anal Anal 1 | Patologia | Patologia | |
| 11-12 | Biochimica | Chim organica | Patologia | Biochimica |
| 12-13 | Biochimica | Chim organica | Biochimica | Biochimica |
| 13-14 | Biochimica | Chim organica | Biochimica | |
| 14-15 | Chim. anal Anal 1 | |||
| 15-16 | Lab chim. org | Chim organica | Chim. anal Anal 1 | |
| 16-17 | Lab chim. org | Chim organica | ||
| 17-18 | Lab chim. org |
si prega Annarita Coronella di inserire l’avviso nella Chat degli studenti di Farmacia

Causa impegni istituzionali del docente presso l’Ateneo Federico II, gli appuntamenti fissati tramite DOODLE per il 12 gennaio sono SPOSTATI a LUNEDI’ 15 gennaio negli stessi orari
You must be logged in to post a comment.