Enoli ed enolati 3. Sintesi

Esercizio n. 1
Mostrare come convertire l’acido benzoico in 3-metil-1-fenil-1-butanone usando una condensazione di Claisen in qualche stadio della sintesi:
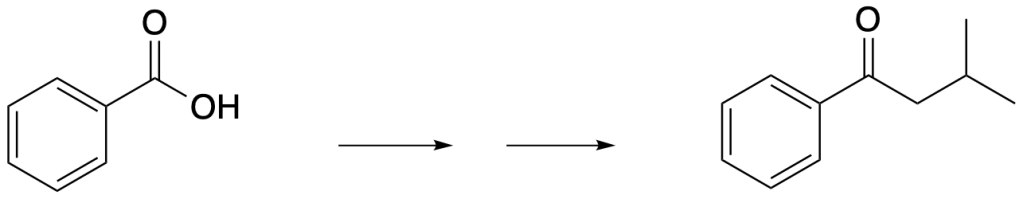
Esercizio n. 2
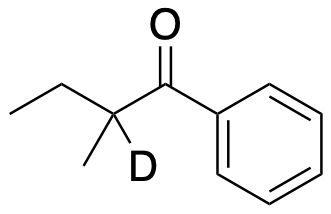
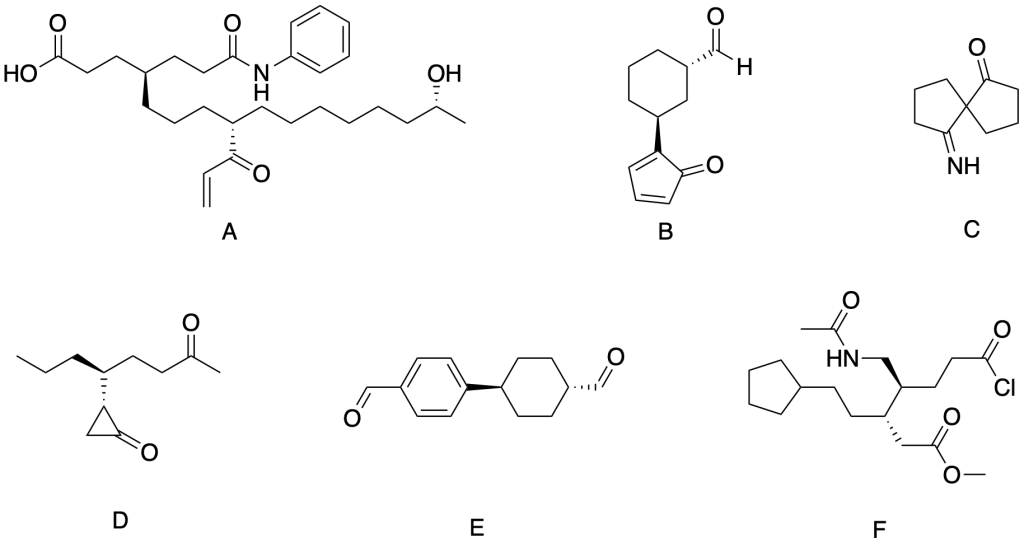
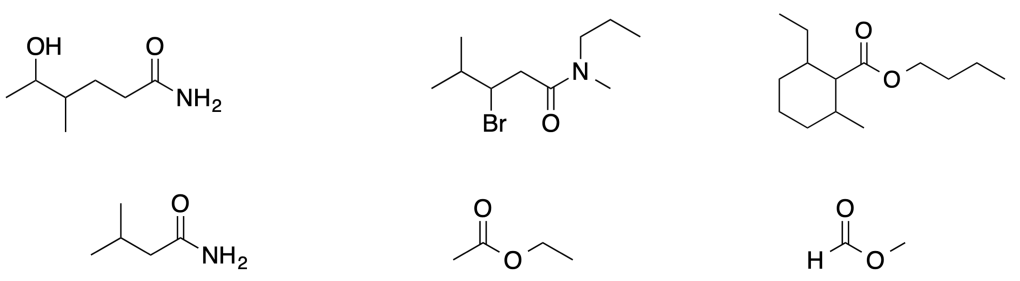
I seguenti composti sono prodotti di condensazione. Individuare i reagenti che hanno portato alla loro sintesi:
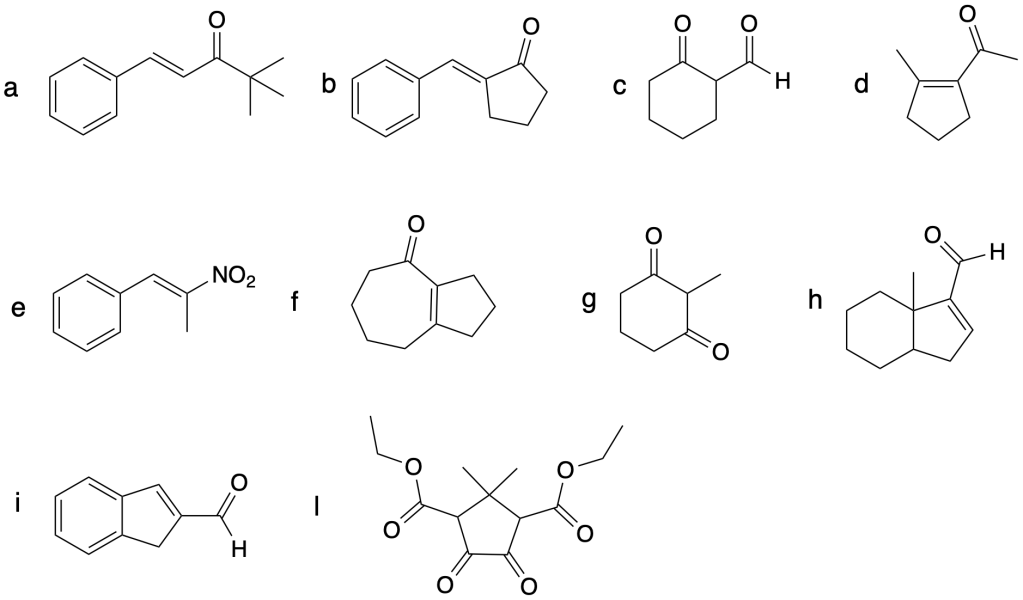
Esercizio n. 3
Proporre la sintesi dei seguenti composti utilizzando la reazione di anellazione di Robinson:
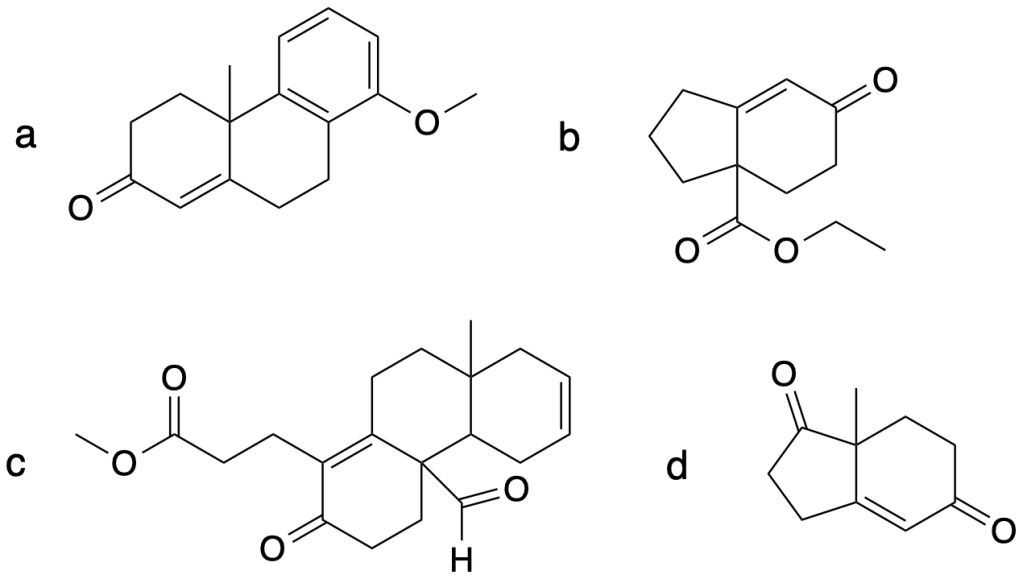
Esercizio n. 4
Descrivere in che modo possa essere sfruttata la sintesi acetoacetica per la preparazione dei seguenti composti:
a. 2-pentanone
b. 3-propil-2-esanone
c.4-fenil-2-butanone
Esercizio n. 5
Ipotizzare un meccanismo che spieghi la sintesi del 4-eptanone a partire dal butanoato di etile.
Esercizio n. 6
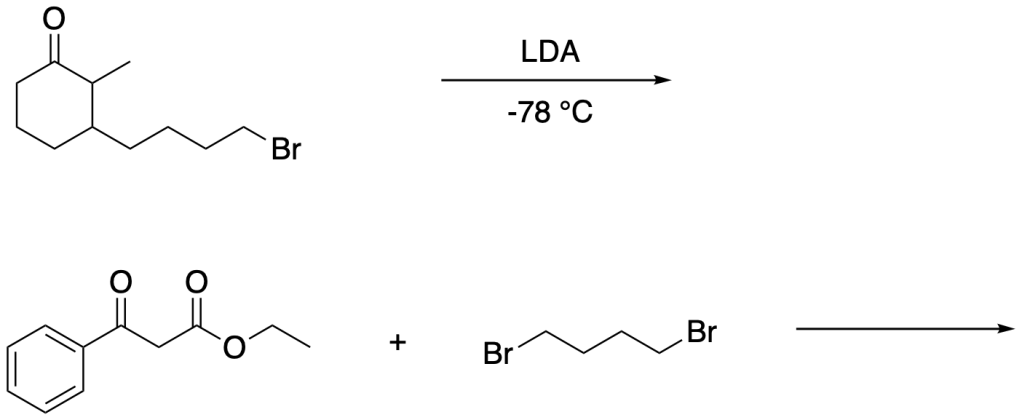
Come potrebbe essere sfruttata la sintesi acetoacetica per la preparazione del seguente composto?
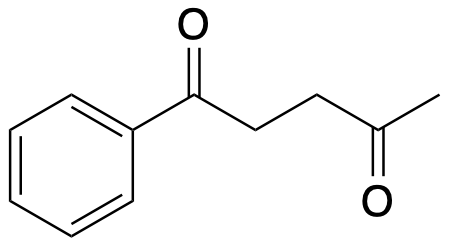
Esercizio n. 7
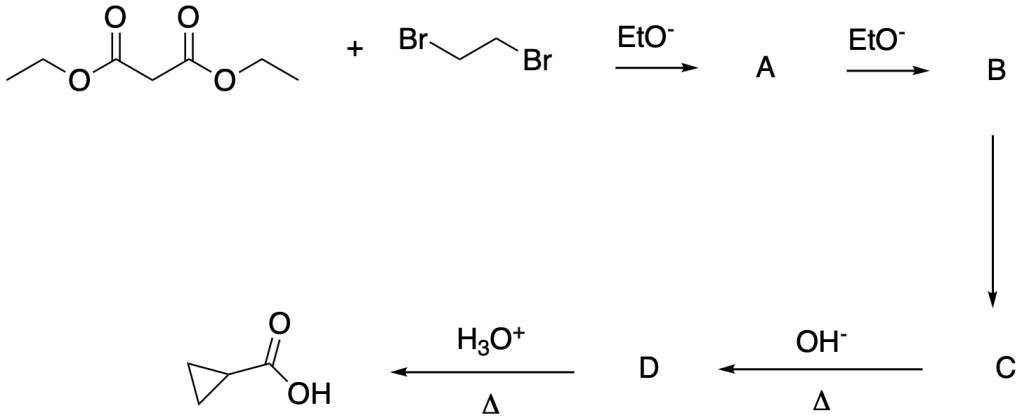
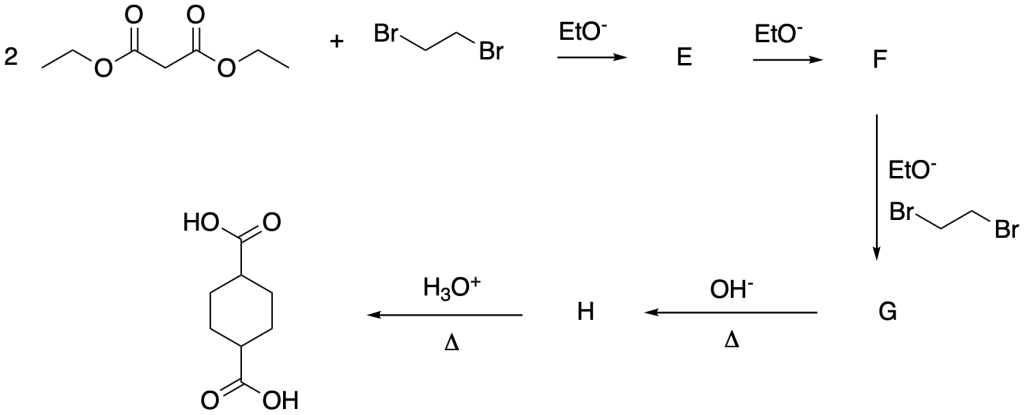
Descrivere in che modo possa essere sfruttata la sintesi malonica per la preparazione dei seguenti composti:
a. acido pentanoico
b. acido 2-metilpentanoico
c. acido 4-metilpentanoico
Esercizio n. 8
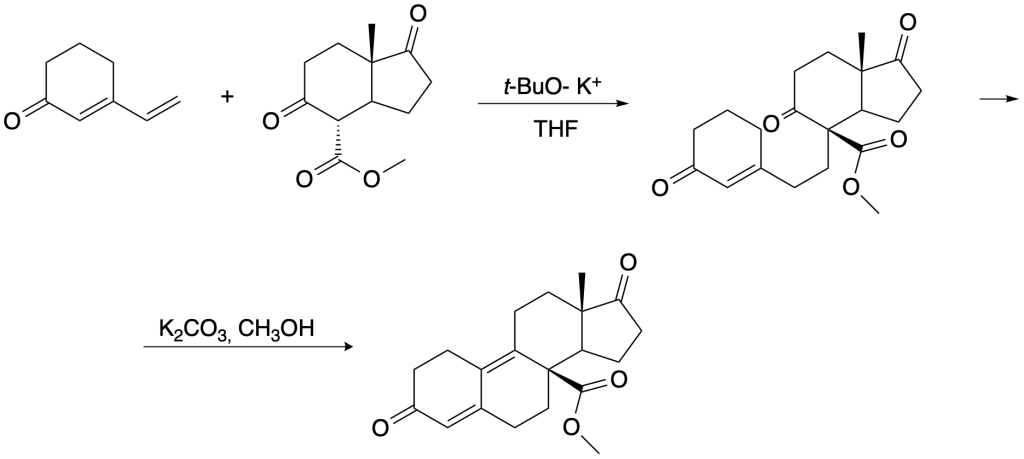
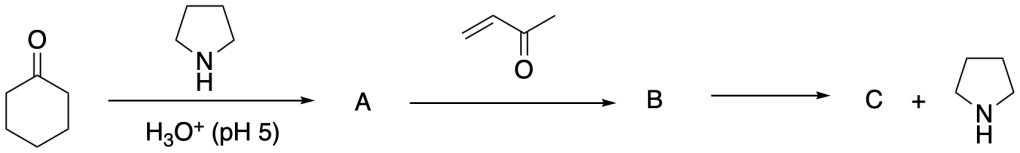
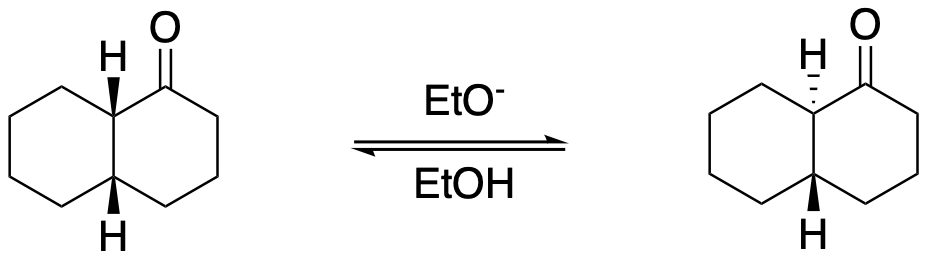
Una sintesi piuttosto insolita degli steroidi correlati al cortisone include le due reazioni riportate di seguito

a. proporre dei meccanismi per queste due trasformazioni. Attenzione nell’individuazione del sito iniziale di deprotonazione dell’enone di partenza.
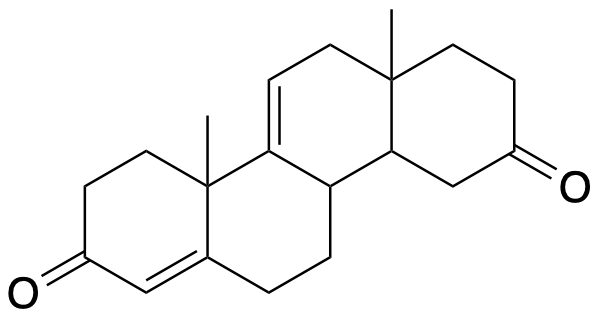
b. Proporre una sequenza di reazioni che a partire dall’ultima struttura precedentemente mostrata permetta di ottenere il seguente prodotto:


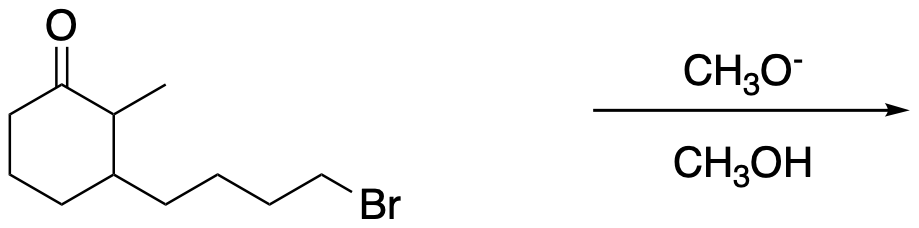

















You must be logged in to post a comment.