CdL Scienze Biologiche-Quarta prova intercorso

Si comunica che la quarta e ultima prova intercorso è posticipata a lunedì 22/12 alle 9:30
Università degli Studi della Campania "Luigi Vanvitelli"

Si comunica che la quarta e ultima prova intercorso è posticipata a lunedì 22/12 alle 9:30

Raccomandazioni prima di affrontare questi esercizi:
1) studiare le reazioni in oggetto. Prendere, inoltre, visione del materiale didattico pubblicato.
2) Alla fine del post troverete un link in cui sono riportati alcuni degli esercizi svolti/guidati che possono essere una guida per affrontare anche gli altri esercizi
1) Come è possibile sintetizzare i seguenti alogenuri alchilici a partre da un alcol
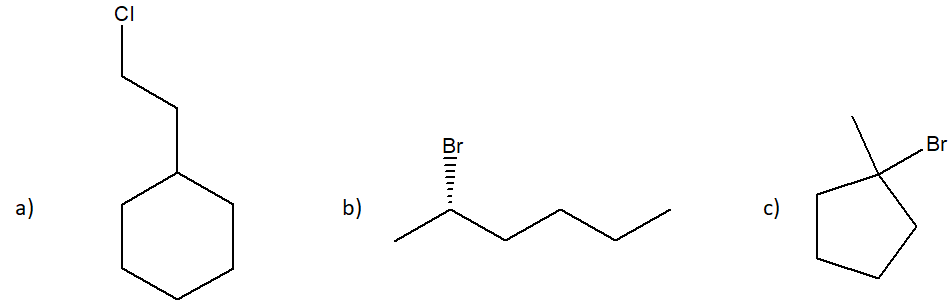
2) Scrivere il prodotto o i prodotti principale della disidratazione con acido solforico ad alta temperatura per ciascuno dei seguenti alcoli
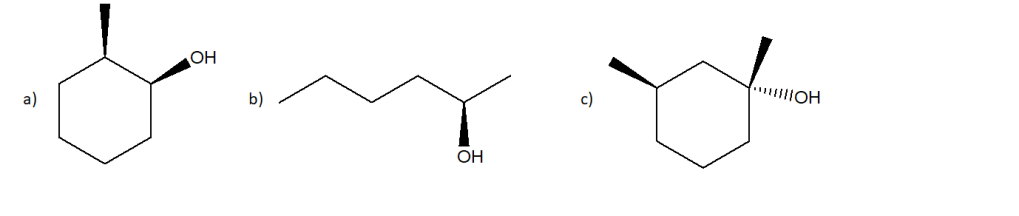
3) Scrivere il prodotto o i prodotti delle seguenti reazioni :

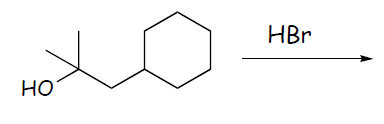
4) Completare le seguenti reazioni

5) Proporre un meccanismo per le seguenti trasformazioni:

6) Proporre una strategia di sintesi dei seguenti eteri mediante sintesi di Williamson. Per ciascun etere, dire se sono possibili metodi di sintesi alternativi.
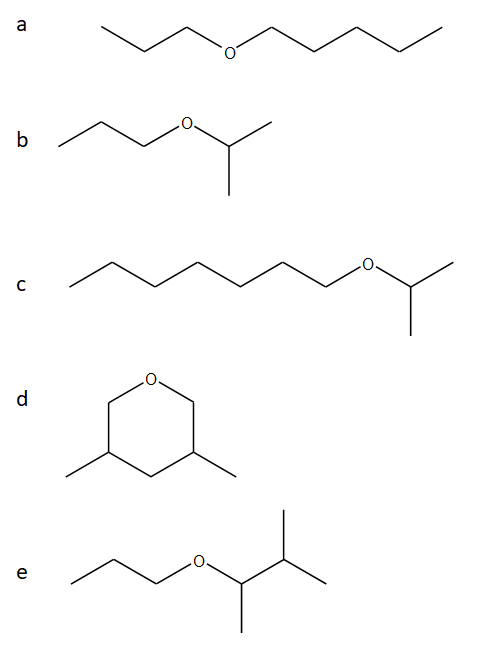
7) Per ciascuno dei seguenti alogenuri alchilici scrivere il principale prodotto di eliminazione specificandone la stereochimica.
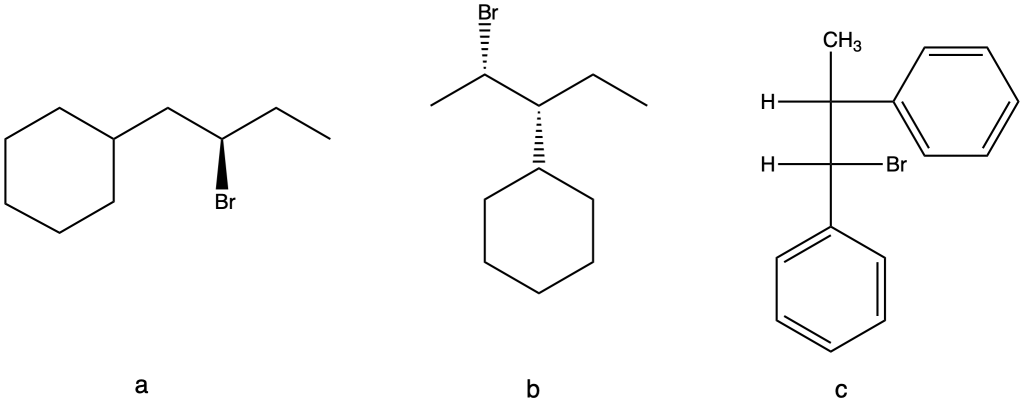
8) Per ciascuno dei seguenti alogenuri alchilici terziari, scrivere il prodotto della reazione di solvolisi con metanolo.
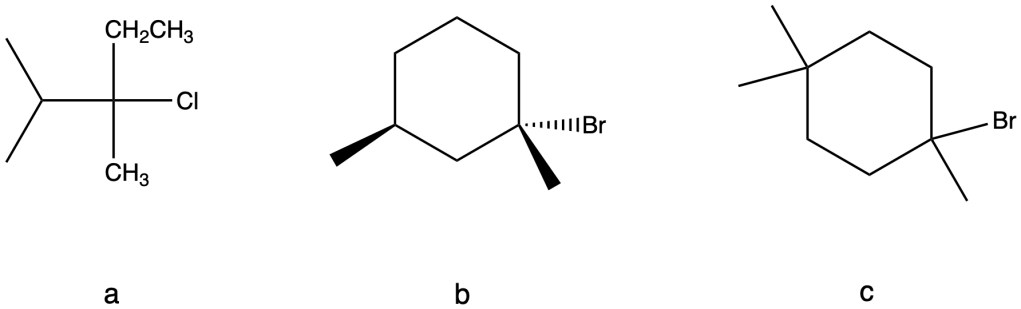
9) Quale sarà il prodotto principale di eliminazione che si otterrà a partire da ciascuno dei seguenti reagenti per trattamento con una base forte e con una base debole?

10) Scrivi la formula di struttura del prodotto organico principale per ognuna delle reazioni e specifica il meccanismo più probabile per la sua formazione

–> ESERCIZI GUIDATI (segui il link)

Esercizio n. 1
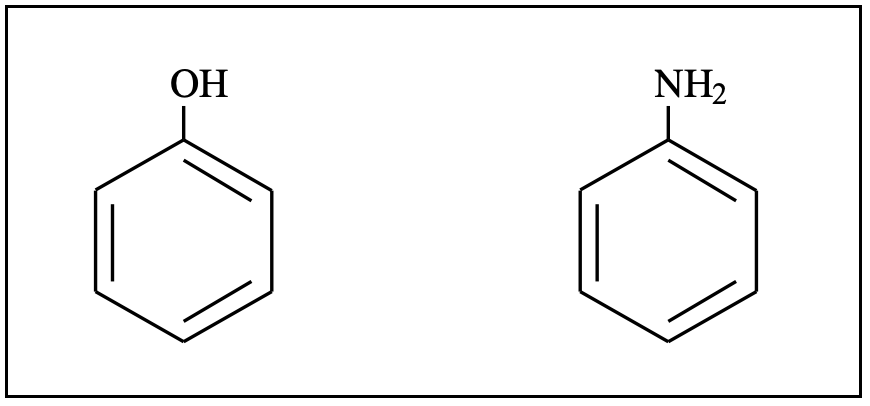
Il fenolo è più acido del cicloesanolo di 6 unità di pK (circa un milione di volte più acido). Così mentre gli alcoli sono neutri, i fenoli sono in realtà degli acidi, con una acidità paragonabile a quella dell’ HCN e reagiscono con NaOH in modo pressoché completo, portando allo ione fenato corrispondente.
L’anilina, invece, è una base più debole della cicloesilammina (per cinque unità di pK). Come si spiegano queste osservazioni?
Esercizio n. 2
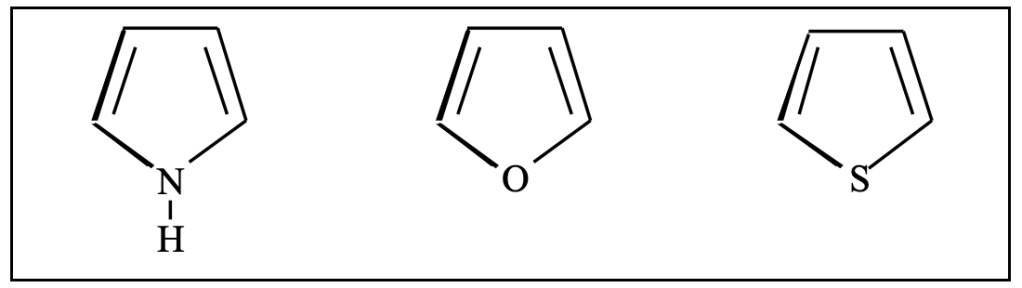
Il pirrolo, il furano e il tiofene sono tre eterociclici aromatici contenenti rispettivamente un atomo di azoto, ossigeno e zolfo. Dire quale di essi è più aromatico e quale meno, motivando la risposta.
Esercizio n. 3
La piridina e il pirrolo sono due composti eterocilici aromatici contenenti un atomo di azoto: mentre però la prima è basica, il secondo non lo è affatto. Come si spiega questa affermazione?

Esercizio n. 4
Disporre le seguenti molecole in ordine crescente di acidità. Spiegare la sequenza usando se necessario le appropriate forme di risonanza.

Esercizio n. 5
Disporre i seguenti fenoli in ordine crescente di acidità.

Esercizio n. 6
Classificare ciascuno dei seguenti composti come aromatico, antiaromatico o non aromatico:

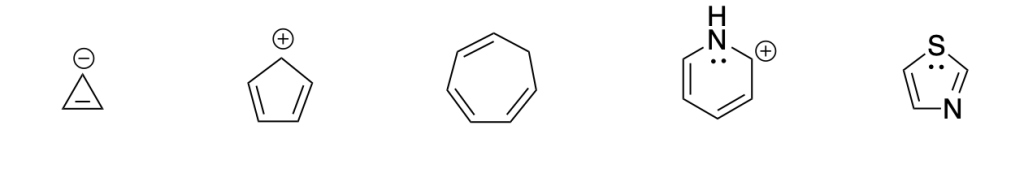




Esercizio n. 1
Disporre i seguenti composti in ordine di acidità crescente e spiegare sinteticamente il perché
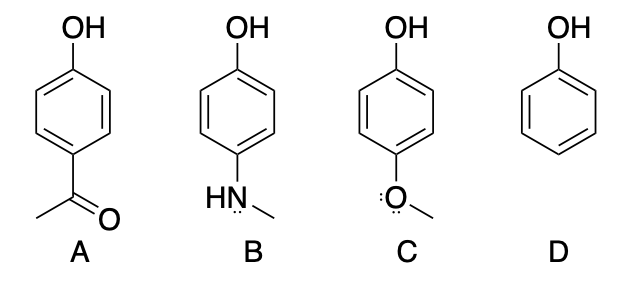
Esercizio n. 2
Disporre i seguenti composti in ordine di basicità decrescente e spiegare sinteticamente il perché

Esercizio n. 3
Classificare ciascuno dei seguenti composti come aromatico (A), antiaromatico (AntiA) o non aromatico (noA).
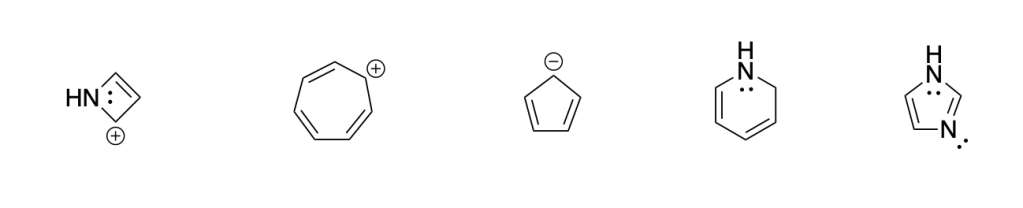
Esercizio n. 4
Scrivere i prodotti principali delle seguenti reazioni illustrando i meccanismi di azione.

Esercizio n. 4
Utilizzando il diagramma degli orbitali molecolari per l’1,3,5-esatriene determinare l’HOMO e il LUMO per la molecola nello stato fondamentale e nello stato eccitato.
Esercizio n. 5
Scrivere il meccanismo della seguente reazione, specificando le strutture di risonanza degli intermedi. Disegnare un diagramma di energia libera/coordinata di reazione e individuare lo stadio cinetico

Esercizio n. 6
Scrivere il/i prodotto/i della seguente reazione di Diels-Alder. Specificare la regiochimica e la stereochimica, se necessario.

Esercizio n. 7
Rappresentare le strutture di risonanza dei seguenti composti:
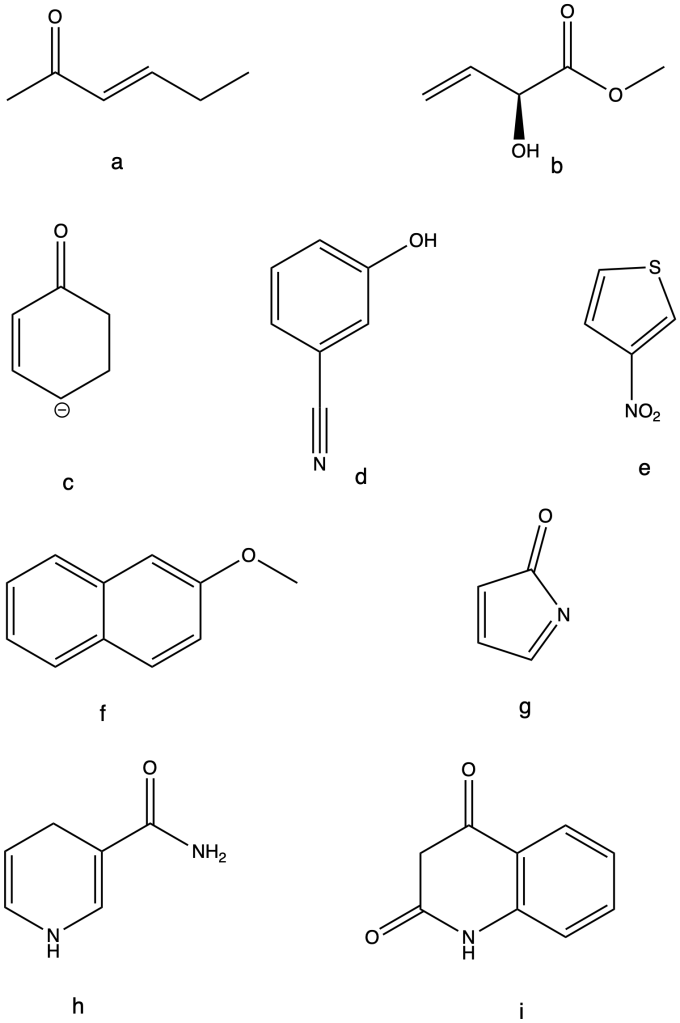

Esercizio n. 1
Prevedete la struttura del prodotto principale che si ottiene dall’addizione 1,2 di una mole di Br2 all’isoprene (2-metil-1,3-butadiene). Prevedete, inoltre, la struttura del principale prodotto di addizione 1,4 nelle medesime condizioni.
Esercizio n. 2
Scrivete le formule di struttura dei due isomeri strutturali a formula molecolare C5H6Br2 che si ottengono dall’addizione di 1 mole di D-Br al ciclopentadiene.
Esercizio n. 3
Quali sono i prodotti principali che si ottengono dall’addizione di una mole di Br2 ai seguenti dieni in condizioni di controllo cinetico o termodinamico?

Esercizio n. 4
Dite quale dei seguenti composti reagisce con anidride maleica (=cis-butendioica) e quale no, spiegando e scrivendo l’equazione chimica delle reazioni che avvengono: a) 1,4-pentadiene; b) butadiene; c) ciclopentadiene; d) 1,4-cicloesadiene; e) 1,3-cicloesadiene; f) 1,3-esadiene; g) 1,4- esadiene; h) 1,5-esadiene.
Esercizio n. 5
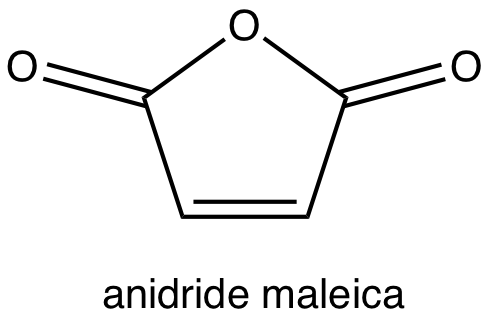
Anche gli alchini possono essere usati come dienofili nelle reazioni di Diels-Alder. Scrivere le strutture dei prodotti che si ottengono dalla reazione del 1-metossi-1,3-butadiene con: a) esafluoro-2-butino; b) propinoato di metile; c) butindioato dimetilico.

Esercizio n. 6
Prevedete i prodotti delle seguenti reazioni di Diels-Alder

Esercizio n. 7
A partire da quali dieni e dienofili si ottengono i seguenti addotti di Diels-Alder ?


Esercizio n. 1
Scrivere i prodotti principali delle seguenti reazioni e il loro meccanismo di formazione

Esercizio n. 2
La reazione riportata in basso forma un solo prodotto: A. Disegnare gli intermedi che conducono a ciascun prodotto e spiegare perché non si osserva la formazione di B.

Esercizio n. 3
Scrivere i prodotti principali delle seguenti reazioni:

Esercizio n. 4
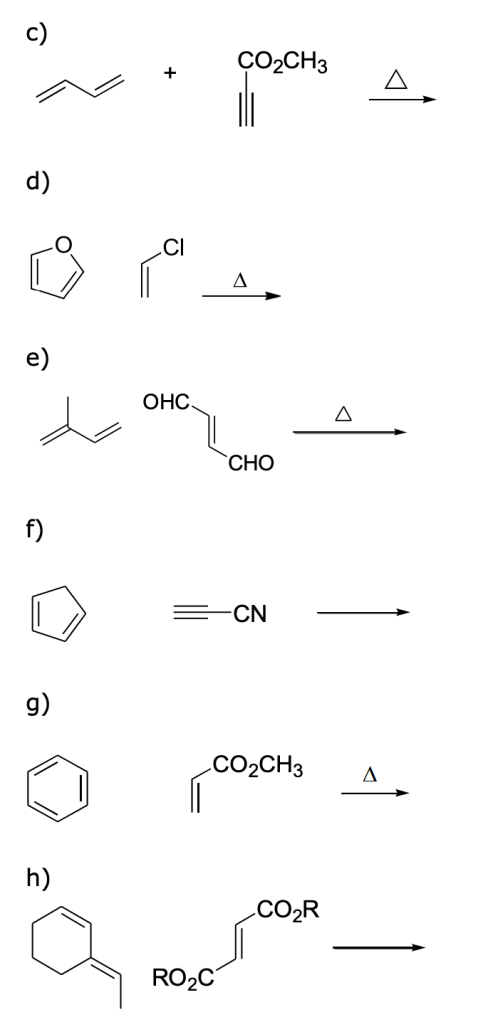
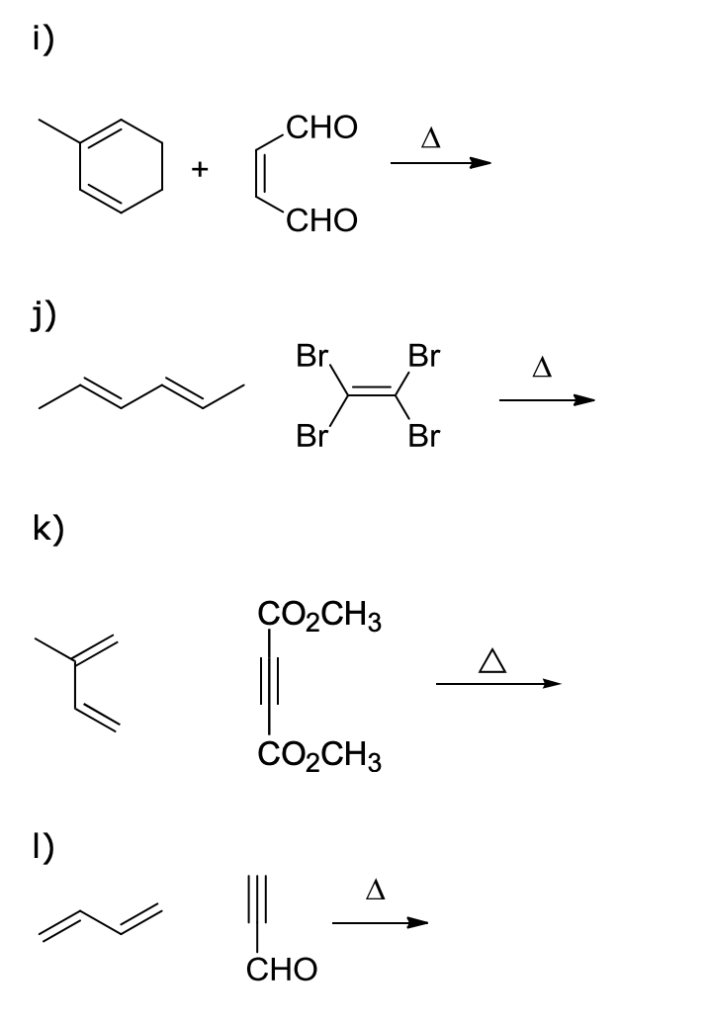
Predire il prodotto principale delle seguenti reazioni. specificare la stereochimica dei prodotti, se necessario.


Esercizio n. 4
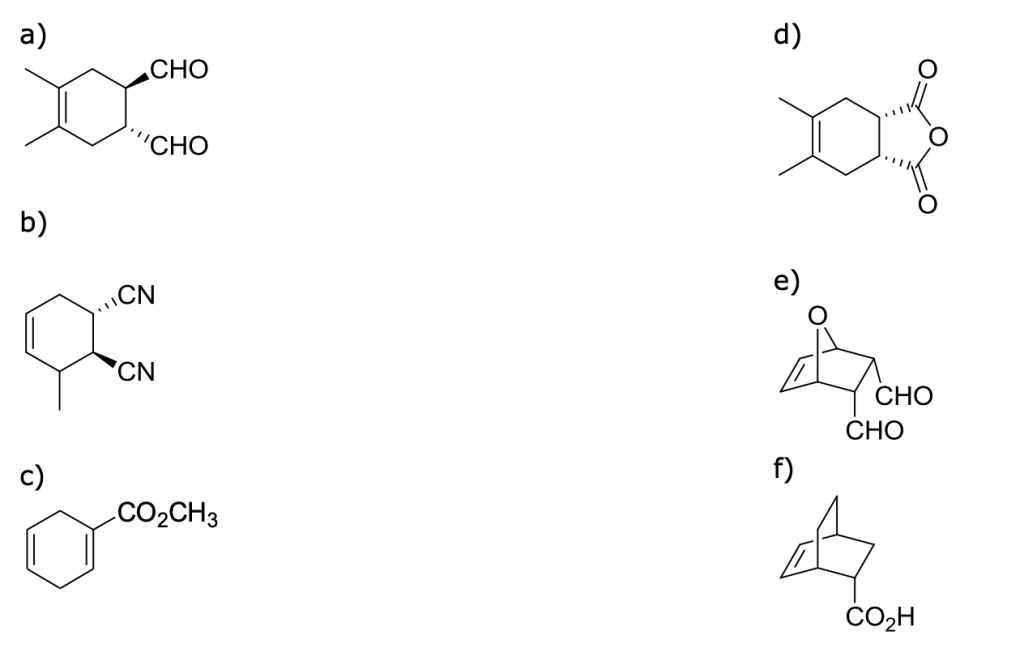
Scrivere i composti di partenza che sono stati utilizzati per formare i seguenti prodotti di Diels-Alder:
Esercizio n. 5
I seguenti composti vanno incontro a due reazioni di Diels-Alder consecutive. Scrivere il prodotto di ciascuna addizione.


Esercizio n. 1
Quali composti si ottengono per reazione di ognuno dei seguenti reagenti con il 2,4-esadiene?
(a) HCl;
(b) Br2 in H2O;
(c) H2SO4 in CH3CH2OH.
Esercizio n. 2
Scrivere i prodotti delle reazioni del trans-1,3-pentadiene con ciascuno dei reagenti elencati nell’esercizio n°1.
Esercizio n. 3
Scrivere i prodotti delle reazioni del 1,3-cicloeptadiene con ciascuno dei reagenti elencati nell’esercizio n°1.
Esercizio n. 4
Scrivere i prodotti delle reazioni del 2-metil-1,3-pentadiene con ciascuno dei reagenti elencati nell’esercizio n°1.
Esercizio n. 5
Predici il prodotto maggioritario formato dall’addizione 1,2 dell’HCl al 2-metil-1,3-butadiene (isoprene).
Esercizio n. 6
Predici il prodotto maggioritario formato dall’addizione 1,4 di HCl all’isoprene.
Esercizio n. 7
Predici la struttura del prodotto maggioritario dell’addizione 1,2 di una mole di Br2 all’isoprene. Predici anche la struttura del prodotto di addizione 1,4 che si forma in queste condizioni nella stessa reazione.
Esercizio n. 8
Quale delle seguenti due molecole ti aspetti sia il prodotto maggioritario nell’addizione 1,2 di HCl al ciclopentadiene? Spiega.

(b) Predici il prodotto maggioritario che si forma dall’addizione 1,4 di HCl al ciclopentadiene.
Esercizio n. 9
Quali sono i prodotti cinetici e termodinamici che ti aspetti dall’addizione di una mole di Br2 ai seguenti dieni:
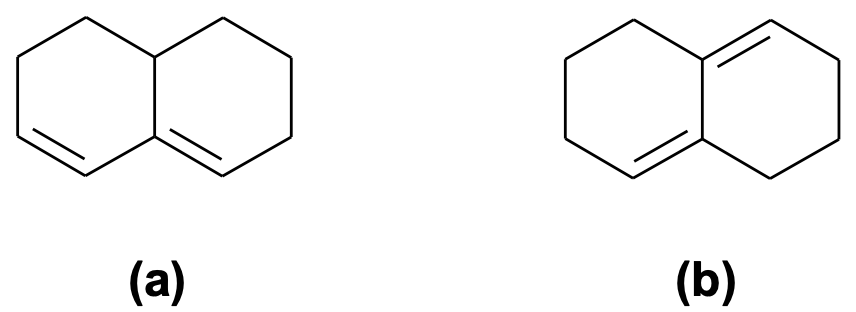
Esercizio n. 10
Scrivete il/i prodotto/i di reazione dei seguenti alcheni con un equivalente di HI. Illustrate il meccanismo di ciascuna reazione.


Esercizio n. 1
Quali delle seguenti specie hanno elettroni delocalizzati?
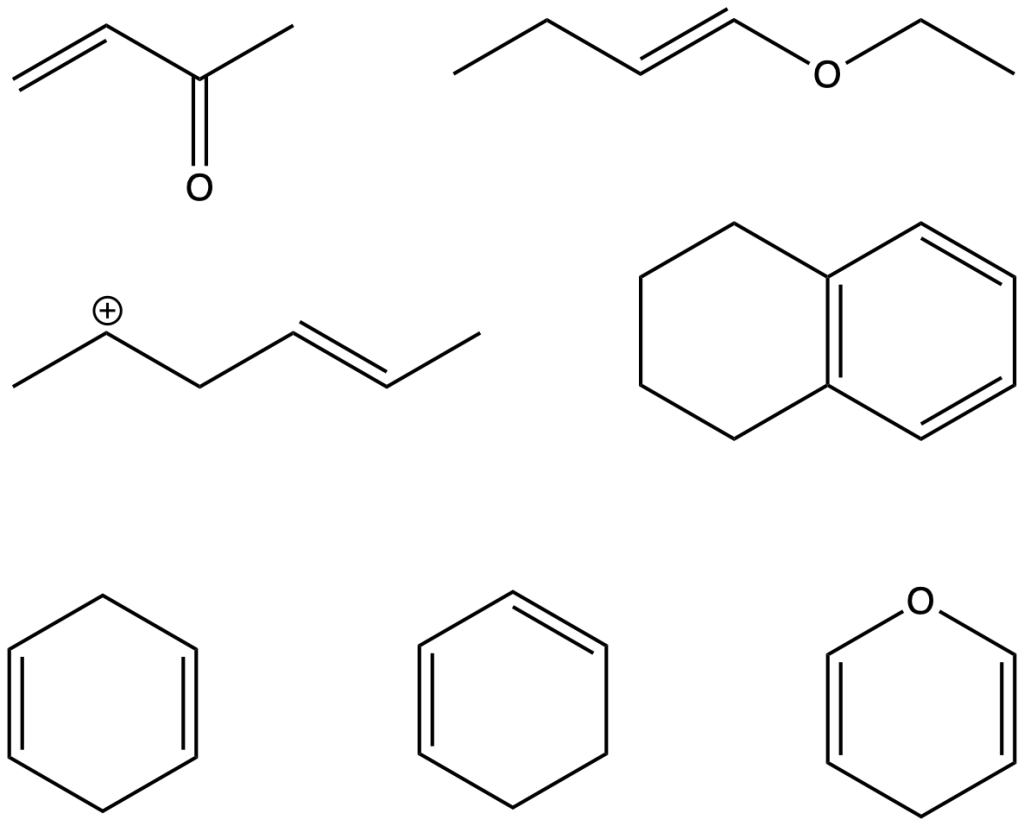
Esercizio n. 2
Disegnate le forme di risonanza, mostrando appropriatamente il movimento degli elettroni) e una rappresentazione dell’ibrido di risonanza più appropriato per ciascuna delle seguenti specie.
Per ciascuna specie, indicate la forma di risonanza che dà il contributo maggiore all’ibrido di risonanza. Spiegate le vostre scelte.

Esercizio n. 3
Quali tra i seguenti carbocationi possono andare incontro a trasposizione?

Esercizio n. 4
Disponete i seguenti composti in ordine di basicità crescente

Esercizio n. 5
Ordinate i seguenti fenoli dal più acido al meno acido
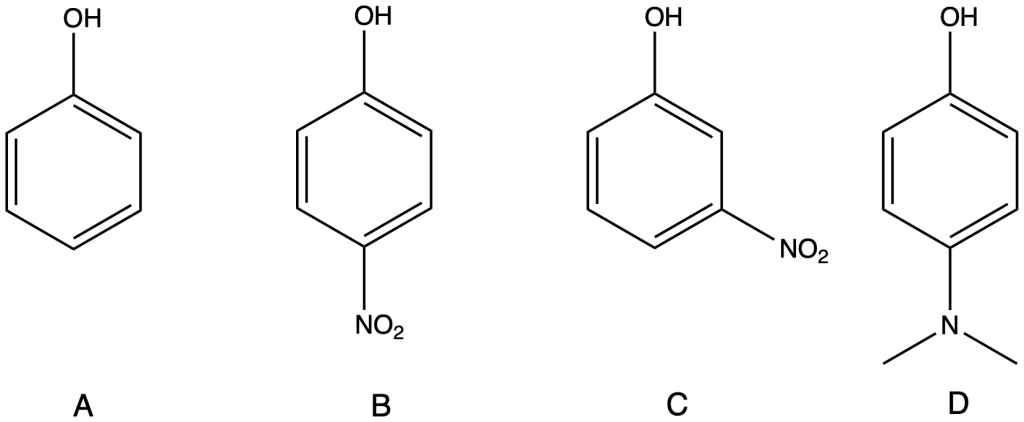
Esercizio n. 6
Quali tra i seguenti carbocationi possono andare incontro a trasposizione? (1 pt)


Le reazioni che avvengono a carico di questi composti, non sono altro che reazioni di sostituzione ed eliminazione, che qui andremo a schematizzare. Per ora abbiamo approfondito solo quelle che avvengono a carico degli alcoli. Gli altri meccanismi saranno approfonditi giovedì a lezione.
ALCOLI
Gli alcoli possono essere convertiti in alogenuri alchilici (i quali possono poi essere convertiti in una grande varietà di composti, in virtù della loro reattività) o alcheni.
La prima trasformazione avviene mediante reazioni di sostituzione, la seconda mediante una reazione di eliminazione (dato che viene eliminata una molecola di acqua, si parla di disidratazione).
Le reazioni da conoscere sono le seguenti:

In blu sono riportate le reazioni di sostituzione, in nero quelle di disidratazione.
HX= HBr, HI, o HCl/ZnCl2
Il meccanismo con cui le reazioni avvengono, dipende dalla natura dell’alcol (primario, secondario o terziario):

Per quanto riguarda gli aspetti stereochimici, valgono le stesse considerazioni fatte per le reazioni che avvengono a carico degli alogenuri alchilici.
ETERI
Gli eteri danno reazioni di sostituzione nucleofila con HBr e HI (la reazione è lenta, per cui la miscela di reazione deve essere riscaldata). Il meccanismo sarà SN1, se, dopo la protonazione del gruppo OR, allontanandosi questo dà luogo ad un carbocatione stabile. Se questo non accade, il meccanismo sarà di tipo SN2.
EPOSSIDI
Gli epossidi possono reagire con un gran numero di nucleofili e il meccanismo di apertura dell’epossido dipende dalle condizioni in cui avviene la reazione:

La reazione di apertura dell’epossido avviene con attacco da retro, determinando la stereochimica del prodotto: l’ossidrile (che deriverà dall’ossigeno dell’epossido) e il nucleofilo (che ha dato l’attacco) si troveranno in anti tra loro.
Tantissimi nucleofili possono reagire con gli epossidi, tra questi, ad esempio, gli ioni acetiluro (portando ad un allungamento della catena carboniosa), ione idrossido (che porta alla sintesi di dioli trans), idruri (sintesi di alcoli senza trasposizione).
Per i dettagli teorico-pratici dei singoli meccanismi, si rimanda al testo

Concetti importanti su questi meccanismi, con approfondimenti sugli orbitali coinvolti:
You must be logged in to post a comment.