CdL Scienze Biologiche- IV prova intercorso-aule

Università degli Studi della Campania "Luigi Vanvitelli"



Con le ultime esercitazioni abbiamo provato a risolvere alcuni dei dubbi relativi agli argomenti e alle tipologie di esercizi che potrebbero essere presenti nella prova.
Qui invece troverete risposta a quei pochi dubbi che non è stato possibile affrontare nel corso dell’esercitazione, del ricevimento o nel file precedentemente condiviso. Come al solito, nel prenderne visione, vi invito a leggere con attenzione la domanda e la risposta (è fondamentale non decontestualizzare la risposta, per non rischiare di interpretare male o applicare-erroneamente-ad altro quanto scritto).
Non è stato possibile rivedere tutti i meccanismi di reazione richiesti nei form, ma in presenza di forti dubbi sarà possibile contattare la docente per chiarimenti. Attenzione, perchè alcuni dei dubbi espressi riguardano esercizi per cui erano state anche pubblicate le soluzioni, quindi vi invito a prenderne visione (se ancora non lo avete fatto). Chi pensa che dubbi che riguardano gli argomenti (e il livello di difficoltà degli esercizi) della prova non siano stati affrontati, pur essendo stati evidenziati nei form, potrà contattare la docente per chiarimenti.
Tutti i dubbi relativi a tipologie di esercizi e argomenti che sicuramente non saranno oggetto della prova, sono ora solo in stand-by…ma faremo in modo di chiarirli a breve.



Regolamento:

Suggerimenti:
1. Mostrare i primi passaggi della reazione utilizzando una rappresentazione a sedia della porzione della molecola costituita dal cicloesanone. Potete anche “sottintendere” la presenza dell’altro anello in questa fase, indicandolo nel modo seguente:

2. Ragionare sempre in riferimento alla reazione tra un nucleofilo ed un elettrofilo piuttosto che per schemi predefiniti. Analogamente, considerare eventuali reazioni acido-base che possono avvenire.
3) Considerare anche i vari fattori che possono stabilizzare o, al contrario, rendere meno stabili gli intermedi eventualmente formati nel corso della reazione!

1) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione
a) del propanone con dimetilammina
b) del butanoato di metile con acqua
c) del cicloesanone con etanolo
d) del cloruro di propanoile con metanolo
2) Illustrare una strategia e il meccanimo per sintetizzare ciascuno dei seguenti composti, a partire dall’opportuno composto carbonilico:

3) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti. Evidenziare la stereochimica quando opportuno.
a)
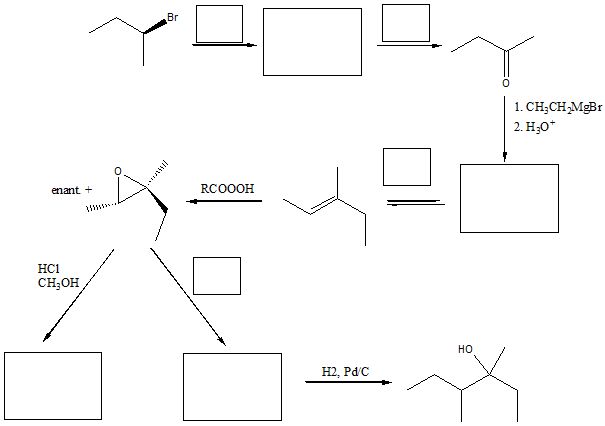
b)
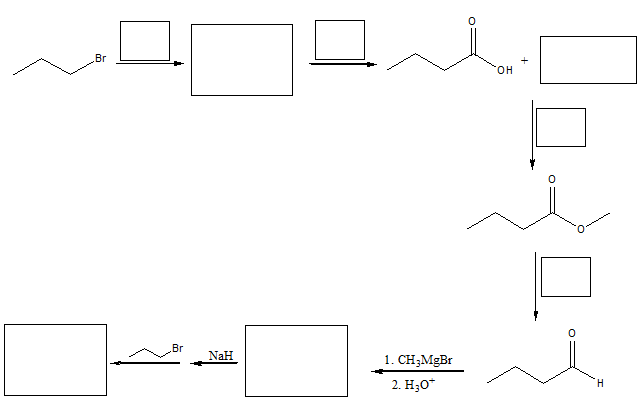
4) Scrivere i prodotti delle seguenti reazioni:
a)

b)

5) Indicare le condizioni di reazione ottimali per ottenere le seguenti trasformazioni:
a)

b)

6a) Quale alogenuro alchilico utilizzeresti per ottenere, mediante una eliminazione E2:
a) (Z)-3-etil-4-metil-2-pentene
b) (E)-3-etil-4-metil-2-pentene
c) (R)-1,3-dimetilcicloesene
d) (S)-1,3-dimetilcicloesene
6b) Chi reagirà più velocemente in una reazione E2 tra (1R,3S)-1-bromo-3-isopropilcicloesano e (1S,3S)-1-bromo-3-isopropilcicloesano? Spiegare sinteticamente perché
7) Assegnare il nome IUPAC ai seguenti composti

8a) Ordina i seguenti composti per reattività crescente in una reazione E2
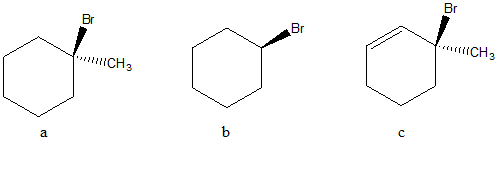
8b) Ordina i seguenti composti per reattività crescente in una reazione SN2

8c) Quale dei seguenti alcoli disidraterà più facilmente? Perchè?






Gli studenti prenotati per il ricevimento di oggi, dovranno raggiungermi nel mio studio (Corpo A, primo piano)



You must be logged in to post a comment.