REAZIONI DEGLI ALCHENI

- La reazione del 2-metil-2-pentene con ognuno dei seguenti reagenti mostra un’alta regioselettività. Disegna la formula di struttura del prodotto maggioritario di ogni reazione e spiega la regioselettività osservata.
- H2O (in presenza di H2SO4)
- HBr
- Br2 in H2O
- Cl2
- Hg(OAc)2, H2O
2. Scrivere i prodotti di ossidazione dei seguenti alcheni. Ove necessario, indicare la stereochimica della reazione.
-
- trans-2-Butene + KMnO4 diluito/a freddo
- (2Z)-3-Metil-2-pentene + OsO4
- Ciclopentene + KMnO4 diluito/a freddo
- 1-Etilciclopentene + KMnO4 a caldo
- 1-Metilciclopentene + O3
- Ciclopentene + CH3COOOH
- cis-2-Pentene + OsO4
3. Disegnare le formule dei prodotti delle seguenti reazioni. Specificare la stereochimica.
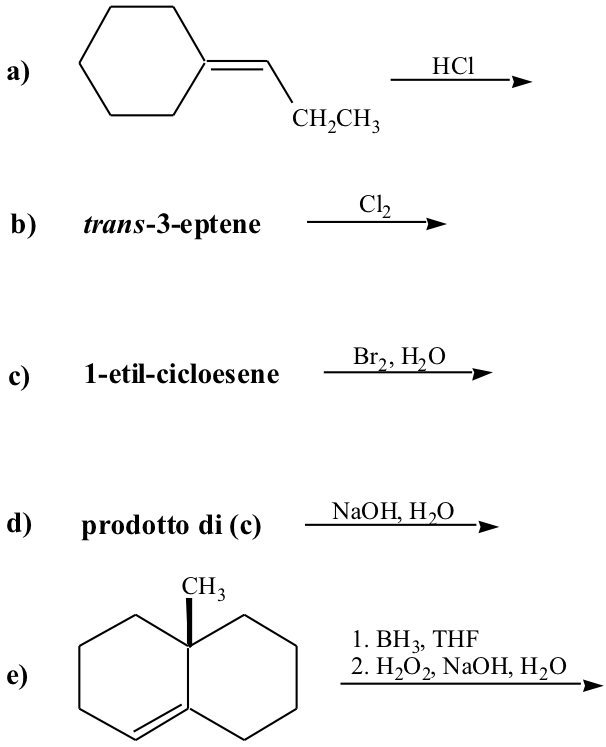
4. Disegnare le formule dei prodotti delle seguenti reazioni. Specificare la stereochimica
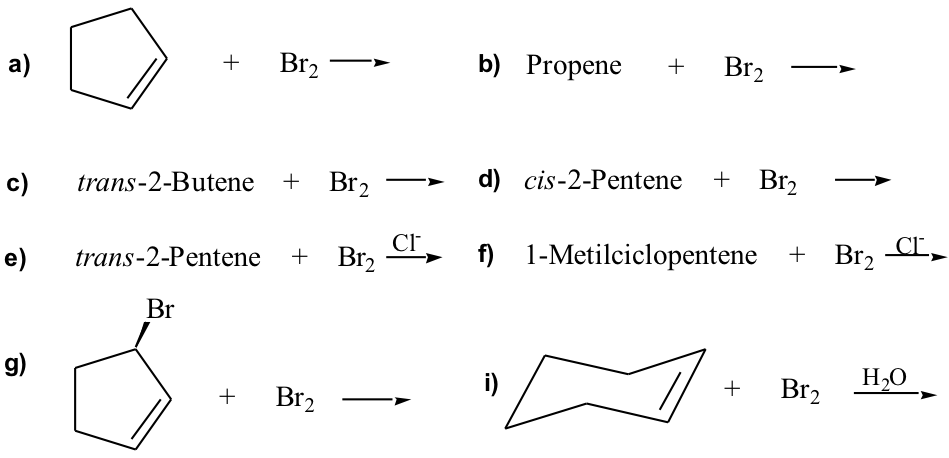
5. Indicare un metodo, a partire da alcheni, per la preparazione dei seguenti alcoli:
a) 1-butanolo
b) 3,4-esandiolo
c) 3-metil-2-pentanolo
d) 2-metil-1-cicloesanolo
6. Il trattamento del cicloesene con HBr in presenza di acido acetico dà il bromocicloesano (85%) e l’acetato di cicloesile (15%). Proponi un meccanismo per la formazione di quest’ultimo prodotto
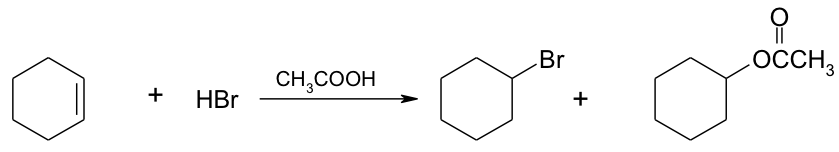
7. Il trattamento del 4-penten-1-olo con bromo in acqua porta ad un bromoestere ciclico. Spiega la formazione di questo prodotto al posto della semplice bromoidrina.
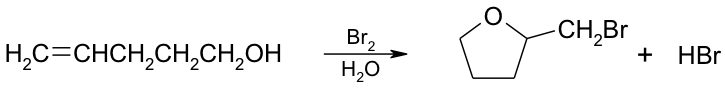
Es. 1
a)2-metilpentene -> 2-metil-2-pentanolo, idratazione acido catalizzata secondo Markovnikov
b)2-metilpentene-> 2-bromo-2-metilpentano, addizione di H-Br secondo Markovnikov
c)2-metilpentene -> 1-bromo-2-metil-2-pentanolo, formazione di aloidrina secondo Markovnikov, stereochimica anti
d)2-metilpentene-> 1,2-dicloro-2-metilpentano,addizione di Cl2, stereochimica anti.
e)2-metilpentene -> 2-metil-2-pentanolo, ossimercuriazione/demercuriazione, secondo Markovnicov (l’-OH si lega al carbonio più sostituito)
LikeLike
Es. n2
1) trans-2-butene+ KMnO4 -> (2R,3S)-2,3-butandiolo + (2S,3R)-2,3-butandiolo, addizione sin
2) (2Z)-3-metil-2-pentene + OsO4 -> (2S,3R)-3-metil-2,3-pentandiolo + (2R,3S)-3-metil-2,3-pentandiolo, addizione sin.
3) ciclopentene + KMnO4 -> cis- 1,2-ciclopentandiolo
4) 1-etilciclopentene + KMnO4 -> cis-(1R,2S)-1-etil-1,2-ciclopentandiolo + cis- (1S,2R)- 1-etil-1,2-ciclopentandiolo.
5) 1-metilciclopentene + O3 -> si rompe il legame C-C il ciclo si apre, ad una estremità c’è il gruppo aldeidico e all’altra chetonico.
6) ciclopentene +CH3COOOH -> 1,2-epossiciclopentano
7) cis-2-pentene + OsO4 -> (2S,3R)-2,3-pentandiolo + (2R,3S)-2,3-pentandiolo, ossidrilazione con addizione sin.
LikeLike
esercizio 2
1. ossidrilazione– stereochimica: treo
2.ossidrilazione–stereochimica:eritro
6.reazione di un perossiacido con formazione dell’epossido : ciclocondensato + acido carbossilico ch3cooh
*Buongiorno professore, non le ho fatte tutte perchè non sono sicura di come stia svolgendo l’esercizio, sopratutto per quanto riguarda la stereochimica.
LikeLike
Attenzione alla terminologia: stereochimica treo/eritro? cosa intendi? che si formano gli enantiomeri treo o eritro? non puoi dire “stereochimica”. ciclocondensato???????
LikeLike
Esercizio 5
A) Si parte da 1-butene tramite reazione di idroborazione-ossidazione
B) Si parte da 3-esene tramite ossidrilazione
C) Si parte da 3-metil-2-pentene tramite idroborazione-ossidazione
D) Si parte da 1-metilcicloesene tramite idroborazione-ossidazione
LikeLike
Esercizio 3
a) 1-cloro-1-propilcicloesano
b) (3R,4S)-3,4-dicloroeptano e (3S,4R)-3,4-dicloroeptano
c) (1R,2R)-2-bromo-1-etil-cicloesanolo e (1S,2S)-2-bromo-1-etil-cicloesanolo
Esercizio 5
a) da 1-butene con reazione di idroborazione-ossidazione
b) da 3-esene con reazione di ossidrilazione
c) da 3-metil-1-pentene con reazione di idratazione
d) da 1-metilcicloesene con reazione di idroborazione-ossidazione
LikeLike
Esercizio 4
a) composto meso 1,2-dibromo-ciclopentano
b) (R)-1,2-dibromopropano e (S)-1,2-dibromopropano.
c) (2S,3R)-2,3-dibromobutano e (2R,3S)-2,3-dibromobutano
d) (2R,3R)-2,3-dibromopentano e (2S,3S)-2,3-dibromopentano
e) (2R,3S)-2-bromo-3-cloropentano e (2S,3R)-2-bromo-3-cloropentano
f) (1S,2S)-2-bromo-1-cloro-1-metilciclopentano e (1R,2R)-2-bromo-1-cloro-1-metilciclopentano
g) (1R,3R)-1,2,3-tribromociclopentano e (1R,3S)-1,2,3-tribromociclopentano
i) (1S,2R)-2-bromo-1-cicloesanolo e (1R,2S)-2-bromo-1-cicloesanolo
LikeLike
3.a) Meso??
3.c) questo è un composto Meso!
LikeLike
Esercizio n.2
1) trans-2-butene+ KMnO4 -> (2R,3S)-2,3-butandiolo + (2S,3R)-2,3-butandiolo, ADDIZIONE SIN.
2) (2Z)-3-metil-2-pentene + OsO4 -> (2S,3R)-3-metil-2,3-pentandiolo + (2R,3S)-3-metil-2,3-pentandiolo, ADDIZIONE SIN.
3) ciclopentene + KMnO4 -> cis- 1,2-ciclopentandiolo
4) 1-etilciclopentene + KMnO4 -> cis-(1R,2S)-1-etil-1,2-ciclopentandiolo + cis- (1S,2R)- 1-etil-1,2-ciclopentandiolo.
5) 1-metilciclopentene + O3 -> con l’ozonilisi si rompe il legame C-C ed il ciclo si apre, ad una estremità si trova il gruppo aldeidico e all’altra il gruppo chetonico.
6) ciclopentene +CH3COOOH -> 1,2-epossiciclopentano
7) cis-2-pentene + OsO4 -> (2S,3R)-2,3-pentandiolo + (2R,3S)-2,3-pentandiolo, OSSIDRILAZIONE con ADDIZIONE SIN.
LikeLike
2.1) Addizione SIN ok, quindi rivedi bene le configurazioni dei carboni chirali dei prodotti
2.4) cis rispetto a chi? è un errore usare cis/trans: bisogna indicare la stereochimica del composto utilizzando SOLO la notazione R/S
LikeLike
Esercizio n.5
A. Partiamo da 1-butene tramite reazione di idroborazione-ossidazione
B. Partiamo da 3-esene tramite ossidrilazione
C. Partiamo da 3-metil-2-pentene tramite idroborazione-ossidazione
D. Partiamo da 1-metilcicloesene tramite idroborazione-ossidazione
LikeLike
Es. n.2
a)2-metil-2-pentene -> 2-metil-2-pentanolo, idratazione, catalizzata secondo Markovnikov
b)2-metil-2-pentene-> 2-bromo-2-metilpentano, addizione di H-Br, secondo Markovnikov
c)2-metil-2-pentene -> 1-bromo-2-metil-2-pentanolo, con formazione di aloidrina secondo Markovnikov, stereochimica anti
d)2-metil-2-pentene->2,3-dicloro-2-metilpentano,addizione di Cl2, stereochimica anti.
e)2-metil-2-pentene -> 2-metil-2-pentanolo, ossimercuriazione/demercuriazione, secondo Markovnicov, l’-OH si lega al carbonio più sostituito.
LikeLike
esercizio n. 1
c) non si applica la regola di Markovnikov in questo caso; solo quando si addizione un H+ ad un doppio legame.
LikeLike
Esercizo 2
1) Otteniamo (2S,3R)-2,3-butandiolo + (2R,3S)-2,3-butandiolo
2) Otteniamo (2S,3R)-3-metil-2,3-pentandiolo + (2R,3S)-3-metil-2,3-pentandiolo
3) Otteniamo (1R,2S)-1,2-ciclopentandiolo
4) Abbiamo una scissione ossidativa con rottura del doppio legame e apertura del ciclo
5) Rottura del doppio legame C-C e apertura del ciclo a causa di ozonolisi
6) Ottenaimo 1,2-epossiciclopentano
7) Otteniamo (2S,3R)-2,3-pentandiolo + (2R,3S)-2,3-pentandiolo
LikeLike
2.1) NO
2.3) Ok, meso
2.4) quali gruppi funzionali si formano?
2.5) idem
LikeLike
esercizio 3
a.1(1-cloroetil)-cicloesano
b.(3s,4s)-3,4-dicloroeptano
c.(1s)-1-bromo-1-etilcicloeptano
d.(1s)-1-etilcicloeptan-1-olo
LikeLike
3.a) assolutamente NO
3.b) + enantiomero
3.c) ? cicloeptanoo da un cicloesene? stereochimica: ci sono due carboni chirali nei prodotti
3.d) ???
LikeLike
es. 1
a) 2-metil-2-pentanolo
b) 2-bromo-2-metilpentano
c) formazione di aloidrina 3-bromo-2-metil-2-pentanolo
d) formazione di un dicloruro vicinale 2,3-dicloro-2-metil-pentano
e) reazione di ossimercurazione 2-metil-2-pentanolo
LikeLike
es 5
a) si parte da 1-butene. La reazione è l’idroborazione-ossidazione
b) si parte da 3-esene. La reazione è l’ossidrilazione
c) si parte da 3-metil-2-pentene. La reazione è l’idroborazione-ossidazione
d) si parte da 1-metilcicloesano. La reazione è l’idroborazione-ossidazione
LikeLike
d) da 1-metilcicloesene*
LikeLike
1)
a. Si ottiene il 2-metil-2-pentanolo mediante addizione di acqua, catalizzata da un acido. La reazione segue la regola di Markovnikov.
b. Si ottiene il 2-bromo-2-metil-pentano mediante addizione di acido bromidrico. La reazione segue la regola di Markovnikov.
c. Si ottiegono il (3R)-3-bromo-2-metil-2-pentanolo e il (3S)-3-bromo-2-metil-2-pentanolo, in miscela racemica. La stereochimica è di tipo anti.
d. Si ottiene il (3S)-2,3-dicloro-2-metil-pentano e il (3R)-2,3-dicloro-2-metil-pentano. La stereochimica è di tipo anti.
e. Si ottiene, mediante ossimercuriazione-riduzione, il 2-metil-2-pentanolo. La stereochimica è di tipo anti.
2.
a. Si ottiene 2,3-butandiolo. La stereochimica è di tipo sin. È un composto meso.
b. Si ottiene (2Z)-3-metil-2-pentene. La stereochimica è di tipo sin.
c. Si ottiene 1,2-ciclopentandiolo. La stereochimica è di tipo sin. È un composto meso.
d. Si ottengono (1R,2S)-1-etil-1,2-ciclopentandiolo e (1S,2R)-1-etil-1,2-ciclopentandiolo in miscela racemica. La stereochimica è di tipo sin.
e.
f. Si ottengono (2R,3S)-1,2-pentandiolo e (2S,3R)-1,2-pentandiolo in miscela racemica. La stereochimica è di tipo sin.
3.
a. 1-cloro-1-propil-cicloesano
b. (3S,4R)-3,4-dicloro-eptano e (3R,4S)-3,4-dicloro-eptano
c. Poiché l’acqua lega il C maggiormente sostituito, il ciclo si rompe e si formano il (3R,4S)-4-bromo-3-ottanolo e il (3S,4R)-4-bromo-3-ottanolo. Questo è il prodotto maggioritario, perché l’acqua è il solvente e quindi si trova in concentrazioni maggiori rispetto allo ione bromuro. Tuttavia, in quantità minime, si formeranno anche il (3R,4S)-3,4-dibromo-ottano e il (3S,4R)-3,4-dibromo-ottano.
d.
e.
4.
a. 1,2-dibromo-ciclopentano. È un composto meso. La stereochimica è di tipo anti.
b. (2R)-1,2-dibromo-propano e (2S)-1,2-dibromo-propano.
c. (2S,3R)-2,3-dibromo-butano e (2R,3S)-2,3-dibromo-butano
d. (2R,3R)-2,3-dibromo-pentano e (2S,3S)-2,3-dibromo-pentano
e. (2R,3S)-2,3-dibromo-pentano e (2S,3R)-2,3-dibromo-pentano + (2R,3S)-2-bromo-3-cloro-pentano e (2S,3R)-2-bromo-3-cloro-pentano
f. (1S,2S)-1,2-dibromo-1-metilciclopentano e (1R,2R)-1,2-dibromo-1-metilciclopentano + (1R,2R)-2-bromo-1-cloro-1-metilciclopentano e (1S,2S)-2-bromo-1-cloro-1-metilciclopentano
g. trans-1,2,3-tribromo-ciclopentano (composto meso) + (1R,3R)-1,2,3-tribromo-ciclopentano e (1S,2S)-1,2,3-tribromo-ciclopentano
i. (1S,2R)-2-bromo-1-cicloesanolo e (1R,2S)-2-bromo-1-cicloesanolo (prodotti maggioritari) + trans-1,2-dibromo-cicloesano (prodotto minoritario, composto meso)
5.
a. Si parte da 1-butene mediante reazione di idroborazione-ossidazione
b. Si parte da 3-esene mediante reazione di ossidazione con OsO4
c. Si parte da 3-metil-2-pentene mediante reazione di idroborazione-ossidazione
d. Si parte da 1-metilcicloesene mediante reazione di idroborazione-ossidazione.
LikeLike
2.b) si ottiene? un alchene?
2.f) ciclopentandiolo. Meso.
3.c) si rompe il doppio legame???? NO!
4.g) trans non indica nulla. non sono assolutamente d’accordo con gli altri due prodotti
4.f) ???
LikeLike
Rettifica: mi sono accorta di aver sbagliato la lettera c dell’esercizio 3. Il risultato è (1S,2S)-2-bromo-1-etil-cicloesanolo e (1R,2R)-2-bromo-1-etil-cicloesanolo
LikeLike
ok
LikeLike