Esercitiamoci per la prova scritta (VIII)

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
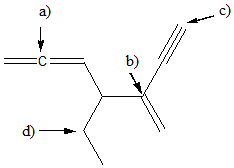
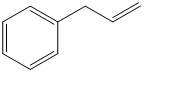
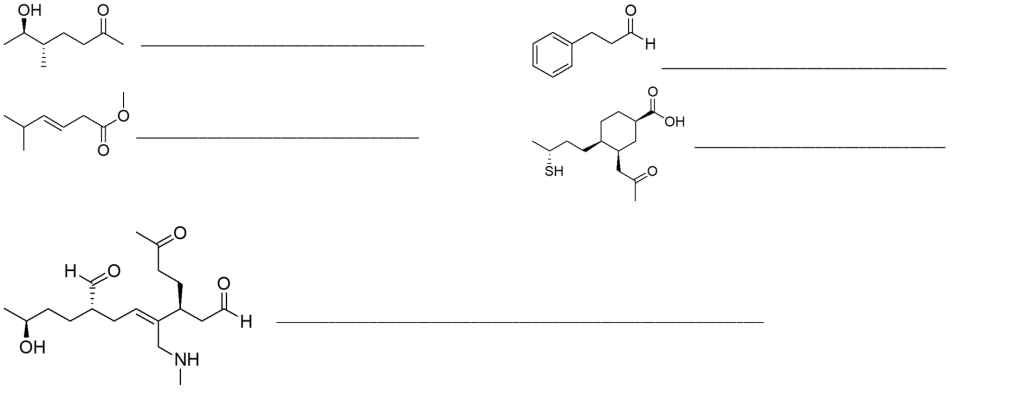
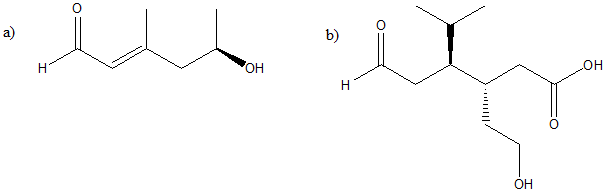
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

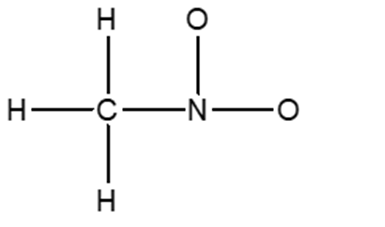
2. Disegnare la struttura di Lewis della seguente molecola: CH3CHO. Calcola le cariche formali per tutti gli atomi diversi dall’idrogeno
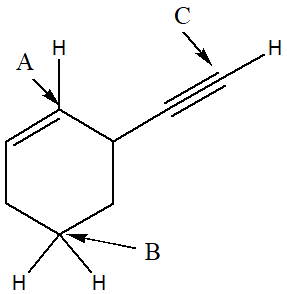
3. Qual è il più corto tra i legami indicati dalle frecce nella seguente molecola?
a) Cerchiare la lettera corrispondente.
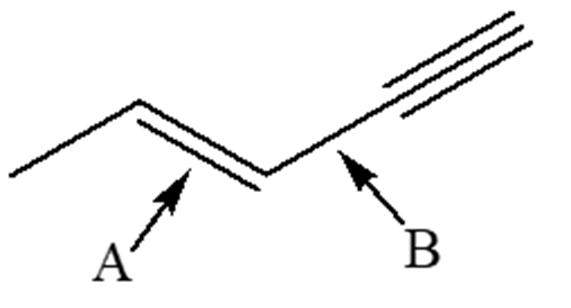
b) In riferimento al legame A, dire:
I) quali orbitali molecolari sono presenti
II) quali orbitali atomici o ibridi sono coinvolti nella formazione del legame
4. Il composto mostrato di seguito è l’acido nicotinico
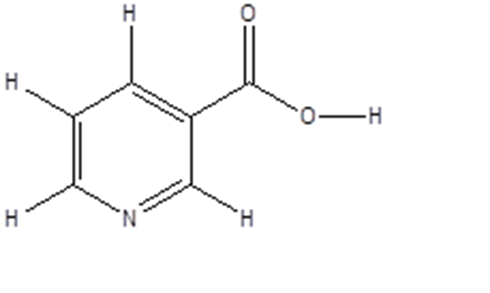
a) indicare con una freccia l’idrogeno più acido;
b) dire quale orbitale occupa la coppia solitaria dell’atomo di azoto
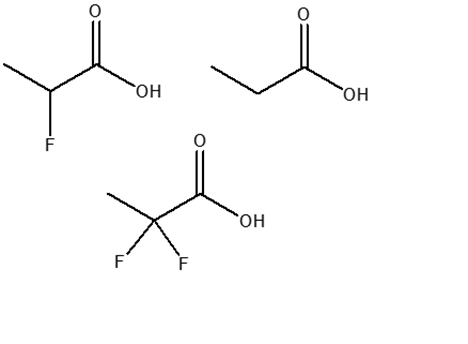
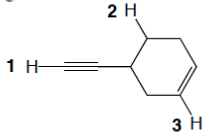
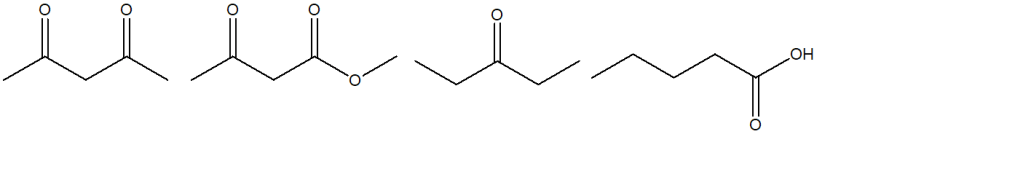
5. Disporre i seguenti composti in ordine di punto di ebollizione crescente. Indicare l’ordine inserendo i numeri nei riquadri sotto le strutture: 1= quello col punto di ebollizione più basso, 5= quello col punto di ebollizione più alto

6. Per l’1,4-dimetilcicloesano esistono due isomeri configurazionali (I e II); per l’1,2-dimetilcicloesano esistono tre isomeri configurazionali (I, II, III). Completare la seguente tabella.

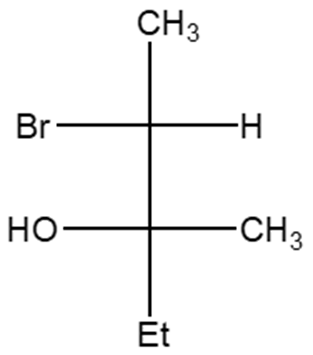
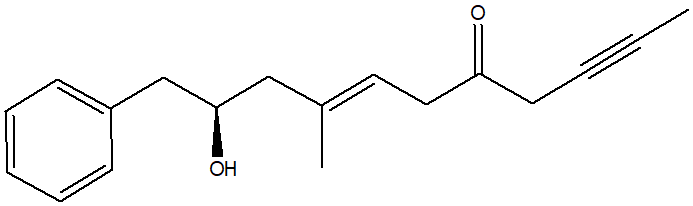
7. Attribuire la configurazione assoluta al seguente carbonio chirale:
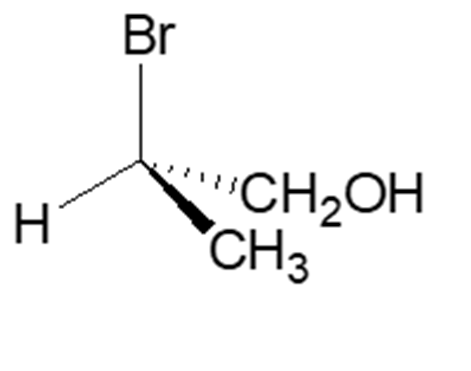
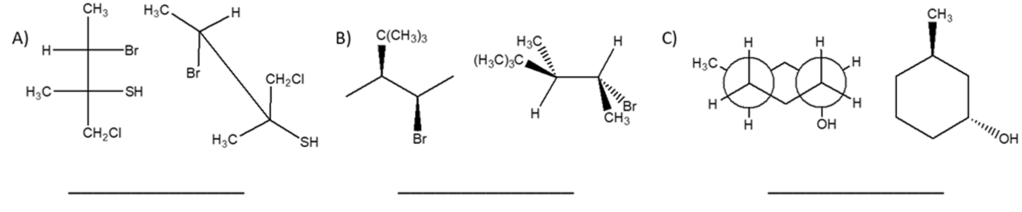
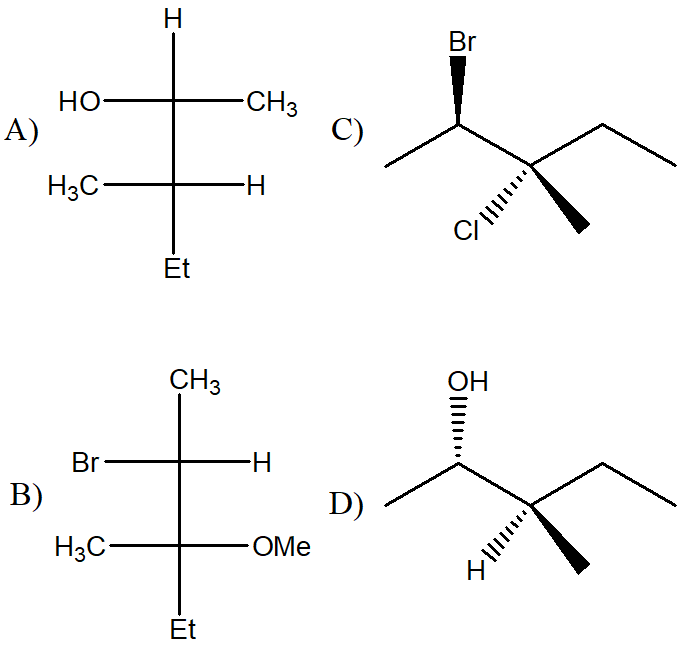
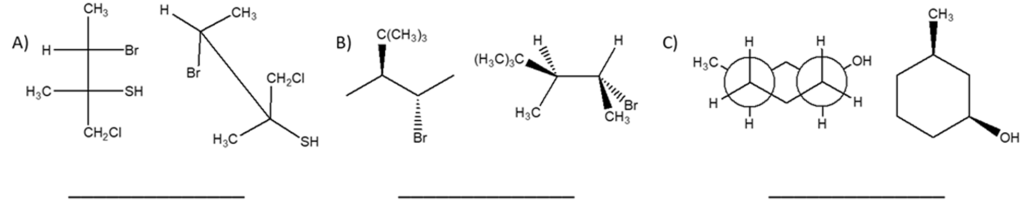
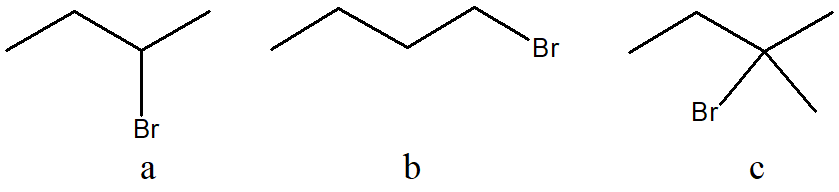
8. Dire quale dei seguenti composti non è otticamente attivo (è possibile scegliere più opzioni):

9. Il 2-metil-2-butene reagirà con Br2 in acqua per dare un’aloidrina (ignorare la stereochimica). La reazione ha Keq>1. Mostrare il meccanismo di reazione, inclusi gli stati di transizione. Poi, disegnare il diagramma energetico della reazione. Indicare nel diagramma le parti corrispondenti a reagenti, prodotti, stato di transizione, intermedio, variazione dell’energia libera di Gibbs, energia di attivazione di ciascuno stadio della reazione.
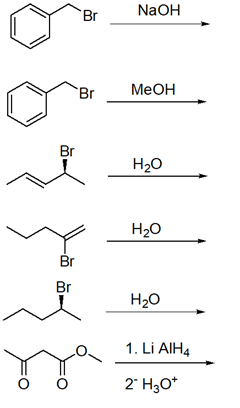
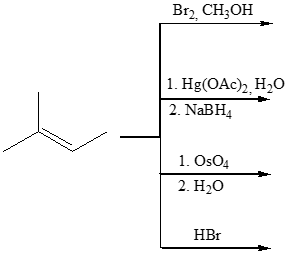
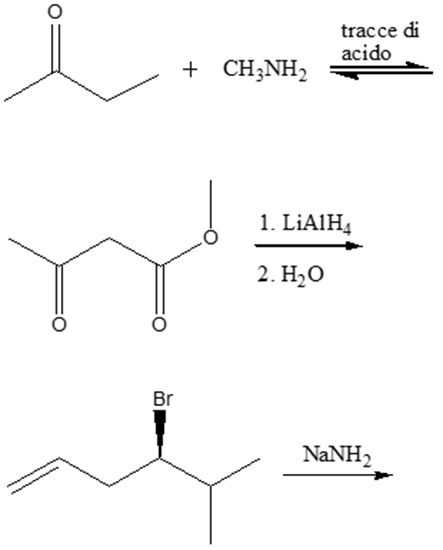
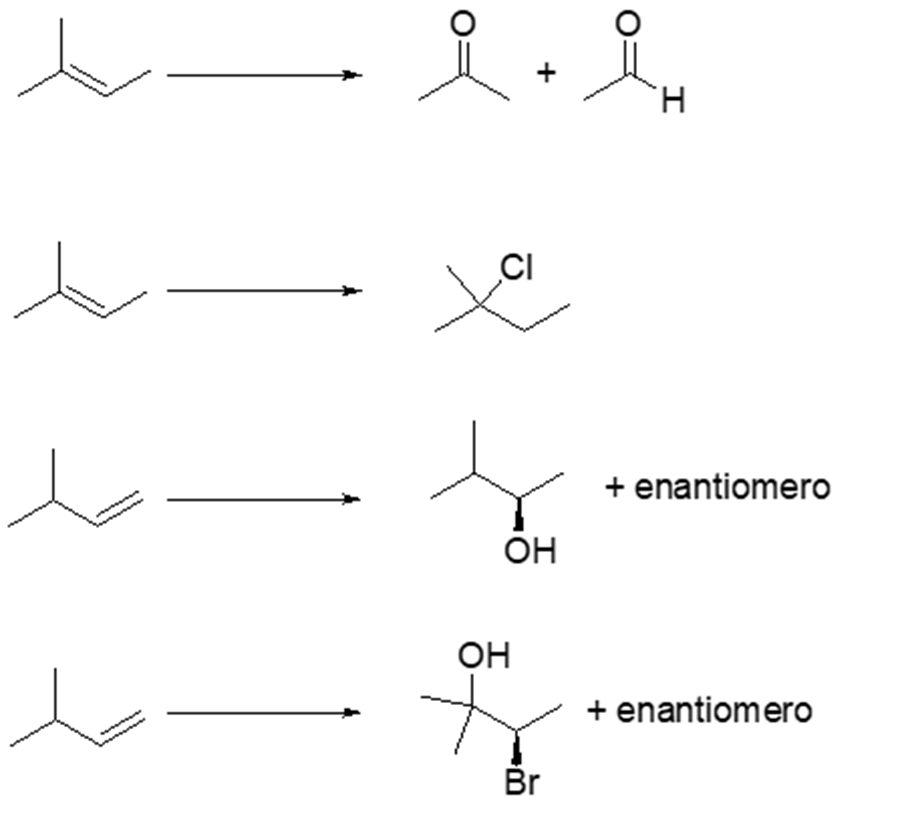
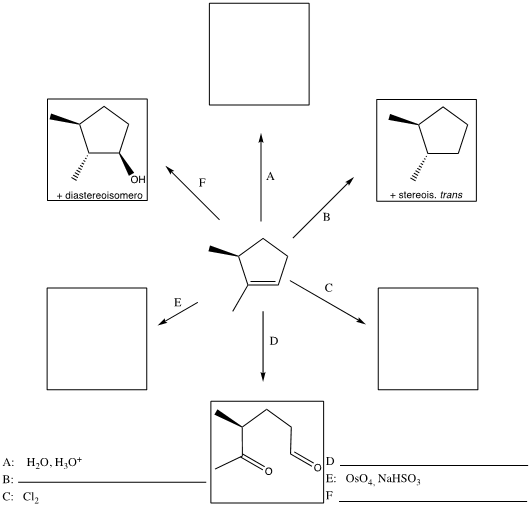
10. Scrivere i prodotti principali delle seguenti reazioni (se avvengono), indicando la stereochimica quando opportuno. Se la reazione non avviene, scrivere “nessuna reazione”
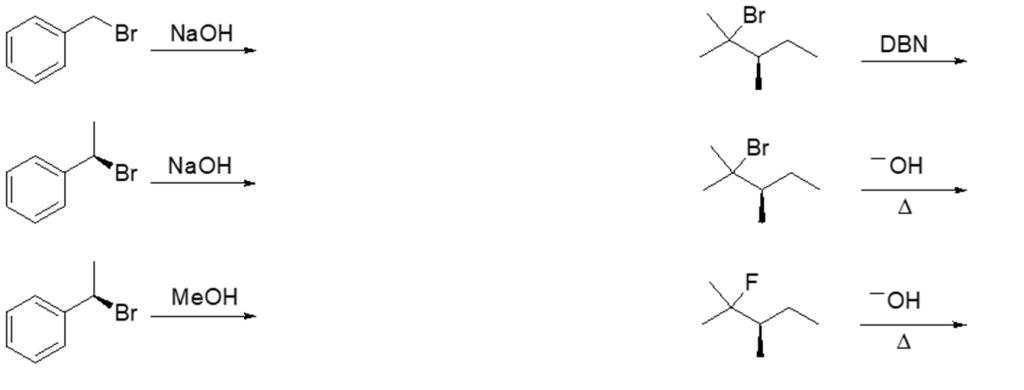
SECONDO SET
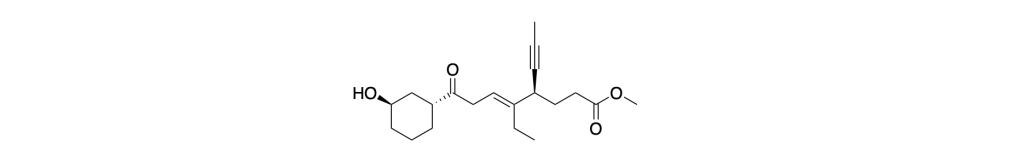
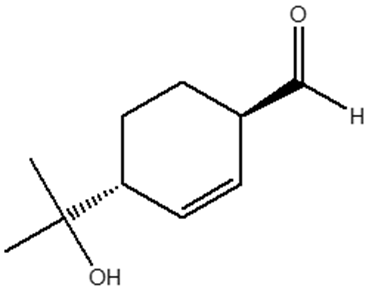
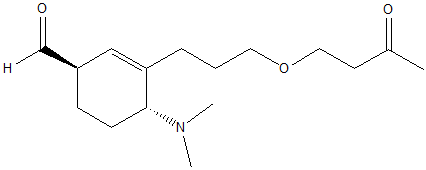
1. Assegnare il nome IUPAC, comprensivo di stereochimica, al seguente composto:
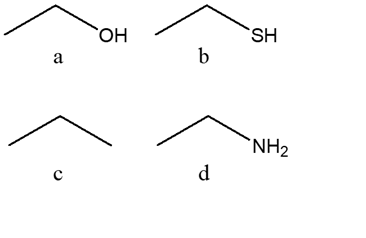
2. Disporre i seguenti composti in ordine di acidità crescente (dal meno acido al più acido) e spiegare sinteticamente il perché
a) CH3CH2SH
b) CH3CH2NH2
c) CH3CH2OH
d) CH3CH2CH3
3. In riferimento ai composti dell’esercizio 2, rispondere alle seguenti domande:
a) quale di esso sarà caratterizzaro dal valore di pKa più elevato?
b) quale dal valore di Ka più elevato?
4. Scrivere la struttura a segmenti del seguente composto e dire se il nome IUPAC è corretto; se non lo è, scrivere il nome corretto: 2-ciclopropilesano
5. Disegnare e scrivere il nome IUPAC di un composto di formula C9H18 che contenga solo idrogeni primari
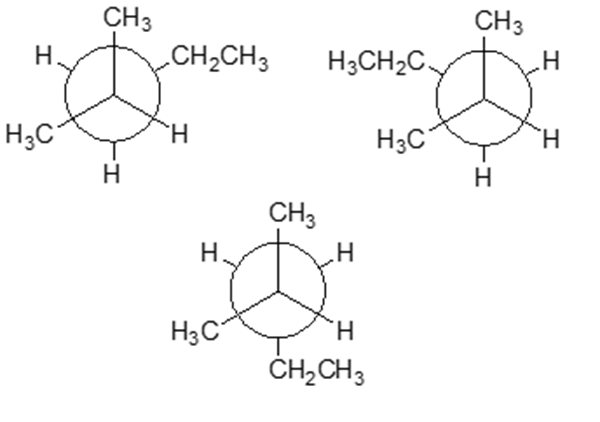
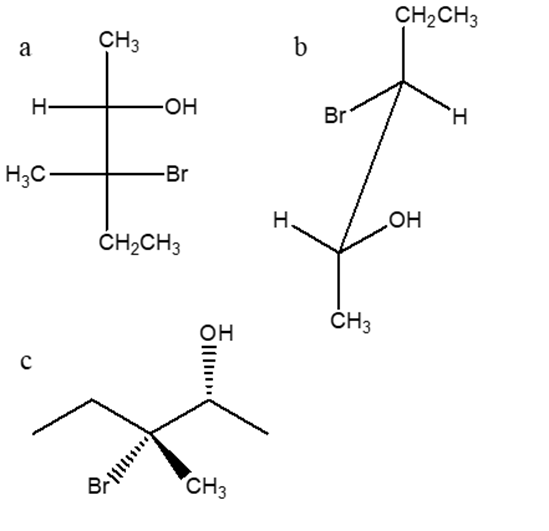
6. Stabilire le configurazioni assolute dei carboni chirali presenti nelle seguenti molecole (NB: la notazione va riportata vicino ai carboni cui fa riferimento) e dire qual è la relazione stereochimica esistente tra i composti di ciascuna coppia (isomeri conformazionali/enantiomeri/diastereoisomeri/stesso composto/altro):


7. Prendendo in considerazione il legame C3-C4 del 2-metilpentano, scrivere la proiezione di Newman del conformero meno stabile in assoluto e la struttura a cavalletto del conformero più stabile in assoluto
8. Disporre i seguenti composti in ordine di basicità crescente e motivare la risposta data

9. Mostrare il meccanismo di apertura del seguente epossido a) con metanolo in ambiente acido; b) con ione metossido. Mostrare la stereochimica dei prodotti. Attribuire il nome IUPAC all’epossido e ai prodotti formati.

10. Spiegate perché il trattamento con base del (1R,2R)-1-bromo-2-metilcicloesano genera il 3-metilcicloes-1-ene, un prodotto di eliminazione non Zeitzev
11. Scrivere iol D-glucosio e mostrare il meccanismo di riarrangiamento enediolico e quello di epimerizzazione.
12. Scrivere un L-amminoacido generico in proiezione di Fischer.
TERZO SET
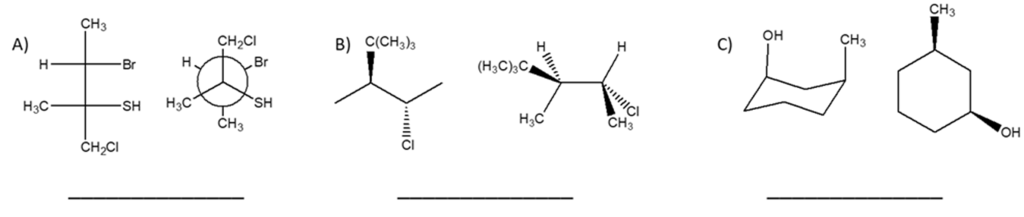
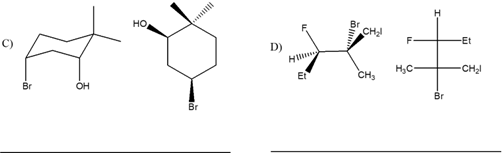
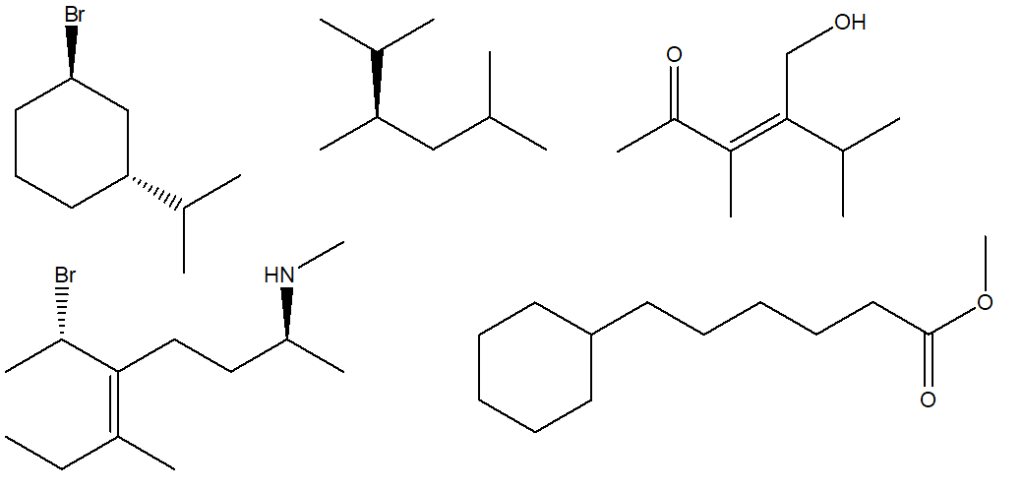
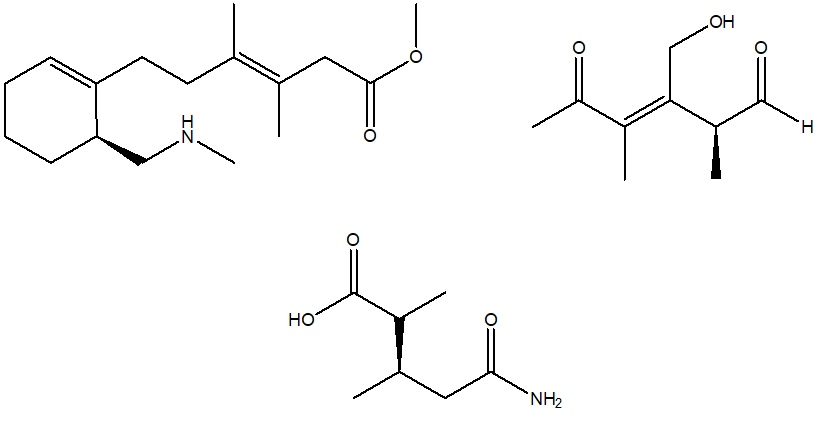
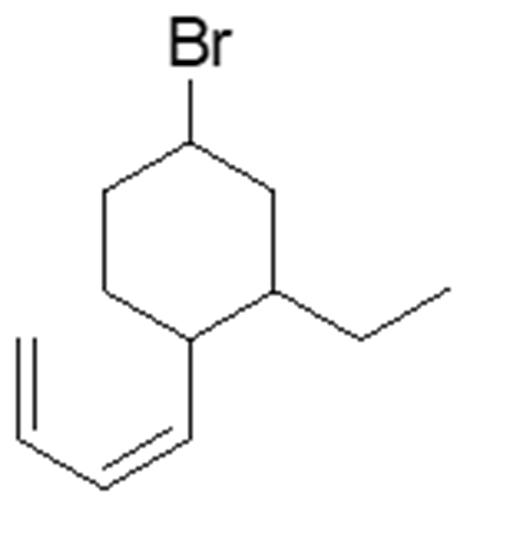
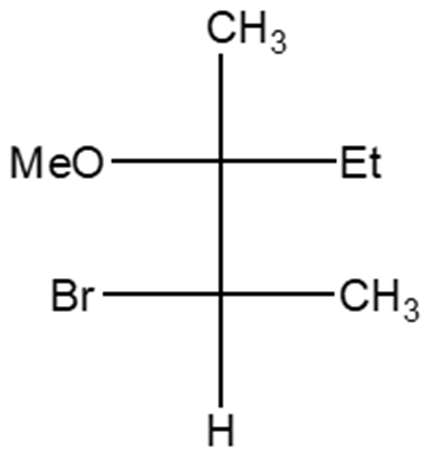
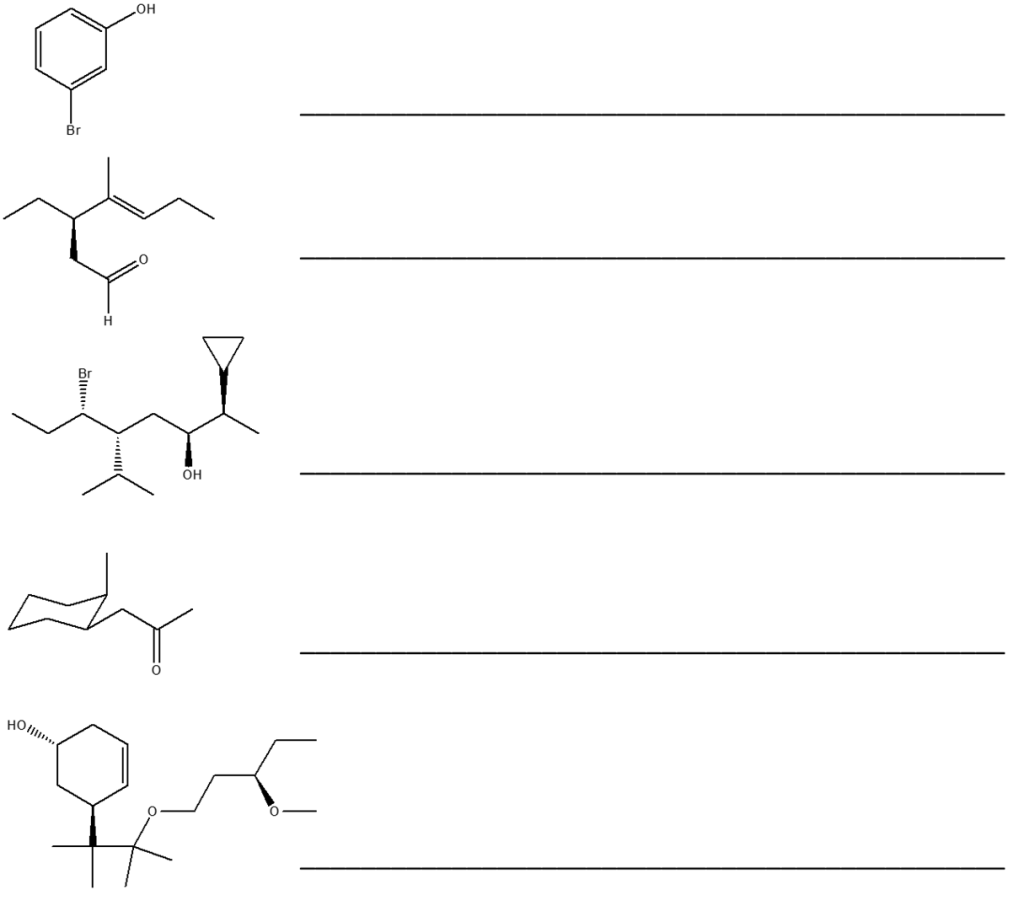
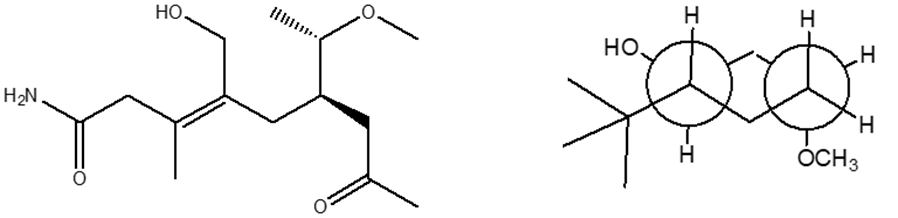
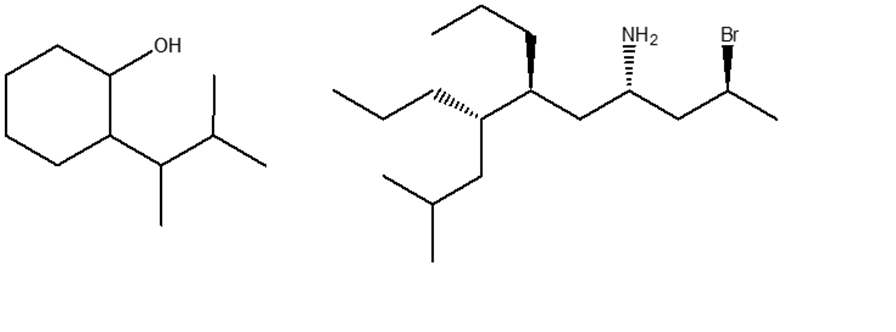
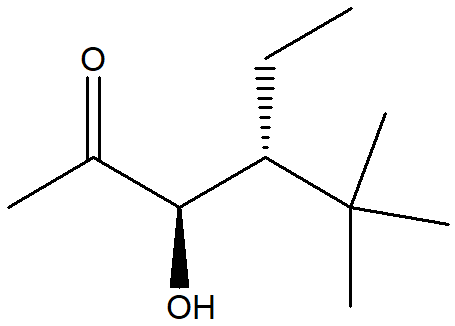
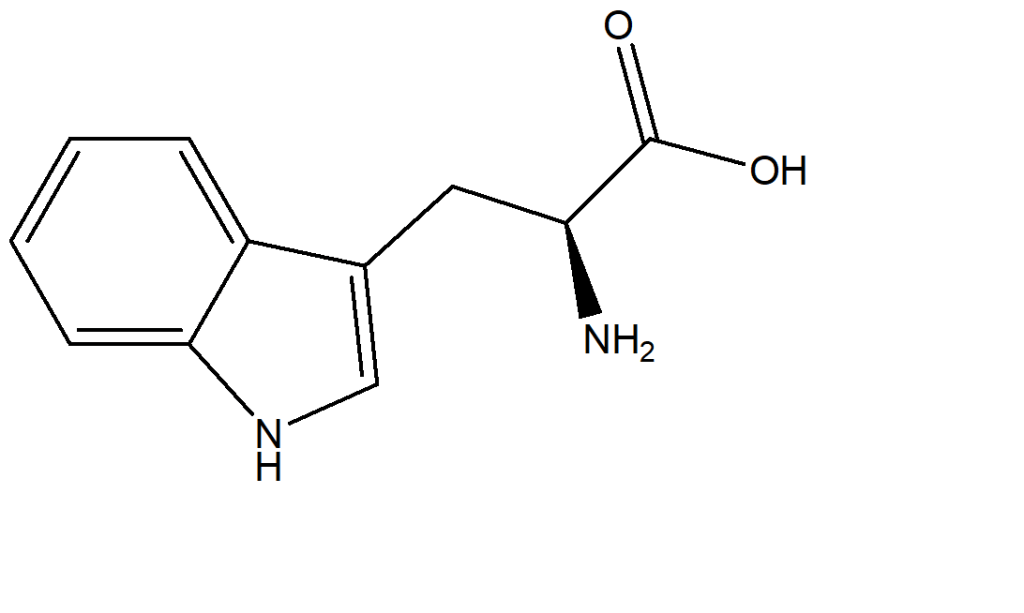
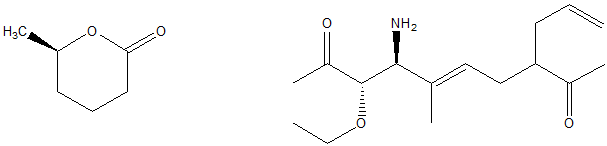
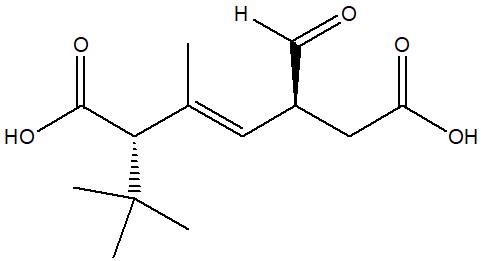
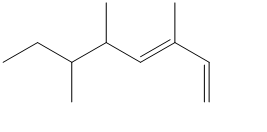
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

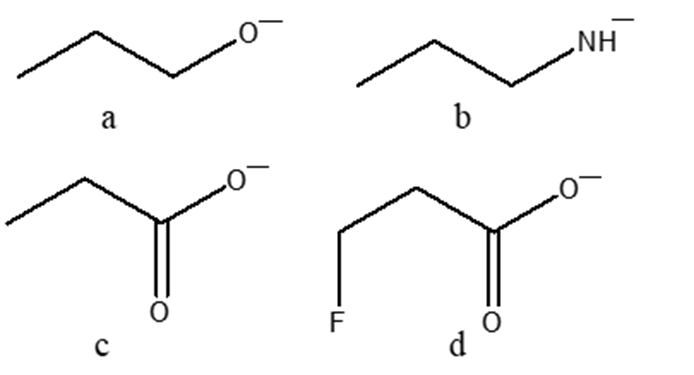
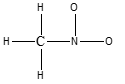
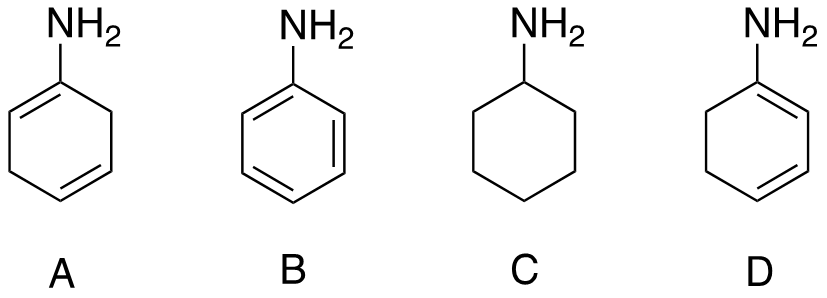
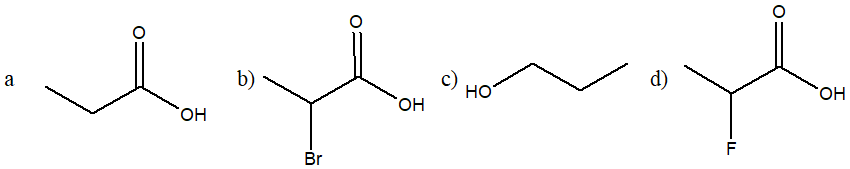
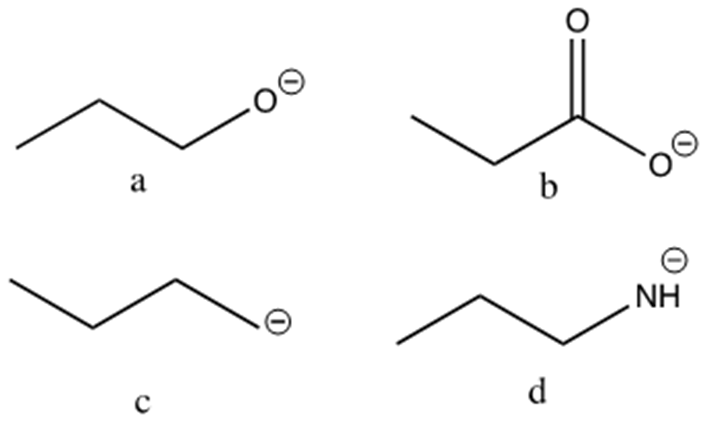
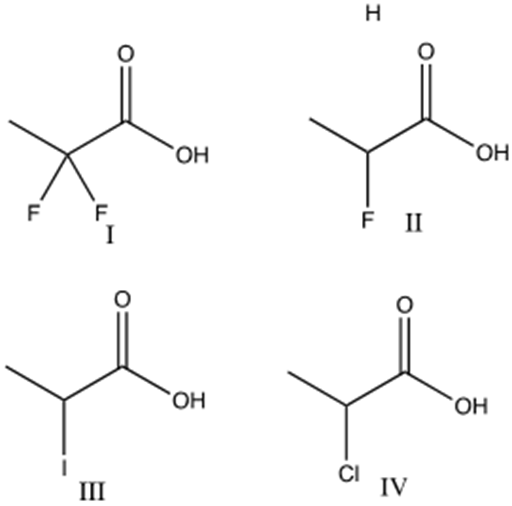
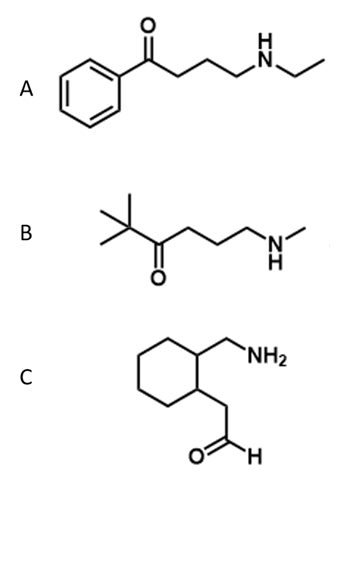
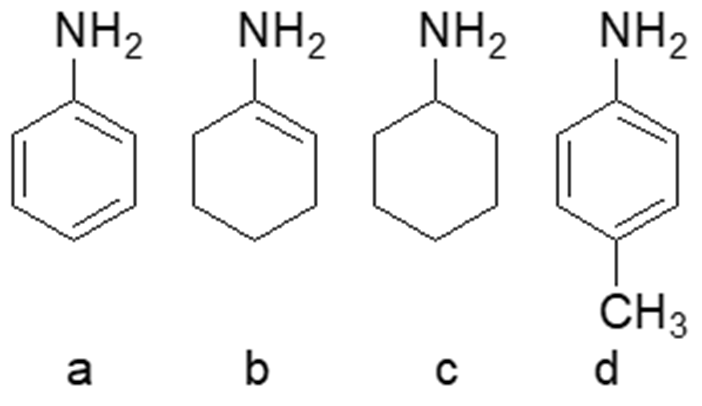
2. Disponi i seguenti composti in ordine di basicità crescente (dal meno basico al più basico), motivando sinteticamente la scelta
3. L’acido acetico ha pKa=4.8.
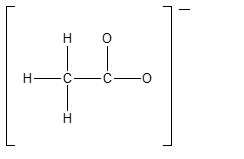
a) Quale sarà la forma predominante in una soluzione a pH 2.8? Disegnarne la formula di Kekulé nel riquadro sotto.
b) In quale rapporto saranno la forma acida e la forma basica a questo valore di pH?
4. Scrivere il seguente composto in proiezione di Newman secondo i legami C1-C6 e C3-C4: (1R,3S,4R)-4-isopropil-3-metilcicloesan-1-olo. Poi, effettuare l’inversione d’anello e dire qual è il conformero più stabile
5. In riferimento alla conformazione più stabile del composto dell’esercizio 4, descrivere le interazioni 1,3-diassiali (se presenti) e altre interazioni gauche (se presenti). NB: è sufficiente indicare i gruppi tra cui si instaurano tali interazioni (es.: tra il sostituente X in assiale e…).
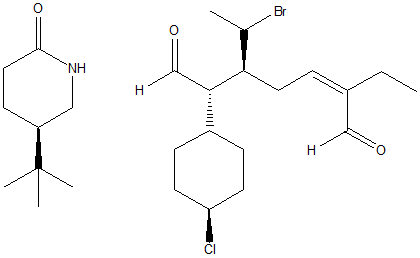
6. Calcolare il numero massimo di stereoisomeri possibili per la seguente struttura. Scriverne uno a scelta e assegnargli il nome IUPAC completo di stereochimica

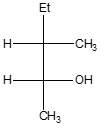
7. Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto utilizzando una reazione di idroborazione/ossidazione. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
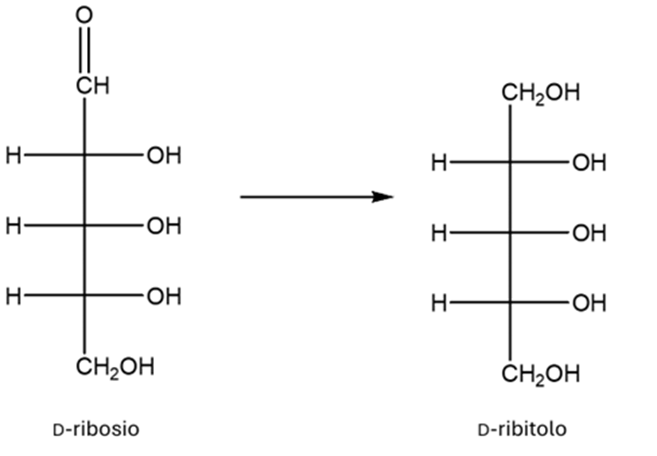
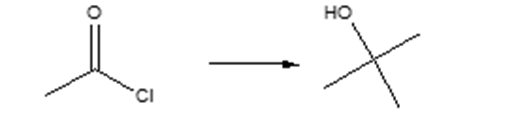
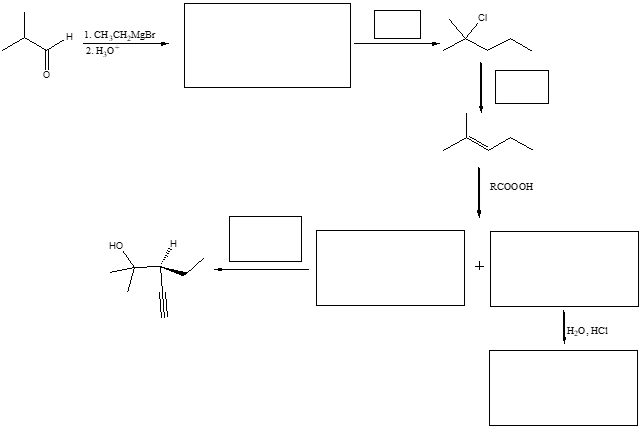
8. Mostrare il meccanismo e i prodotti della seguente reazione:
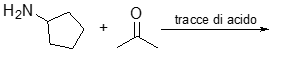
9. Scrivere un legame peptidico tra due amminoacidi (usare R per indicare le catene laterali degli amminoacidi). Dimostrare che tale legame ha parziale carattere di doppio legame.
10. Scrivere la proiezione di Fischer dell’L-alanina (R=-CH3) e determinare la configurazione assoluta del carbonio chirale
















































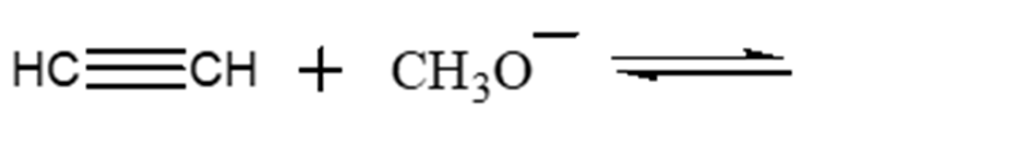







































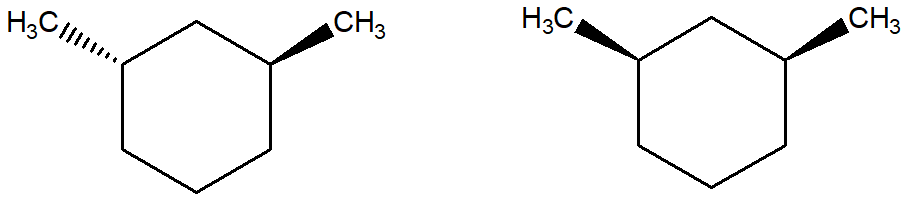

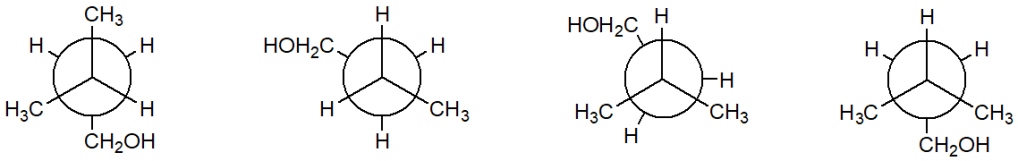



You must be logged in to post a comment.