Molecole con più unità stereogeniche e con più carboni asimmetrici

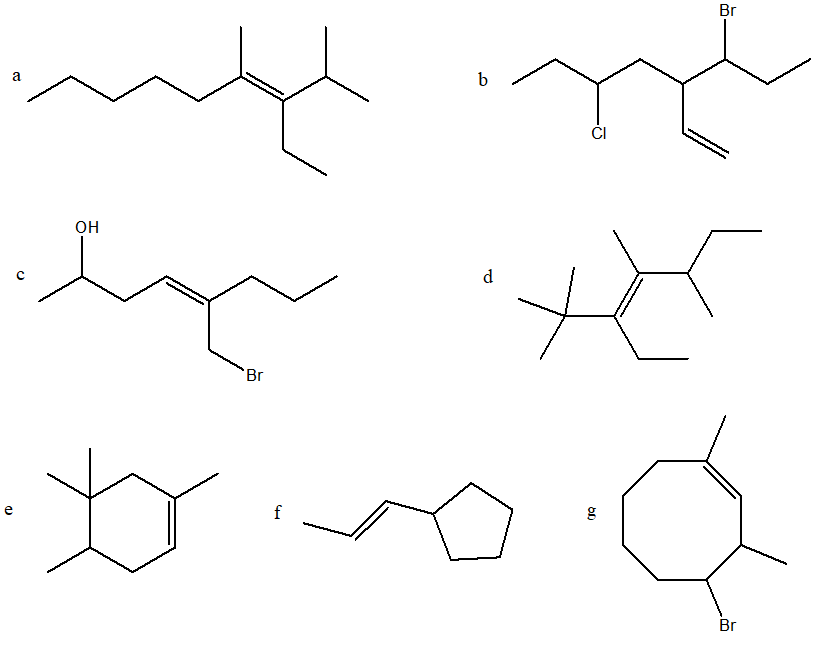
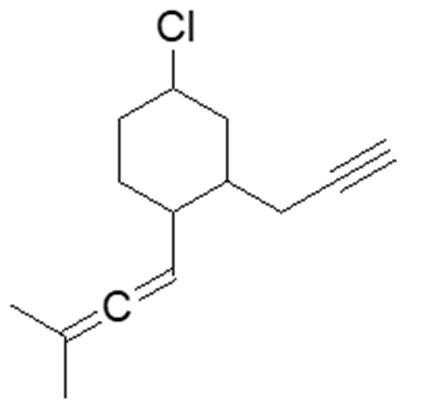
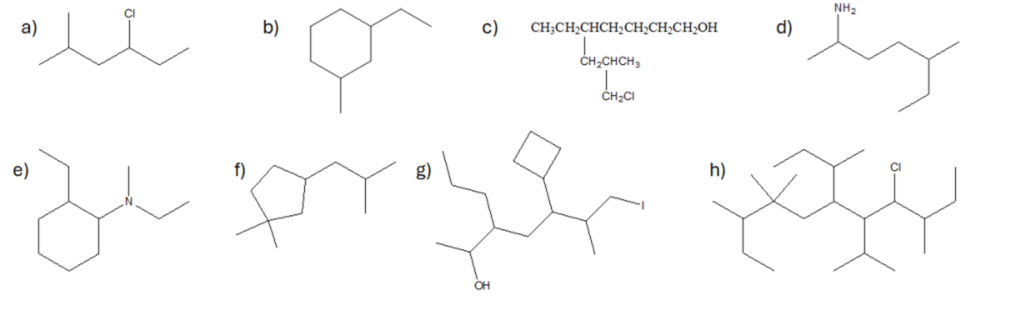
1. Per ciascuna delle seguenti molecole prevedere il numero massimo di stereoisomeri
I) Individuare gli elementi stereogenici (o unità stereogeniche= carbonio chirale, doppio legame che ammette isomeria geometrica, ciclo con due sostituenti che non possiede carboni chirali ma che dà origine ad isomeria cis-trans); II) definire il numero massimo di stereoisomeri (2n dove n è il numero di elementi stereogenici)

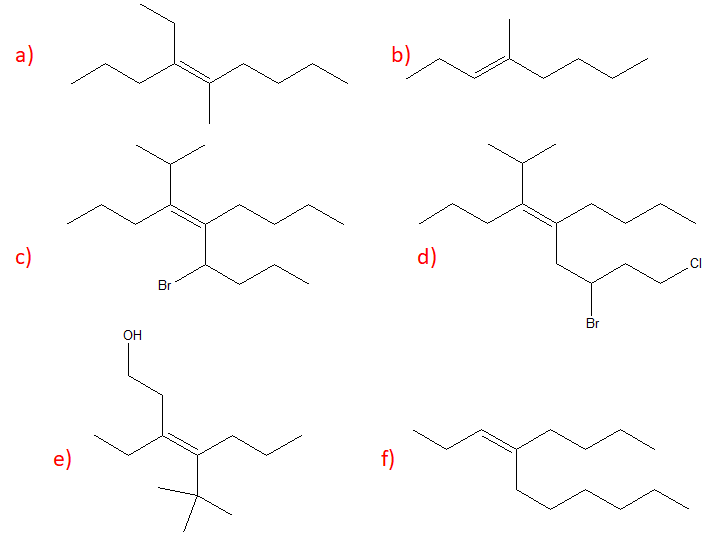
2. Definire la geometria (E o Z) dei doppi legami presenti nelle seguenti molecole
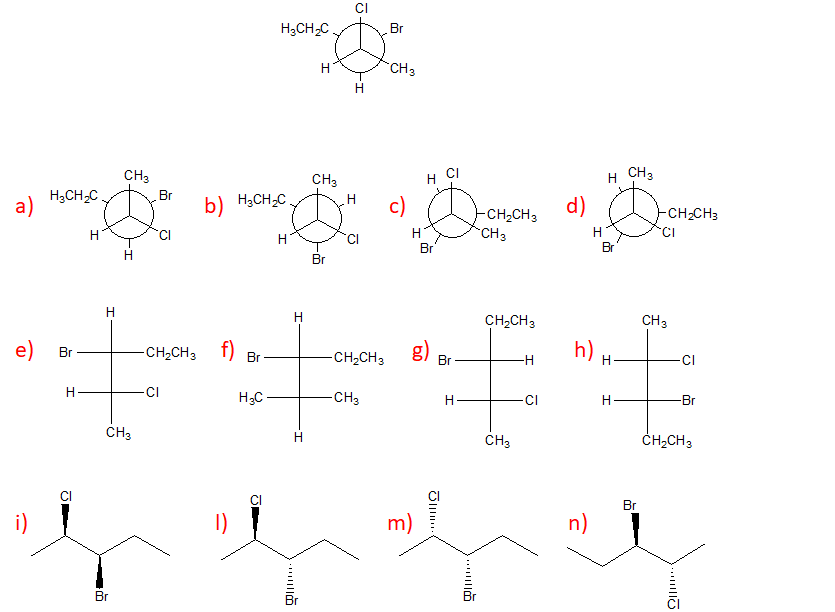
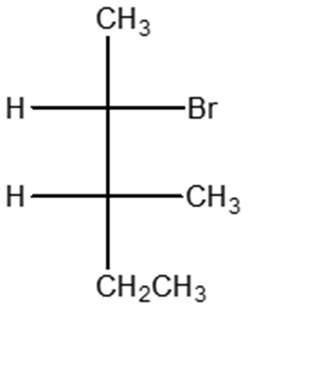
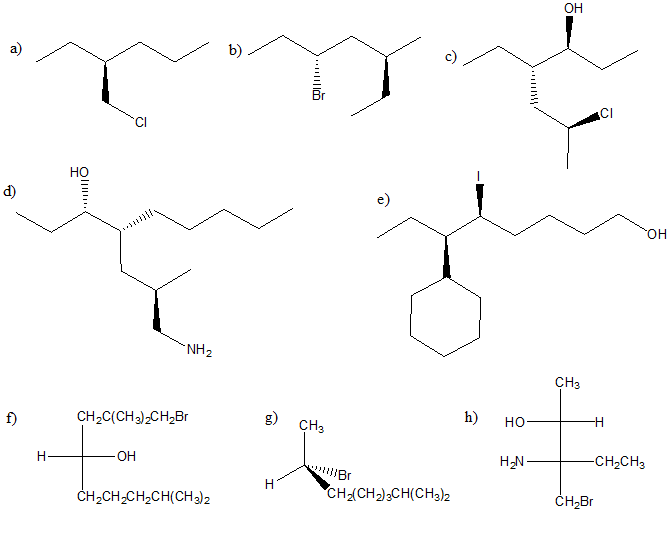
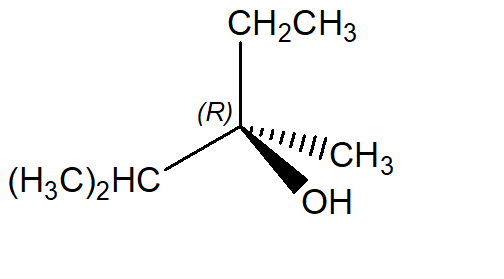
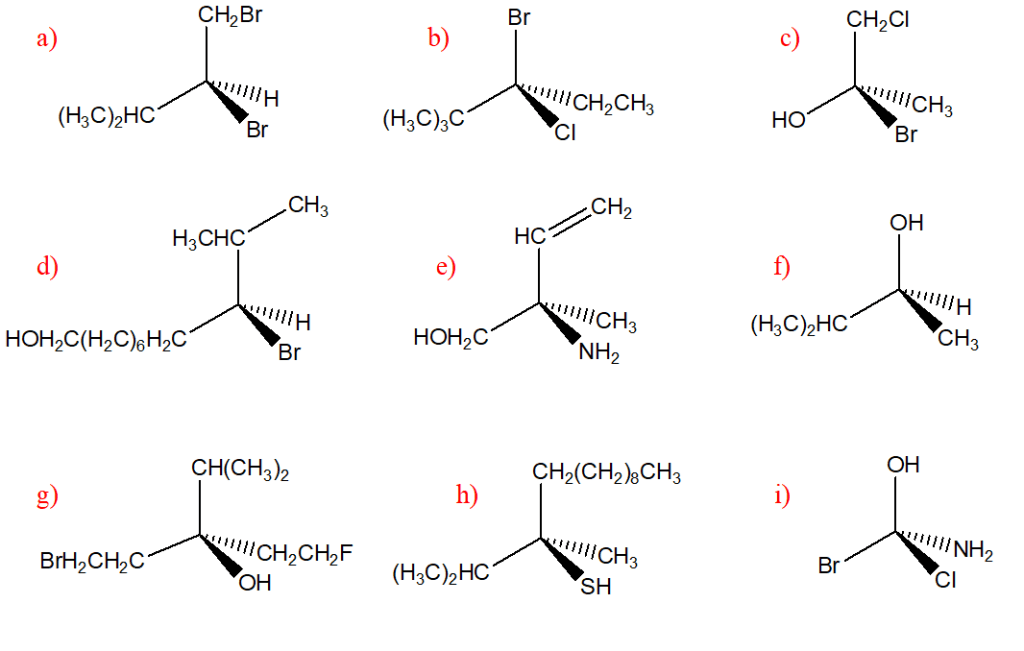
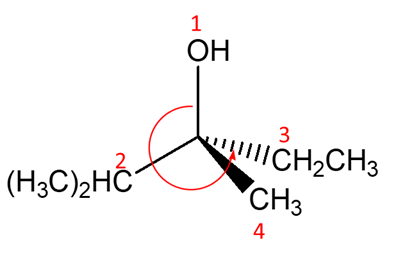
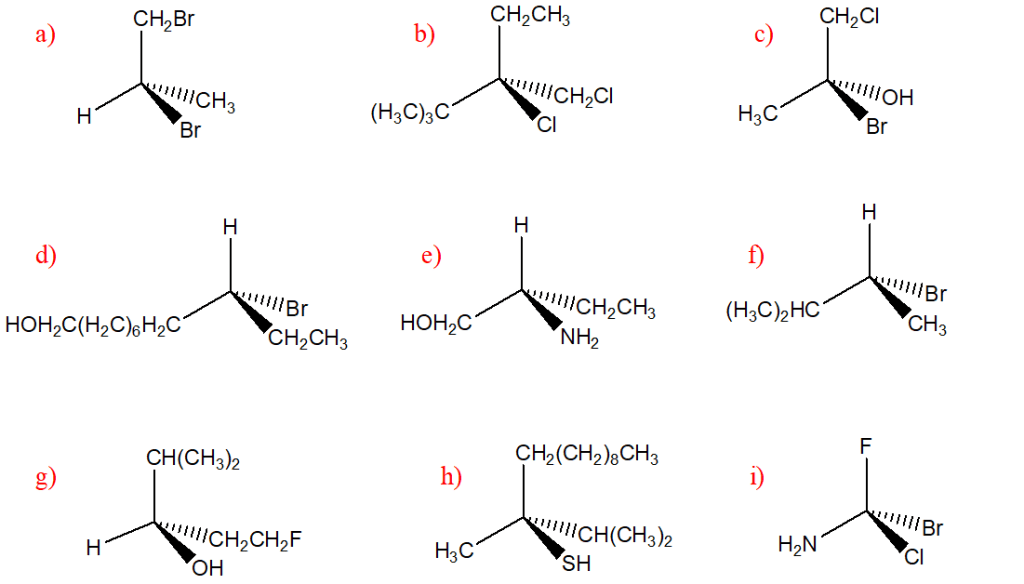
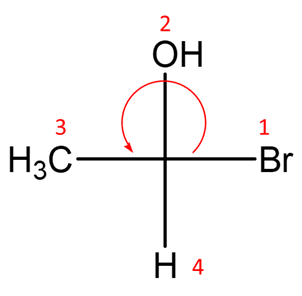
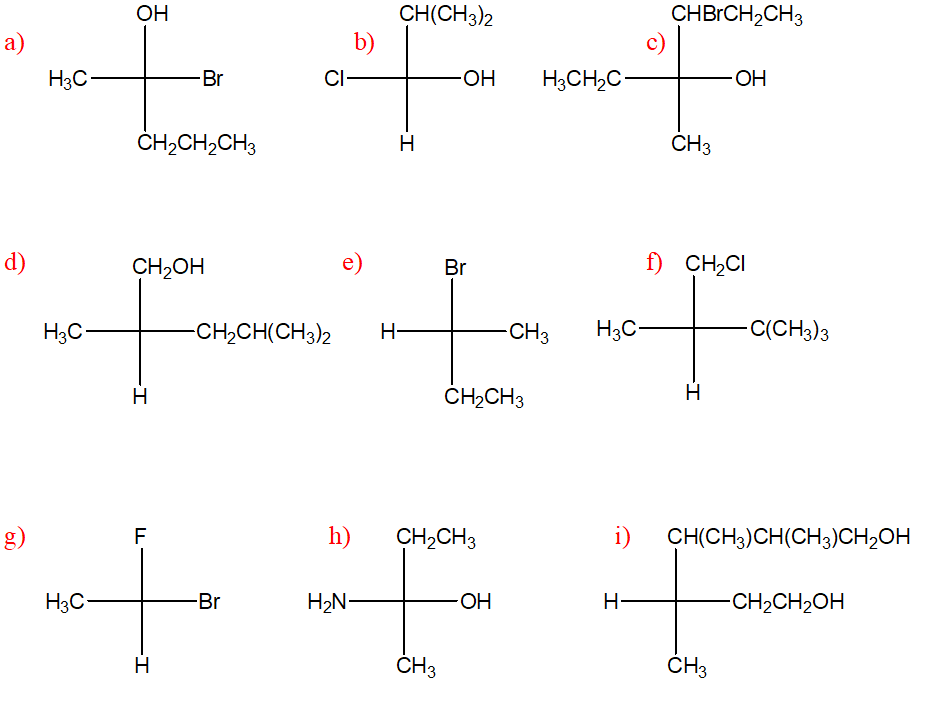
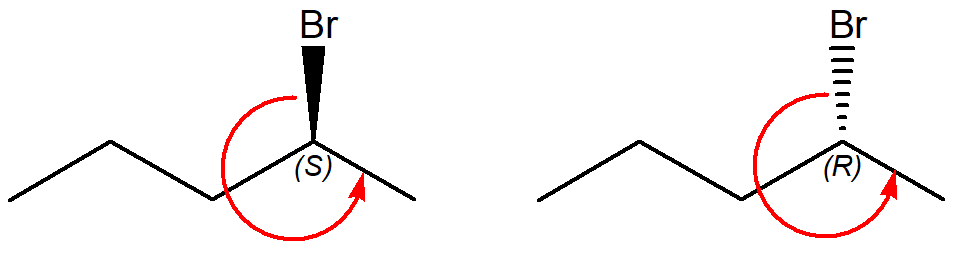
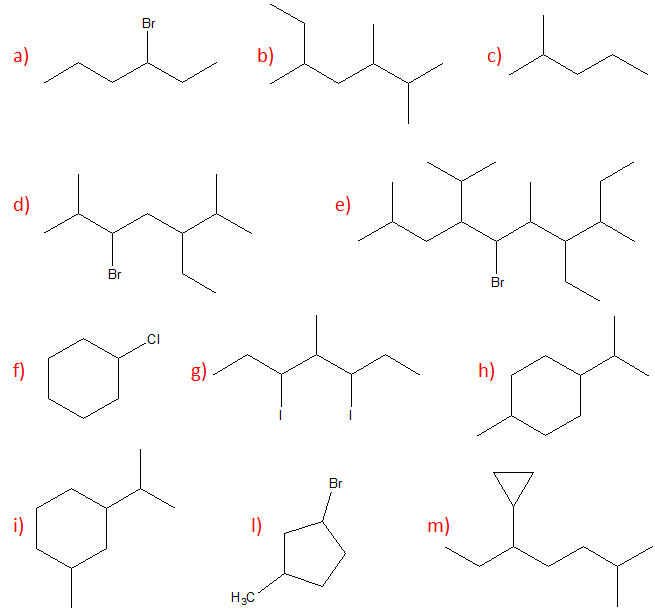
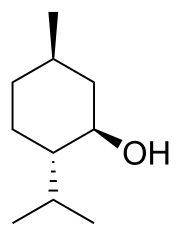
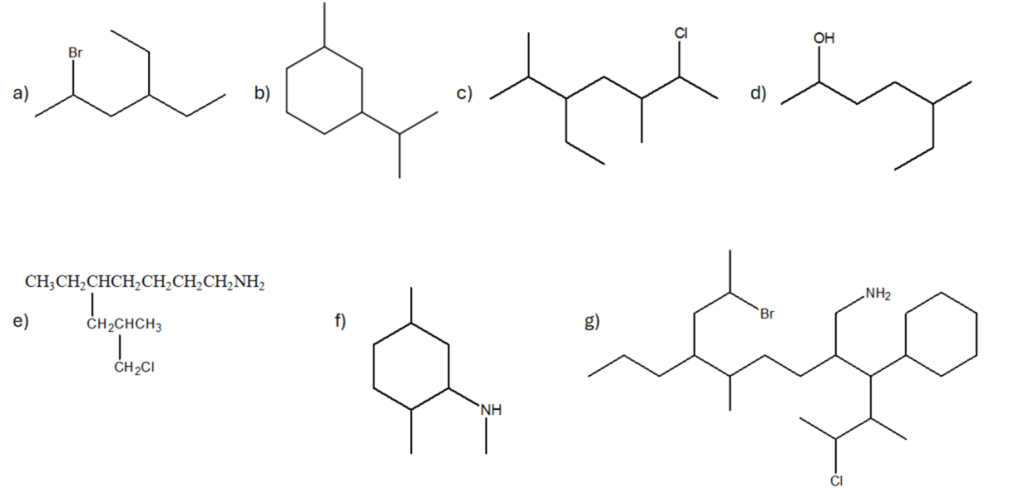
3. Confrontare ciascuna delle strutture indicate dalle lettere a-n con quella riportata qui sotto. Definire la relazione esistente tra la struttura in questione e le strutture a-n (cioè dire se sono tra loro enantiomeri, diastereoisomeri, stesso composto, isomeri costituzionali, isomeri geometrici, isomeri conformazionali o altro).
Nel confrontare due strutture:
I) capire se gli atomi sono connessi allo stesso modo (se non lo sono, ma la formula molecolare è la stessa–> isomeri costituzionali; se la formula molecolare è diversa–> altro)
II) se I è vero, capire se i carboni chirali hanno configurazione assoluta corrispondente. Se non è così, determinare se ci troviamo di fronte ad enantiomeri o a diastereoisomeri. NB: nel primo caso (enantiomeri), tutte le configurazioni saranno opposte. Per verificare questo punto è quindi necessario attribuire le configurazioni assolute. Se necessario, convertire la rappresentazione in quella più utile per determinare la configurazione assoluta* (es. da proiezione di Newman a Fischer).
III) se le configurazioni dei carboni chirali corrispondono, capire se ci troviamo di fronte a isomeri conformazionali.
IV) Se le molecole non sono distinguibili sulla base dei punti elencati in I, II e III, siamo di fronte allo stesso composto.
*NB: In questo caso specifino, l’unica rappresentazione da convertire è quella di Newman (QUESTA PARTE DELL’ESERCIZIO SARA’ CHIARITA DOMANI A LEZIONE), in quanto le altre rappresentazioni permettono di determinare in maniera agevole la configurazione assoluta.
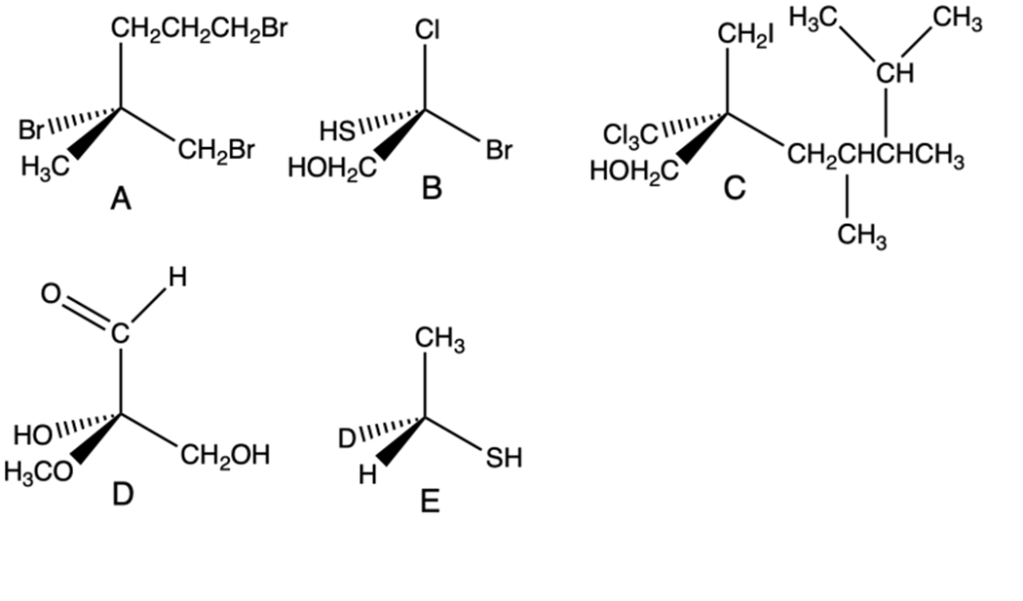
4. Dire in che relazione tra loro sono i componenti delle seguenti coppie di strutture (stesso composto/entantiomeri/diastereoisomeri/composti diversi, ecc.). Inoltre, per ciascun composto dire se è o meno chirale:
Per il primo punto, far riferimento alle linee guida degli esercizi precedenti. Per l’ultimo, dobbiamo capire 1) se ci sono carboni chirali 2) nel caso in cui ci sono due o più carboni chirali, dobbiamo capire se siamo o meno di fronte al composto meso.

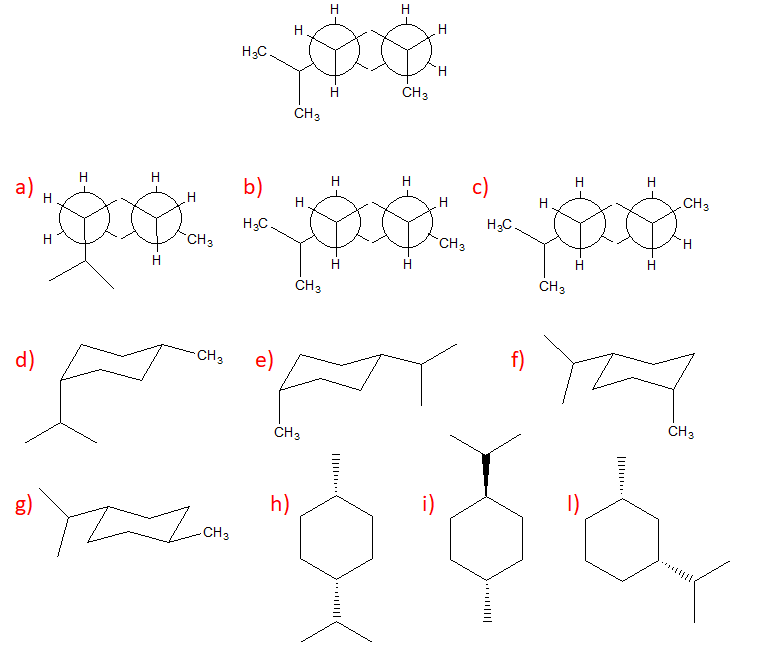
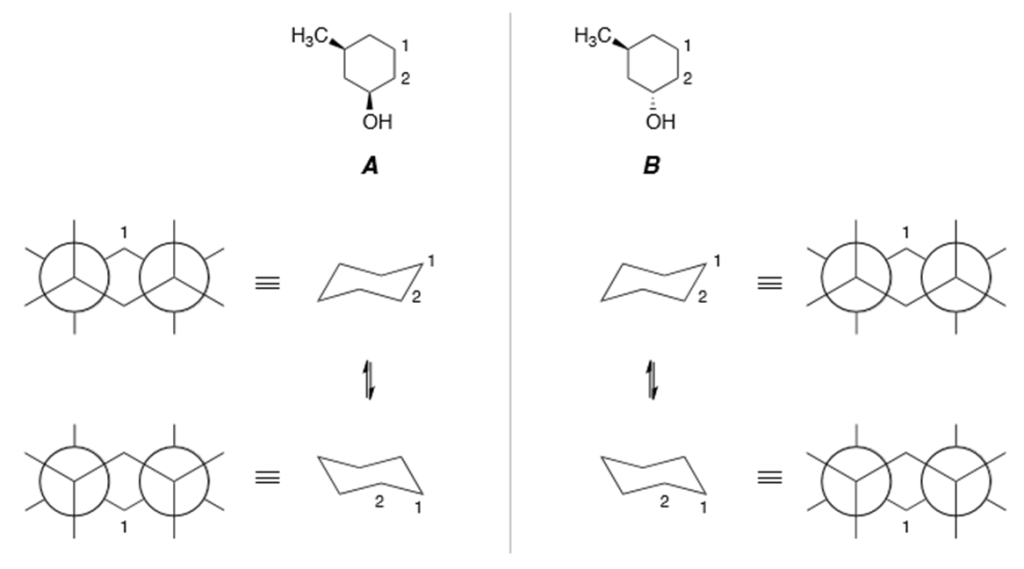
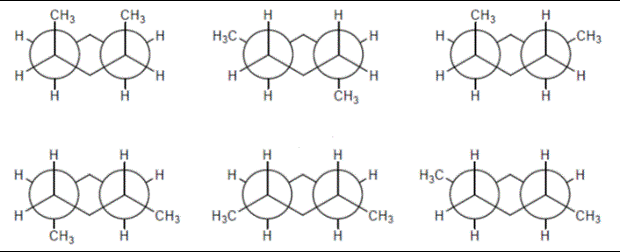
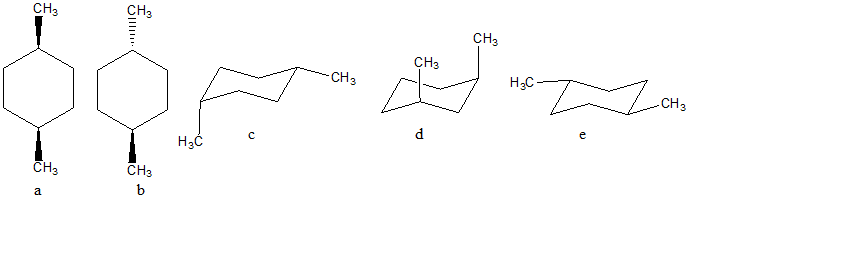
5. Confrontare ciascuna delle strutture indicate dalle lettere a-l con quella riportata qui sotto. Definire la relazione esistente tra la struttura in questione e le strutture a-l (cioè dire se sono tra loro enantiomeri, diastereoisomeri, stesso composto, isomeri costituzionali, isomeri geometrici, isomeri conformazionali o altro).
Nel caso del cicloesano sostituito, dobbiamo far attenzione anche alla posizione relativa dei sostituenti (es. 1-3, 1-4) per capire se abbiamo o meno carboni chirali. Dobbiamo, inoltre, tenere in conto che in questo caso possiamo avere anche isomeri geometrici (NB: se ad es. il cicloesano è sostituito 1-4, saranno possibili solo isomeri geometrici e non sarà possiile avere isomeri ottici). Per quanto riguarda i carboni chirali, per evitare errori, convertire le proiezioni di Newman e la rappresentazione a sedia in strutture a segmenti prima di determinare la configurazione assoluta.
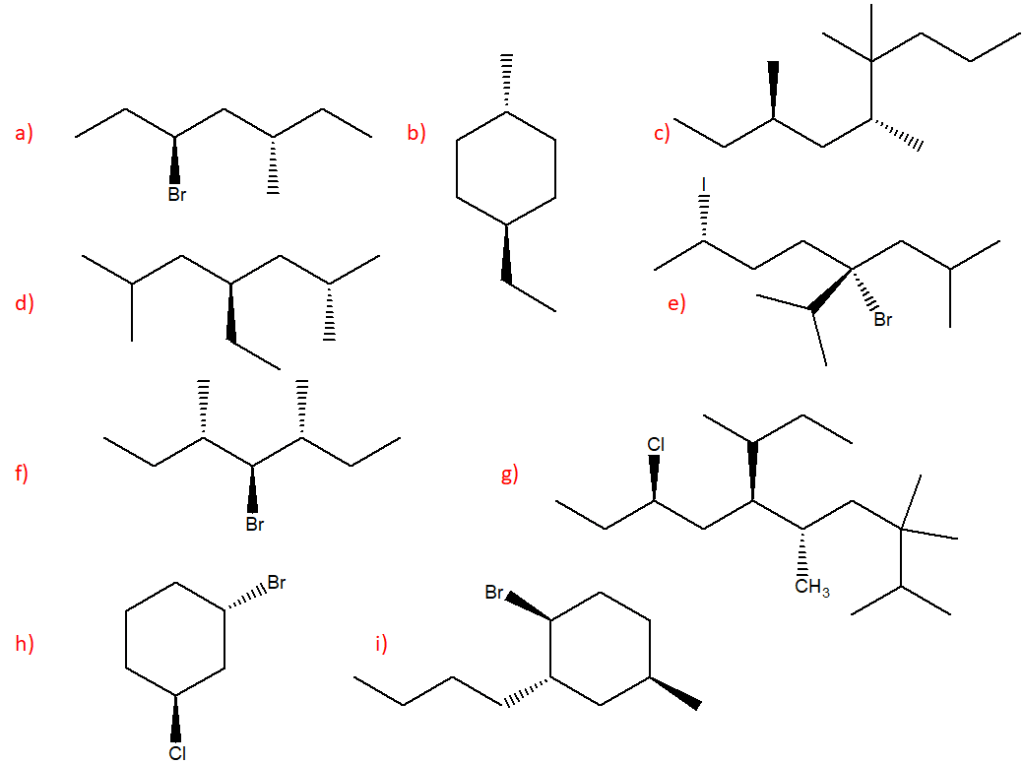
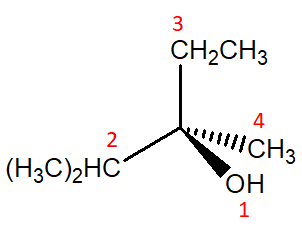
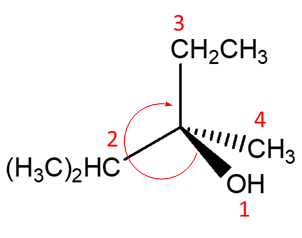
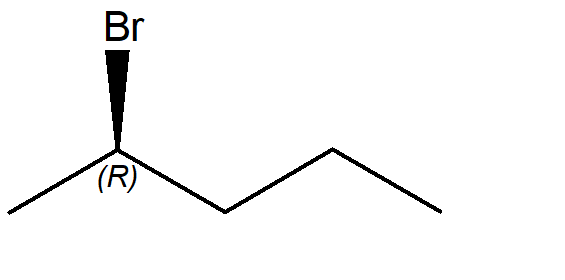
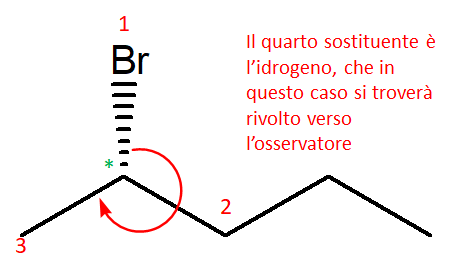
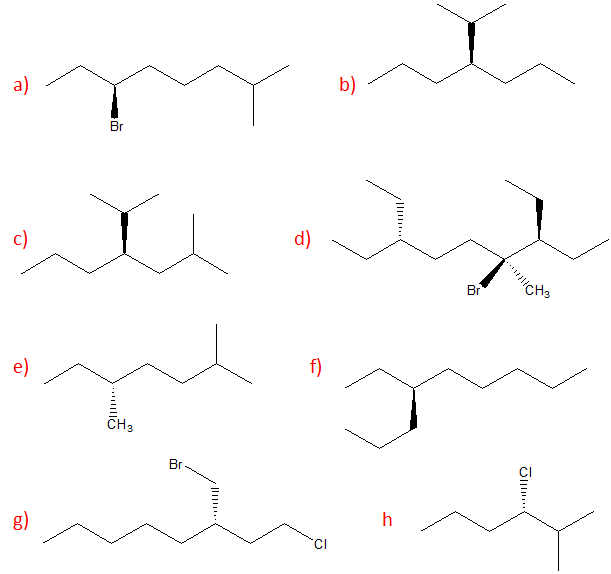
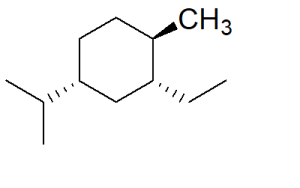
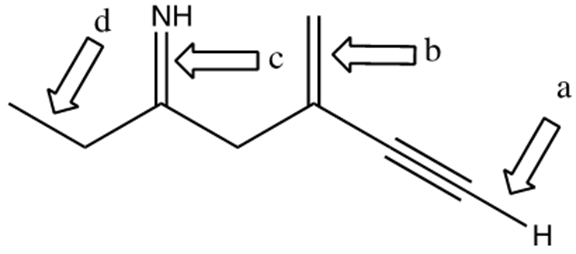
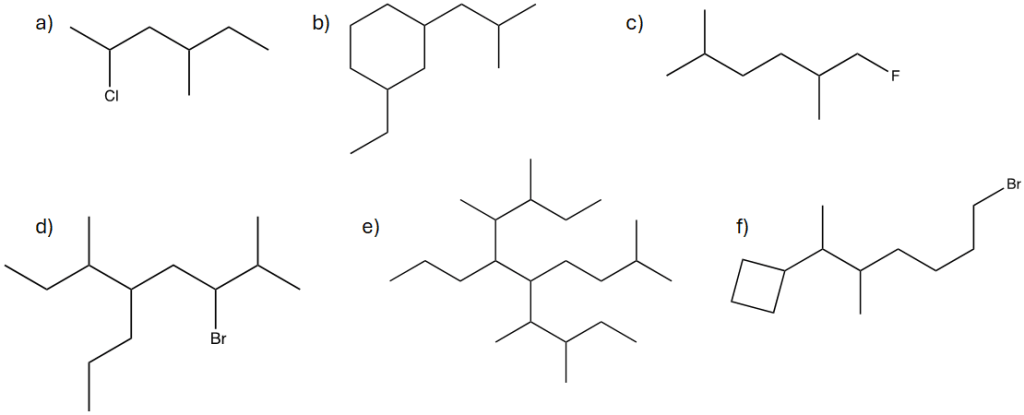
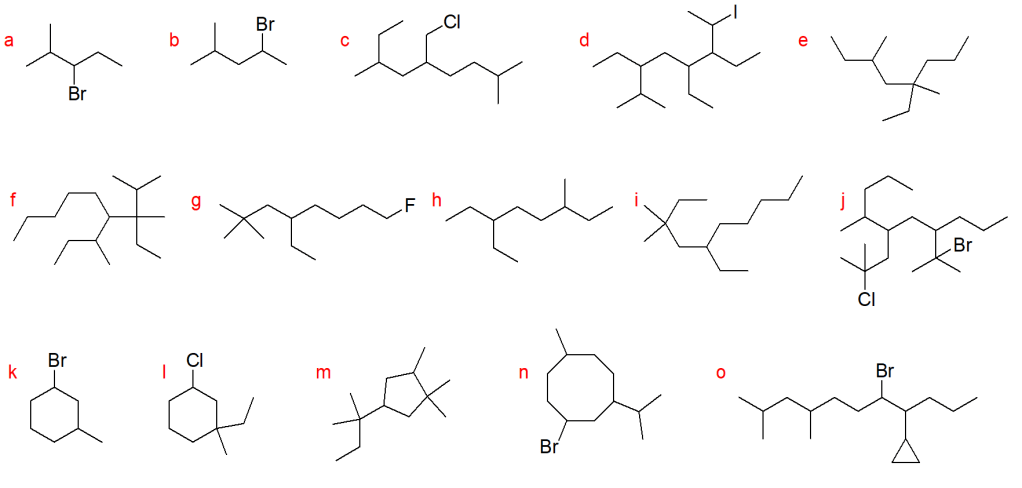
6. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti.
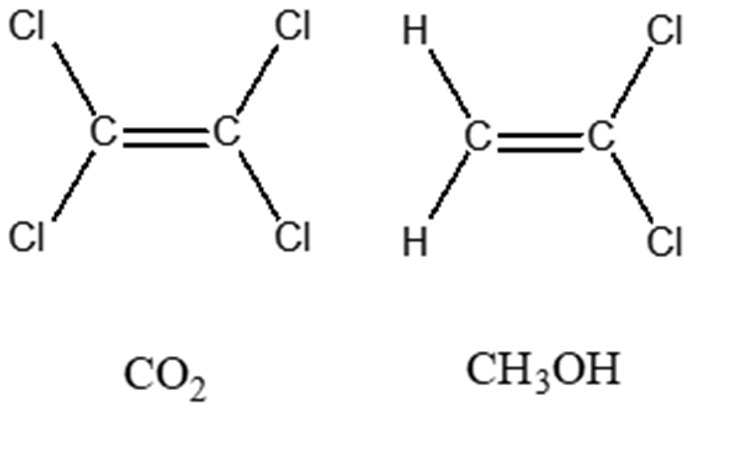
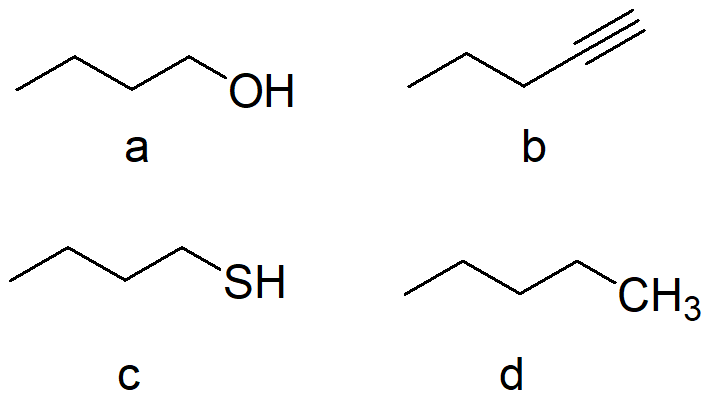
7) Quale/i dei seguenti composti non è/non sono chirale/i?
In questo esercizio e nel successivo bisogna innanzitutto valutare se ci sono carboni chirali. In presenza di più carboni chirali, dobbiamo capire se siamo di fronte al composto meso

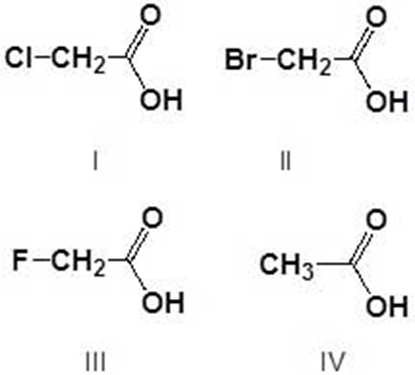
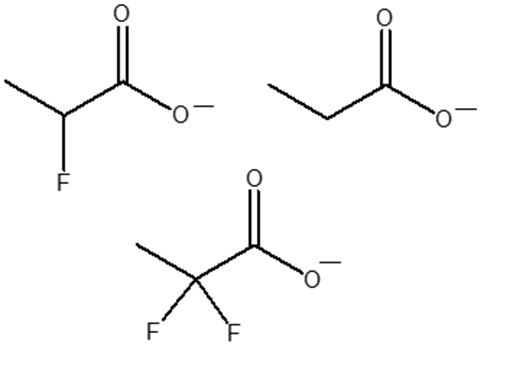
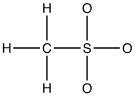
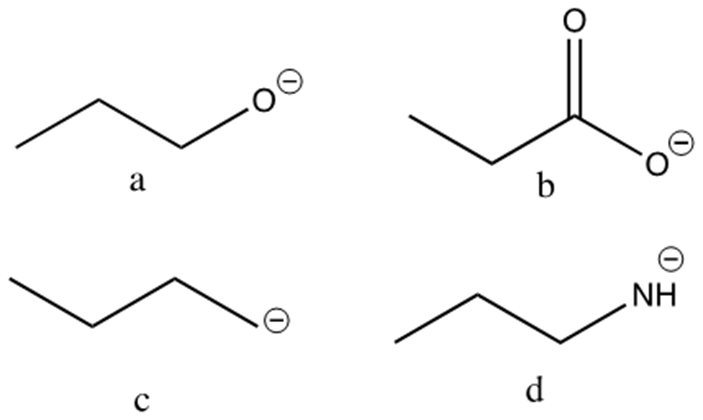
8. Dire se i seguenti composti sono otticamente attivi

9. Rispondere alle domande A-D relative ai seguenti composti:

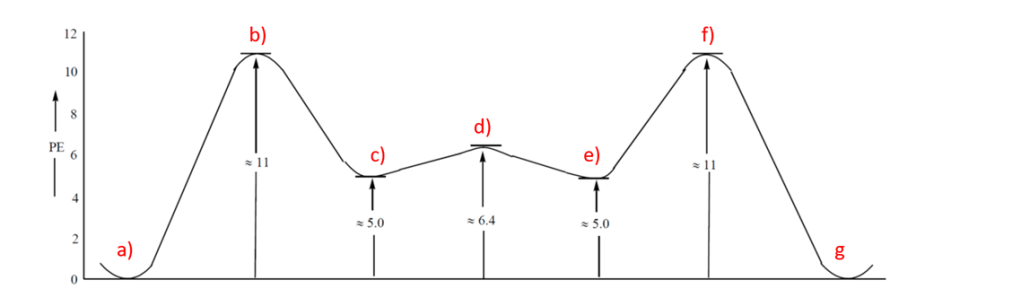
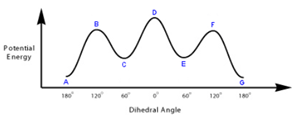
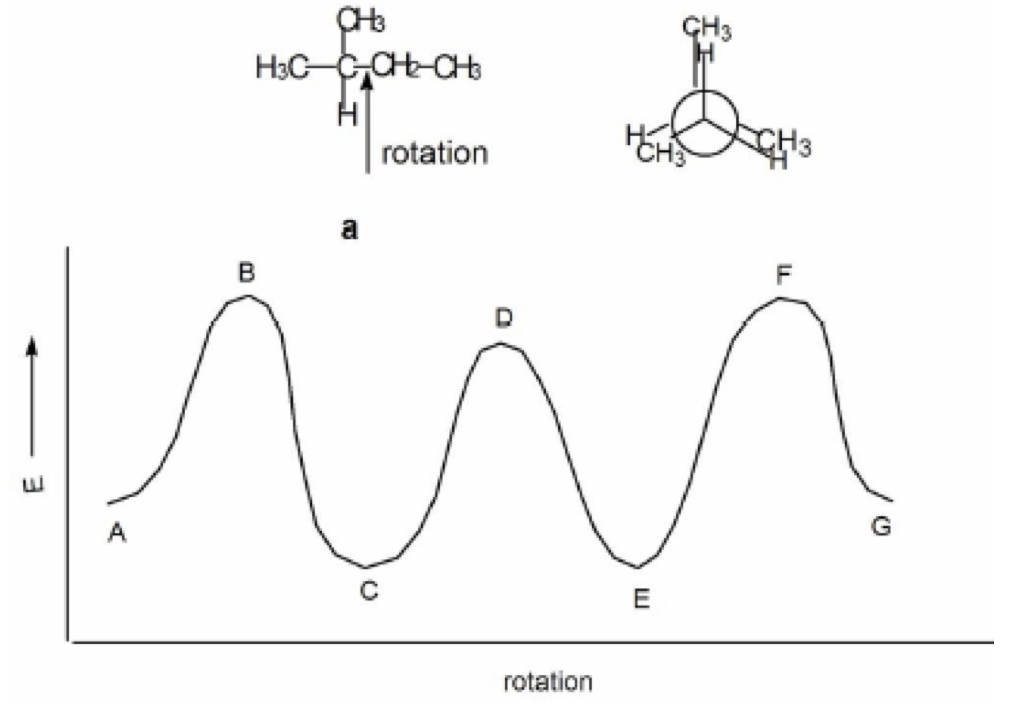
10. Disegnare la proiezione di Newman secondo il legame C2-C3 del conformero più stabile del seguente composto (ANCHE QUESTO ESERCIZIO SARA’ CHIARITO DOMANI A LEZIONE)





































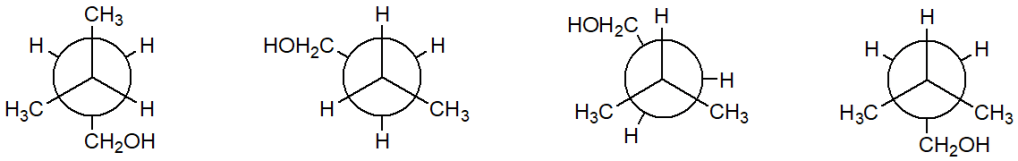






















You must be logged in to post a comment.