Reazioni di addizione elettrofila agli alcheni che prevedono la formazione di intermedi carbocationici

NB: PRIMA di AFFRONTARE GLI ESERCIZI DI QUESTO POST è NECESSARIO AVER STUDIATO E COMPRESO AL FONDO LA PARTE RELATIVA AGLI ASPETTI TERMODINAMICI E CINETICI DELLE REAZIONI, OLTRE AI MECCANISMI DI ADDIZIONE DI HX, ACQUA E ALCOL AD UN ALCHENE (INCLUSI GLI ASPETTI STEREOCHIMICI)
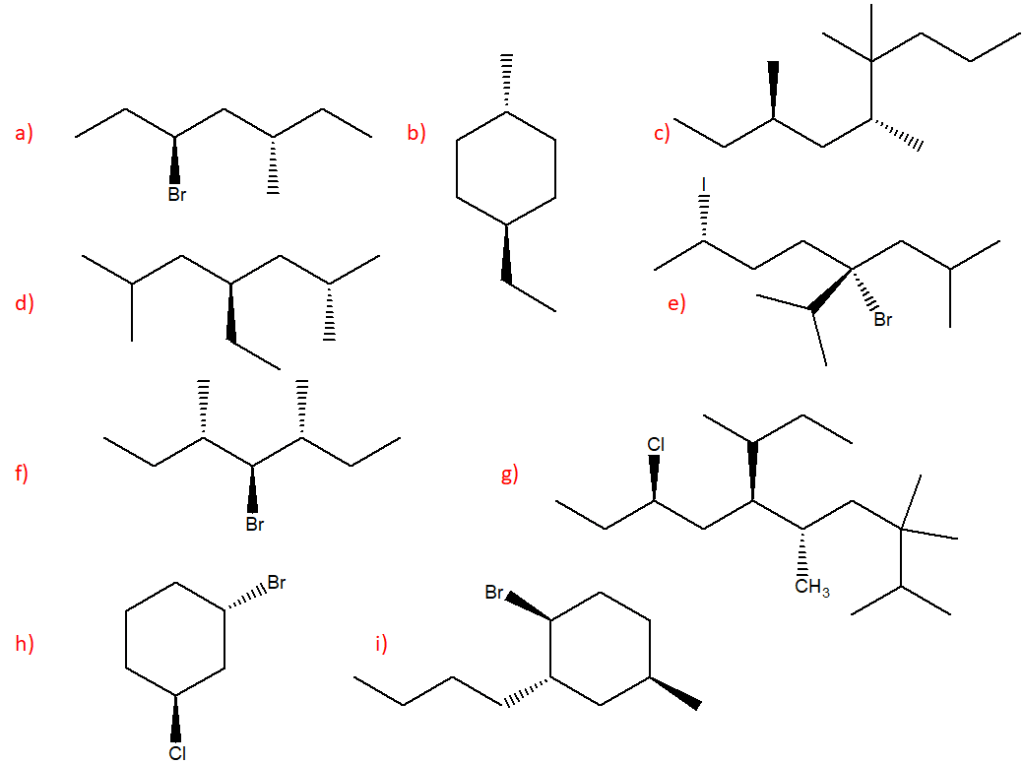
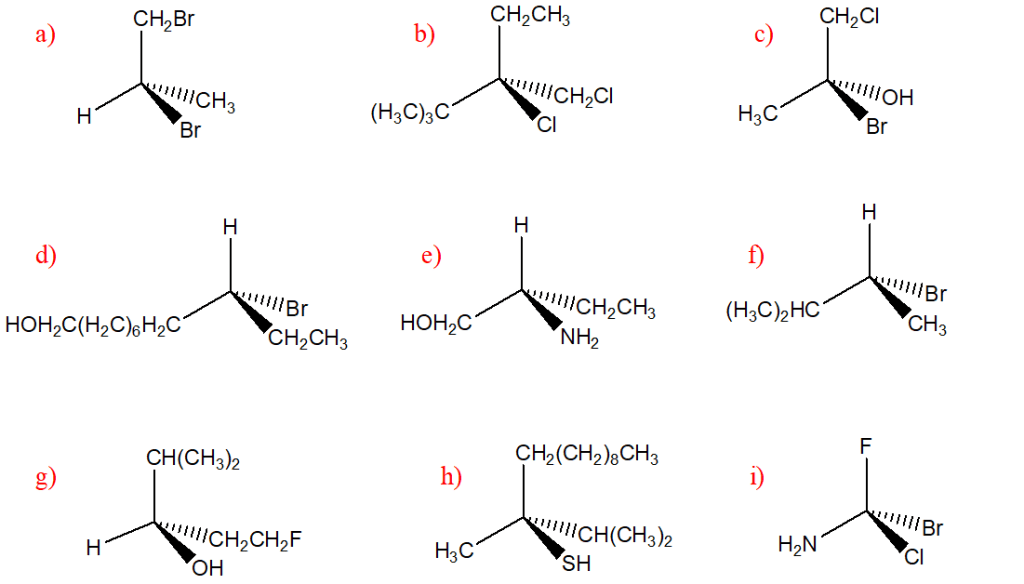
1) Scrivere il meccanismo e il/i prodotto/i (indicando qual è il principale, quando necessario) della reazione dei seguenti composti con HCl. Indicare anche la stereochimica dei prodotti e assegnare il nome IUPAC a ciascuno di essi.
a) 2-metil-2-pentene
b) 2-metil-1-pentene
c) (2E)-4-metil-2-pentene
d) 4-metil-1-pentene
e) (R)-4-metil-1-esene
f) 4-etil-2-esene
g) (2Z)-4,4-dimetil-2-pentene
h) (2E)-4,4-dimetil-2-pentene
i) 1-metil-1-cicloesene
l) (6S)-1,6-dimetilcicloesene
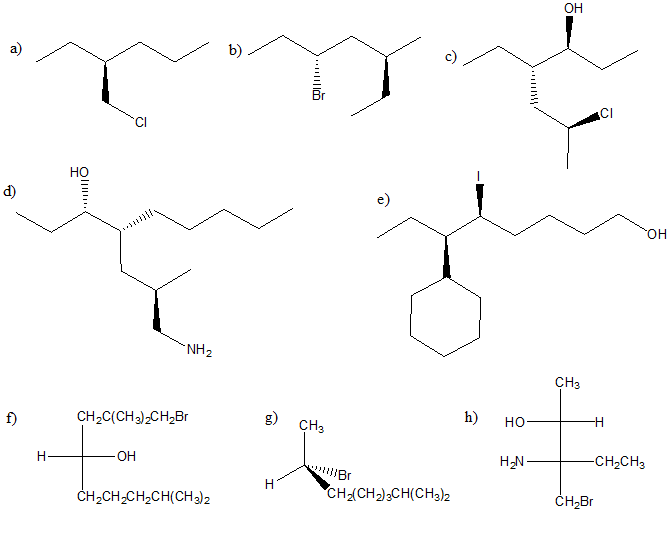
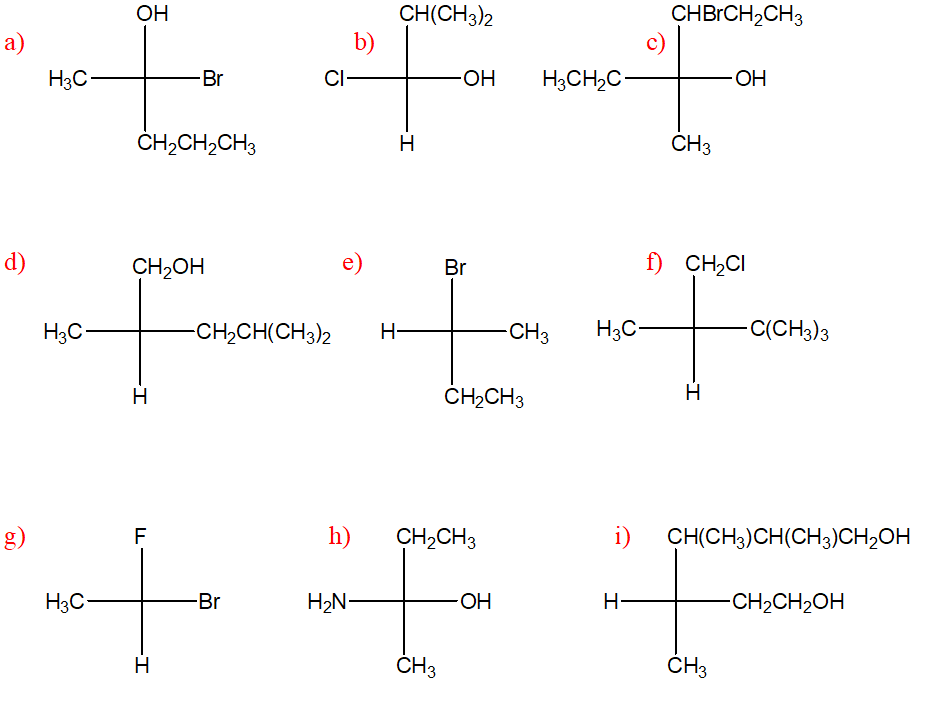
2) Proporre una strategia per la sintesi dei seguenti alogenuri alchilici partendo da un alchene. Quando sono possibili più opzioni, scegliere quella che darà il composto desiderato come prodotto principale o come unico prodotto e argomentare la scelta. Infine, per ogni reazione, indicare la stereochimica dei prodotti.
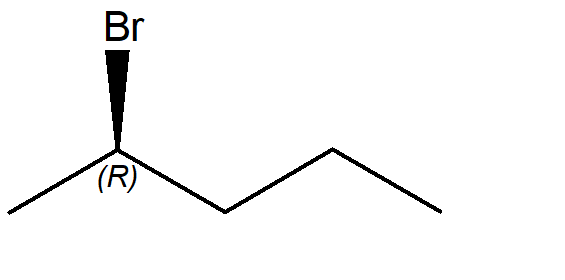
a) 2-cloropentano
b) 2-bromo-2-metilbutano
c) 2-cloro-2,3-dimetilbutano
d) 2-cloro-2,3-dimetilpentano
3) Per le reazioni dell’1-butene e del 2-butene con I) acido bromidrico e II) con acqua in ambiente acido:
1) mostrare i meccanismi;
2) disegnare, per ciascuna reazione, un grafico della variazione dell’energia potenziale rispetto alla coordinata di reazione in cui vengono indicate le strutture dei reagenti, degli stati di transizione, degli intermedi e dei prodotti;
3) se i carbocationi che si formano sono caratterizzati da stabilità differente, dire quali fattori stabilizzano i carbocationi più stabili
4) indicare se le reazioni sono o meno regioselettive (e quando possibile indicare anche il grado di regioselettività).
4) Determinare l’ordine di reattività in una reazione di addizione di acido alogenidrico per i seguenti alcheni: 2-metilpropene; (Z)-2-butene; (E)-2-butene. Motivare la risposta.
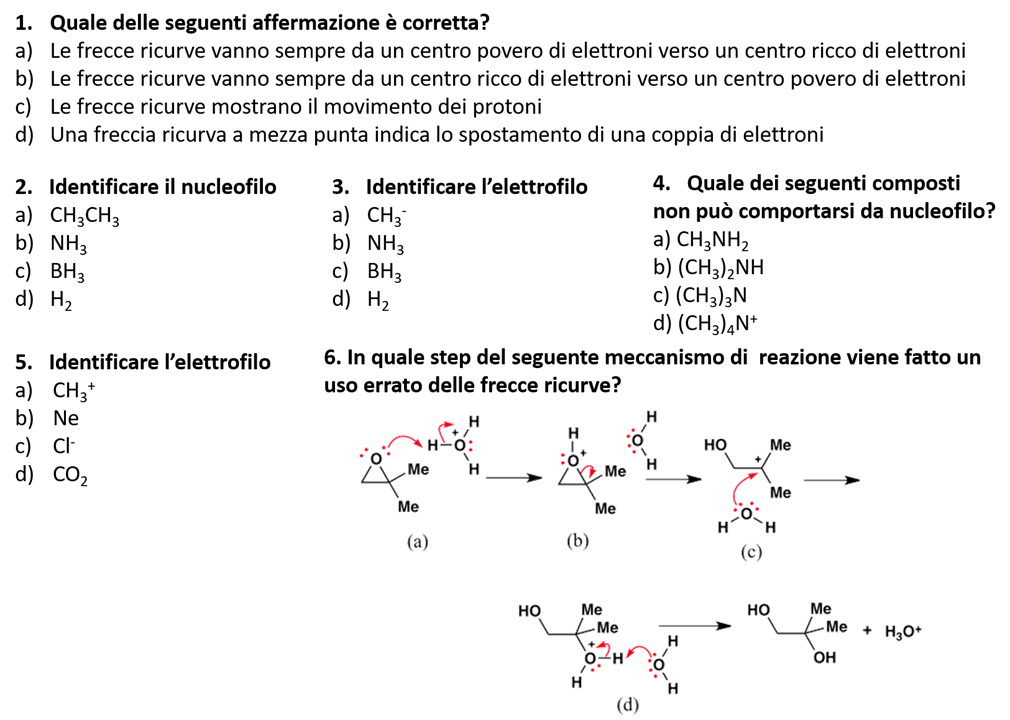
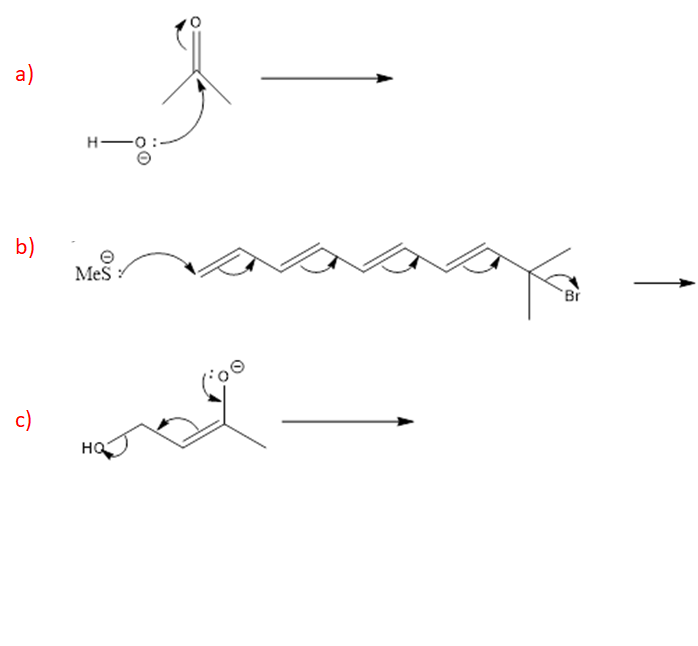
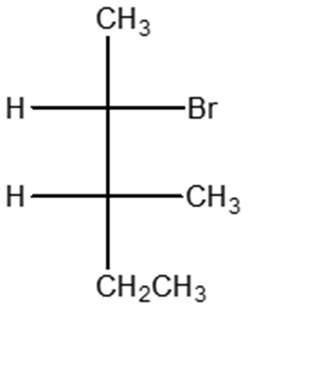
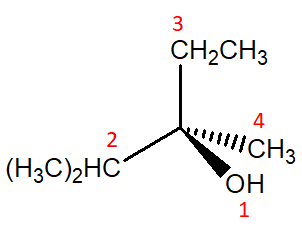
5) I seguenti meccanismi di reazione sono caratterizzati da un certo numero di errori gravissimi. Individuarli e correggerli.

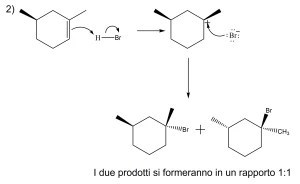
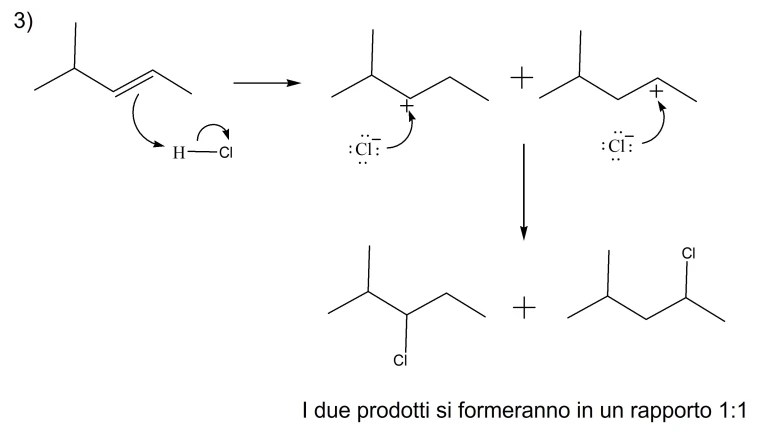
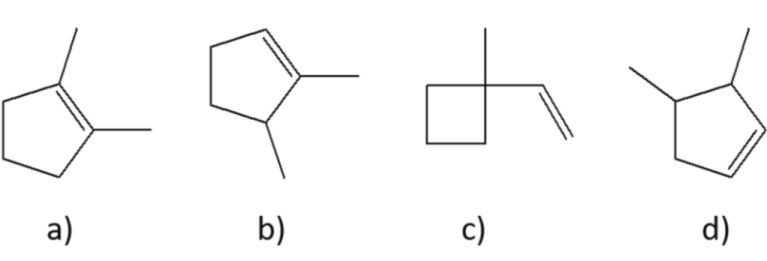
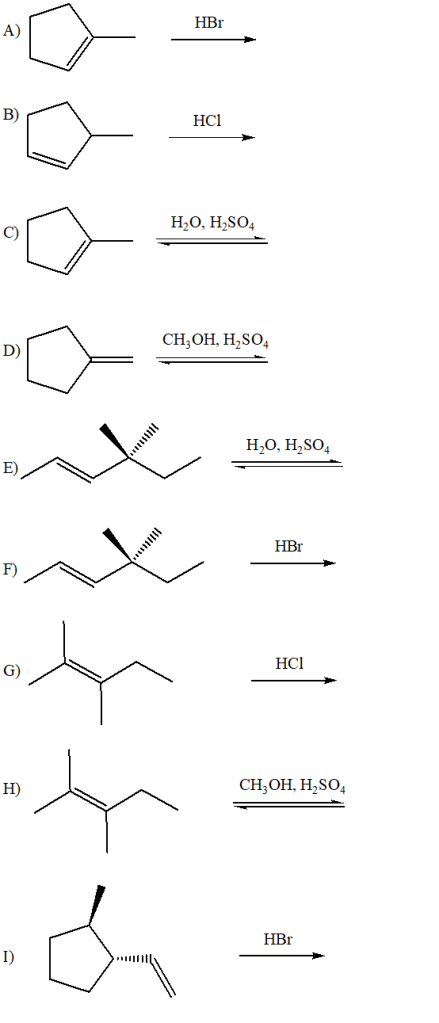
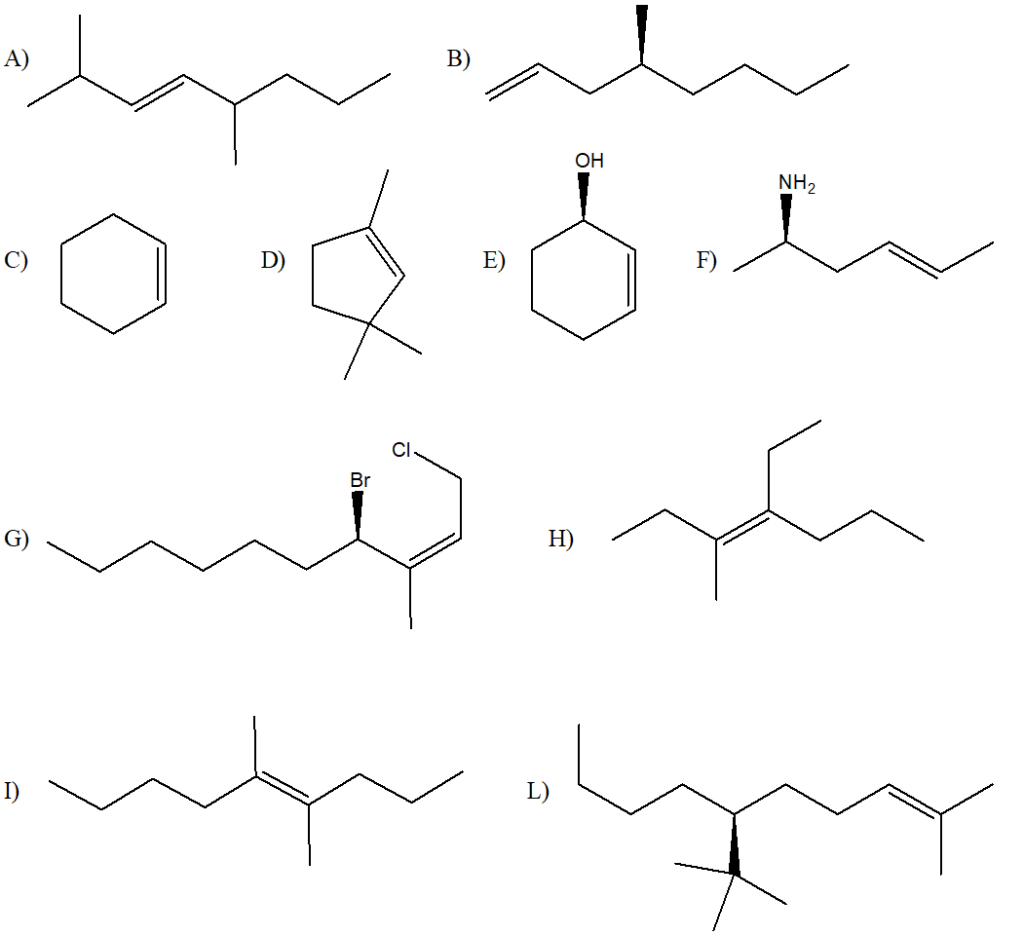
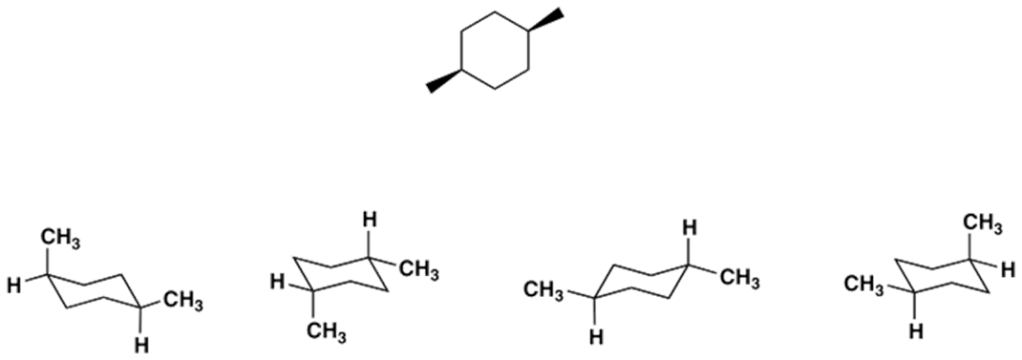
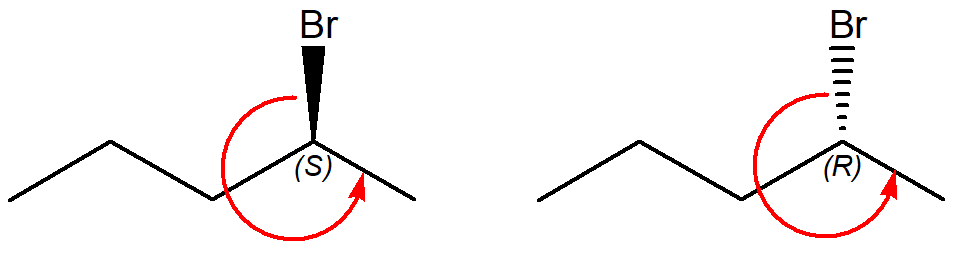
5) Quale/i dei seguenti alcheni darà l’1-bromo-1,2-dimetilciclopentano come prodotto principale della reazione con HBr?
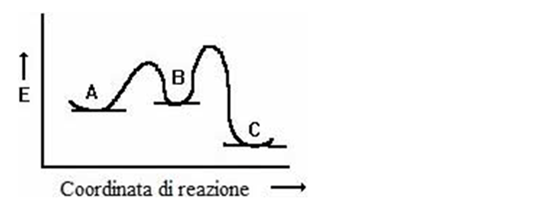
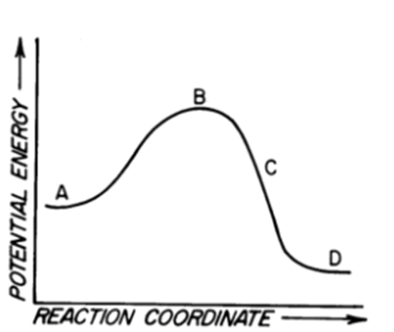
6) La coordinata di reazione qui sotto mostra il profilo energetico della reazione di 3 alcheni diversi con HBr. Identificare alla reazione di quale alchene si riferisce ciascuna curva:

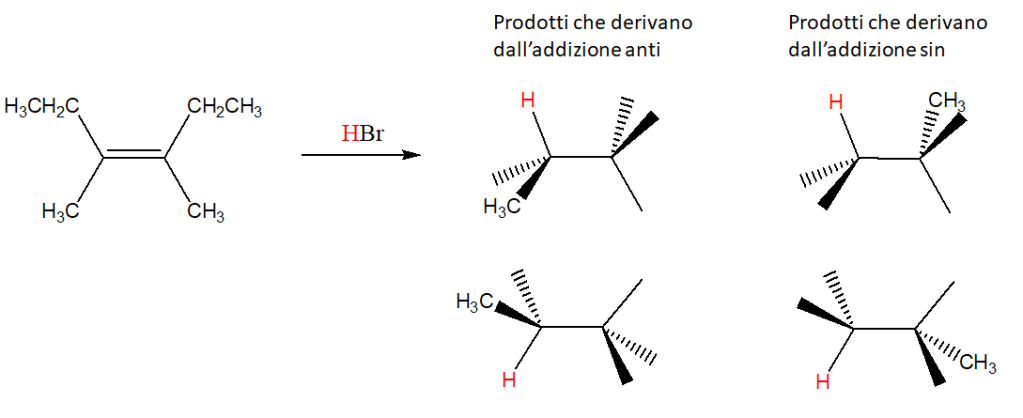
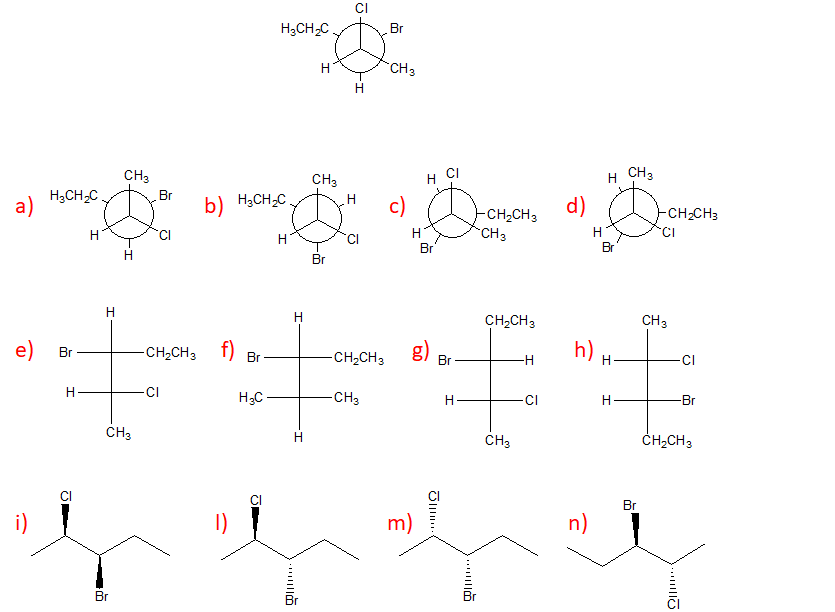
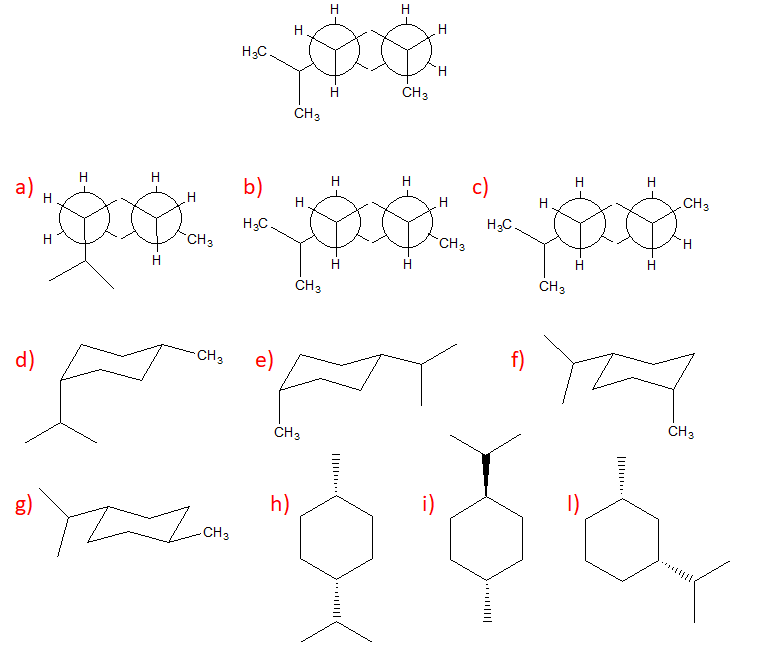
7) Completare i prodotti della seguente reazione, prendendo in considerazione quella che è la posizione relativa dei sostituenti già indicati (attenzione: tutte le strutture dei prodotti sono qui riportate come conformazioni eclissate, anche quelle che derivano dall’addizione sin).
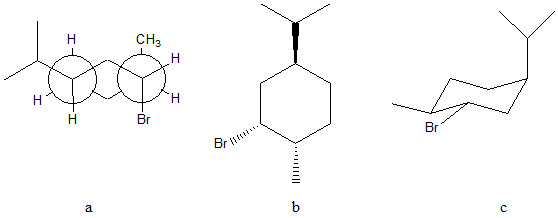
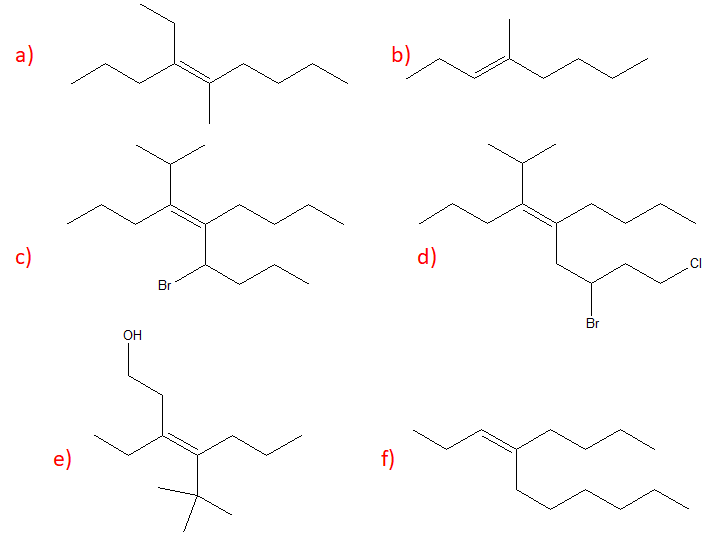
8) Disegnare la formula di struttura dell’alchene di formula molecolare C8H14 che, per reazione con HBr, dà come prodotto principale 1-bromo-1-isopropilciclopentano.
9) Scrivere il meccanismo e il/i prodotto/i principale/i della reazione di idratazione acido-catalizzata dei composti dell’esercizio 1. Indicare anche la stereochimica e assegnare il nome IUPAC a ciascuno dei prodotti.
10.A) Di seguito è mostrato il diagramma energetico della reazione di idratazione acido-catalizzata del 2-butene:
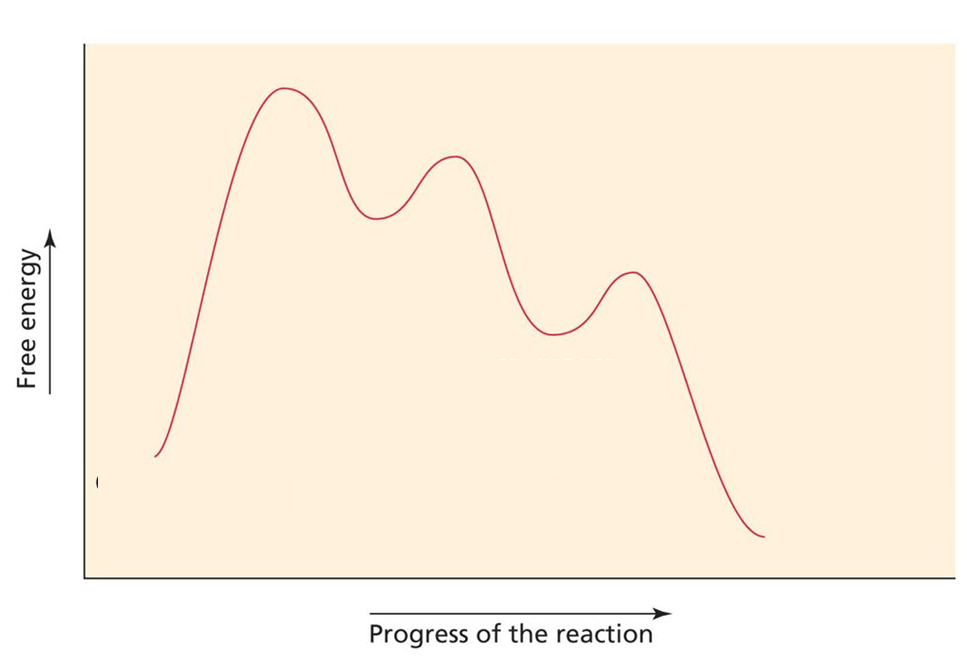
a) Cosa possiamo dire circa il ΔG° della reazione?
b) Cosa possiamo dire circa la Keq della reazione?
c) Di quanti stadi si compone la reazione?
d) Qual è lo stadio cineticamente determinante?
e) Indicare sul grafico l’energia di attivazione relativa a ciascuno stadio
f) Disegnare lo stato di transizione dello stadio cineticamente determinante.
g) Quanti intermedi si formano nel corso della reazione? Disegnarne la/le struttura/e.
10.B) Disegnare il diagramma energetico della reazione del 2-metil-2-butene con HCl e giustificare la regioselettività della reazione.
11) Proporre un metodo per sintetizzare l’1,2-dimetilcicloesanolo a partire dal 3,3-dimetilcicloes-1-ene.
12) Spiegare perché è impossibile sintetizzare il seguente etere utilizzando la reazione tra un alchene e un alcol:

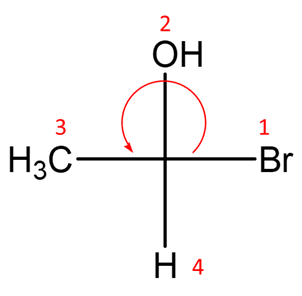
13) Spiegare perchè il prodotto della reazione di idratazione acido-catalizzata del (4R)-4-metil-1-esene ruota il piano della luce polarizzata
14) Mostrare il meccanismo e i prodotti delle seguenti reazioni. Nel caso, indicare il/i prodotti principali. Indicare la stereochimica e attribuire il nome IUPAC a tutti i prodotti.
15) Proporre un meccanismo per le seguenti trasformazioni

16) Indicare le condizioni di reazione e proporre un meccanismo per le seguenti trasformazioni
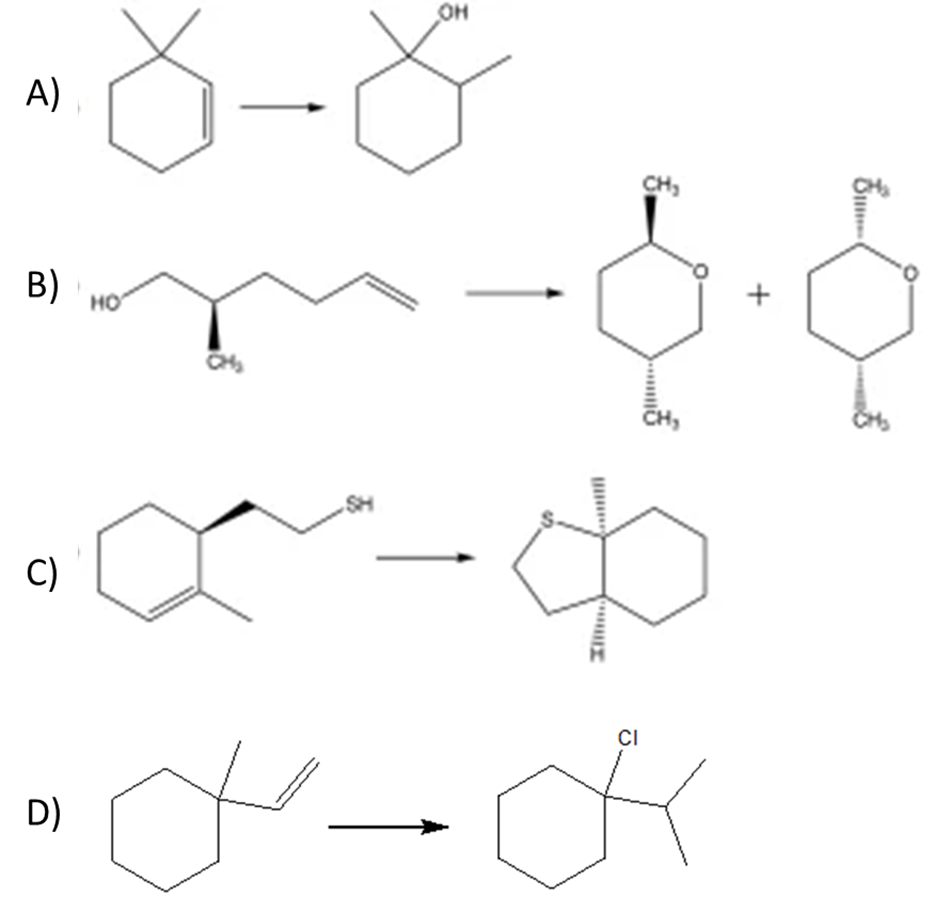
12) Mostrare il meccanismo della seguente trasformazione:



























































You must be logged in to post a comment.