Esercitazione su reazioni di sostituzione ed eliminazione di vari composti organici

1) Disegnare la formula di struttura per il prodotto di ogni reazione SN2.
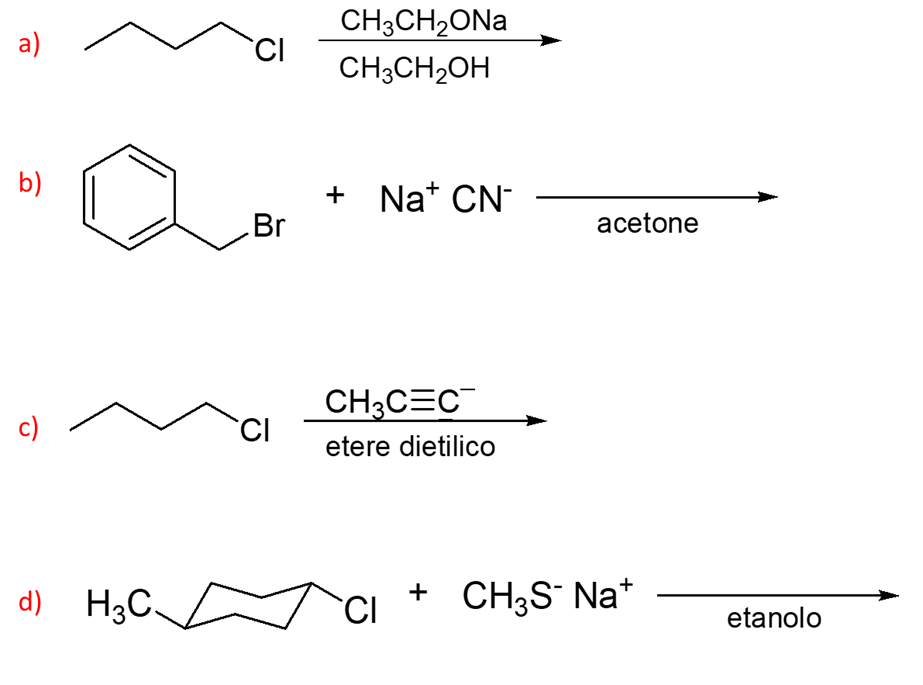
2) Disegnare la formula di struttura per il prodotto di ogni reazione SN1 (se avviene).

3) L’1-cloro-2-butene in acqua dà una miscela di 2-buten-1-olo e 3-buten-2-olo (racemo). Proporre un meccanismo che spieghi la loro formazione.
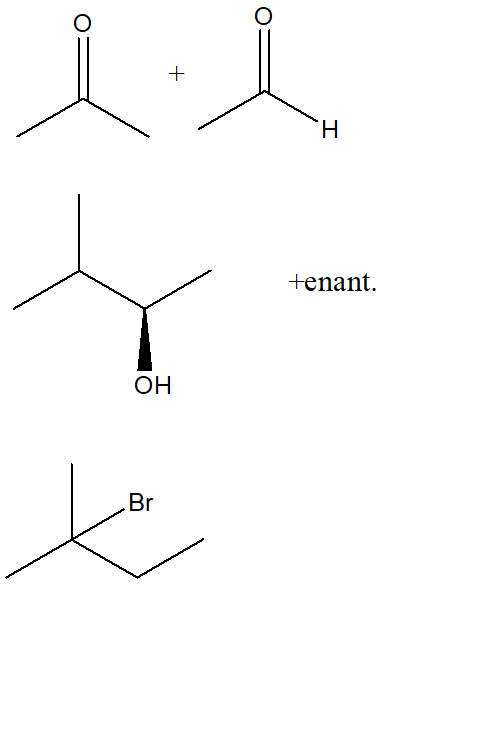
4) Indicare come si potrebbero sintetizzare i seguenti composti a partire da un alogenuro alchilico e da un nucleofilo.

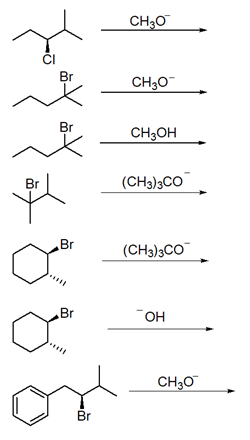
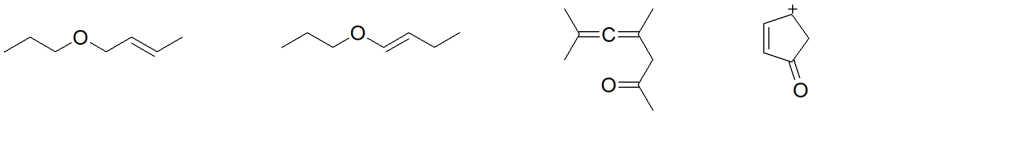
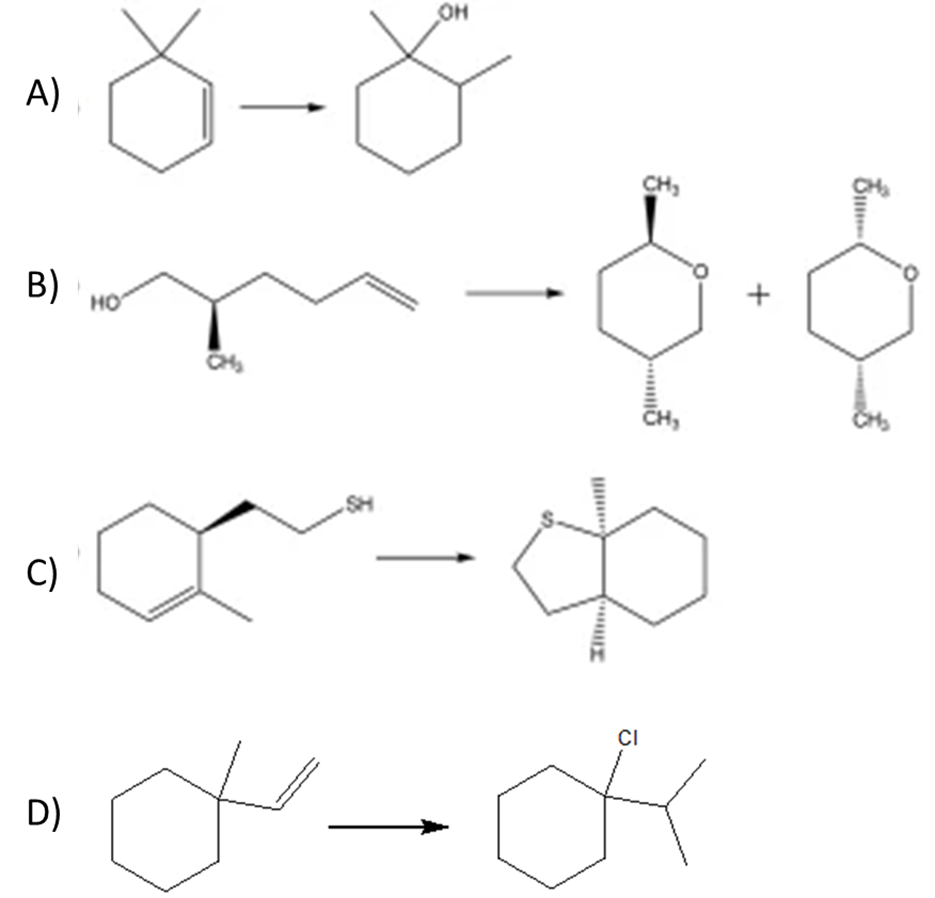
5) Scrivere il prodotto principale delle seguenti reazioni:
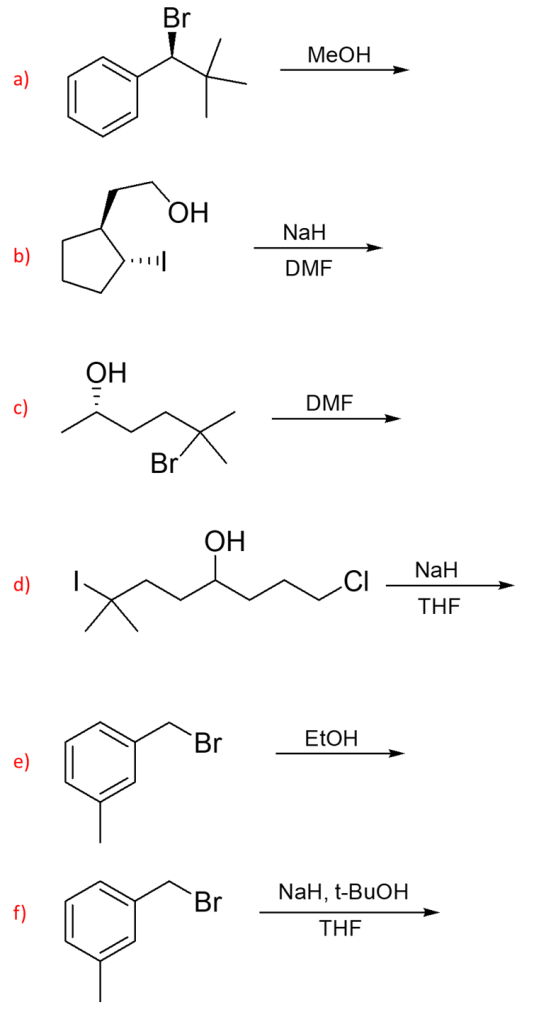
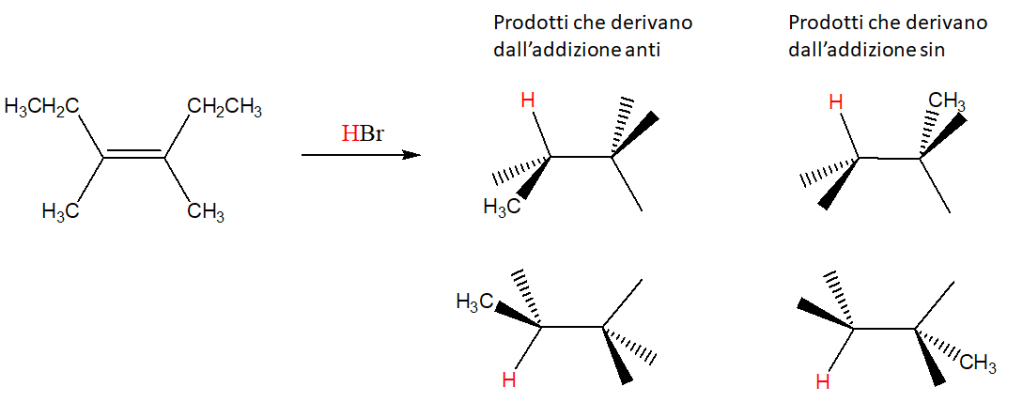
6) Scrivere un meccanismo di reazione che spieghi le seguenti trasformazioni. Motivare la formazione dei prodotti mostrati in a e b come prodotti principali delle reazioni in questione.

7) Scrivere la struttura e il nome IUPAC di tutti i possibili prodotti ottenuti dalla reazione E2 del (3R)-3-bromo-3-metilottano
8) Scrivere i prodotti delle seguenti reazioni E2 (se avvengono) ed indicare, in caso di formazione di più prodotti, quale sarà quello principale

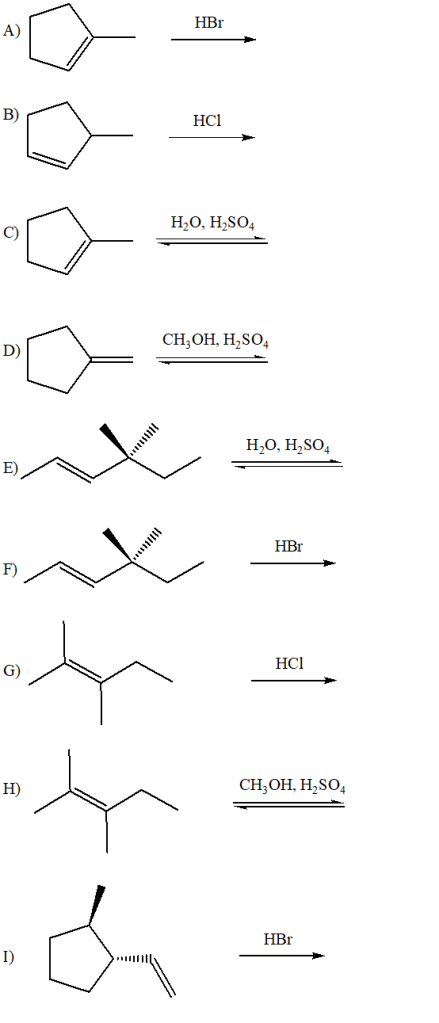
9) Scrivere i prodotti principali delle seguenti reazioni:

10) La velocità della seguente reazione è 1000 volte maggiore in DMSO che in metanolo. Spiegare questa differenza di velocità:

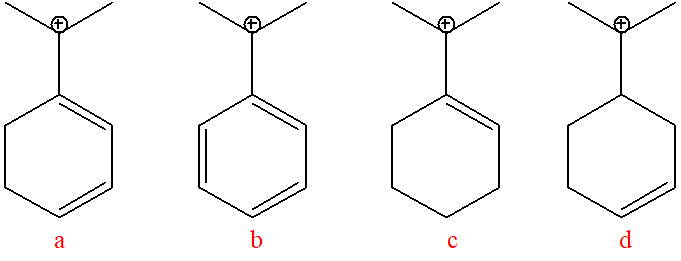
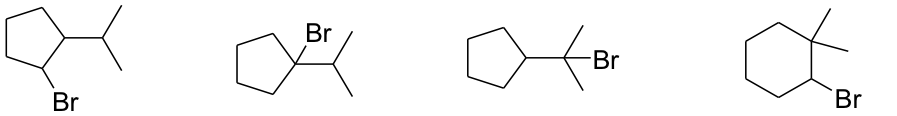
11) Scegliere quale membro di ciascuna coppia reagisce più velocemente in una reazione SN1?
a) 1-clorobutano o 2-cloro-2-metilpropano
b) 2-cloro-2-metilpropano o 2-bromo-2-metilpropano
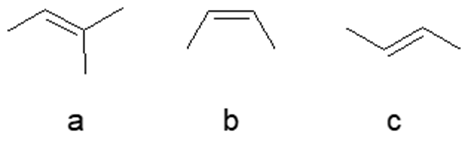
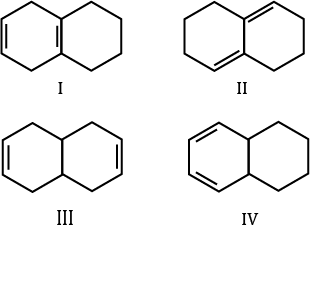
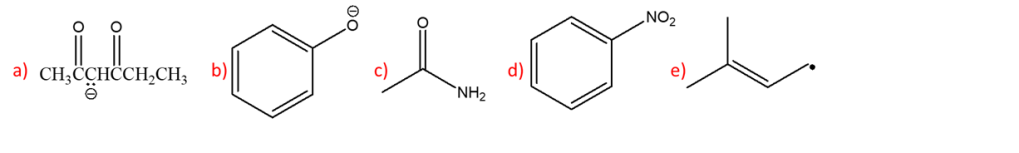
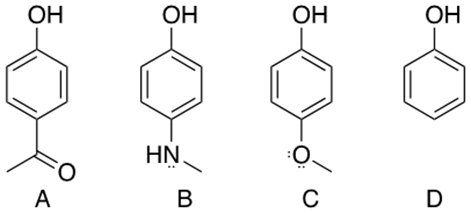
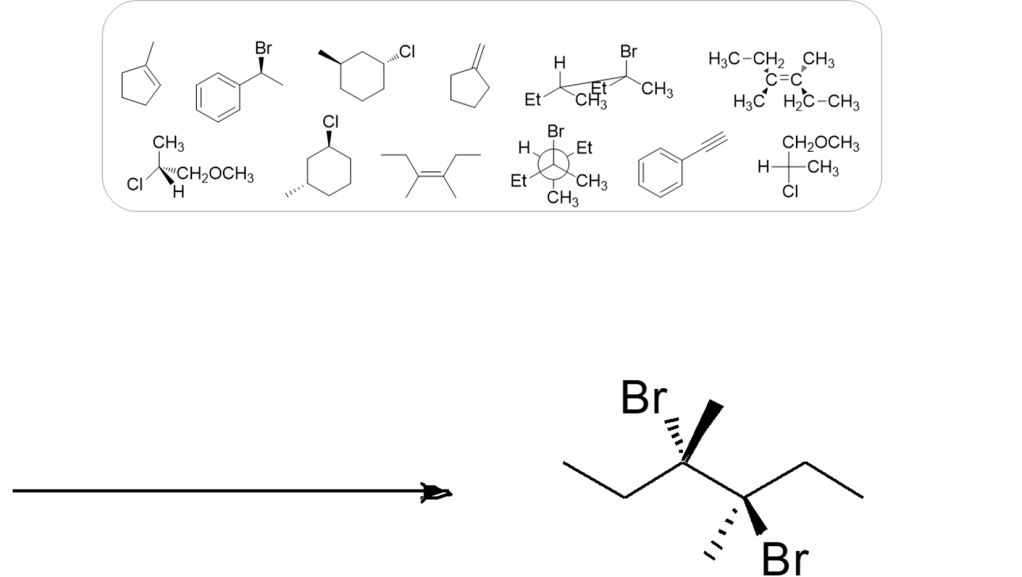
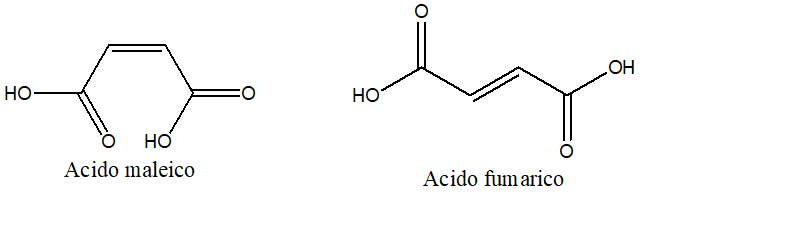
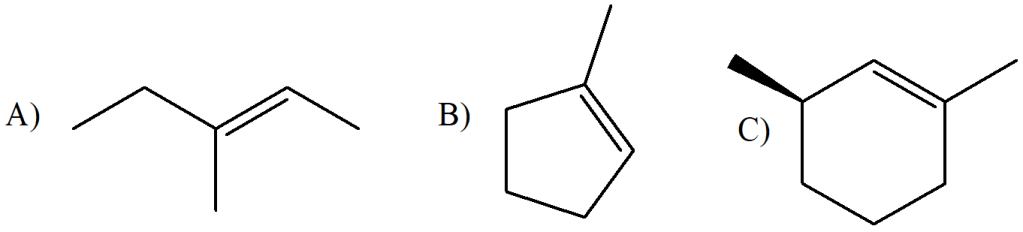
12) Ordinare secondo reattività descrescente in eliminazione E2 i seguenti composti:
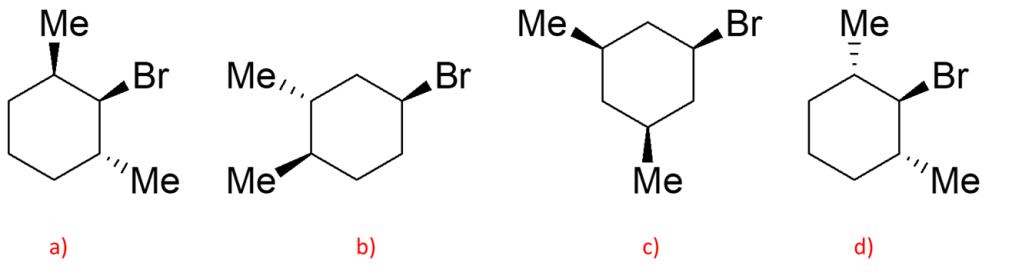
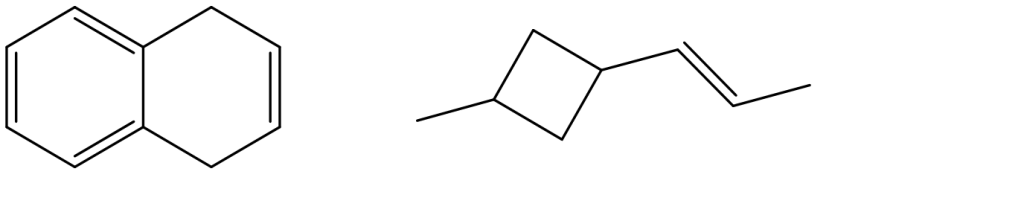
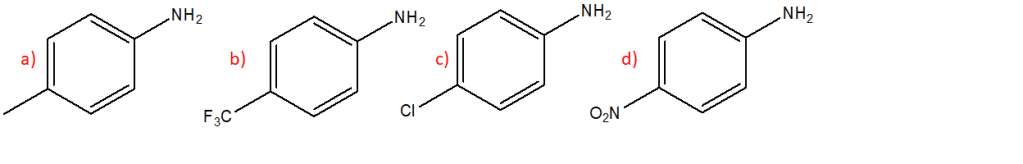
13) Quale dei seguenti composti reagirà più velocemente in una E2?

14) Il diastereoisomero A del (+)-2-cloro-3-metilpentano e il diastereoisometo B del (-)-2-cloro-3-metilpentano reagiscono in una reazione E2 quando scaldati in piridina. A darà come prodotti (2E)-3-metil- 2-pentene e (3S)-3-metil-1-pentene; B darà come prodotti (2Z)-3-metil- 2-pentene e (3S)-3-metil-1-pentene.
a) Proporre la struttura di A e B
b) spiegare perchè A converte stereoselettivamente nell’alchene E, e B nell’alchene Z
c) quale alchene è il prodotto maggioritario della reazione?
15) Scrivere il prodotto principale delle seguenti reazioni, specificando il meccanismo più probabile per la sua formazione
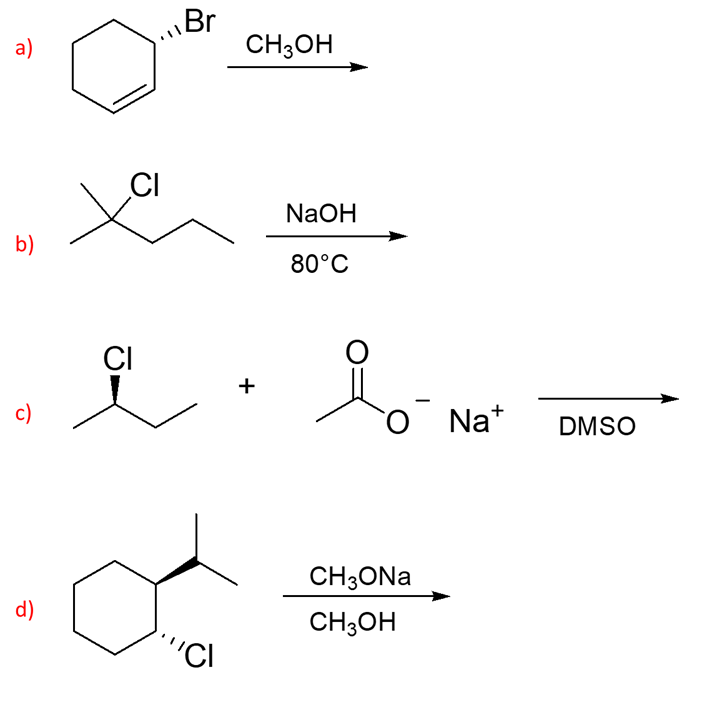
16) La reazione del composto mostrato in figura con una base forte, come il metossido di sodio, non produce come prodotti di eliminazione cicloseni sostituiti in quantità apprezzabile. D’altra parte, la solvolisi in metanolo dà una miscela di prodotti, incluso il cicloesene sostituito. Spiegare queste osservazioni.

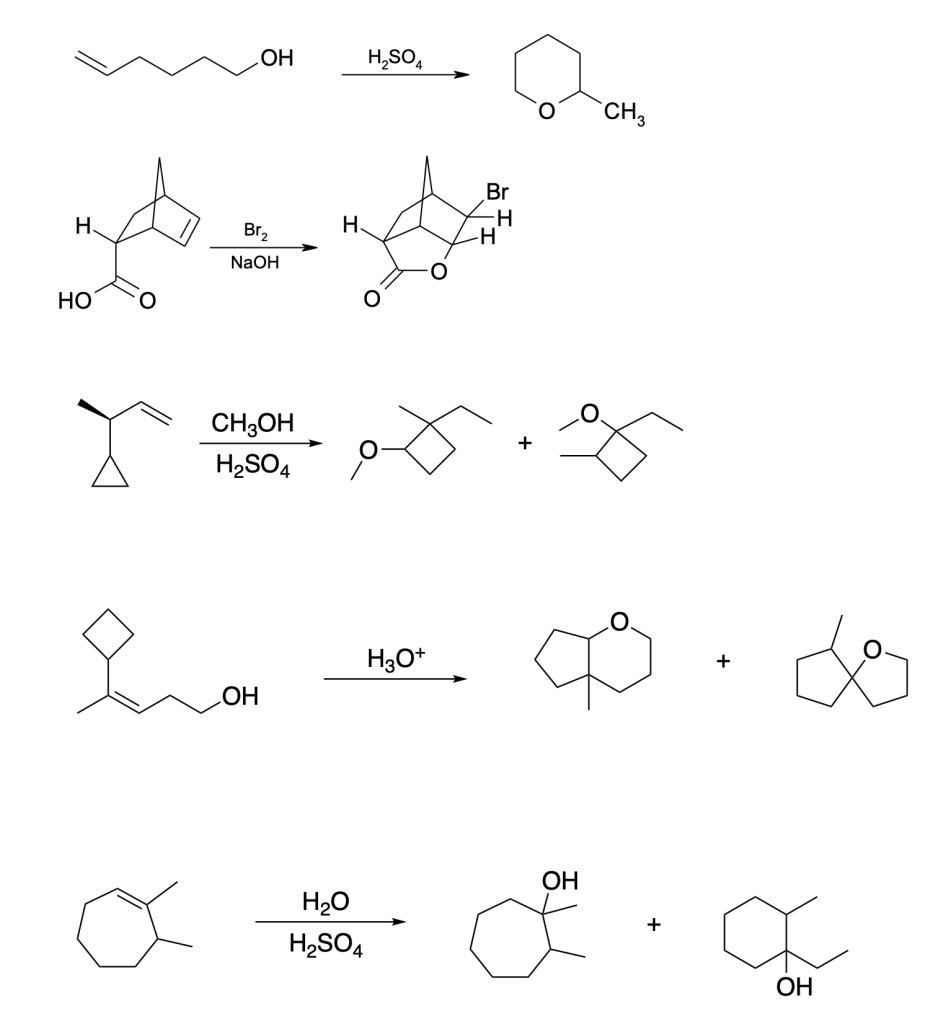
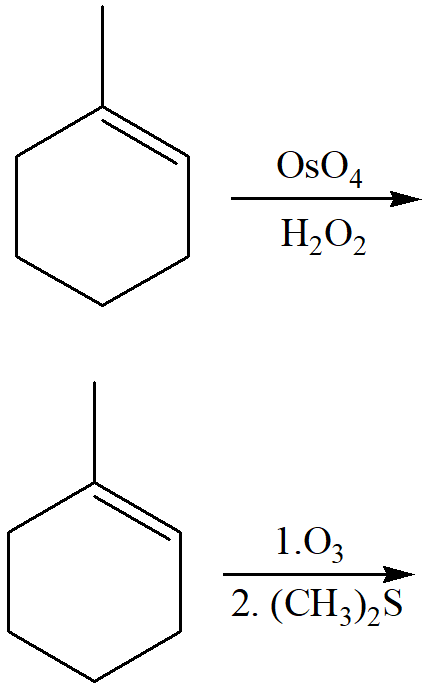
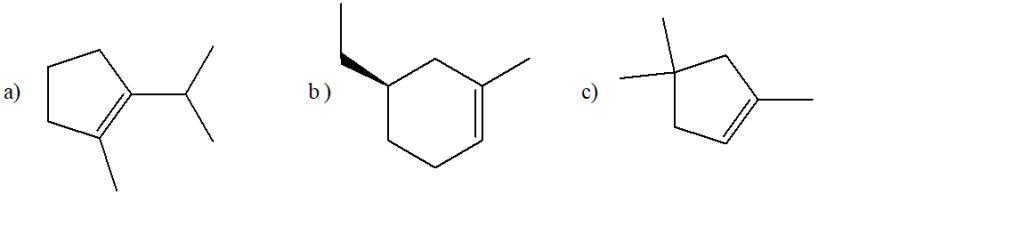
17) Scrivere i prodotti principali delle seguenti reazioni:

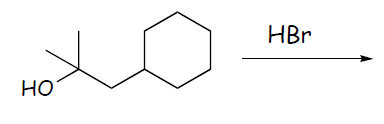
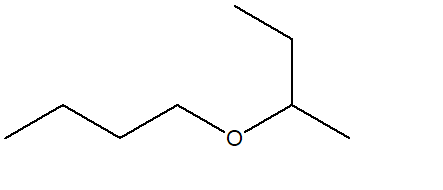
18) Scrivere i prodotti ottenuti trattando il seguente composto con acido solforico a caldo

19) La disidratazione acido-catalizzata del 2-metilciclopentanolo fornisce tre alcheni: 3-metilciclopentene, 1-metilciclopentene e metilenciclopentano. Proporre un meccanismo che ne spieghi la formazione e dire quale sarà il prodotto principale.
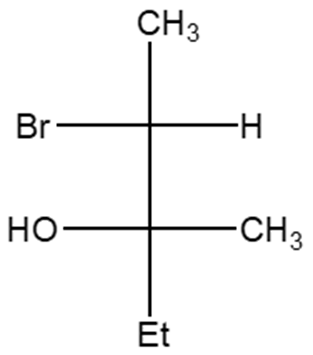
20) Per il 3-bromo-2-butanolo esistono due coppie di enantiomeri [A (R,R) e B (S,S); C (R,S) e D (S,R)], diastereoisomere tra loro. Quando uno tra gli enantiomeri A o B viene trattato con HBr si ottiene solo il 2,3-dibromobutano racemo, senza traccia dell’isomero meso. Quando l’enantiomero C o D viene trattato con HBr si ottiene il 2,3-dibromobutano meso, senza traccia del 2,3-dibromobutano racemo. Giustificare queste osservazioni sperimentali.
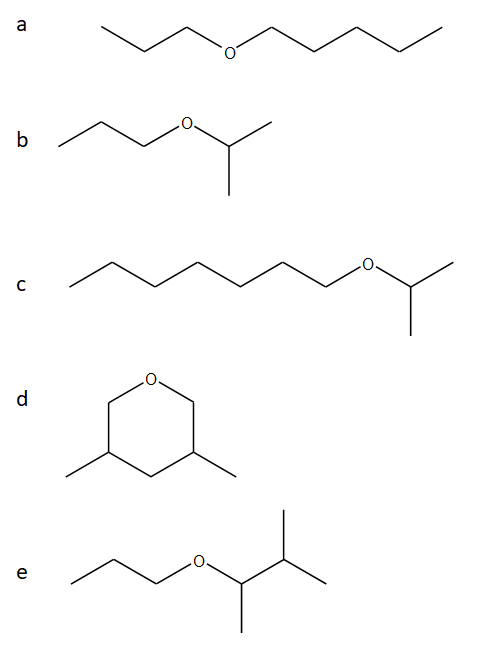
21) Disegnare le formule di struttura dei prodotti che si formano per trattamento dei seguenti composti con HI a caldo

22) Mostrare i meccanismi delle reazioni dell’esercizio 21
23) Come potrsti sintetizzare i composti dell’esercizio 21 mediante sintesi di Willliamson? Mostrare condizioni e meccanismo di reazione.
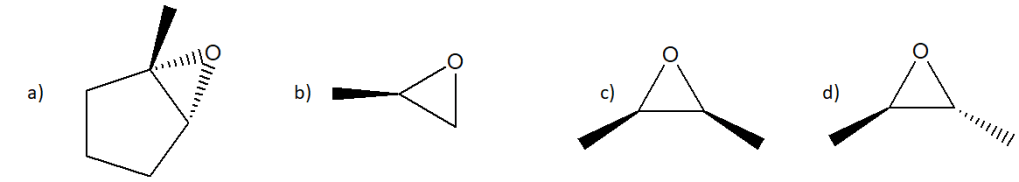
24) Prevedere la struttura del prodotto principale ottenuto nella reazione del 2-etilossirano con ciascuno dei seguenti reagenti:
a) acqua/ambiente acido
b) soluzione acquosa di idrossido di sodio
c) 
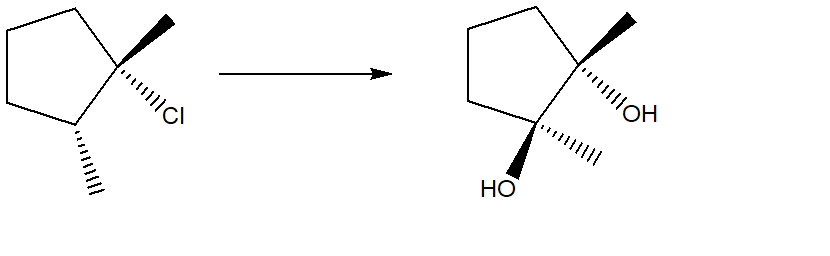
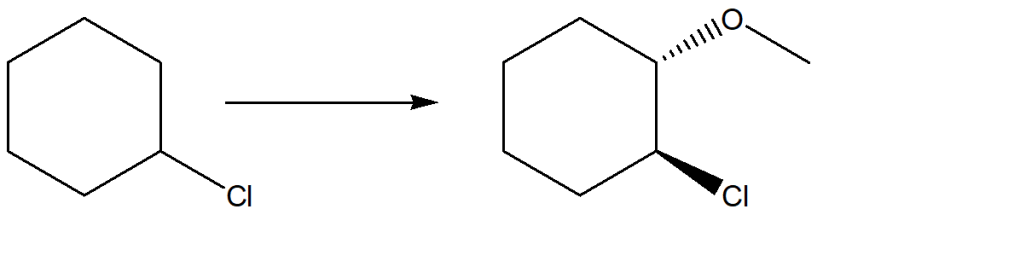
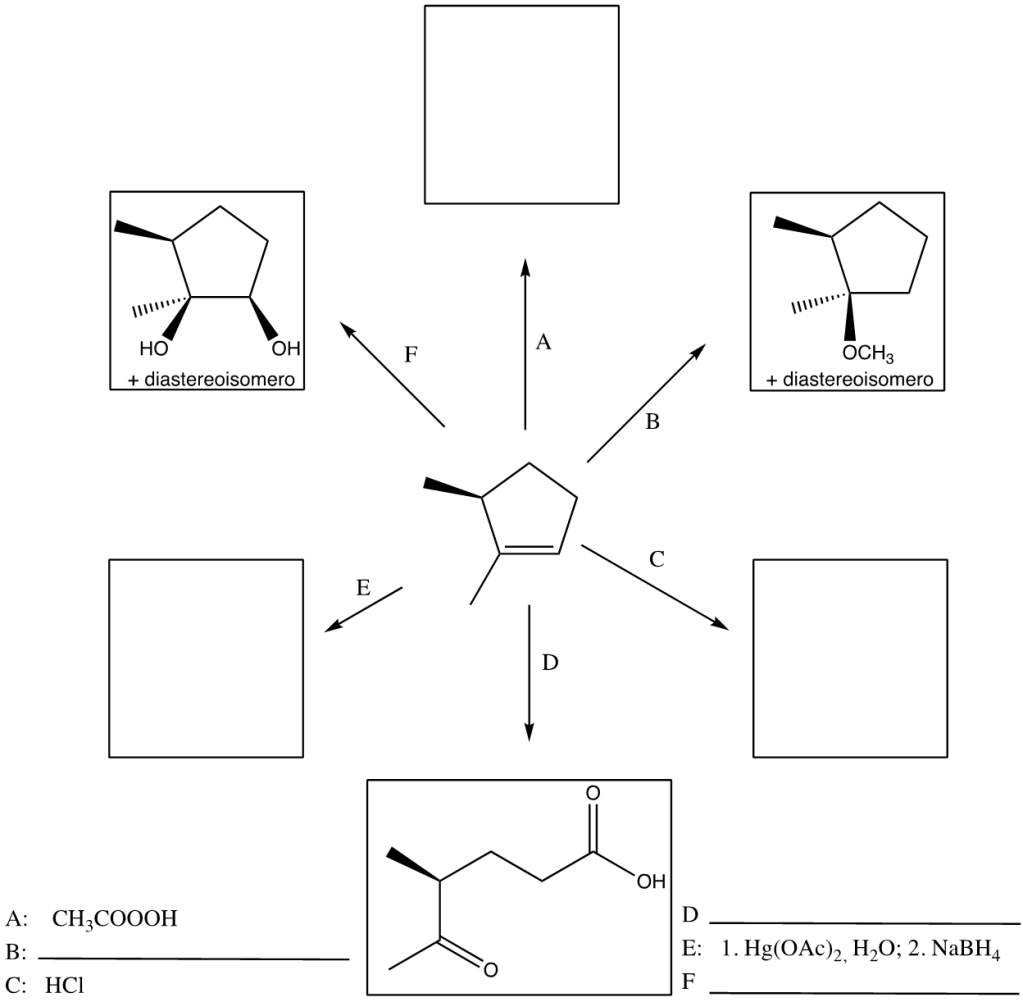
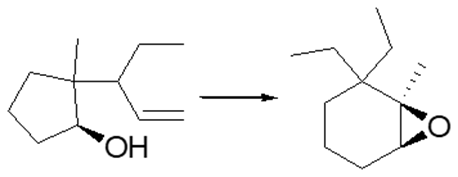
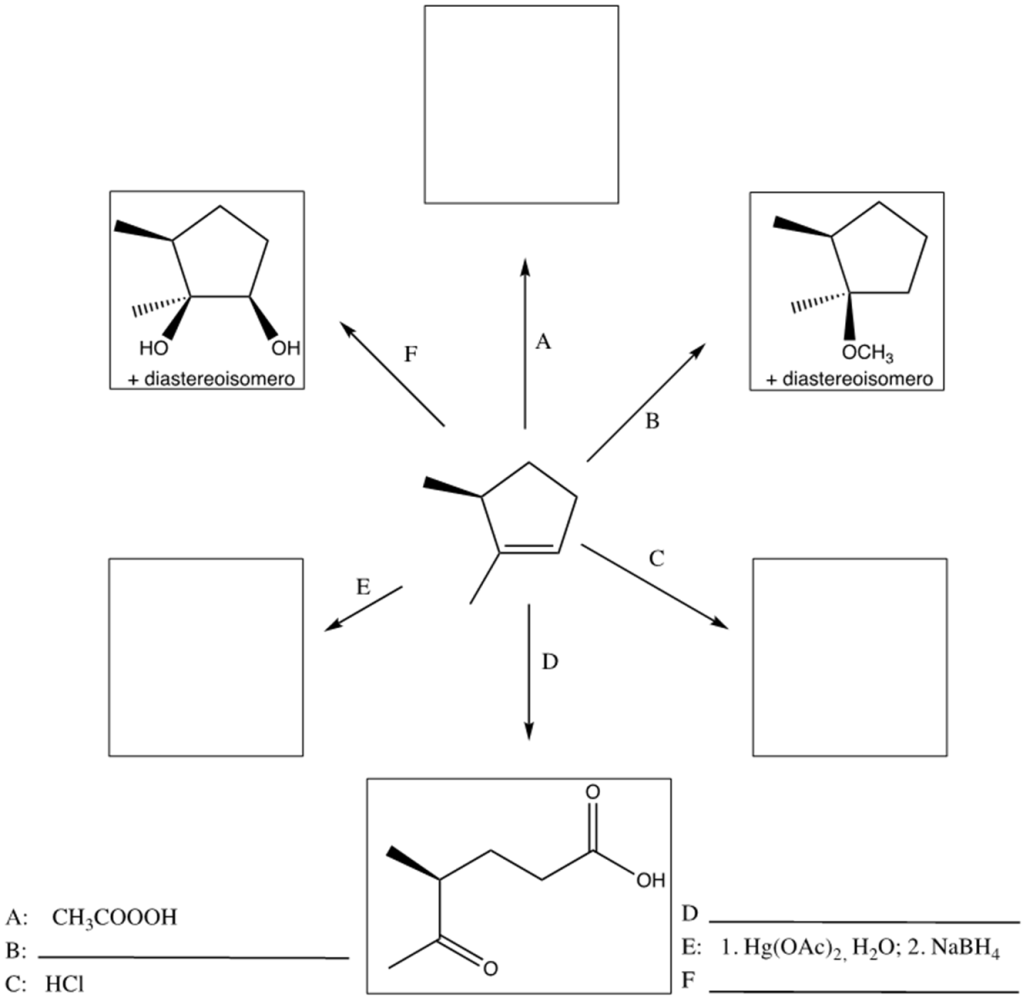
25) Completare il seguente schema
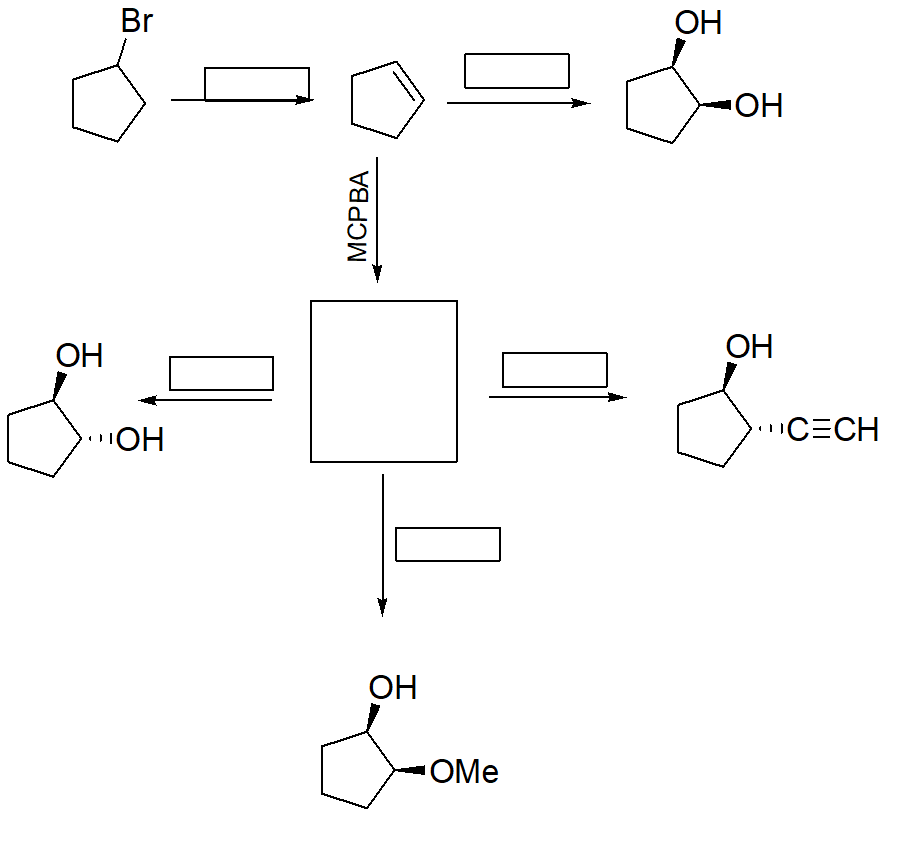
Errata corrige: il metossile è su un cuneo tratteggiato
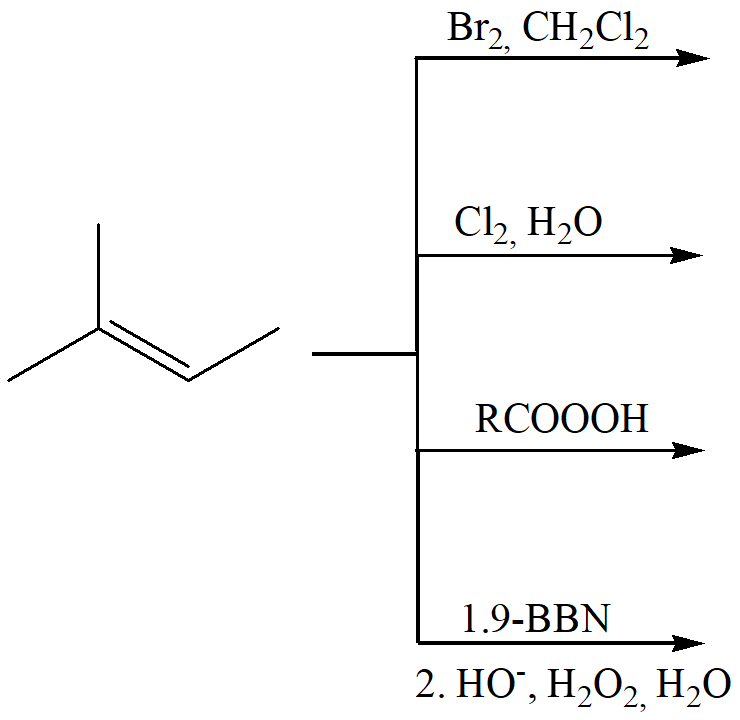
26) Completare il seguente schema

27) Completare il seguente schema

Errata corrige: L’epossido che porta ai dioli in basso è quello che deriva dall’alchene che è il prodotto minoritario della reazione di disidratazione
28) Scrivere i meccanismi delle reazioni degli esercizi 25-27, prendendo in considerazione anche la formazione di eventuali altri prodotti non riportati negli schemi id reazione.
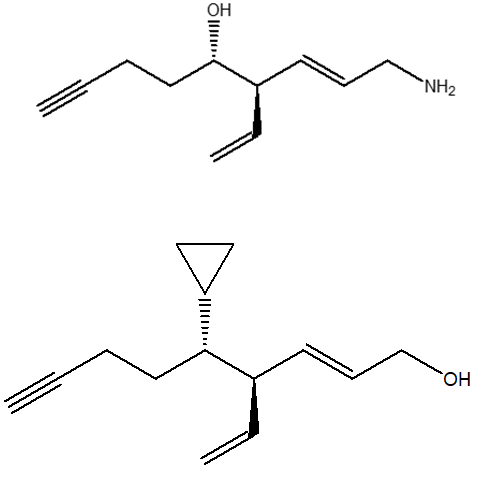
29) Mostrare come è possibile ottenere le seguenti trasformazioni (indicare le condizioni di reazione e mostrare il meccanismo). In alcuni casi potrebbero essere necessari più passaggi.
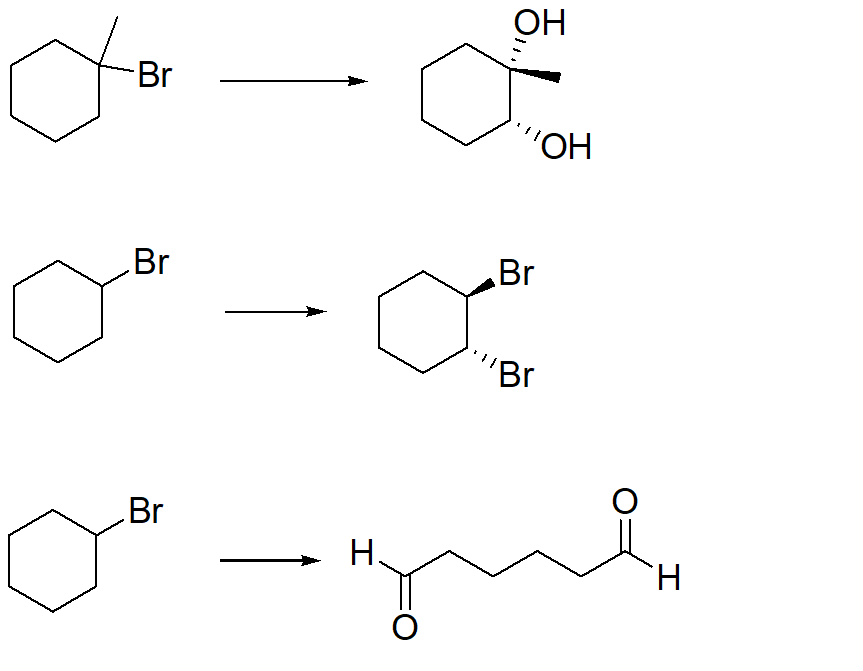
30) Come sintetizzeresti l’1-isobutossi-2-metilpropano utilizzando solo 1-bromo-2-metilpropano come fonte di atomi di carbonio?
Sigle utilizzate
DMF= Dimetilformammide
DMSO= Dimetilsolfossido
THF= tetraidrofurano
Et=etile
Me=metile
t-Bu=terz-butile























































You must be logged in to post a comment.