Esercizi di Riscaldamento

Qui troverete qualche esercizio che, insieme al test di ingresso, può essere utile per rivedere la Chimica generale

Altri esercizi saranno pubblicati nel weekend…
Università degli Studi della Campania "Luigi Vanvitelli"

Qui troverete qualche esercizio che, insieme al test di ingresso, può essere utile per rivedere la Chimica generale

Altri esercizi saranno pubblicati nel weekend…
I risultati del test di ingresso possono essere consultati seguendo il link condiviso sulla pagina del corso:

AULE CORSO
Il lunedì e il mercoledì le lezioni si terranno in AULA A3
Il venerdì in AULA A1

Simboli di Lewis e Strutture di Lewis: DOWNLOAD (NB: il file è protetto da password. Tutti gli studenti regolarmente registrati riceveranno la password via e-mail*).
* si fa riferimento alla mail al dominio studenti.unicampania.it
Come formulare la struttura di Lewis di una specie poliatomica
Fase 1: Contiamo il numero totale degli elettroni di valenza degli atomi che compongono la specie poliatomica. Nel caso di ioni, aggiungere 1 per ogni carica negativa e sottrarre 1 per ogni carica positiva.
Dividendo il numero totale degli elettroni di valenza per due otteniamo il numero delle coppie di elettroni.
Fase 2: Scriviamo i simboli chimici mostrandone la disposizione.
Come scegliere l’atomo centrale? L’atomo centrale è di solito quello meno elettronegativo (o quello dell’elemento dotato della minore energia di ionizzazione). Nelle formule chimiche semplici l’atomo centrale si trova spesso scritto per primo. L’H è sempre un atomo terminale. Se il composto in esame è un ossiacido, gli atomi di H sono legati a quelli dell’O.
Disporre gli atomi simmetricamente intorno a quello centrale.
Fase 3: Collochiamo una coppia di elettroni tra gli atomi di ciascuna coppia.
Fase 4: Completiamo l’ottetto (il doppietto nel caso dell’H) di ciascun atomo collocando tutte le coppie residue intorno agli atomi. Se le coppie di elettroni non sono sufficienti per formare l’ottetto di tutti gli atomi, riordiniamo gli elettroni per formare doppi o tripli legami
Calcolo della carica formale
Carica formale= V- (L+1/2 S)
dove
V= numero di elettroni di valenza
L=numero di elettroni presenti come coppie solitarie
S= numero di elettroni condivisi
Fonte: Principi di Chimica, Atkins e Jones
NB: per una versione più completa e per vari esempi consultare i testi di riferimento sia per la chimica generale sia per la chimica organica (o scaricare il file al link riportato in alto).
Di seguito delle risorse online per esercitarci:
Construct a Lewis Structure: scegliendo un composto dal menù a sinistra è possibile esercitarsi a completare le strutture di Lewis. In basso a destra c’è una tabella che ci aiuta col conteggio degli elettroni.
Lewis structure tutorials: esercitiamoci a formulare le strutture di Lewis delle specie poliatomiche in tabella. Cliccando su ogni singola specie è possibile guardare un video esplicativo.
Lewis dot structures: una serie di esercizi. Cliccando su “answers” sarà possibile visualizzare le risposte.

Come anticipato a lezione, tutti coloro che hanno intenzione di seguire il corso (e che quindi hanno compilato il form di inizio corso) dovranno compilare un secondo form che si chiuderà domenica 2/10 alle 18:00. Il link è presente anche sulla pagina dedicata al corso:


Le Lezioni del II anno del CdL Scienze Biologiche si terranno in AULA A1

Tutti gli studenti del II anno dovranno compilare il test! Vi ricordo che il forms si aprirà alle 11:00 e che avrete 1 ora di tempo. Alle 12:00 il form si chiuderà e non sarà più possibile inviare le risposte!
Trovate il link alla pagina: https://chimicaorganicadistabif.com/blog/scienze-biologiche/chimica-organica/

Come fare per essere sempre aggiornati sui nostri contenuti?
–> Segui il blog! Come? Vai a fondo pagina e segui le istruzioni.
Vuoi aggiornamenti ancora più immediati? Segui le nostre pagine Facebook e Instagram (segui questi link o i link a fondo pagina)!

Il link per la prenotazione del ricevimento sarà attivo solo dopo l’inizio del corso.
Gli studenti che hanno necessità di prenotare il ricevimento prima del 26/09/2022 potranno farlo ESCLUSIVAMENTE inviando una mail alla docente (monica.scognamiglio@unicampania.it ).
Si comunica, inotre, che il canale preferenziale di comunicazione con la docente a partire da questo mese è l’e-mail. Si invitano quindi gli studenti ad utilizzare questo canale anzichè la chat di Teams.

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, al seguente composto:
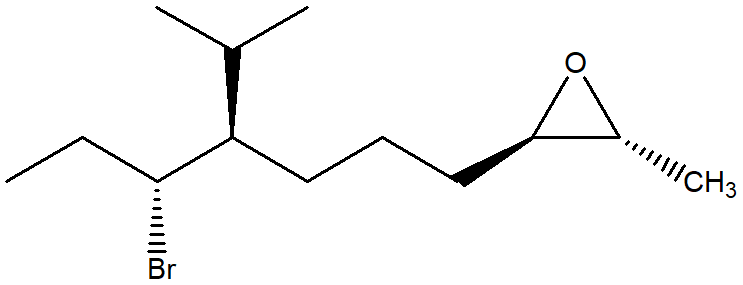
2) Scrivere un composto di formula C9H18 che contenga solo idrogeni primari
3) Dire quale tra le seguenti strutture è il (2R, 3S)-2-bromo-3-pentanolo
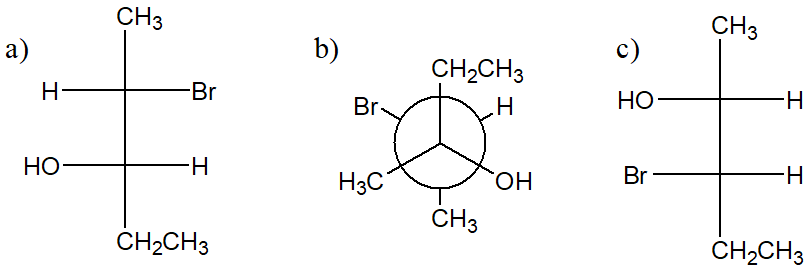
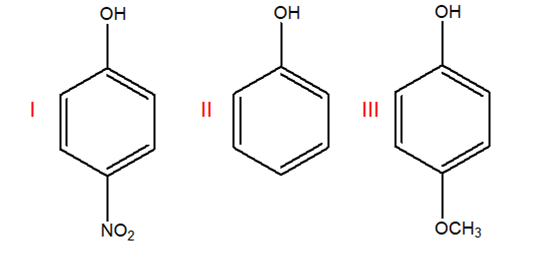
4) Mettere i seguenti composti in ordine di acidità crescente. Giustificare la risposta.
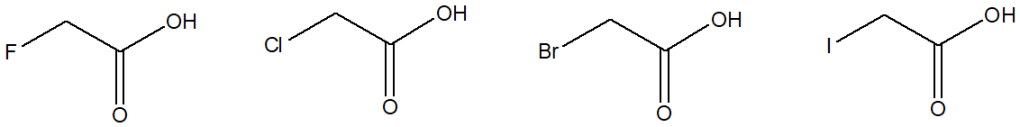
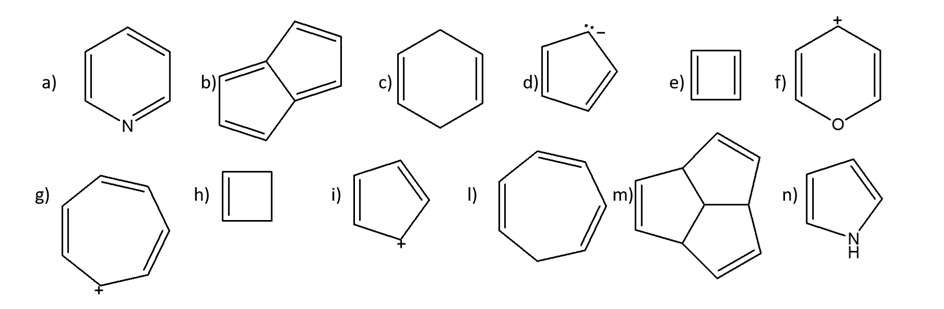
5) Individuare i composti aromatici tra quelli mostrati di seguito
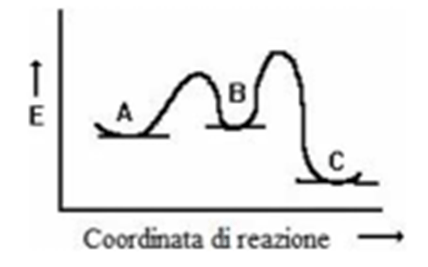
6) Basandosi sul seguente diagramma energetico, completare le seguenti frasi: A) il composto_____si formerà più velocemente a partire da B. B) Il composto più stabile è____perchè___________________________________
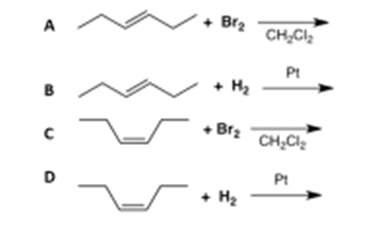
7) Da quale/i delle seguenti reazioni si forma un composto meso?
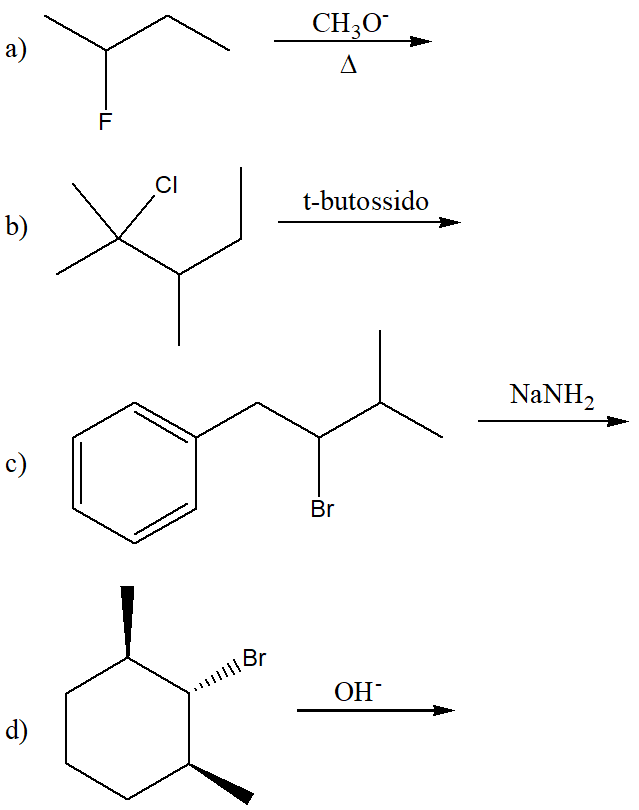
8) Scrivere i prodotti principali delle seguenti reazioni:
9) Mostrare il meccanismo di reazione del cicloesanone con la pirrolidina (=azaciclopentano)
10)Scrivere il dipeptide Gly-Ala (R=H per Gly, CH3 per Ala)
SECONDO SET
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2. Scrivere i seguenti composti in proiezione di Fischer e rispondere alle domande I e II:

3) Quali sono la geometria, l’angolo di legame e l’ibridazione previste per il radicale metile?
4) Mettere i seguenti composti in ordine di acidità decrescente. Giustificare la risposta.
5) Disegnare il conformero a sedia meno stabile del trans-1-t-butil-3-metilcicloesano. Spiegare brevemente i fattori che rendono questo conformero meno stabile rispetto a quello che si ottiene effettuando l’inversione della sedia
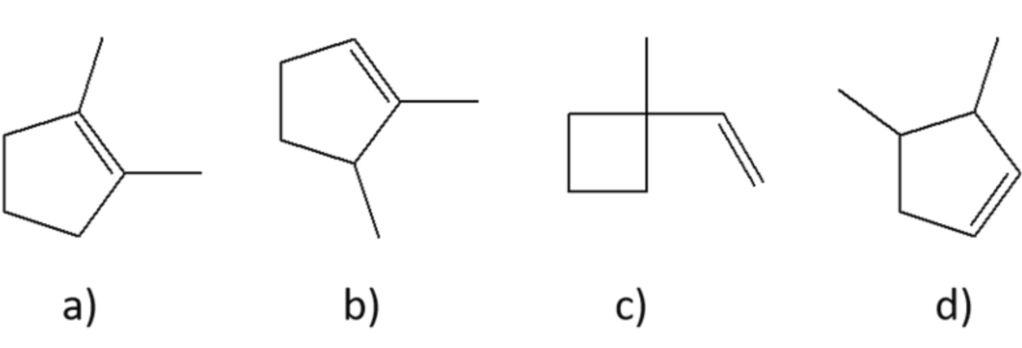
6) Quale/i dei seguenti alcheni darà come prodotto l’1-bromo-1,2-dimetilciclopentano come prodotto principale della reazione con HBr?
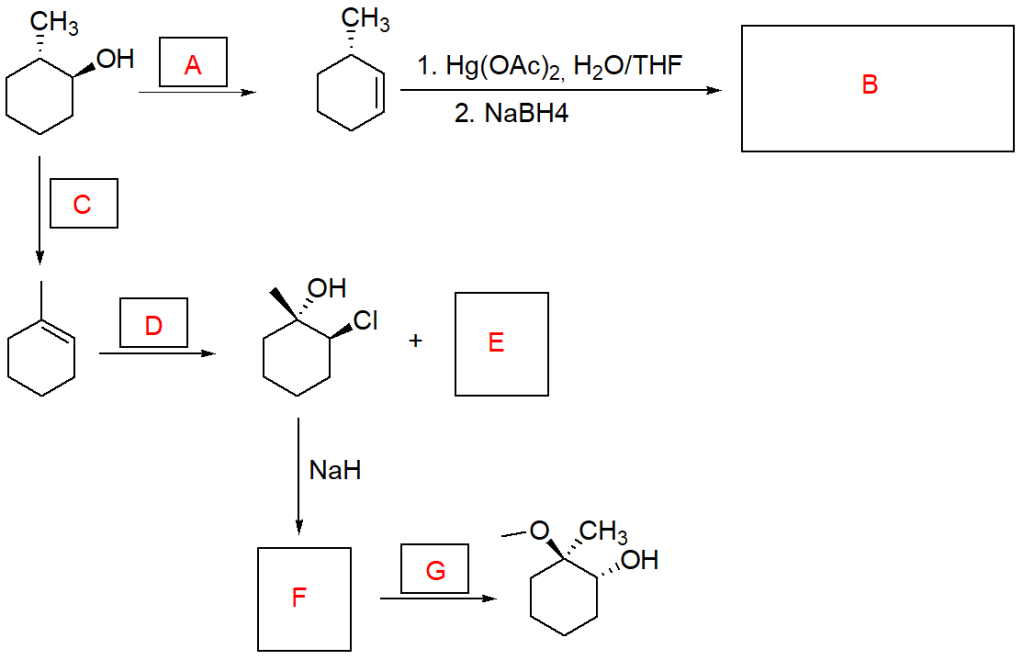
7) Completare il seguente schema di sintesi
8) Mostrare la strategia e il meccanismo di reazione per sintetizzare il 3-metil-2-cicloesenone mediante condensazione aldolica a partire dall’opportuno composto a catena lineare.
9) Il mannosio è l’epimero in 2 del glucosio. Scriverere il β-D-mannopiranosio in proiezione di Haworth
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate

Di seguito sono riportati i risultati della prova in oggetto. In verde sono indicati tutti gli studenti che hanno superato la prova scritta (tonalità diverse indicano l’appartenenza a diverse fasce di voto).
In giallo sono indicati gli studenti che hanno superato CON RISERVA (voto <18).
Per tutti gli altri studenti la prova si intende NON superata:
in arancione è indicata un’insufficienza grave (voto<15),
in rosso o nero è indicata una insufficienza gravissima (rosso–> voto<12, nero <6). In nero sono indicati anche gli studenti ritirati.
Si ricorda che i voti sono espressi in trentesimi!

ESAME ORALE: Gli studenti riportati in verde e in giallo sono ammessi a sostenere la prova orale, che si terrà lunedì 25 luglio alle ore 9:30
Tutti coloro che hanno sostenuto la prova potranno prenderne visione prenotandosi per il ricevimento e/o fissando appuntamento con il docente.
Si rende noto che sulla pagina dedicata al corso di Chimica Organica per il corso di Laurea in Scienze Biologiche sono disponibili delle esercitazioni in preparazione alla prova scritta, oltre che esercizi sui diversi argomenti oggetto del corso.
Di seguito sono indicate le fonti degli esercizi della prova di oggi:
Primo set: esercizio 2
Primo set: esercizi 1, 2, 8
Terzo set: esercizi 3, 5, 6
Secondo set: esercizi 7, 9 (semplificato).
Dai risultati della prova, è chiaro che molti non affrontano quest’esame nel modo corretto, ossia STUDIANDO.
SI SOTTOLINEA LA DISPONIBILITA’ DEL DOCENTE A DARE CHIARIMENTI SUI VARI ARGOMENTI durante il ricevimento, prenotabile seguendo il link “prenotazione ricevimento” o inviando un messaggio via chat di Teams.
Disponibilità del docente che è andata ben oltre il dovuto, dato che si è appena concluso un ciclo di esercitazioni di recupero, cui solo pochi studenti hanno partecipato. Il numero esiguo di persone che hanno dimostrato di volersi impegnare a capire e studiare la Chimica Organica è sconvolgente. Forse è il caso di chiarire ancora una volta che il superamento dell’esame prevede che si raggiungano dei requisiti minimi di sufficienza e non di certo una “collezione” di un certo numero di “tentativi”.
You must be logged in to post a comment.