Avviso esami orali del 2/11

Gli esami orali di oggi si terranno in AULA B2
Università degli Studi della Campania "Luigi Vanvitelli"

Gli esami orali di oggi si terranno in AULA B2

Sono state pubblicate le soluzioni del penutimo set di esercizi e alcuni esercizi svolti sulla nomenclatura dell’ultimo set.
Chi ha ancora dei dubbi sulla STEREOCHIMICA può rispondere al seguente questionario https://forms.office.com/Pages/ResponsePage.aspx?id=73pUj9cUykmk1FGmxcuSwXTRdKT1SyhLnKfYH_H9vfJUNFpPSFMyRDY0UVFWUDNJTEdXSURWWDBERCQlQCNjPTEu
Altre informazioni saranno fornite domani mattina a lezione.
Gli elenchi degli ammessi alla prova, con la distrubizone delle aule, saranno pubblicati domani dopo la lezione (gli ammessi saranno coloro che hanno superato la prima prova E che non avranno fatto più di due assenze)

1. Scegliere tra le seguenti opzioni quella che riporta i composti nel corretto ordine di punto di ebollizione crescente

2. Quale dei seguenti composti è meno solubile in acqua?
3. Spiegare perchè il neopentano ha un punto di ebollizione più basso rispetto al pentano.
4. Disegna un diagramma di energia potenziale per la rotazione di 360° del legame C2-C3 del pentano, partendo dal conformero meno stabile e disegnando le conformazioni corrispondenti ai massimi e ai minimi di energia.
5. Quale sarà più stabile tra l’isomero cis e l’isomero trans del 1-isobutil-4-metilcicloesano. Perchè? Utilizzare le proiezioni di Newman per mostrarlo.
6. Disegnare il conformero a minore energia del trans-1-terz-butil-4-metilcicloesano e del cis-1-terz-butil-4-metilcicloesano. Poi, confrontare tra loro i due isomeri geometrici. Quale dei due sarà quello più stabile? Perché?
7. Disegnare la proiezione di Newman secondo il legame C2-C3 del conformero meno stabile del 2,4- dimetilesano
8. Dare una definizione sintetica (massimo 20 parole per ciascuna definizione) di: a) tensione torsionale; b) tensione sterica; c) tensione angolare; d) iperconiugazione; e) interazioni 1,3-diassiali.
9. Assegnare il nome IUPAC, comprensivo di stereochimica quando necessario, ai seguenti composti:
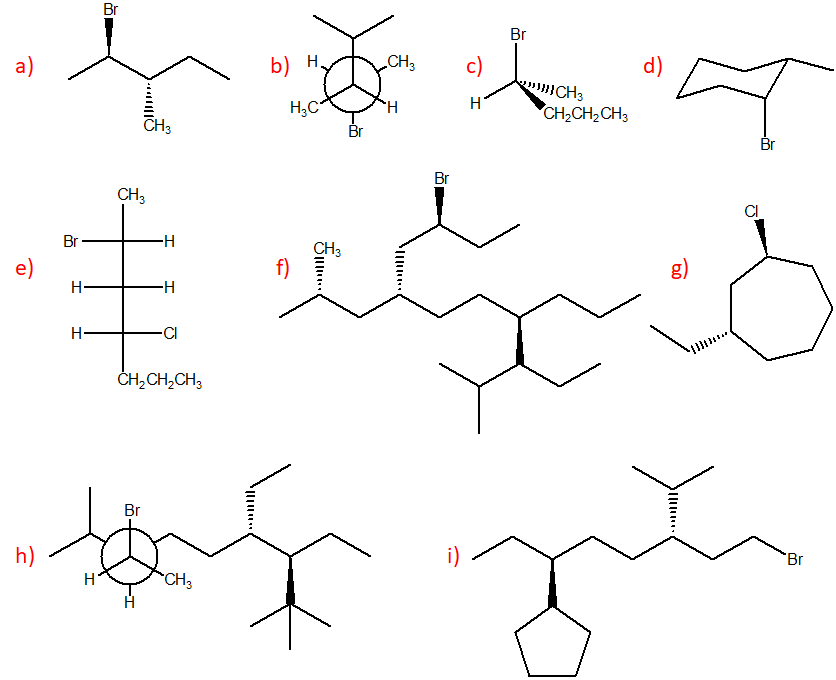

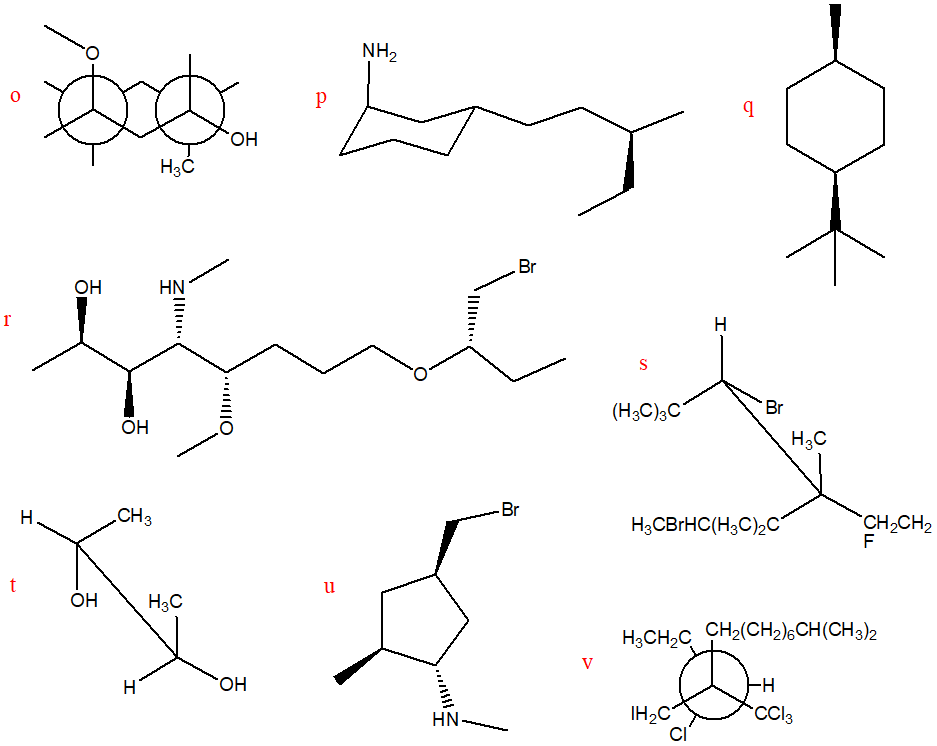
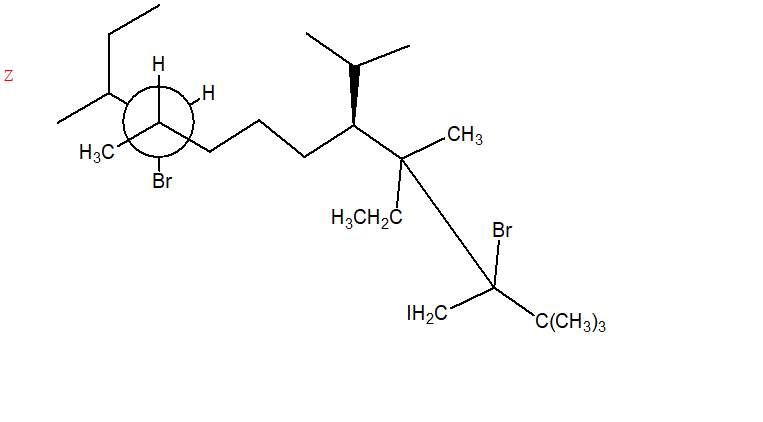
10. Disegnare il composto di formula molecolare C5H9Br che contenga 2 carboni chirali. Disegnare e attribuire il nome IUPAC a tutti i possibili stereoisomeri.
11. Disegna l’enantiomero di ciascuno dei seguenti composti:
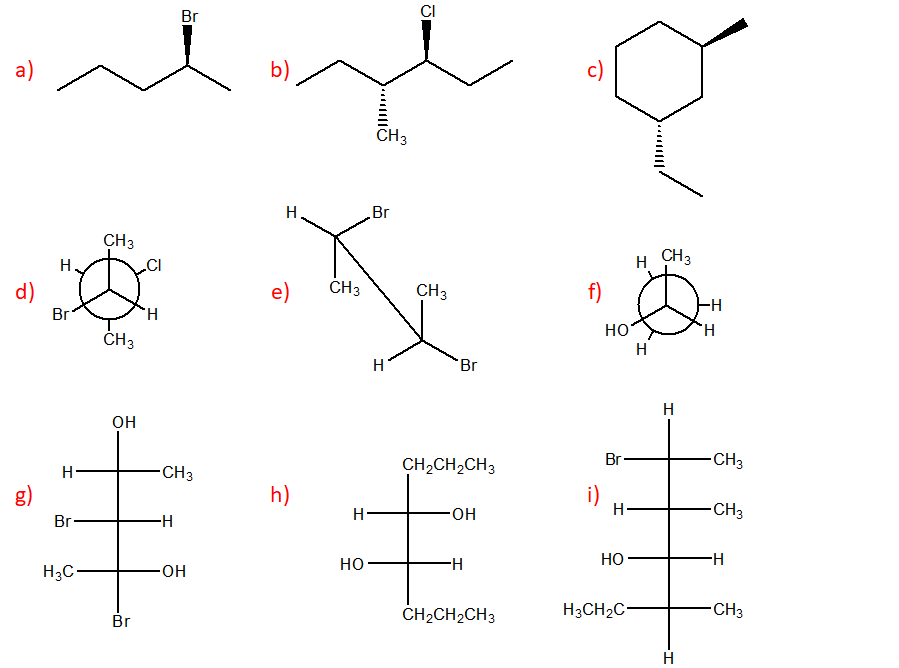
12. Qual è il numero massimo di stereoisomeri per i seguenti composti:
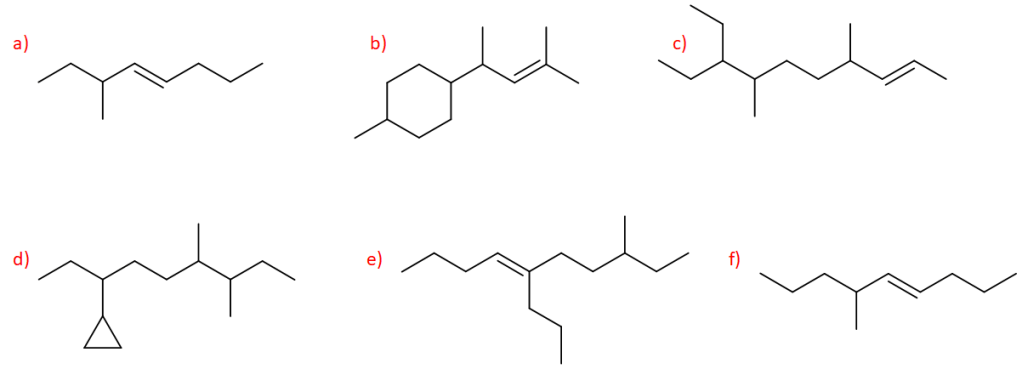
Per i composti che contengono doppi legami, dire se si tratta dell’isomero E o Z.
13. Qual è il numero massimo di stereoisomeri per il seguente composto?

14. Individuare tra le strutture riportate sotto quella che rappresenta l’enantiomero del seguente composto:
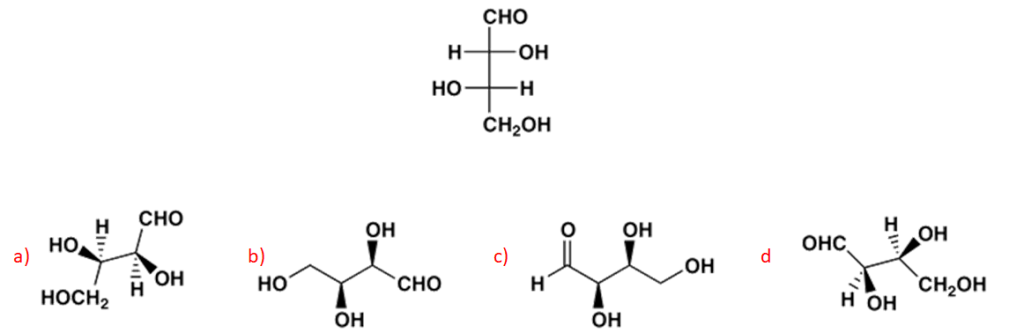
15. Individuare tra le strutture riportate sotto (a-c) quella che corrisponde alla seguente:

16. Attribuire la configurazione assoluta a tutti i carboni chirali e individuare la relazione stereochimica esistente tra le seguenti strutture:
A)
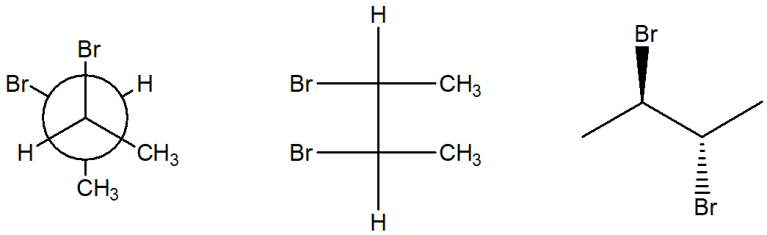
B)

C)

D)

E)
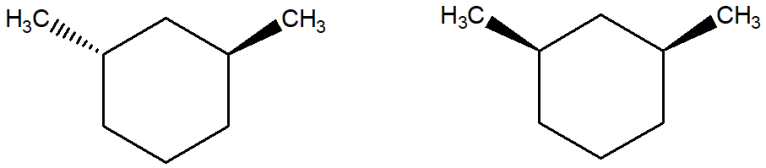
17. Dire se le seguenti molecole sono chirali:

18. Quale dei seguenti è un composto meso?
a) (2R,3S)-diclorobutano
b) (2R,3R)-diclorobutano
c) (2R,3S)-3-cloro-2-butanolo
d) (2R,3R)-3-cloro-2-butanolo
19. Quale dei seguenti composti non è chirale?
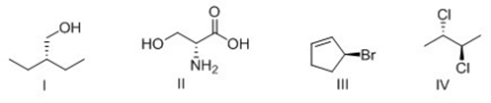
20. Scrivete le formule di struttura dei seguenti composti:
a) una molecola ciclica, isomero costituzionale del cicloesano
b) molecole di formula C6H12 che contengano un anello ed esistano come coppia di enantiomeri
c) molecole di formula C6H12 che contengano un anello e siano diastereoisomere tra loro
21. Scrivere le formule di struttura di tutti gli stereoisomeri e di tutti i conformeri corrispondenti a ciascuno dei seguenti nomi. Indicate le coppie di enantiomeri e i composti achirali eventuali:
a) 1-bromo-2-clorocicloesano
b) 1-bromo-3-clorocicloesano
c) 1-bromo-4-clorocicloesano
Attribuire la configurazione R,S a ciascuno dei composti indicati nelle risposte
22. Il (2R,3R)-2,3-butandiolo ha una rotazione ottica specifica di -13,2° e una temperatura di ebollizione di 77,3° C. Quale delle seguenti affermazioni è falsa?
A) Il (2R,3R)-2,3-butandiolo è un enantiomero treo
B) Il (2S,3R)-2,3-butandiolo è un composto meso
C) Il (2S,3R)-2,3-butandiolo ruota il piano della luce polarizzata di +13,2°
D) Il (2R,3S)-2,3-butandiolo non ruota il piano della luce polarizzata
E) Il (2S,3S)-2,3-butandiolo ha una temperatura di ebollizione di 77.3°C
23. Dire quale dei seguenti composti ruota il piano della luce polarizzata
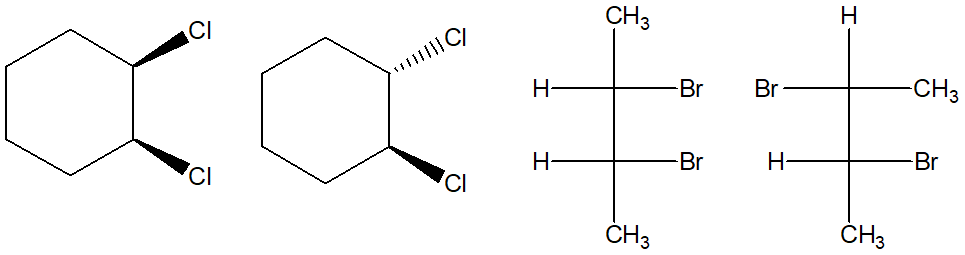
24. Dire qual è la relazione stereochimica esistente tra i seguenti composti (confrontare a/b; a/c; a/d; b/c; b/d; c/d).

25. Confrontare i seguenti composti e definirne le relazioni stereochimiche. In particolare, dire se sono enantiomeri, diastereoisomeri o isomeri conformazionali.
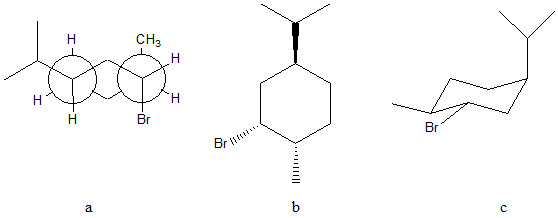
a e b sono___________________
a e c sono___________________
b e c sono___________________
26. Quale/i struttura/e è/sono diversa/e dalla seguente?
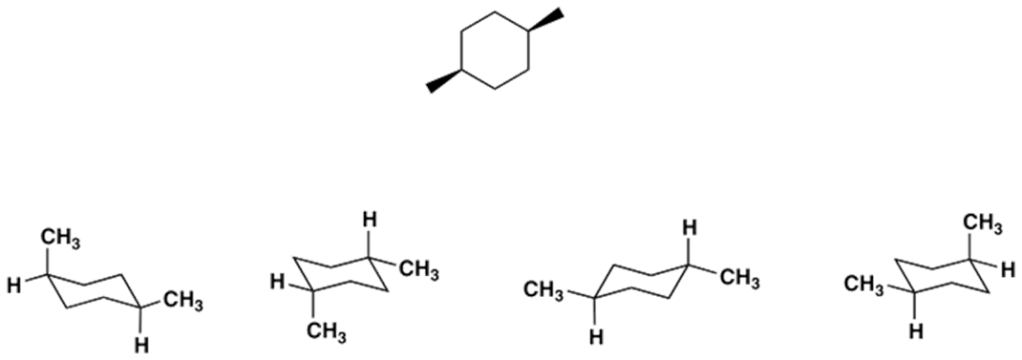
27.Scrivere, in proiezione di Fischer, formula prospettica e struttura a segmenti il (2S,3R)-2-bromo-3-metil-3-esanolo.
28. Scrivere la proiezione di Fischer del (2R,3R)-2-bromo-3-metilpentano. Poi scrivere la proiezione di Newman del conformero più e meno stabile lungo il legame C2-C3.
29. Quale delle seguenti strutture è la (2S,3R)-3-bromo-2-butanammina? (NB: è possibile scegliere più di una opzione):

30. Scrivere il (2R,3S)-3-bromopentan-2-olo (struttura a segmenti).
Questo composto sarà quello cui si farà riferimento in tutte le domande seguenti (se non indicato diversamente).
a) Scrivere un isomero di struttura che contenga comunque due carboni chirali e attribuirgli il nome IUPAC (sempre comprensivo di stereochimica
b) Scrivi un isomero costituzionale che non contenga carboni chirali.
c) Scrivi un composto costituito dallo stesso numero di atomi di C, Br e O, ma che sia caratterizzato da un grado di insaturazione e che non contenga carboni chirali.
d) Scrivi la proiezione di Fischer
e) Scrivi la proiezione di Newman del conformero più stabile in assoluto.
f) in che relazione stereochimica sono la struttura descritta in d e quella in e?
g) disegna un diagramma di energia potenziale per la rotazione di 360° del legame C2-C3, disegnando tutti i conformeri che corrispondono ai minimi e ai massimi di energia.
h) analizzare i singoli conformeri eclissati e valutare quali tipi di tensione contribuiscono a renderli meno stabili
i) quale fenomeno fa sì che i conformeri sfalsati siano a più bassa energia?
l) Scrivi l’enantiomero
m) Scrivi un diastereoisomero
n) Scrivi la struttura a cavalletto del conformero più stabile in assoluto per i composti scritti in l ed m
o) qualora conoscessi il potere ottico rotatorio specifico di h, potresti dire qualcosa circa il potere ottico rotatorio specifico del composto iniziale?
p) e qualora conoscessi il potere ottico rotatorio specifico di i?
q) immagina di aver sintetizzato il composto in laboratorio, di averne determinato la struttura, ma la misura del potere ottico rotatorio ti ha fornito un valore pari a 0 nonostante la presenza dei carboni chirali nella molecola. Cosa è possibile dedurre?

Al seguente link, troverete un TEST DI AUTOVALUTAZIONE sulla stereochimica. Avrete 1 ora per rispondere alle domande e alla fine potrete verificare il punteggio ottenuto e se avete risposto correttamente o meno.

Non sarà possibile fare ricevimento in concomitanza con la prova intercorso. Quindi, gli studenti prenotati per il 3 novembre dovranno provvedere a prenotare un nuovo appuntamento

Regolamento:

L’acido tartarico, la cui struttura è riportata di seguito, ha svolto un ruolo importante nella storia della stereochimica organica.

Due forme di acido tartarico diffuse in natura sono otticamente inattive. Una fonde a 260 °C e l’altra a 140 °C.
L’acido tartarico inattivo con punto di fusione di 260°C può essere separato in due forme attive con punto di fusione identico (170 °C). Un acido tartarico otticamente attivo ha un valore di [a]D =+12°, l’altro di -12°.
Invece, tutti i tentativi di separare i componenti della miscela dell’acido tartarico otticamente inattivo con punto di fusione di 140 °C in composti otticamente attivi falliscono.
A) Qual è la configurazione assoluta dei carboni chirali dell’acido tartarico con punto di fusione di 140°C?
B) Qual è la configurazione assoluta dei carboni chirali degli acidi tartarici otticamente attivi con punto di fusione di 170°C?
C) è possibile identificare l’acido tartarico a cui corrisponde la rotazione positiva e quello cui compete la rotazione negativa?
D) Qual è la natura della forma dell’acido tartarico con punto di fusione di 260°C?
E) Qual è la natura della forma dell’acido tartarico con punto di fusione di 140°C?

Che cosa hanno a che fare i composti mostrati in figura con le streghe?

Iosciamina e scopolamina sono alcaloidi prodotti da diverse piante della famiglia delle Solanaceae tra cui belladonna (Atropa belladonna), stramonio (Datura stramonium), giusquiamo (Hyoscyamus niger), mandragora (Mandragora officinarum). Questi composti hanno vari effetti, inclusa la capacità di indurre l’allucinazione del volo.
Potete leggere di più sull’argomento qui: https://phyto-chem.com/italian-version/18/ o nel post originale in inglese https://phyto-chem.com/2023/08/06/the-unbearable-lightness-of-flying/.

1. Per ciascuna delle seguenti molecole prevedere il numero massimo di stereoisomeri
I) Individuare gli elementi stereogenici (= carbonio chirale, doppio legame che ammette isomeria geometrica, ciclo con due sostituenti che non possiede carboni chirali ma che dà origine ad isomeria cis-trans); II) definire il numero massimo di stereoisomeri (2n dove n è il numero di elementi stereogenici)

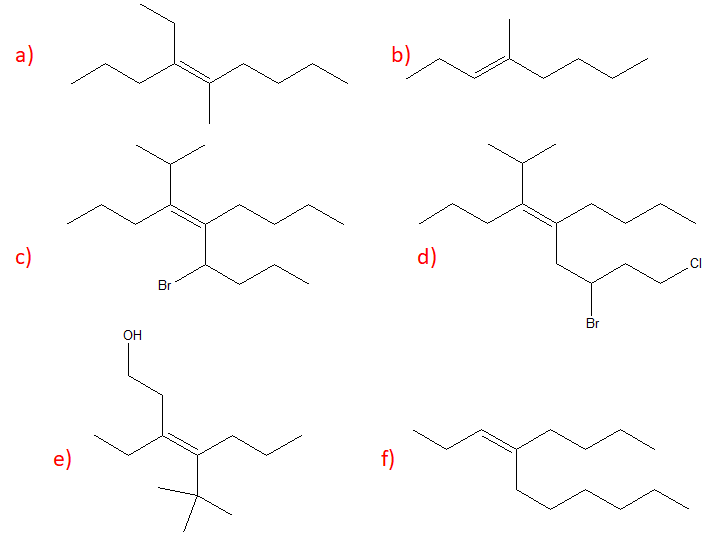
2. Definire la geometria (E o Z) dei doppi legami presenti nelle seguenti molecole
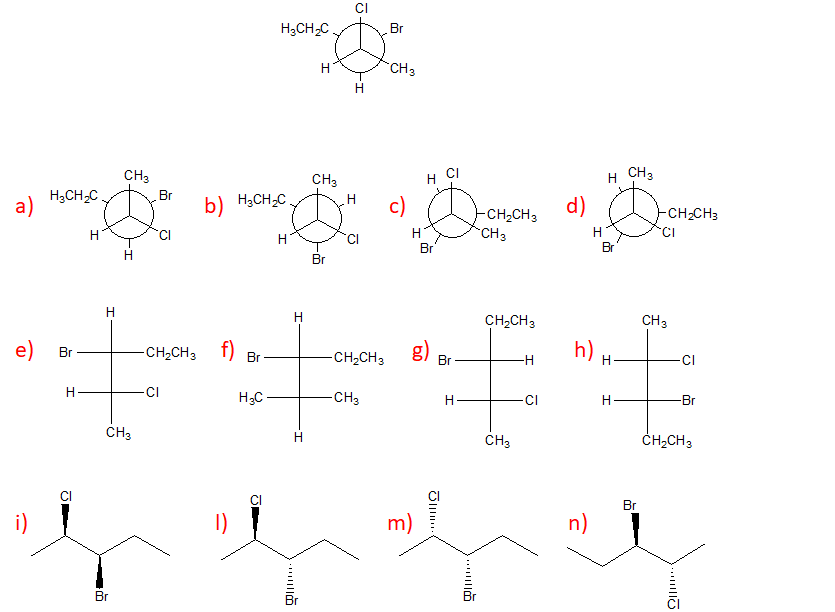
3. Confrontare ciascuna delle strutture indicate dalle lettere a-n con quella riportata qui sotto. Definire la relazione esistente tra la struttura in questione e le strutture a-n (cioè dire se sono tra loro enantiomeri, diastereoisomeri, stesso composto, isomeri costituzionali, isomeri geometrici, isomeri conformazionali o altro).
Nel confrontare due strutture:
I) capire se gli atomi sono connessi allo stesso modo (se non lo sono, ma la formula molecolare è la stessa–> isomeri costituzionali; se la formula molecolare è diversa–> altro)
II) se I è vero, capire se i carboni chirali hanno configurazione assoluta corrispondente. Se non è così, determinare se ci troviamo di fronte ad enantiomeri o a diastereoisomeri. NB: nel primo caso (enantiomeri), tutte le configurazioni saranno opposte. Per verificare questo punto è quindi necessario attribuire le configurazioni assolute. Se necessario, convertire la rappresentazione in quella più utile per determinare la configurazione assoluta* (es. da proiezione di Newman a Fischer).
III) se le configurazioni dei carboni chirali corrispondono, capire se ci troviamo di fronte a isomeri conformazionali.
IV) Se le molecole non sono distinguibili sulla base dei punti elencati in I, II e III, siamo di fronte allo stesso composto.
*NB: In questo caso specifino, l’unica rappresentazione da convertire è quella di Newman, in quanto le altre rappresentazioni permettono di determinare in maniera agevole la configurazione assoluta.
4. Dire in che relazione tra loro sono i componenti delle seguenti coppie di strutture (stesso composto/entantiomeri/diastereoisomeri/composti diversi, ecc.). Inoltre, per ciascun composto dire se è o meno chirale:
Per il primo punto, far riferimento alle linee guida degli esercizi precedenti. Per l’ultimo, dobbiamo capire 1) se ci sono carboni chirali 2) nel caso in cui ci sono due o più carboni chirali, dobbiamo capire se siamo o meno di fronte al composto meso.

5. Confrontare ciascuna delle strutture indicate dalle lettere a-l con quella riportata qui sotto. Definire la relazione esistente tra la struttura in questione e le strutture a-l (cioè dire se sono tra loro enantiomeri, diastereoisomeri, stesso composto, isomeri costituzionali, isomeri geometrici, isomeri conformazionali o altro).
Nel caso del cicloesano sostituito, dobbiamo far attenzione anche alla posizione relativa dei sostituenti (es. 1-3, 1-4 per capire se abbiamo o meno carboni chirali. Dobbiamo, inoltre, tenere in conto che in questo caso possiamo avere anche isomeri geometrici. Per le proiezioni di Newman e la rappresentazione a sedia, convertire prima in strutture a segmenti.
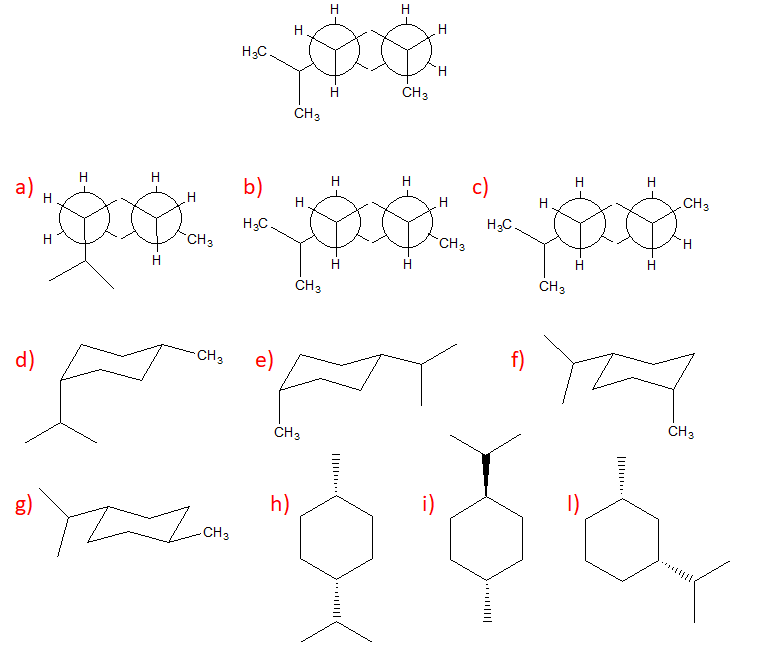
6. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti.
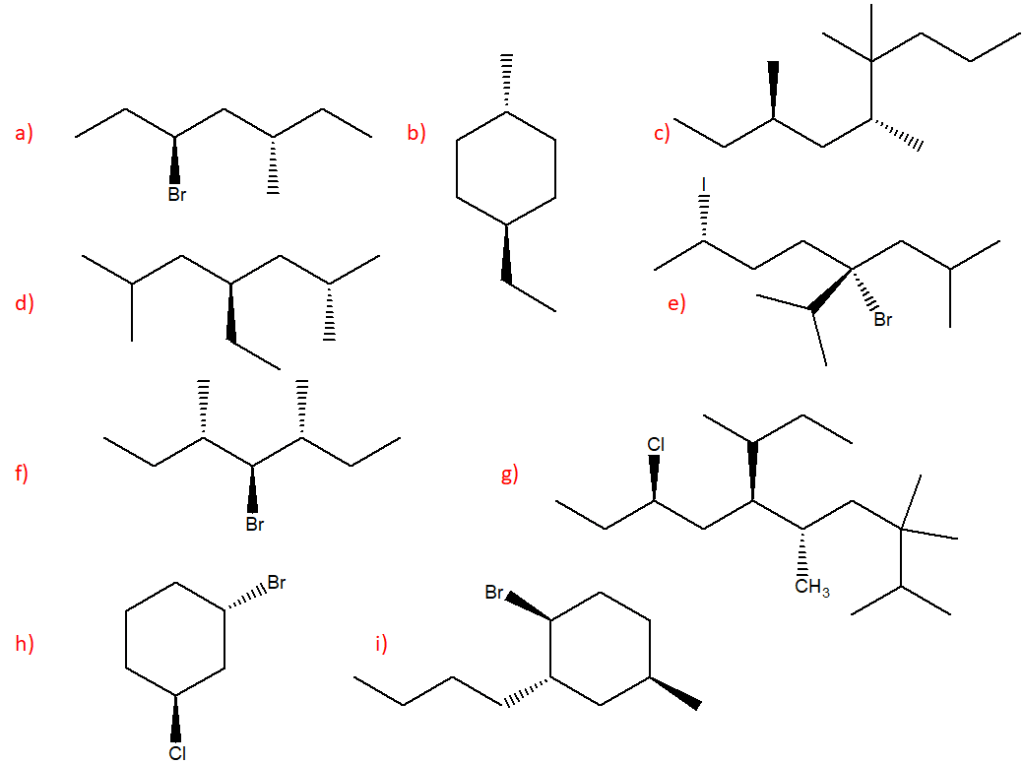
7) Quale/i dei seguenti composti non è/non sono chirale/i?
In questo esercizio e nel successivo bisogna innanzitutto valutare se ci sono carboni chirali. In presenza di più carboni chirali, dobbiamo capire se siamo di fronte al composto meso

8. Dire se i seguenti composti sono otticamente attivi

9. Rispondere alle domande A-D relative ai seguenti composti:

10. Quale delle seguenti affermazioni è vera per qualsiasi enantiomero S?

11. Disegnare la proiezione di Newman secondo il legame C2-C3 del conformero più stabile del seguente composto
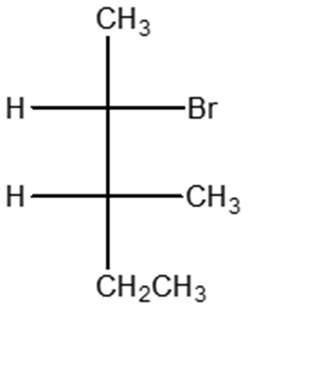
12. Quanti carboni chirali con configurazone assoluta S e quanti con configurazione assoluta R sono presenti nel taxolo (un farmaco antitumorale)? La struttura è riportata di seguito:


1) Assegnare la configurazione assoluta (R/S) ai carboni chirali delle seguenti molecole.

2) Rappresentare i seguenti composti come con: I) formule prospettiche, II) strutture a segmenti; III) proiezioni di Fischer:
a) (2S)-2-bromobutano
b) (3R)-3-cloro-2-metilpentano
c) (2S,3R)-3-cloro-2-pentanolo
d) (2R,3R)-3-etil-2-metilesano
e) (2S,3S)-3-isopropil-2-pentanolo
3) Assegnare il nome IUPAC comprensivo di stereochimica ai seguenti composti:
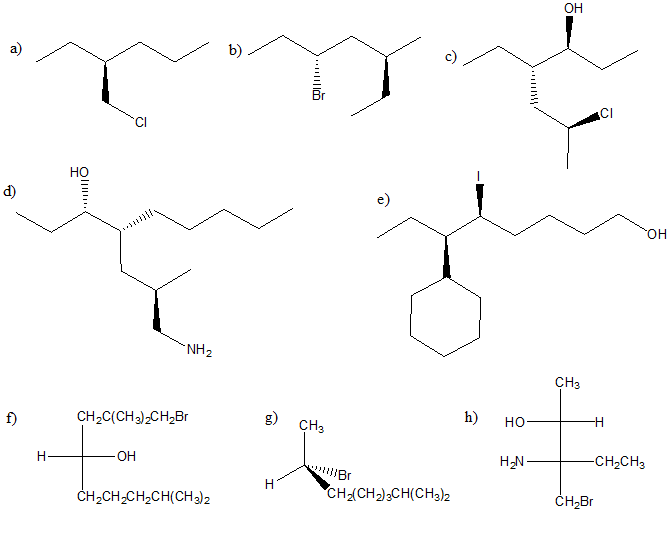
4) Individuare, tra le seguenti strutture, l’enantiomero del (2R)-2-bromo-1-esanolo

5) Dire quale tra le strutture a-d è un’altra rappresentazione del seguente composto:

6) Scrivi i quattro composti (inclusi gli enantiomeri) di formula molecolare C5H11Br che abbiano almeno un carbonio chirale. Attribuisci il nome, comprensivo di stereochimica, a ciascuno di essi.

Diversi tipi di rappresentazioni strutturali dei composti organici sono disponibili e ciascuna di esse è utile per mettere in evidenza determinati aspetti spaziali (e non solo). Saperle scrivere e leggere è fondamentale. Inoltre, è importante saper convertire queste rappresentazioni tra loro.
Sicuramente una struttura che vedremo spesso è quella a segmenti, in cui l’orientamento nello spazio dei sostituenti viene indicato usando un cuneo pieno (verso l’osservatore) e un cuneo tratteggiato (lontano dall’osservatore). Questo tipo di rappresentazione però non è adatta per l’analisi conformazionale, nè utile per mostrare gli aspetti stereochimici delle reazioni.
Nelle formule prospettiche, i legami sul piano del foglio sono disegnati come linee continue (vicine tra loro), quelli diretti fuori dal foglio sono cunei pieni, quelli lontani dall’osservatore cunei tratteggiati. Come disegnare le formule prospettiche? Indicazioni sono presenti nel paragrafo 4.7*. Come fare quando ci sono due centri asimmetrici? Indicazioni sono riportate nella “strategia per la risoluzione dei problemi” a pag. 175. Le formule prospettiche che troverete sul libro mostrano per lo più la struttura tridimensionale della molecola in una conformazione sfalsata. In ogni caso, è possibile anche scrivere la formula prospettica della conformazione eclissata (vedere pag. 166).
Nel paragafo 4.7 vengono introdotte anche le proiezioni di Fischer, mentre nel paragrafo 4.12 si analizzano le proiezioni di Fischer di molecole con più centri chirali. Le proiezioni di Fischer rappresentano sempre il composto in una conformazione eclissata e si ottengono osservando la molecola al centro della V definita da due dei legami del carbonio con i sostituenti. Queste rappresentazioni sono molto utili per riportare molecole con più centri chirali e rendono agevole l’attribuzione della configurazione assoluta.
Le proiezioni di Newman sono usate per rappresentare su carta le strutture tridimensionali che derivano dalla rotazione intorno ai legami sigma. Indicazioni su come scriverle sono riportate nel paragrafo 3.11. Le strutture a cavalletto mostrano il legame C-C in modo prospettico. In particolare, stiamo osservando la molecola da un angolo. I legami possono essere eclissati o sfalsati.
Una nota a parte è essenziale per le rappresentazioni del cicloesano, che sono ampiamente trattate sul libro. Nel paragrafo 3.13 vedrete come disegnare i conformeri a sedia e come effettuare la conversione d’anello. A pagina 133 sono disponibili invece informazioni su come disegnare la proiezione di Newman del cicloesano.
Sul libro, a pagg. 187-189 troverete anche un tutorial su come interconvertire le rappresentazioni strutturali.
Qui vedremo in maniera più dettagliata la conversione delle strutture a cavalletto e proiezioni di Newman in proiezioni di Fischer e viceversa.
Prima però vediamo la relazione esistente tra la proiezione a cavalletto e la proiezione di Newman. Se immaginiamo la proiezione di Newman come una rappresentazione 2D della struttura a cavalletto, che invece ci mostra il legame C-C da un certo angolo, il passaggio dall’una all’altra dovrebbe essere immediato.

Per passare dalla proiezione a cavalletto a quella di Newman, immaginiamo di proiettare i legami (e gli atomi) sul foglio; per fare il contrario, immaginiamo di estendere la proiezione di Newman fuori dal foglio.
CONVERTIRE UNA STRUTTURA A CAVALLETTO IN PROIEZIONE DI FISCHER
Vediamo che succede se abbiamo una struttura a cavalletto e vogliamo ottenere la proiezione di Fischer corrispondente.
Ricordiamo che la proiezione di Fischer rappresenta un conformero eclissato. Quindi, se la proiezione a cavalletto riporta un conformero sfalsato, il primo passo è quello di eclissarla. Vediamo qui due esempi di come è possibile ottenere un conformero eclissato.
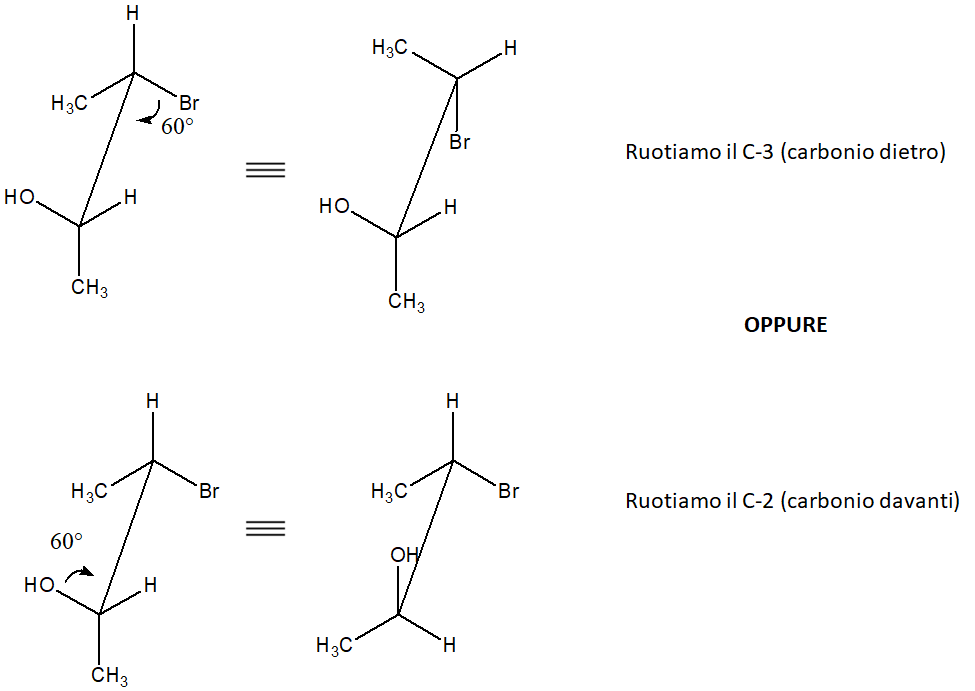
Ora prendiamo la prima struttura a cavalletto eclissata (quella in alto). Per convertirla ad una proiezione di Fischer, dobbiamo innanzitutto guardarla al centro della V costituita dai legami tra i carboni chirali e due sostituenti legati a ciascun carbonio. Dobbiamo anche scegliere il punto di osservazione. Quello più immediato per chi sta guardando la struttura sul foglio è dall’alto, con lo stereocentro davanti collocato più vicino a noi. Questo carbonio sarà in basso sulla proiezione di Fischer. Così facendo, nell’esempio in questione, il bromo e il metile dovranno stare sulla linea verticale (che, ricordiamo, indica i legami lontani dall’osservatore). Il bromo però starà in alto e il metile starà in basso sulla linea verticale della proiezione di Fischer.

Mantenendo fisso il punto di osservazione, ora possiamo riportare sulla proiezione di Fischer tutti i sostituenti alla nostra sinistra (che andranno sulle linee orizzontali a sinistra) e tutti quelli che stanno alla nostra destra (che andranno sulle linee orizzontali a destra).
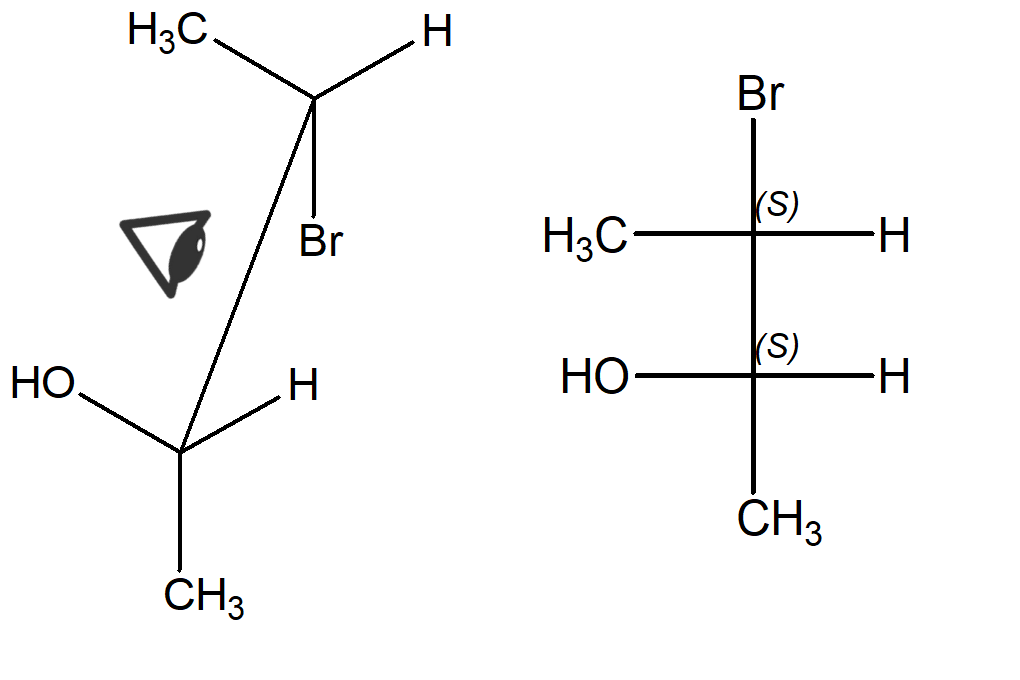
Possiamo guardare la molecola da altre angolazioni? Sì, però è necessario fare molta attenzione a posizionare bene i sostituenti. Immaginiamo per esempio di guardarla sempredall’alto, ma con le spalle rivolte al foglio e quindi con il C-3 (quello che lega il bromo) più vicino a noi. In quel caso avremo sempre il metile e il bromo lontani da noi, ma il metile sarà sul carbonio in alto e il bromo su quello in basso. Inoltre, i sostituenti a destra saranno l’ossidrile e il metile e a sinistra avremo i due atomi di idrogeno.
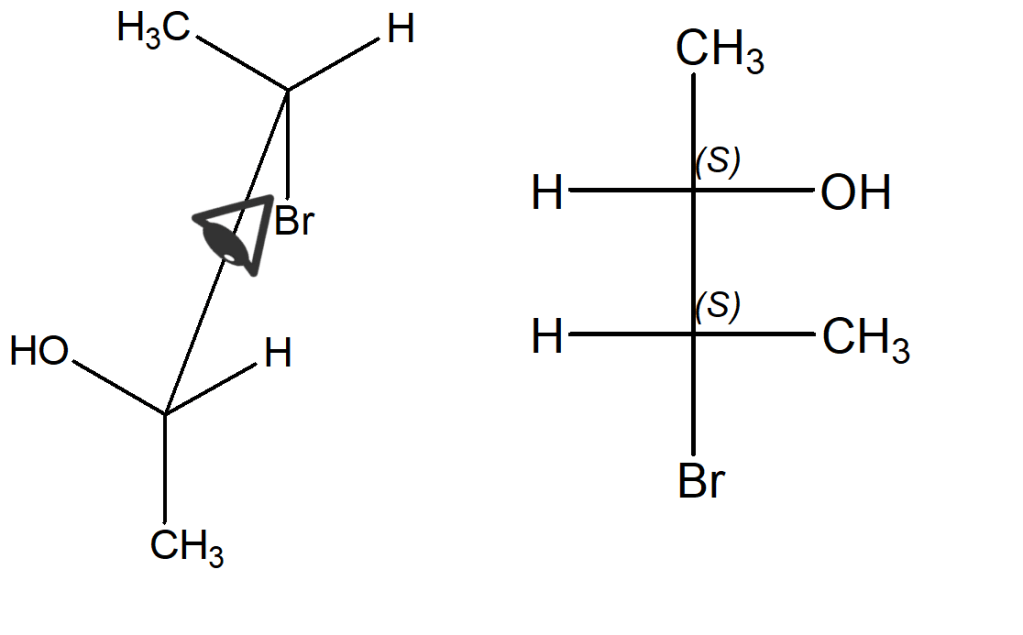
Notiamo che questa proiezione di Fischer è praticamente quella in alto, ruotata di 180° sul foglio (e quindi, sono lo stesso composto come evidenziato anche dalla configurazione assoluta dei due stereocentri).
Potremmo guardarla anche da altre angolazioni, ma queste richiedono un maggiore sforzo di immaginazione. Ad esempio, immaginiamo di guardarla tra i legami indicati in rosso nell’immagine seguente, con il carbonio davanti (C-2) più vicino a noi. In questo caso, lontani da noi sono collocati i due idrogeni. Ancora una volta dobbiamo far attenzione alla posizione relativa degli altri sostituenti (altrimenti scriveremmo uno stereoisomero del nostro composto).

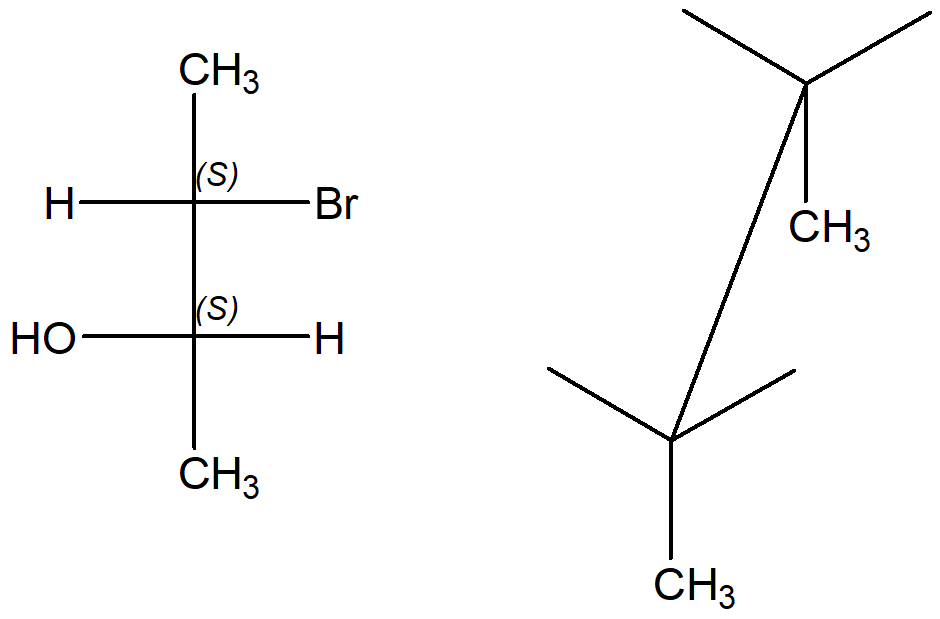
Ora prendiamo il secondo conformero eclissato, quello che abbiamo ottenuto nel primo passaggio, ruotando il carbonio 2. Anche qui possiamo scegliere la prospettiva di osservazione. Immaginiamo di guardarlo dal basso e frontale (non dando le spalle al foglio). In tal caso, possiamo anche immaginare semplicemente di”ribaltare” la struttura sul foglio. Immaginiamo di appoggiare la mano nel punto indicato dalla freccia blu qui sotto e di spingere il carbonio verso l’alto, mentre l’altro carbonio resta fisso sul foglio. Otterremo il ribaltamento della struttura. Quindi l’OH starà verso l’alto e l’H verso il basso. Facciamo attenzione alla disposizione degli altri sostituenti.
Ancora una volta è comunque possibile osservarla da più angolazioni, ma bisogna sempre fare molta attenzione.

Notiamo come la configurazione dei carboni chirali è sempre la stessa. Abbiamo infatti lavorato su un singolo stereoisomero.
Consiglio: provate a lavorare con l’aiuto dei modellini!
CONVERTIRE UNA PROIEZIONE DI FISCHER IN PROIEZIONE A CAVALLETTO
Come passare da proiezione di Fischer ad una a cavalletto? Ci ricordiamo che la proiezione di Fischer è relativa ad un conformero eclissato e che i due sostituenti sulla linea verticale sono lontani dall’osservatore. Quindi, li posizioniamo come mostrato in figura
A questo punto, mettiamo sulla destra i sostituenti che stanno a destra sulla proiezione di Fischer e a sinistra quelli a sinistra (attenzione! Il nostro punto di osservazione della struttura a cavalletto in questo momento è dall’alto guardando verso il foglio).

PROIEZIONE DI NEWMAN/PROIEZIONE DI FISCHER
E per quanto concerne la conversione proiezione di Newman/proiezione di Fischer e viceversa? Se è chiara la relazione tra la proiezione di Newman e le strutture a cavalletto, non dovrebbe essere difficile…
Vediamo un esempio di passaggio dalla proiezione di Newman a quella di Fischer.

Qui la stiamo osservando sempre dall’alto e rivolti verso il foglio (o lo schermo).
E se l’abbiamo eclissata nel modo seguente?

In questo caso, possiamo seguire il consiglio del libro e quindi “muovere” verso il basso il legame che coinvolge il metile sul carbonio posteriore (o in generale quello che punta verso l’alto sul carbonio in questione). Così facendo, il metile starà in basso e legherà alla sua sinistra il bromo e alla sua destra l’H. L’altro legame che punta verso l’alto, quello con l’H, sarà sul carbonio in alto nella proiezione di Fischer. L’ossigeno sarà alla sua sinistra e il metile alla sua destra.

Si può passare dalla proiezione di Fischer a quella di Newman agevolmente se si ricorda che Fischer rappresenta un conformero eclissato. Bisogna però essere attenti nel definire il punto di osservazione sulla proiezione di Newman e scrivere il conformero eclissato corretto. All’inizio, potrebbe essere utile “passare” per la struttura a cavalletto (vedere sopra la descrizione del metodo) e poi convertire quella in proiezione di Newman.
Passare da una rapprensentazione all’altra può sembrare complesso all’inizio. Per poterlo fare in maniera consapevole è essenziale aver capito bene ciascun tipo di rappresentazione…e tanto esercizio.
*In questo post di fa spesso riferimento al libro: in questo caso ci riferiamo all’ultima edizione del Bruice. Chi ha un libro diverso, potrà avvalersi dell’aiuto dell’indice analitico
You must be logged in to post a comment.