Esercitazione per la prova scritta (V)

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
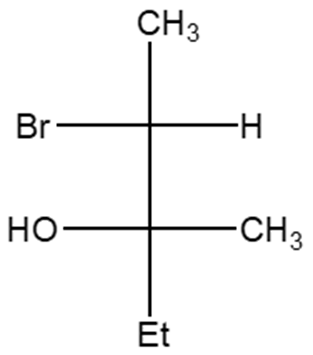
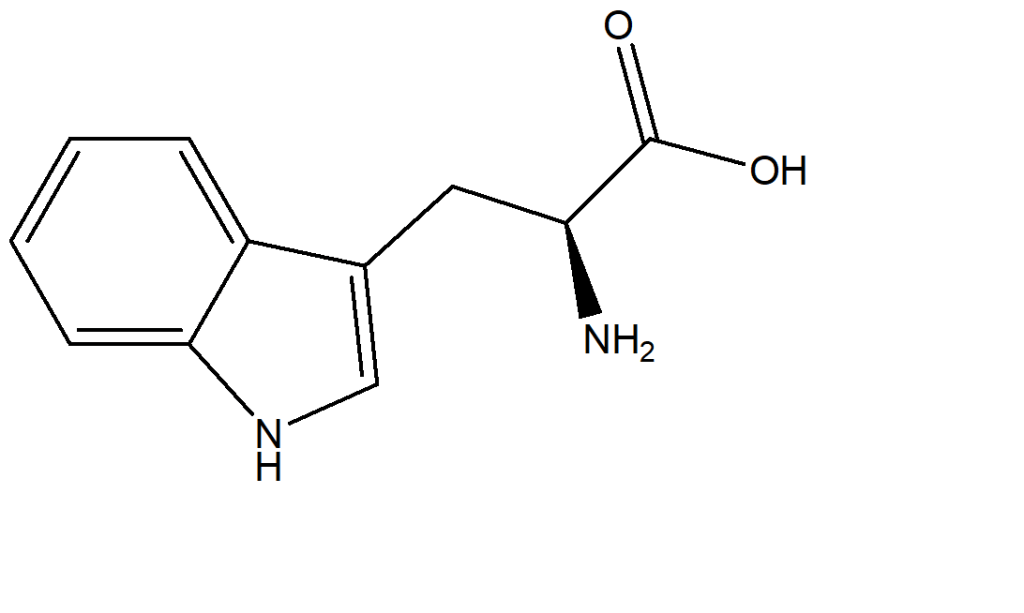
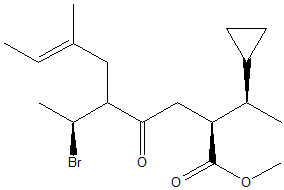
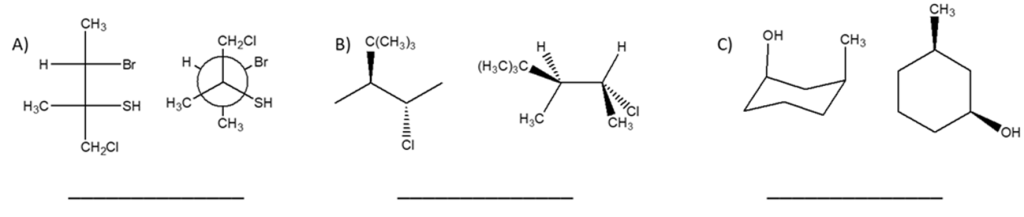
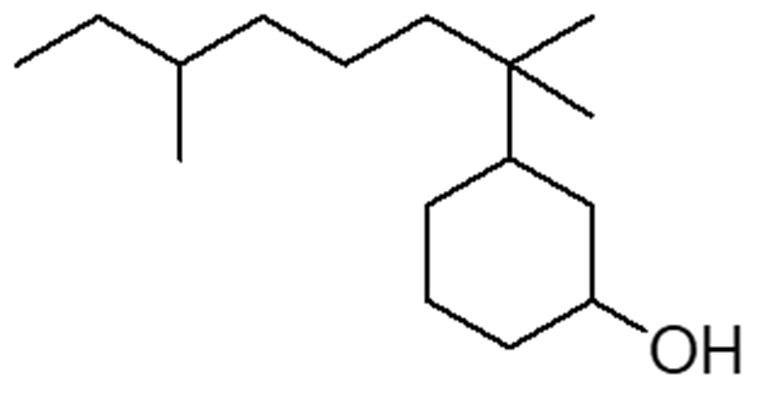
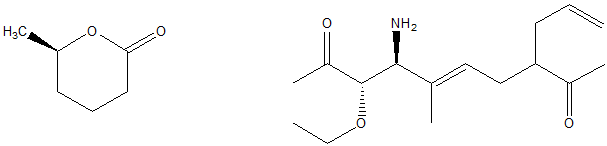
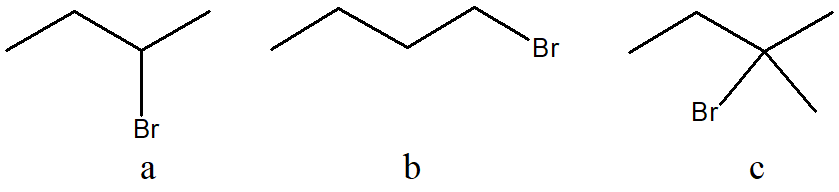
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:

2) Scrivere e attribuire il nome IUPAC al composto di formula C6H12 che possiede solo idrogeni primari e terziari
3) Disegnare il conformero a minore energia del cis-1-terz-butil-4-etilcicloesano e del trans-1- terz-butil-4-etilcicloesano. Poi, confrontare tra loro i due isomeri geometrici. Quale dei due sarà quello più stabile? Perché?
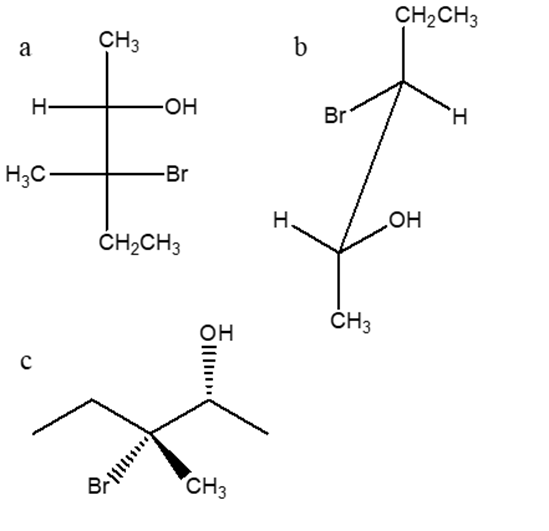
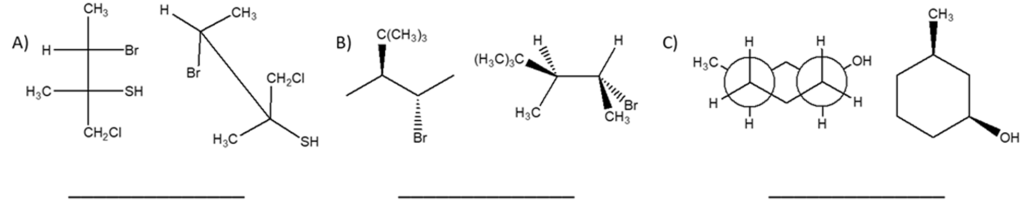
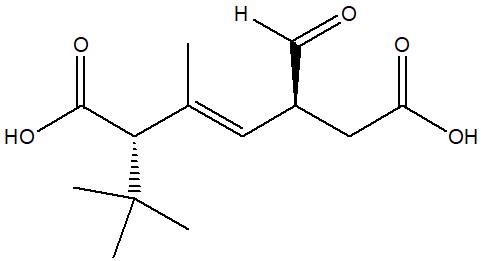
4) Stabilire le configurazioni assolute dei carboni chirali e dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/stesso composto/isomeri costituzionali/altro).
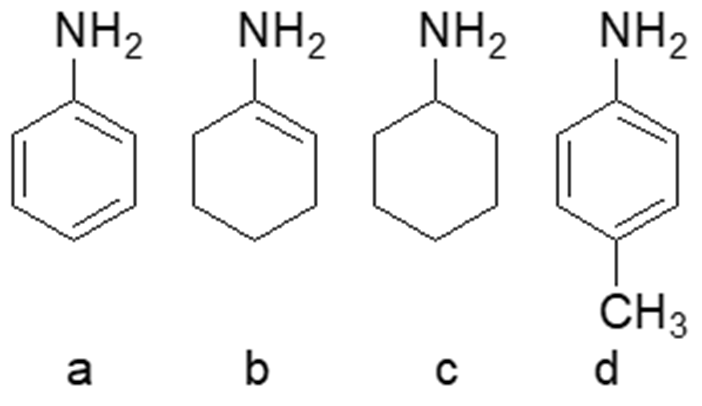
5) Disporre i seguenti composti in ordine di basicità decrescente (dal più basico al meno basico) e spiegare sinteticamente il perché:

6) Disporre i seguenti composti in ordine di acidità decrescente e motivare la risposta data

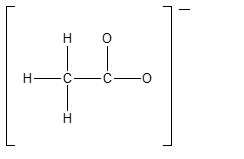
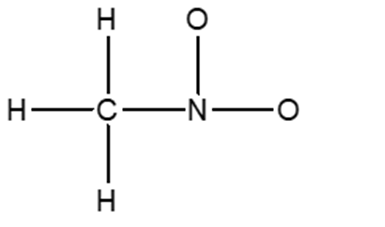
7) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di carbonio e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza
8) Analizzare il diagramma di energia libera/coordinata di reazione dell’addizione di HBr al 1-butene e rispondere ai seguenti quesiti.

a) Cosa possiamo dire circa la Keq della reazione?
b) Cosa possiamo dire circa il ΔG° della reazione?
c) Di quanti stadi si compone la reazione?
d) Qual è lo stadio cineticamente determinante?
e) Indicare sul grafico l’energia di attivazione relativa allo stadio veloce.
f) Cosa sono, rispettivamente B, C e D?
g) Disegnare la struttura di C e D
h) Spiegare perché la reazione è regioselettiva
9) Mostrare la strategia di sintesi e il meccanismo che permette di ottenere il 2-cicloesenone mediante una reazione di condensazione aldolica
SECONDO SET
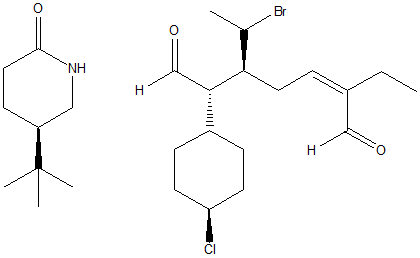
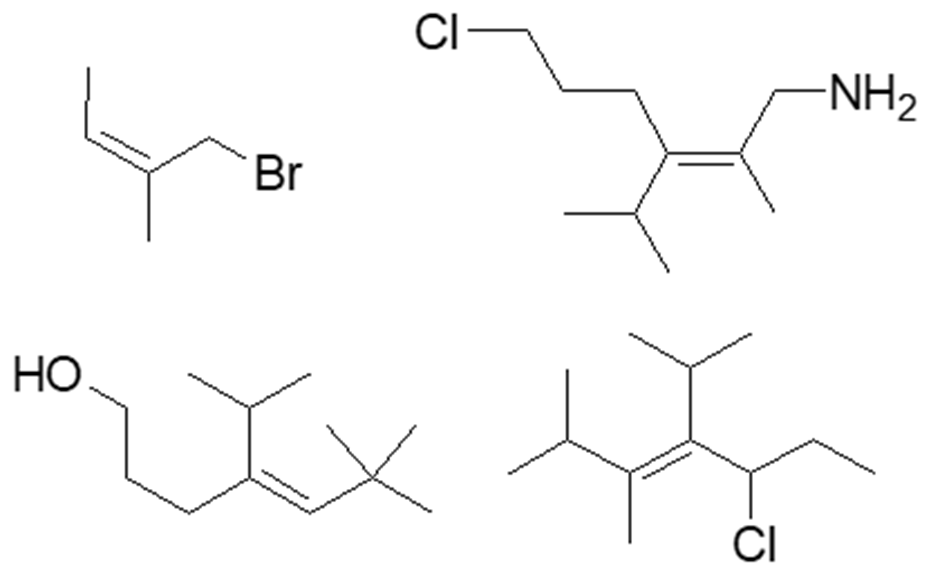
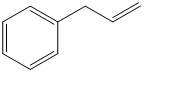
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
2. Disegnare il 1-sec-butil-4-etil-2-metilciclopentano
3. Identificare il tipo di orbitali (indicati dalle lettere a-g nell’immagine seguente); specificare anche se si tratta di orbitali atomici o molecolari.

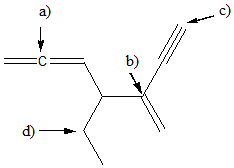
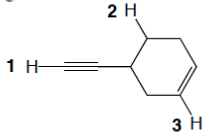
4) Indicare il tipo di ibridazione per ognuno degli atomi indicati da una freccia:

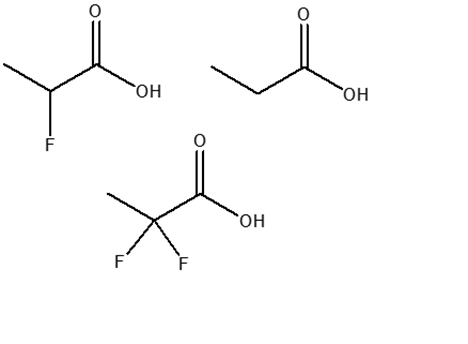
5) Cerchiare l’acido più debole e motivare sinteticamente la scelta.
6) Mettere i seguenti composti in ordine di acidità crescente e motivare la scelta:
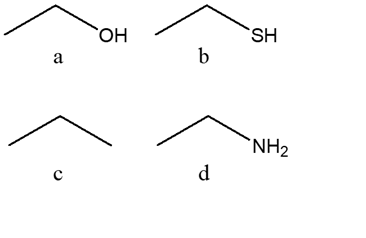
a) CH3CH2CH2SH b) CH3CH2CH2NH2 c) CH3CH2CH2OH d) CH3CH2CH2CH3
7) Qual è il numero massimo di stereoisomeri per il seguente composto?

8) Dire quale tra le strutture a-d è l’enantiomero del seguente composto:

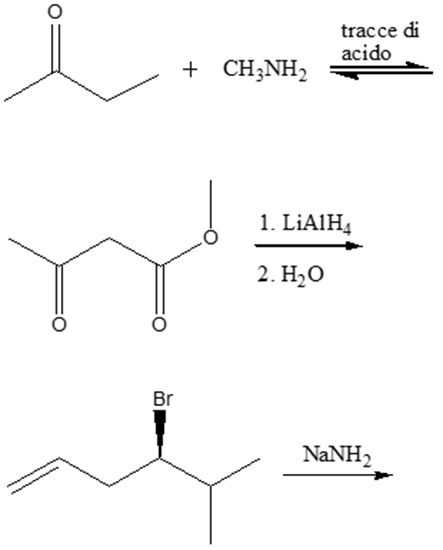
9) Mostrare le condizioni di reazione, il meccanismo e i prodotti della reazione del ciclopentanone con etanammina
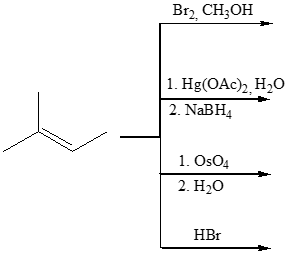
10) Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica, quando opportuno.
11. Classifica i seguenti composti o ioni come aromatici, antiaromatici o non aromatici:
TERZO SET
1a. Rispondi alle domande sulla seguente molecola:

a) Quante coppie solitarie sono presenti sul cloro e quali orbitali occupano? ____________________
b) Quanti carboni ibridati sp sono presenti? ________________________________________
c) Indicare con una freccia sulla figura il legame singolo carbonio-carbonio più corto
1b. Nella molecola dell’esercizio 1a, sono presenti diversi legami multipli. Fornire una descrizione dettagliata dei legami formati dai due carboni impegnati nel triplo legame (informazioni necessarie: atomi con cui formano i legami; orbitali molecolari formati; orbitali atomici/ibridi coinvolti)
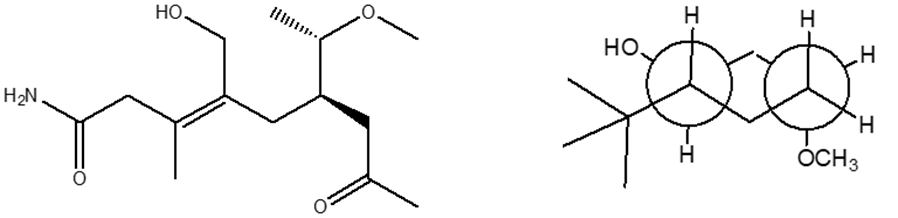
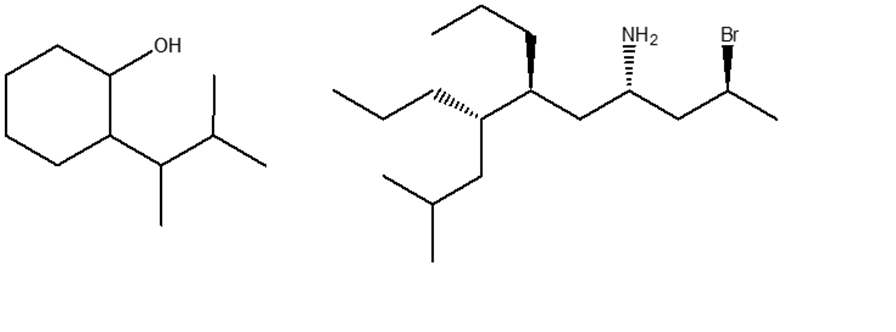
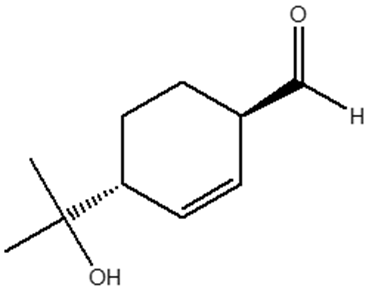
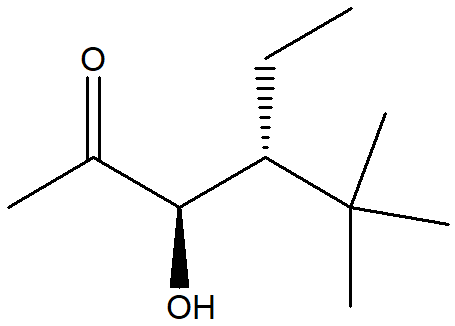
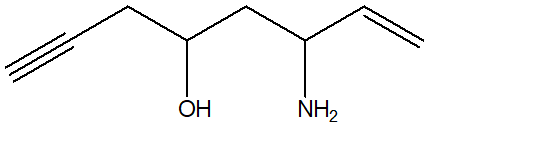
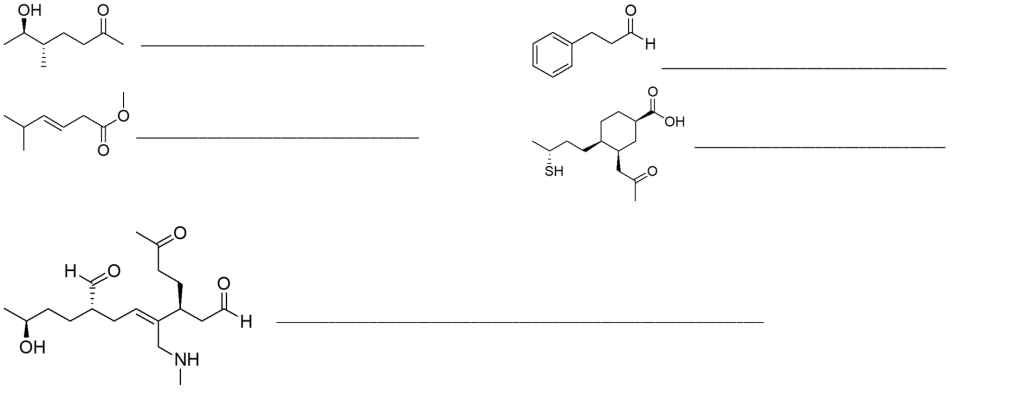
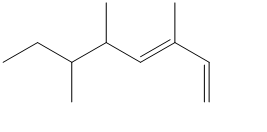
2. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
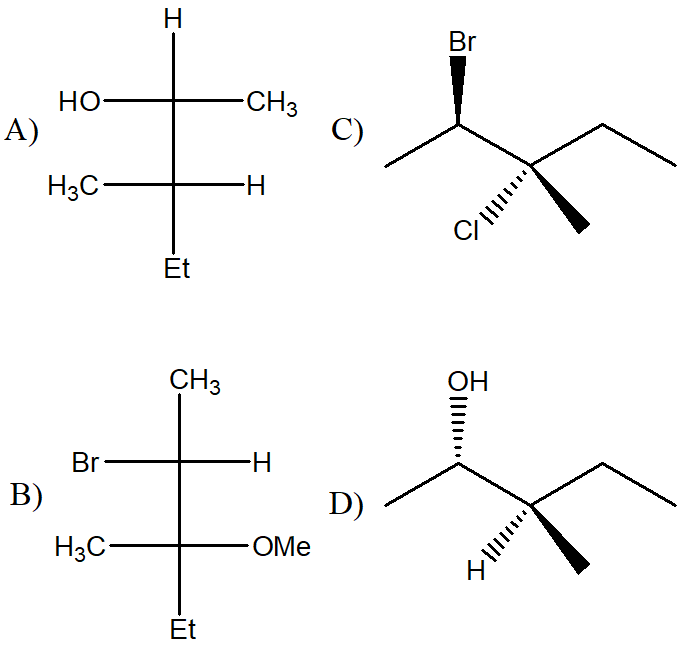

3. Dire se le strutture riportate a destra sono isomeri conformazionali, isomeri geometrici, isomeri ottici, isomeri costituzionali, o lo strutture identiche rispetto alla seguente struttura a segmenti:

4) Scrivi il (2R,3S)-2-bromo-3,4-dimetilpentano in proiezione di Fischer.
Scrivi, poi, la proiezione di Newman lungo il legame C2-C3 del conformero a minore energia.
5) a. Individuare gli idrogeni più acidi in ciascuno dei seguenti composti. b. ordinare i seguenti composti in ordine di acidità crescente
a) 3-ossobutanoato di metile
b) acetone (=propanone)
c) 2,4-pentandione
d) etanoato di metile
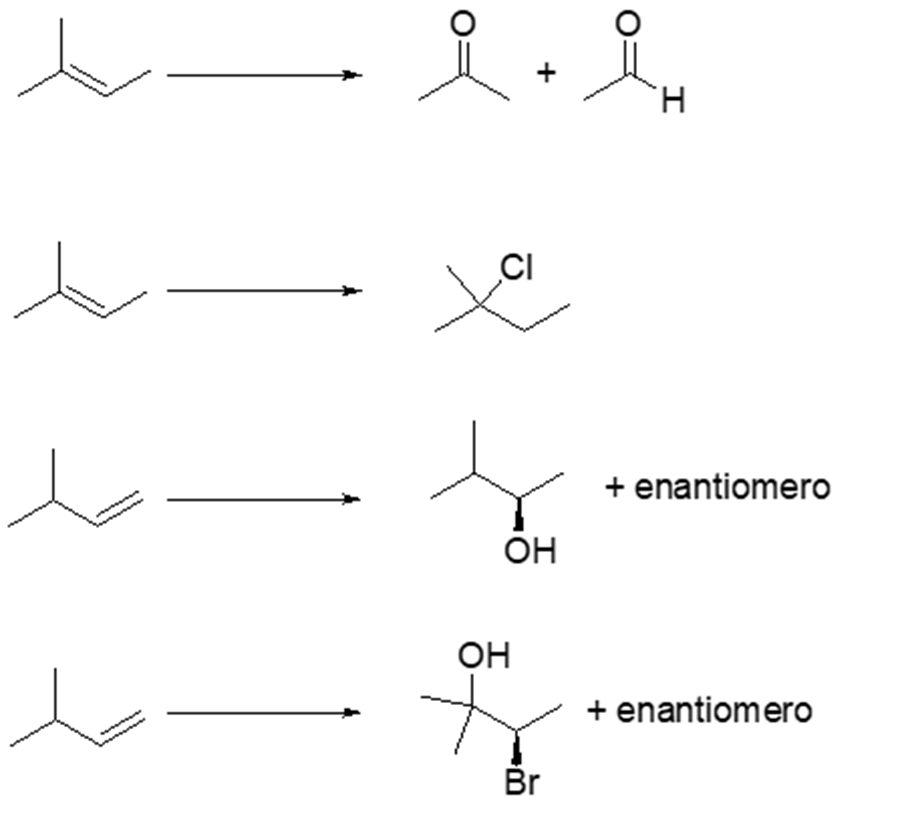
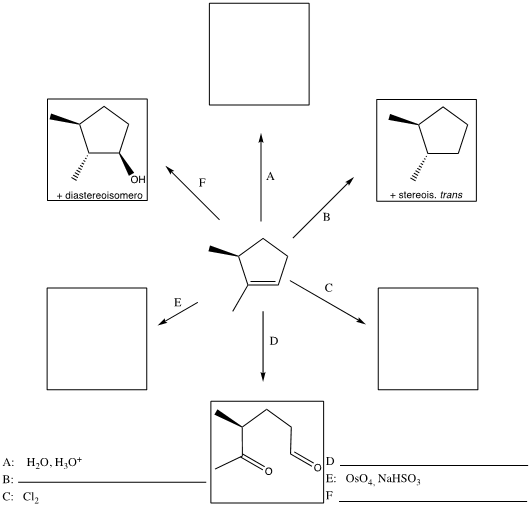
6) Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal (S)-3-metilciclopentene. Se quello ottenuto non è l’unico prodotto di reazione, indicare gli ulteriori altri prodotti formati, dire in che relazione sono col prodotto riportato e indicare se si formano o meno in quantità equimolari rispetto a quest’ultimo. NB: se non si formano ulteriori prodotti, scrivere “nessuno” nella casella dedicata.

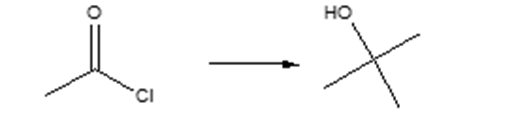
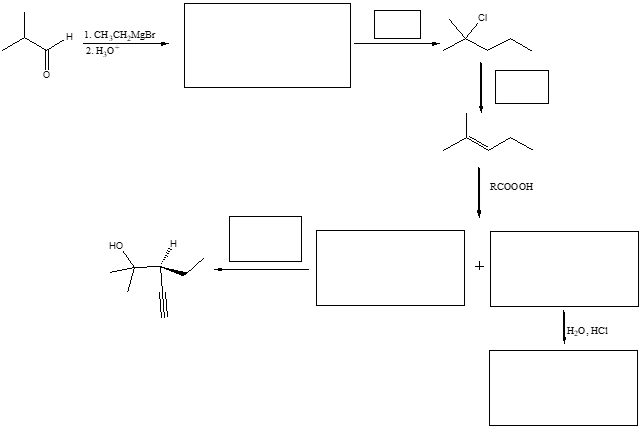
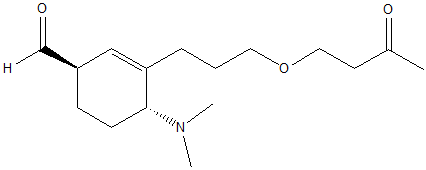
7) Indicare le condizioni di reazione ottimali per ottenere la seguente trasformazione e mostrare il meccanismo di reazione:
8) Scrivere la struttura di un trigliceride semplice in cui il glicerolo (1,2,3-propantriolo) è esterificato con un acido grasso a 18 atomi di carbonio
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate







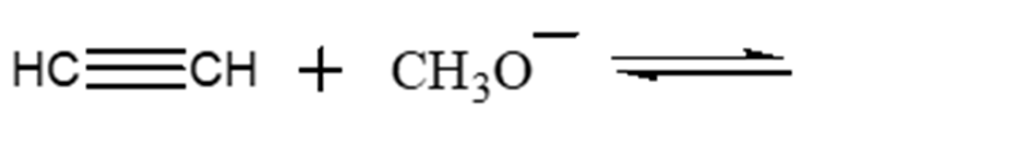












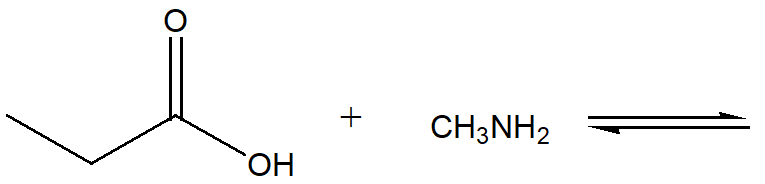


































You must be logged in to post a comment.