CdL Scienze Biologiche – I prova intercorso: Aule

Gli studenti dalla A alla L dovranno recarsi in AULA A2;
Dalla M alla Z in AULA A3
Università degli Studi della Campania "Luigi Vanvitelli"

Gli studenti dalla A alla L dovranno recarsi in AULA A2;
Dalla M alla Z in AULA A3

Prima di controllare la presenza del proprio nome, leggere attentamente quanto segue.
Chi DEVE contattare al più presto la docente:
1-chi non è nell’elenco, ma vuole sostenere la prova intercorso;
2-chi è nell’elenco, ma non intende sostenere la prova.
Gli studenti i cui nomi sono indicati in giallo sono ammessi con riserva (hanno accumulato più assenze di quante permesse) e per ora non dovranno fare nulla (si prega di non inviare mail in questa fase, anche se si pensa di essere erroneamente assegnati a questo gruppo, dato che un secondo controllo sarà effettuato dopo la pubblicazione dei risultati). L’ammissione con riserva non ha alcun effetto sulla valutazione della prova, ma comporterà il fatto che non si tollereranno più di due assenze prima della prova successiva. Lo stesso vale per coloro che, pur essendo riportati in verde, hanno già accumulato 2 assenze, nel caso di un’ulteriore assenza alla lezione di domani 16/10.
Sono, per ora esclusi di default tutti coloro che sono stati assenti a più del 50% delle lezioni. In ogni caso, nell’ottica della tolleranza applicata in via eccezionale per questa prova, se qualcuno tra gli studenti esclusi ritiene di aver studiato e di voler sostenere la prova, deve contattare la docente al più presto.
Tutte le comunicazioni di cui sopra dovranno essere fatte via e-mail.
L’oggetto della mail dovrà essere “prova intercorso” e nella mail è necessario indicare nome, cognome, matricola.
Le comunicazioni dovranno pervenire entro domattina alle ore 8:00
Elenco

Sono state caricate le ultime soluzioni relative al post
Non saranno caricate ulteriori soluzioni prima della prova. In caso di dubbi, è possibile rivolgersi alla docente domani a lezione o commentando i post. Non sarà possibile farlo invece via email fino all’inizio della prova.
In serata saranno pubblicati gli elenchi degli ammessi alla prova. Chi non è intenzionato a sostenerla deve comunicarlo alla docente via email entro domani alle 8:00 (NB: non riceverete risposta alla mail in questione, ma vi ringrazio in anticipo per la comunicazione.

Regolamento:
Assegnare il nome IUPAC al seguente composto (NB: ai fini della challenge non è permesso l’utilizzo dei nomi d’uso per i sostituenti ramificati)
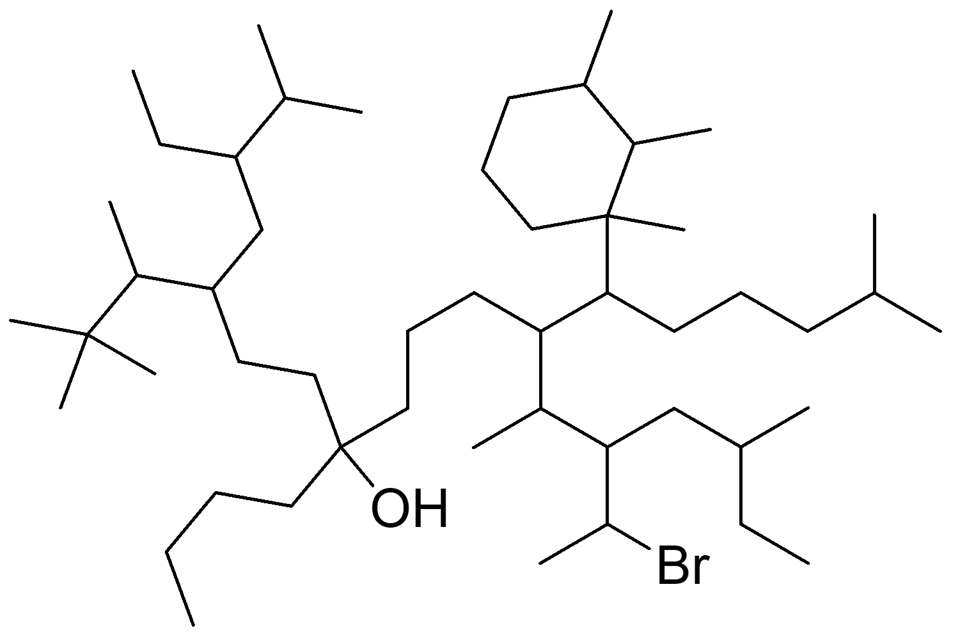

Per chi ha difficoltà a svolgere esercizi del tipo “Scrivere e assegnare il nome IUPAC ad un alcano (o cicloalcano) che abbia: a) formula bruta C6H14 e che contenga solo idrogeni primari e terziari” potrebbe essere utile consultare le soluzioni di questo set di esercizi https://chimicaorganicadistabif.com/2024/10/09/nomenclatura-sostituenti-ramificati-e-cicloalcani-alogenuri-alchilici-2/ dove vi viene riportato il ragionamento che è possibile seguire. Ovviamente bisogna sapere cos’è un C primario, secondario, terziario e quaternario e che cos’è un H primario, secondario e terziario, ma per il resto basta applicare il ragionamento logico.
Ricordo inoltre a tutti che sul blog è disponibile del materiale didattico che siete invitati vivamente a consultare/studiare


Seguendo questo link, potrai accedere al test di autovalutazione, che comprende domande su tutti gli argomenti trattati fino ad ora.
Si consiglia di affrontare il test solo dopo aver studiato tutti gli argomenti, in modo da mettere in evidenza eventuali dubbi/lacune. Si consiglia anche di farlo con un certo anticipo rispetto alla prima prova intercorso, in modo da avere anche tempo per chiedere chiarimenti alla docente, se necessario.
Il test ha una durata di 90 minuti. Alla fine riceverai il punteggio e potrai controllare le tue risposte.
Puoi accedere solo se sei uno studente @unicampania. Il nome dell’utente sarà registrato e visibile solo al docente del corso.

Di seguito troverete 3 set di esercizi che possono essere usati come simulazioni per la prova stessa per capire se ci sono argomenti ancora poco chiari o su cui dovete ancora esercitarvi.
Suggerimento: per poter usare questi esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 90 minuti per ciascun set.
PRIMO SET
1. Per lo ione solfato (SO42-) è possibile scrivere diverse strutture di risonanza. Scrivere la struttura di Lewis che rappresenta una delle strutture che contribuisce maggiormente all’ibrido di risonanza. Calcolare le cariche formali per tutti gli atomi.
2. Quali sono la geometria, l’angolo di legame e l’ibridazione previste per il catione metile?
3. Rispondi alle domande sulla seguente molecola:
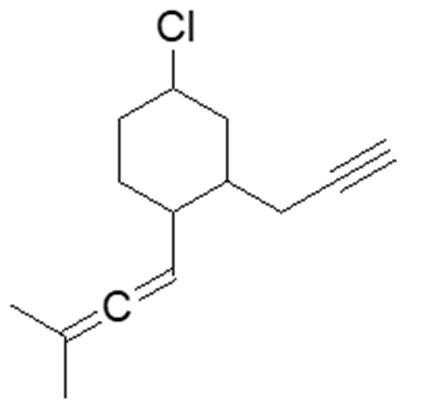
a) Quante coppie solitarie sono presenti sul cloro e quali orbitali occupano?
b) Quanti atomi di carbonio ibridati sp sono presenti?
c) Indicare con una freccia sulla figura il legame singolo carbonio-carbonio più corto.
4. Nella molecola dell’esercizio 3, sono presenti diversi legami multipli. Fornire una descrizione dettagliata dei legami formati dai due carboni impegnati nel triplo legame (informazioni necessarie: atomi con cui formano i legami; orbitali molecolari formati; orbitali atomici/ibridi coinvolti).
5. Disporre i seguenti composti in ordine di acidità crescente (dal meno acido al più acido) e spiegare sinteticamente il perché:
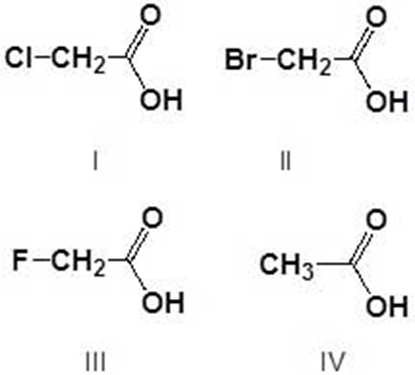
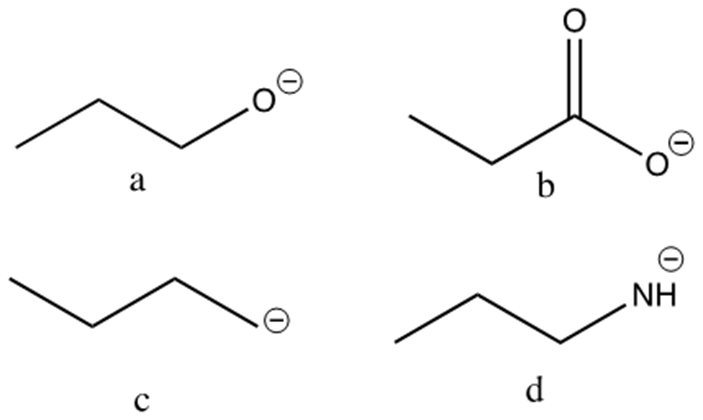
6. Disporre i seguenti composti in ordine di basicità crescente (dal meno basico al più basico) e spiegare sinteticamente il perché:
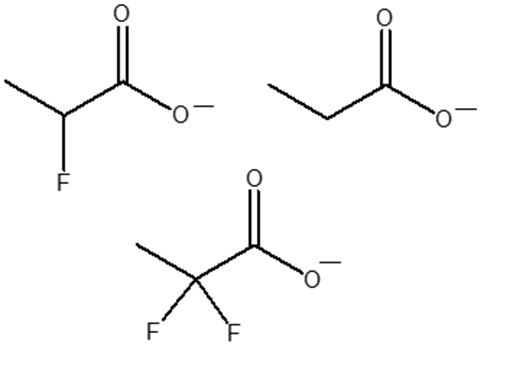
7. A quale valore di pH un composto con pKa 7.2 sarà presente in soluzione al 50% nella forma acida?
8. Scrivere e attribuire il nome IUPAC al composto di formula C5H12 che possiede solo idrogeni primari.
9. Scrivere la formula condensata e la formula molecolare del seguente composto:
4-bromo-2,2-dimetilesano
10. Scrivere la struttura a segmenti del seguente composto e dire se il nome IUPAC è corretto; se non lo è, apportare le dovute correzioni:
1-butil-1-metil-3-cicloesanolo
11. Assegnare il nome IUPAC ai seguenti composti:

SECONDO SET
1. Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di carbonio e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza.

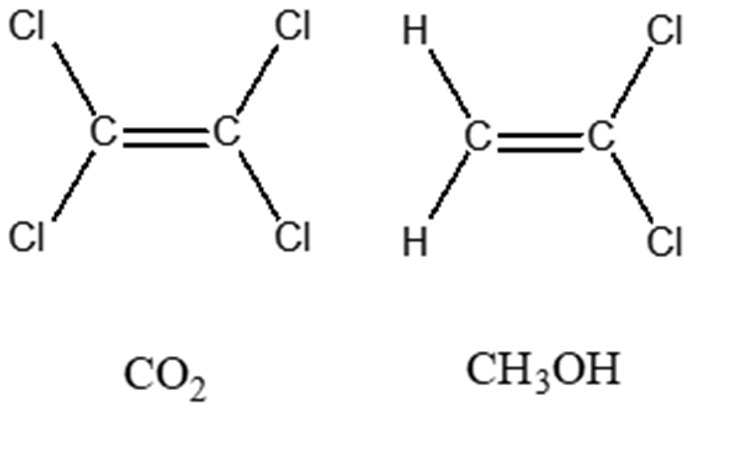
2. Cerchiare la/le molecola/e che ha/hanno momento dipolare nullo.
3. La struttura di seguito riportata è quella della chinina. Osservare gli atomi e i legami indicati da lettere e numeri e completare le seguenti frasi o rispondere alle seguenti domande.

I) La coppia solitaria dell’atomo di azoto a si trovano in un orbitale_______; quella dell’atomo di azoto b si trova in un orbitale_______
II) Osservare il legame indicato dalla c ed indicare il tipo di orbitale/i molecolare/i:
III) Quali orbitali atomici si sovrappongono per formare il legame c?
IV) Qual è il legame più corto tra quelli indicati dai numeri da 1 a 4?
4. Disporre i seguenti composti in ordine di basicità decrescente (dal più basico al meno basico) e spiegare sinteticamente il perché:

5. Cerchiare l’acido più debole e motivare sinteticamente la scelta.

6. Completare la reazione e dire dove è spostato il seguente equilibrio:

7. Scrivere e attribuire il nome IUPAC al composto di formula C6H12 che possiede solo idrogeni primari e terziari.
8. Disegnare l’ 1-sec-butil-4-etil-2-metilciclopentano.
9. Scrivere la formula condensata di un isomero strutturale del 2,3-dimetilpentano.
10. Assegnare il nome IUPAC ai seguenti composti:

TERZO SET
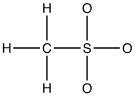
1. Completare la seguente struttura di Lewis e calcolare la carica formale per tutti gli atomi diversi dall’idrogeno:
2. Quali sono la geometria, l’angolo di legame e l’ibridazione previste per l’anione metile?
3. Nella seguente figura, alcuni dei legami sono indicati da freccia e da una lettera.
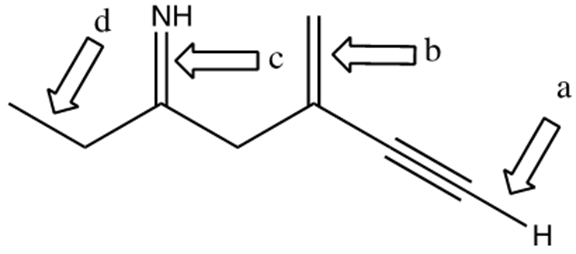
1) Etichettare i legami a-d come singoli, doppi o tripli;
2) indicare il tipo di orbitale/i molecolare/i;
3) dire quali orbitali atomici sono coinvolti nella formazione del legame.
4) Considerando tutti i legami singoli della molecola (ed escludendo i legami C-H) qual è il legame più corto?
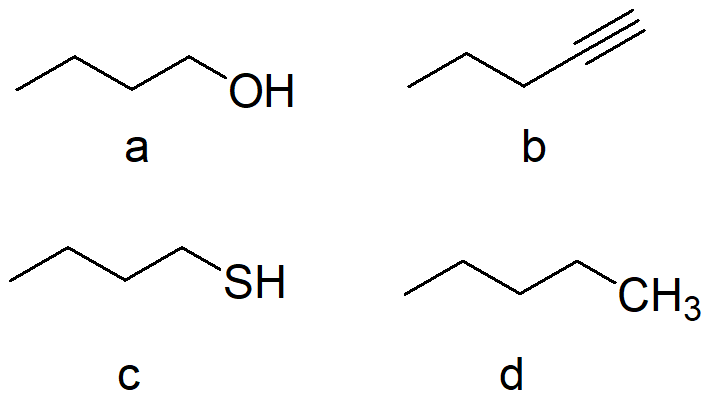
4. Disporre i seguenti composti in ordine di acidità decrescente (dal più acido al meno acido) e spiegare sinteticamente il perché:
5. Disporre i seguenti composti in ordine di basicità decrescente e spiegare sinteticamente il perché:
6. Scrivere la formula condensata e la formula molecolare del seguente composto: 2,2-dibromo-4-metilesano.
7. Scrivere e attribuire il nome IUPAC al composto di formula C9H18 che possiede solo idrogeni primari.
8. Dire se il seguente nome è corretto. Se non lo è, scrivere il nome IUPAC corretto.
1-bromo-3,4-dietilcicloesano
9. Disegnare il 4-(3-bromo-3-metilbutil)-2-terz-butil-1-etilcicloesano.
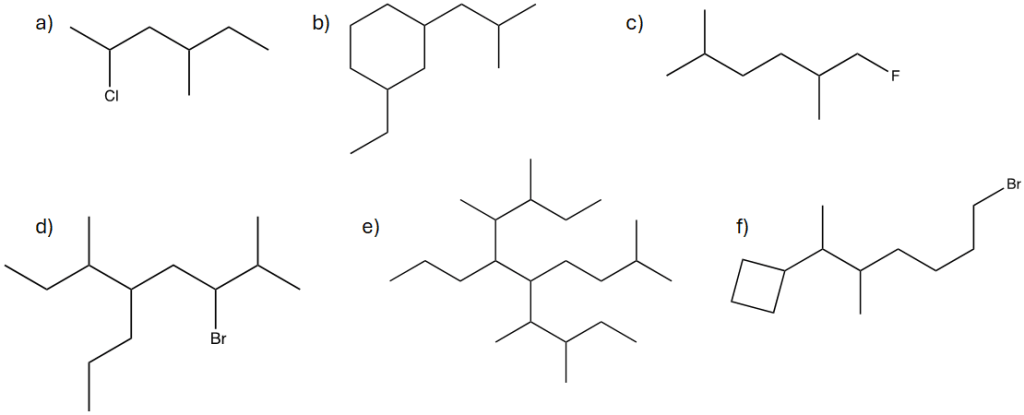
10. Denominare le seguenti molecole secondo le regole del sistema di nomenclatura IUPAC:
Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni a lezione, sia fare ricevimento (anche in gruppo)

Sono ora disponibili le soluzioni di molti degli esercizi precedentemente pubblicati.
Trovate le soluzioni (quando già disponibili) nei commenti ai post. Per visualizzarle/scaricarle dovete utilizzare la password comunicata a lezione.
Altre soluzioni (relative ai post più recenti) saranno caricate nei prossimi giorni. Per gli esercizi sulla nomenclatura, è possibile ricevere un feedback anche commentando i post per i quali non ci sono ancora le correzioni.
Avviso importante per gli esercizi di nomenclatura: nel caso in cui abbiate fatto riferimento anche ad esercizi vecchi, fate attenzione dato che le regole IUPAC aggiornate sono state prese in considerazione e introdotte gradualmente solo negli ultimi anni. In quel caso (per post relativi ai corsi degli anni accademici precedenti), non potete utilizzare i commenti ai post per vedere se avete svolto l’esercizio in maniera corretta!
Nel caso in cui non dovesse esservi chiara una correzione, potete rivolgervi alla docente a lezione, al ricevimento o (se necessario) via email.

Regolamento:
Anche questa settimana siamo alle prese con due isomeri geometrici (parleremo a breve di questo tipo di isomeria). Si tratta di composti diversi, in quanto, intorno al doppio legame non è possibile libera rotazione. Pur avendo entrambi due gruppi carbossilici e, la maggior parte delle caratteristiche strutturali in comune, essi sono caratterizzati da valori di pKa1 diversi (i valori sono riportati in figura). Fornire una spiegazione della diversa forza acida osservata per i due composti.
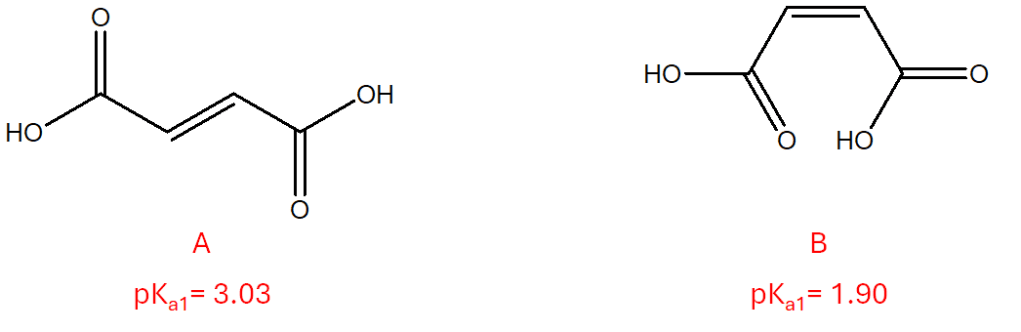

Proviamo a testare la nostra preparazione sulla nomenclatura di alcani, cicloalcani, alogenuri alchilici, alcoli, eteri, ammine
Al seguente link, troverete un TEST DI AUTOVALUTAZIONE. Avrete 1 ora per rispondere alle domande e alla fine potrete verificare il punteggio ottenuto e se avete risposto correttamente o meno. Questo form non sarà chiuso.
Dopo aver fatto il test di autovalutazione, nel seguente form sarà possibile esprimere i propri dubbi relativi alla nomenclatura. Sarà possibile rispondere a questo questionario fino alle 18 del 13/10. NB: non saranno presi in considerazione questionari compilati senza aver prima fatto il test di autovalutazione.
You must be logged in to post a comment.