Ricevimento

Dato che non sono più disponibili appuntamenti di ricevimento per la settimana prossima, chiunque volesse far ricevimento può prenotarlo mandando una mail alla docente
Università degli Studi della Campania "Luigi Vanvitelli"

Dato che non sono più disponibili appuntamenti di ricevimento per la settimana prossima, chiunque volesse far ricevimento può prenotarlo mandando una mail alla docente



1) Come si potrebbero sintetizzare i seguenti composti mediante una reazione tra un aldeide o un chetone e un reattivo di Grignard?
a) 2-pentanolo
b) 1-butanolo
c) 1-fenilcicloesan-1-olo
Mostrare i meccanismi di reazione
2) Trattando l’aldeide 4-idrossibutanale con metanolo in presenza di un catalizzatore acido (HCl), si ottiene il 2-metossitetraidrofurano (la cui struttura è qui riportata). Proporre un meccanismo per la reazione.

3) (R)-carvone è il principale componente dell’essenza di menta. Quali sono i prodotti attesi dalla reazione del carvone con i seguenti reagenti? a) HOCH2CH2OH, HCl; b) metanammina; c) 2 equivalenti H2, Pd/C; d) litio alluminio idruro, poi H3O+, e) bromuro di etilmagnesio, poi H3O+.

4) Il carbonio carbonilico del propanale viene attaccato dallo ione cianuro. Quale saranno gli orbitali HOMO e LUMO coinvolti nella reazione?
5) Mostrare le condizioni di reazione, il meccanismo e indicare i prodotti delle seguenti reazioni. Classificare i prodotti come immine o enammine

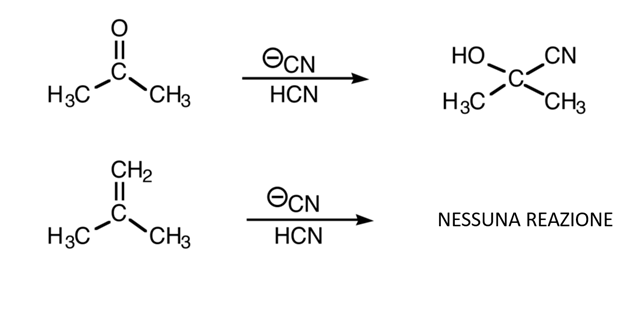
6) Spiegare perchè delle due reazioni mostrate in basso la prima avviene velocemente e la seconda non avviene
7) Quale composto carbonilico e quale alcol sono necessari per sintetizzare i seguenti composti?

8) Mostrare i prodotti ottenuti a partire dai seguenti composti posti in presenza di tracce di acido

9) Mostrare il meccanismo e scrivere il prodotto della seguente reazione
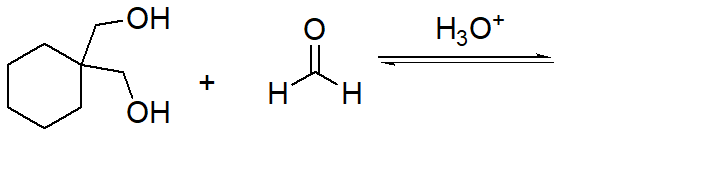
10) Proporre il meccanismo di idrolisi del composto formato nell’esercizio 9
11) Completare il seguente schema:
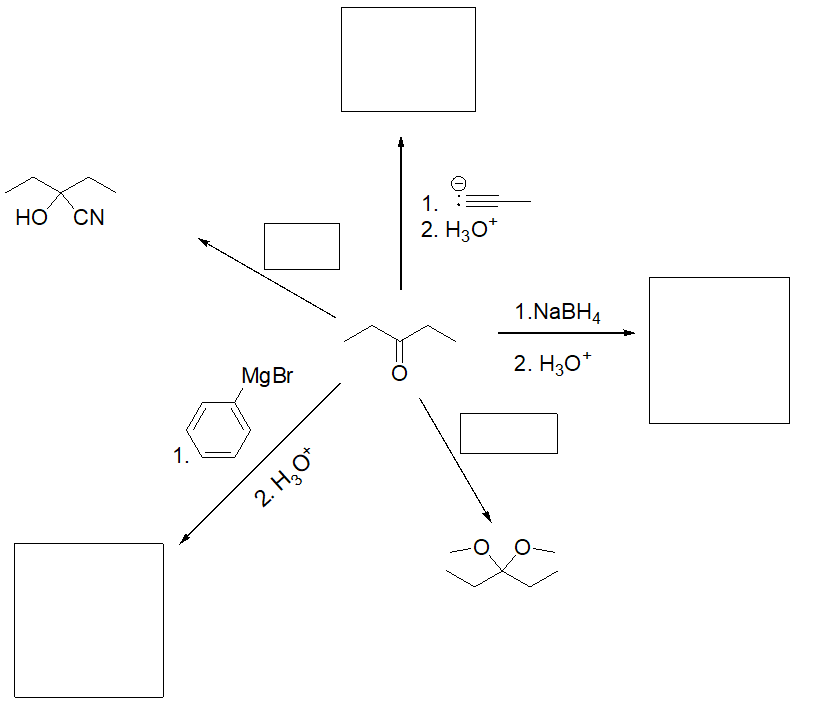
12. Scrivere i prodotti delle seguenti reazioni:

13) Come si potrebbe convertire l’acido butanoico nei seguenti composti?
a) 1-butanolo
b)1-bromobutano
c) acido pentanoico
d) 1-butene
Le trasformazioni potrebbero richiedere più passaggi.
Mostrare i meccanismi di reazione
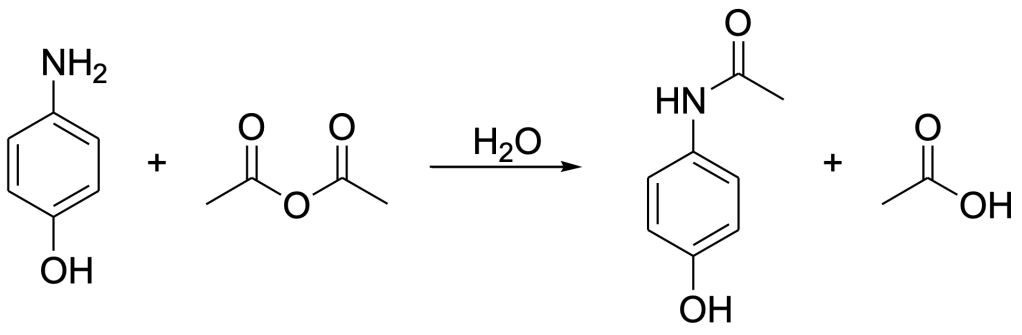
14) Il paracetamolo, N-(4-idrossifenil)acetammide, è un farmaco ad azione analgesica ed antipiretica molto utilizzato. Tachipirina ed Efferalgan sono i nomi commerciali più conosciuti dei farmaci che lo contengono. il paracetamolo può essere preparato per acetilazione selettiva del gruppo amminico del 4-amminofenolo con anidride acetica in H2O (vedi figura). Proporre il meccanismo di reazione utilizzato nella sintesi del paracetamolo a partire dal 4-amminofenolo
15) Completare il seguente schema:

16) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Indicare la stereochimica quando opportuno.

17) Scrivere i prodotti delle seguenti reazioni:
18) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Evidenziare la stereochimica quando opportuno.

19) Proporre una strategia per la sintesi della butanammide a partire da acido butanoico
20) Proporre una strategia per la sintesi di 1-butanammina a partire da 1-bromobutano

PRIMA DI SVOLGERE QUESTI ESERCIZI è NECESSARIO STUDIARE I CAP. 15 e 16 del Bruice
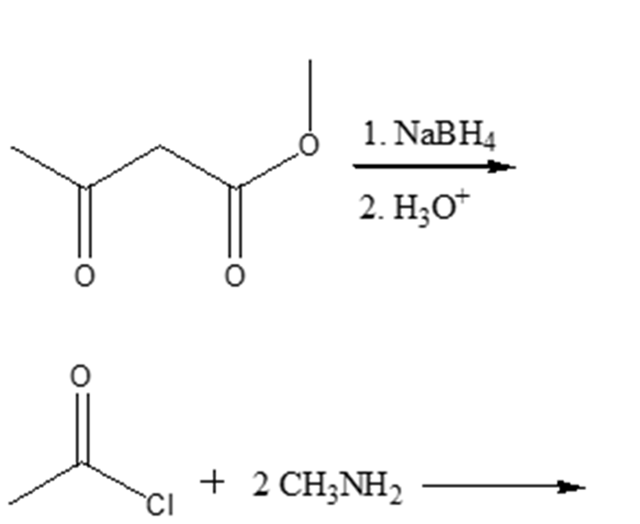
1) Indicare i prodotti della reazione dell’acetone (=propanone) e dell’acetato di etile con i seguenti composti (se la reazione avviene). Indicare le opportune condizioni di reazione e mostrare il meccanismo.
a) metanammina
b) dimetilammina
c) metanolo
d) bromuro di etilmagnesio
e) NaBH4
2) Indicare il reattivo di Grignard e il composto carbonilico opportuni per ottenere i seguenti alcoli. Quando sono possibili più strategie, mostrarle tutte. Mostrare il meccanismo e indicare la stereochimica dei prodotti, se opportuno.
a) 1-esanolo
b) 2-esanolo
c) 1-cicloesil-1-pentanolo
d) 1-etilcicloesan-1-olo
e) 2-ciclopentil-2-propanolo
Esercizi guida
3) Partendo da acido acetico (=acido etanoico) indicare le condizioni e il meccanismo di reazione (quando possibile) per ottenere i seguenti composti:
a) cloruro di acetile
b) anidride acetica
c) acetato di etile
d) N-metilacetammide
e) etanolo
f) 2-metil-2-propanolo
g) 2-metil-1-propanolo
h) etanale
i) (1R)-1-cicloesiletanolo + (1S)-1-cicloesiletanolo
l) 2-propanolo
m) (2R)-1-ammino-2-propanolo + (2S)-1-ammino-2-propanolo
n) 2-metil-4-penten-2-olo
o) 2-metil-1,2-propandiolo
p) 1,2-propandiolo
q) 1-bromo-1-etilciclopentano
r) etanoato di etile (utilizzando l’acido acetico come unica fonte di atomi di carbonio)
s) (3R)-3-bromo-3-metilesano + (3S)-3-bromo-3-metilesano
t) 3-etossi-3-metilpentano (utilizzando l’acido acetico come unica fonte di atomi di carbonio)
u) 2-eptanone
v) 2,2-dimetossipropano
z) (2S,3S)-3-metil-2-pentanolo + (2S,3S)-3-metil-2-pentanolo (utilizzando l’acido acetico come unica fonte di atomi di carbonio)
NB: per la sintesi di molti di questi composti sono necessari più passaggi (sintesi che richiedono numerosi passaggi non saranno oggetto della prova intercorso, ma potranno ovviamente essere oggetto dell’esame orale). Fare attenzione alla corretta sequenza di reazioni e alla reattività dei diversi gruppi funzionali nei confronti dei diversi reattivi. E’ possibile aggiungere fonti di atomi di C diverse dall’acido acetico, ammenochè non sia diversamente indicato nella traccia.
Esercizi guida
4) Mostrare come è possibile convertire l’1-bromobutano in:
a) 1-pentanolo
b) 3-eptanolo
c) 1-esanolo
d) 2-metil-2-esanolo
d) pentanammide
e) butanammide
5) Mostrare come è possibile ottenere il 2-metil-2-butanolo a partire dal 1-propanolo
6) Proporre un meccanismo per le seguenti trasformazioni:


Di seguito il risultato della votazione di oggi

Visto che l’87% dei votanti si è detto favorevole, saranno effettuate le modifiche proposte.
Dunque:
La lezione del 20 è anticipata a venerdì 13. Faremo, quindi, lezione di chimica organica dalle 9 alle 13 (con un’ampia pausa tra le prime due ore e il resto della lezione).
Le lezioni del 16 e del 18 restano invariate.
La prova intercorso si terrà il giorno 20 dicembre, dalle 9 alle 11.
Qui è possibile scaricare la lista degli argomenti oggetto della prova intercorso: https://www.dropbox.com/scl/fi/xldgns31j2falxrx27fov/Argomenti-ultima-prova.pdf?rlkey=gcq76vjdwykdjcycvl238i48z&st=8ezsu021&dl=0 per chi non era a lezione, si consiglia di visionare la legenda presente nella seconda pagina. Per chi era a lezione, si consiglia comunque di visionare questa versione, che è stata attentamente revisionata. Qualsiasi dubbio potrà essere sciolto venerdì nel corso della lezione.



Come discusso stamattina a lezione, si propone la seguente variazione di orario.
Premesso che mancano 4 lezioni, ovvero 8 ore alla fine del corso (e che OVVIAMENTE le utilizzeremo tutte), al fine di potervi permettere di affrontare la prova intercorso con maggiore tranquillità, si propone la seguente variazione:
La lezione del 20 è anticipata a venerdì 13 (avendo ricevuto conferma dalla docente di Anatomia del fatto che non farà lezione questo venerdì). Faremo, quindi, lezione di chimica organica dalle 9 alle 13 (con un’ampia pausa tra le prime due ore e il resto della lezione).
Le lezioni del 16 e del 18 restano invariate.
La necessità di dedicare del tempo, nell’ambito di queste lezioni, ad una esercitazione sarà valutata sulla base di form che saranno condivisi con voi nei prossimi giorni.
Nel caso in cui approviate questa variazione di orario, la prova intercorso si terrà sempre il giorno 20, ma dalle 9 alle 11 (nel corso di quello che sarebbe stato l’orario di lezione).
La decisione sarà presa a maggioranza, per cui chiedo a tutti di votare utilizzando il form qui sotto:
https://forms.office.com/e/qwRxb0QXuT
Nel caso in cui i voti sfavorevoli fossero più abbondanti di quelli favorevoli, l’orario resterebbe invariato con lezioni dalle 9 alle 11 nei giorni 13, 16, 18, 20 e con la prova intercorso nel pomeriggio del 20 con inizio da definire sulla base della disponibilità delle aule (molto probabilmente, ore 16:00, data l’indisponibilità di aule prima di quell’orario).
Sarà possibile votare fino alle 21:00 di questa sera.
In serata sarà pubblicato anche il programma dettagliato degli argomenti oggetto della prova intercorso (che è stato già mostrato stamattina a lezione).
L’esercitazione comprenderà esercizi relativi a:
-reazioni di sostituzione ed eliminazione di ALOGENURI ALCHILICI e alcoli, eteri, epossidi, etc. con particolare attenzione agli aspetti stereochimici
-Per le reazioni di sostituzione ed eliminazione, si andranno ad analizzare i metodi per capire quali sono i prodotti e quali sono i prodotti principali di una reazione (e di conseguenza come capire se avviene sostituzione, eliminazione o entrambe)
-Sintesi di Williamson degli eteri
-Apertura dell’epossido
-analisi retrosintetica per sintesi che prevedono l’utilizzo di più reazioni consecutive
Se avete dubbi su argomenti diversi da quelli sopra siete invitati a compilare il form che si chiuderà a breve oppure dovrete farlo presente domani all’esercitazione.
La nomenclatura non sarà oggetto dell’esercitazione, dato che solo 2 persone hanno risposto al form. Nel caso in cui la partecipazione così esigua sia dovuta al fatto che tutte le regole sono chiare, non si terrà nessuna esercitazione in merito. Se, invece, è una conseguenza del fatto che non avete ancora provveduto a studiare questi argomenti, l’esercitazione sarebbe assolutamente inutile, per cui in tal caso si provvederà a fare un’esercitazione ulteriore nel corso della prossima settimana. Ne parleremo domani a lezione.



Qui è possibile scaricare:
a) Schema relativo alle reazioni dei derivati degli acidi carbossilici*
b) Schema relativo alle reazioni degli acidi carbossilici con i nucleofili al carbonio e con gli idruri*
c) Linee guida per la sintesi multistadio e l’analisi retrosintetica (con focus su analisi retrosintetica dei prodotti di condensazione di composti carbonilici).
*Per i meccanismi e le specifiche condizioni di reazione, si rimanda al libro
NB: per ora, vi interessa solo il punto a); i punti b e c riguardano argomenti non ancora affrontati a lezione
You must be logged in to post a comment.