Esercitazione su analisi conformazionale, isomeri geometrici di cicloalcani e proprietà fisiche dei composti organici

1. Quale dei seguenti composti sarà più solubile in acqua? Spiegare perchè
I) dietiletere
II) 1-butanolo
III) butano
2. Ordina i seguenti alcani secondo il punto di ebollizione crescente

3. Ordina i seguenti alcani secondo il punto di ebollizione crescente:
I) esano
II) ottano
III) 2-metilpentano
IV) 2,2-dimetilbutano
4. Metti i seguenti composti in ordine di solubilità crescente in acqua:

5. Disporre i seguenti composti in ordine di solubilità crescente in acqua. Indicare l’ordine inserendo i numeri nei riquadri sotto le strutture: 1= il meno solubile, 4= il più solubile

6. Disporre i seguenti composti in ordine di punto di ebollizione crescente. Indicare l’ordine inserendo i numeri nei riquadri sotto le strutture: 1= p.eb. più basso, 4= p.eb. più alto

7. Le vitamine sono spesso distinte in idrosolubili e liposolubili. Di seguito è riportata la struttura di tre vitamine. Sapresti dire, sulla base delle caratteristiche strutturali, per ciascuna struttura, se si tratta di una vitamina lipo- o idrosolubile?

8. Scrivere tutti gli alcani di formula molecolare C7H16 e prevedere quale ha il punto di ebollizione più alto e quale il punto di ebollizione più basso. Motivare la risposta.
9. Quale dei due composti ha punto di ebollizione maggiore: 1-bromopentano o 1-bromoesano? Perchè? Quali interazioni intermolecolari intervengono?
10. Quale dei due composti ha punto di ebollizione maggiore: 1-esanolo o 1-metossipentano? Perchè?
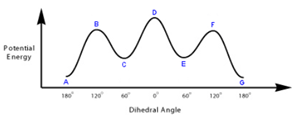
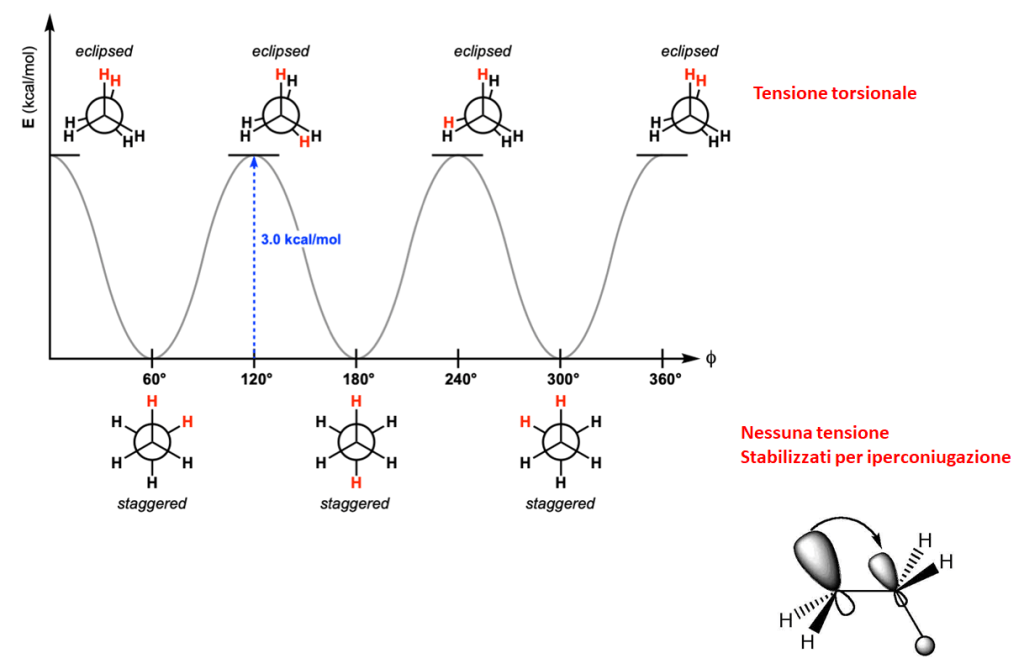
11. Il seguente grafico mostra la variazione di energia torsionale del propano in seguito alla rotazione intorno al legame C-C. Cosa indicano I, II, III?

12. Disegnare i conformeri anti e gauche del 1,2-dibromoetano usando sia le proiezioni di Newman sia le strutture a cavalletto.
13. Quale tra i due conformeri dell’esercizio 12 avrà momento dipolare maggiore?
14. Quale tra i seguenti è il conformero più stabile del 3-metil-1-butanolo?
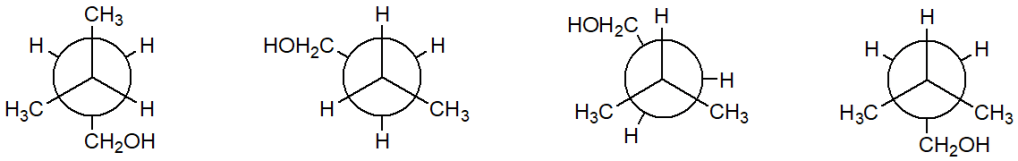
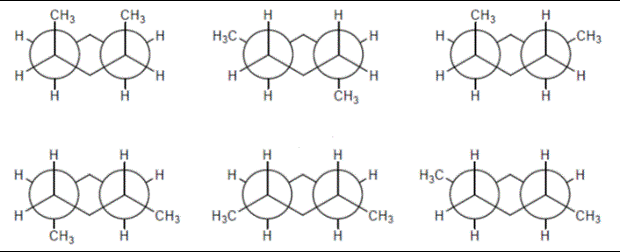
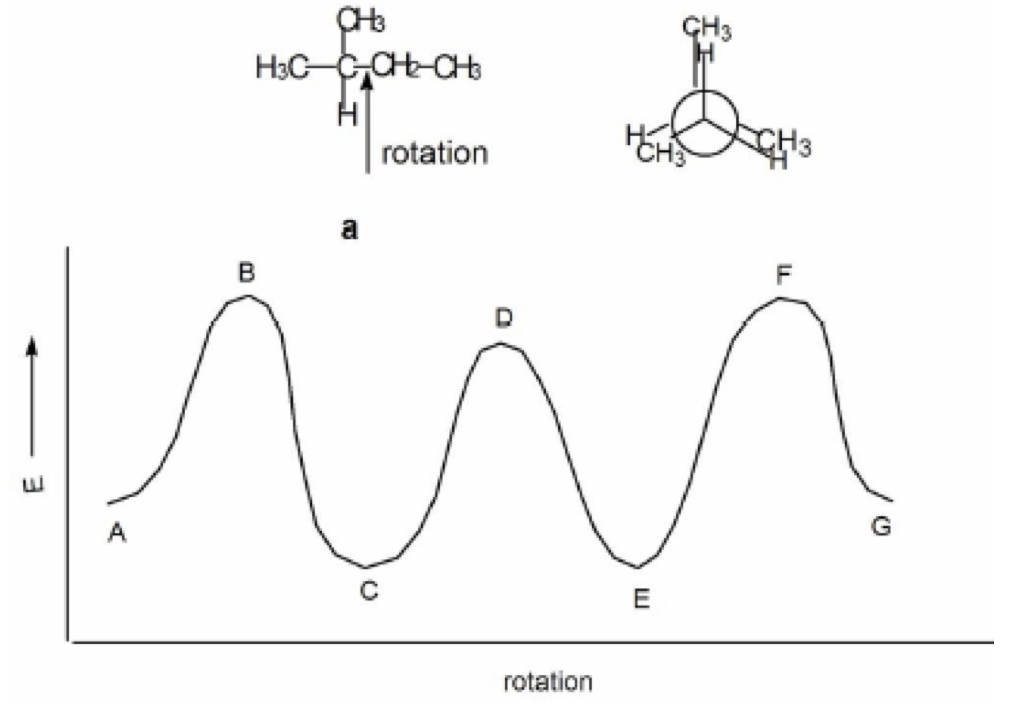
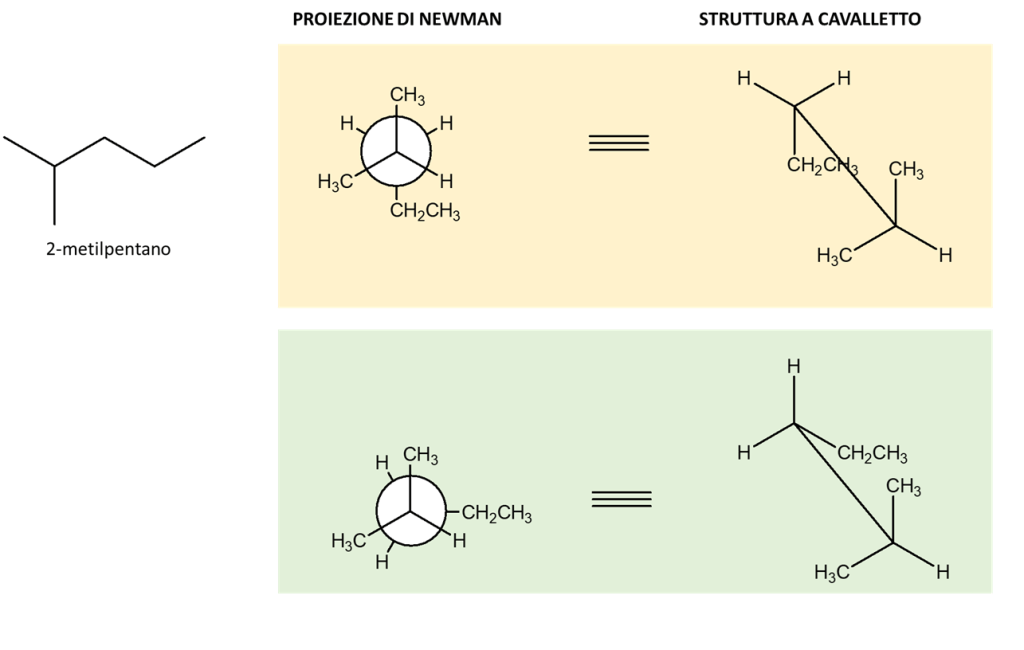
15. Cerchiare quella che, tra le seguenti, è la conformazione meno stabile del 2-metilpentano e spiegare quali sono i fattori che la rendono tale:

16. Cerchiare quella che, tra le seguenti, è la conformazione meno stabile del 2-metilpentano e spiegare quali sono i fattori che la rendono tale:

17. Cerchiare quella che, tra le seguenti, è la conformazione più stabile del 2-metilpentano e spiegare quali sono i fattori che la rendono tale:

18. Disegnare il cis-1-isopropil-4-metilcicloesano in proiezione di Newman (rispetto ai legami C1-C6 e C3-C4). Effettuare l’inversione d’anello. Indicare qual è tra i due il conformero a più alta energia e spiegare perchè individuando le interazioni che lo rendono meno stabile rispetto all’altro (Potrebbe essere utile rivedere i paragrafi 3.14 e 3.15).
19. Scrivere le strutture a sedia che corrispondono ai due conformeri dell’esercizio 18.
20. Scrivere le formule di struttura per le due conformazioni a sedia del cis-1-isopropil-4-metilcicloesano. b) Le due conformazioni sono equivalenti? c) In caso negativo, spiegate quale sia la più stabile. d) Qual è la conformazione preferita all’equilibrio?
21. Scrivere i due isomeri geometrici (=isomeri cis/trans) del 1,4-dimetilcicloesano. Poi, per ciascun isomero geometrico disegnare le due conformazioni a sedia possibili e valutare la stabilità relativa delle due conformazioni a sedia di ciascun isomero geometrico.
22. Dalla tabella che riporta le costanti di equilibrio per i cicloesani monosostituiti (tabella 3.9 del Bruice) si evince che le costanti per gli alogeni sono le seguenti: F 1.5; Cl 2.4; Br 2.2; I 2.2. Fornire una spiegazione plausibile di questi dati sperimentali.
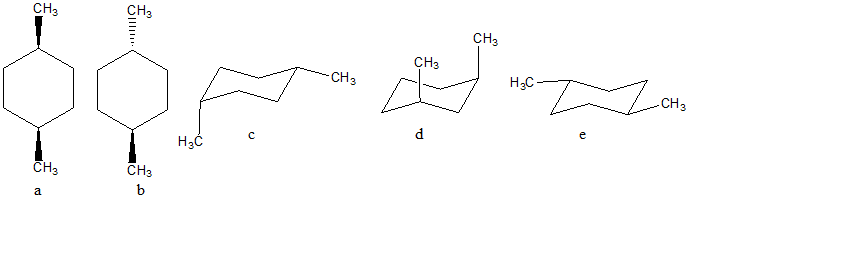
23. Dire se le seguenti coppie di composti sono: isomeri costituzionali, isomeri geometrici (=isomeri cis/trans), isomeri conformazionali o composti diversi:

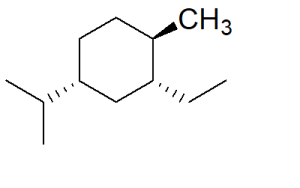
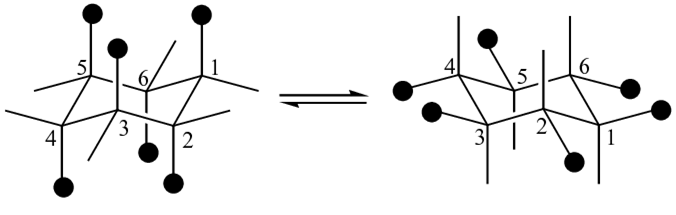
24. Completare la tabella per il seguente composto, disegnando quanto richiesto:

| Conformero a sedia più stabile | Conformero ottenuto in seguito all’inversione di anello |
| Proiezione di Newman secondo i legami C1-C2 e C5-C4 del conformero pù stabile | Proiezione di Newman secondo i legami C1-C2 e C5-C4 ottenuta in seguito all’inversione di anello |
25. Scrivere gli isomeri conformazionali dei seguenti composti A e B, completando le proiezioni di Newman (secondo i legami C3-C2 e C5-C6) e le rappresentazioni a sedia (NB: i numeri 1 e 2 non hanno nulla a che vedere con la numerazione relativa alla nomenclatura).
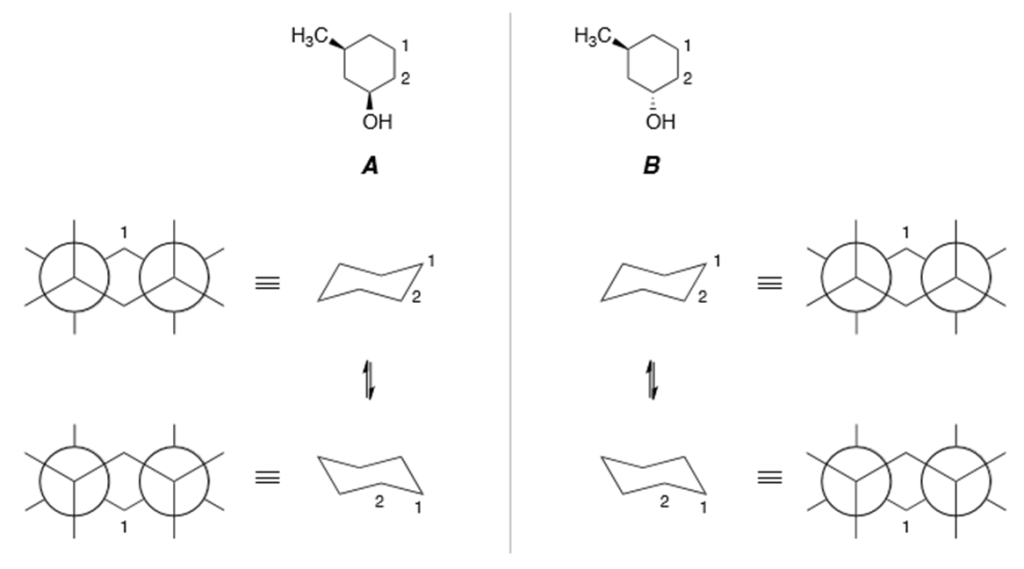
26. Prendendo in considerazione le strutture dell’esercizio 26,
a) per ciascun isomero geometrico, dire quale è la conformazione più stabile, motivando la scelta
b) dire chi è più stabile tra A e B, motivando la scelta.
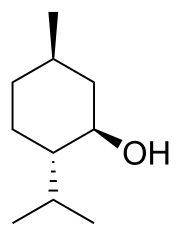
27. Completare la seguente tabella:
| Composto | Conformazione a sedia più stabile | Inversione d’anello | Proiezione di Newman | Inversione d’anello |
| 1,1-dimetilcicloesano | Legame C1-C2; C5-C4 | |||
| cis-1,2-dimetilcicloesano | Legame C2-C1; C4-C5 | |||
| trans-1,2-dimetilcicloesano | Legame C1-C2; C5-C4 | |||
| cis-1,3-dimetilcicloesano | Legame C2-C3; C6-C5 | |||
| trans-1,3-dimetilcicloesano | Legame C2-C3; C6-C5 | |||
| cis-1,4-dimetilcicloesano | Legame C2-C1; C4-C5 | |||
| trans-1,4-dimetilcicloesano | Legame C1-C2; C5-C4 |
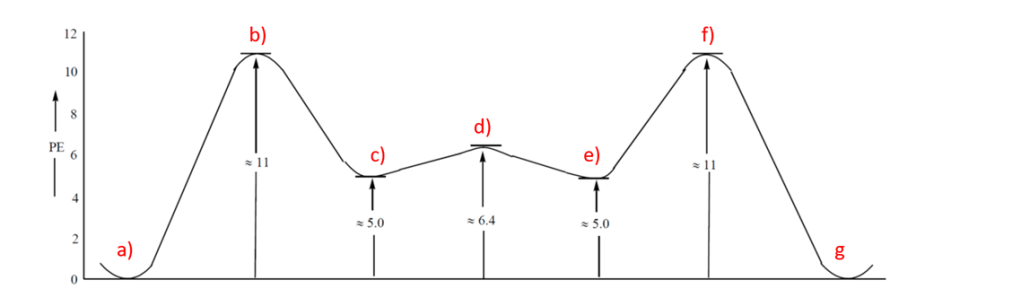
28. Disegnare un diagramma di energia potenziale per la rotazione di 360° del legame C2-C3 del 2-metilbutano, partendo da uno dei conformeri più stabili e disegnando tutte le conformazioni corrispondenti ai massimi e ai minimi di energia
29. Disegnare un diagramma di energia potenziale per la rotazione di 360° del legame C2-C3 del 2-metilbutano, partendo da uno dei conformeri meno stabili e disegnando tutte le conformazioni corrispondenti ai massimi e ai minimi di energia.
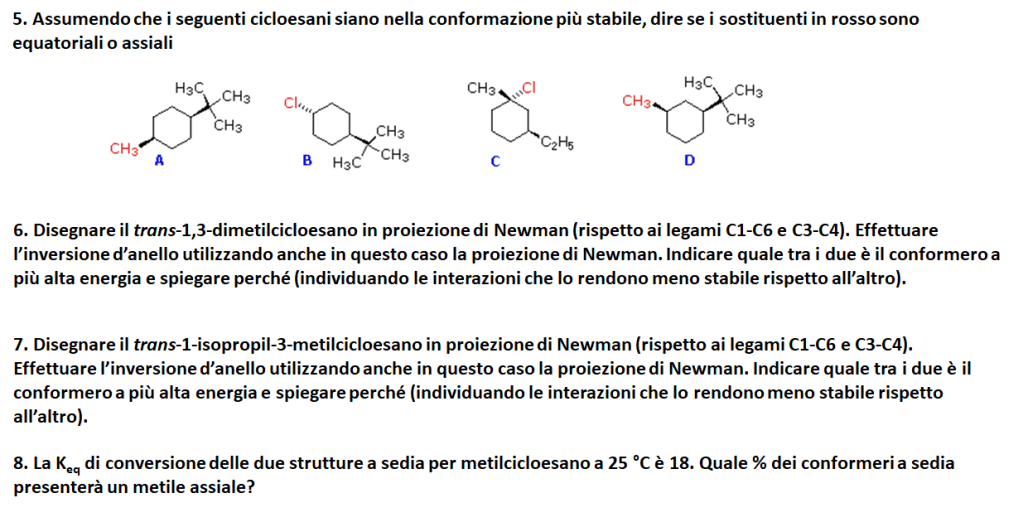
30. Esistono 4 combinazioni cis/trans per l’1,2,4-trimetilcicloesano. a) Disegnare le due possibili conformazioni della sedia per ciascuna struttura e determinare quale sia la conformazione a sedia più stabile. b) Confrontando le conformazioni a sedia più stabili per ciascuna struttura, quale dei 4 isomeri sarebbe più stabile?




















You must be logged in to post a comment.