PROVA SCRITTA DI LUGLIO

Corso di Laurea Magistrale in Farmacia
Prova scritta di Chimica Organica 22/7/2024
Cognome, Nome____________________________________ Matricola__________________
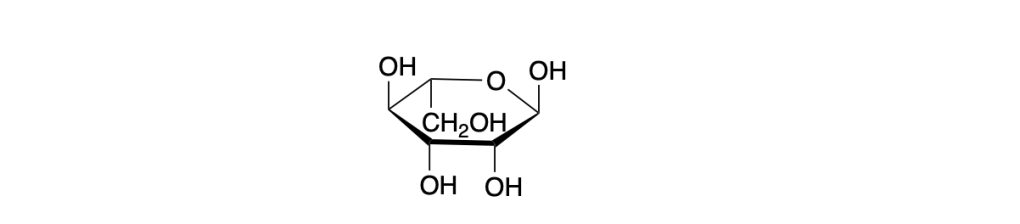
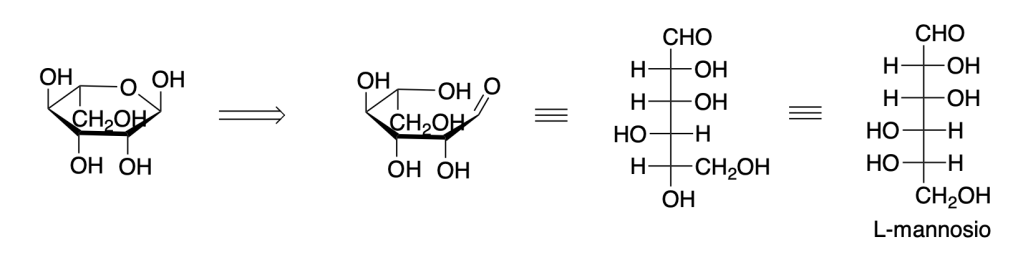
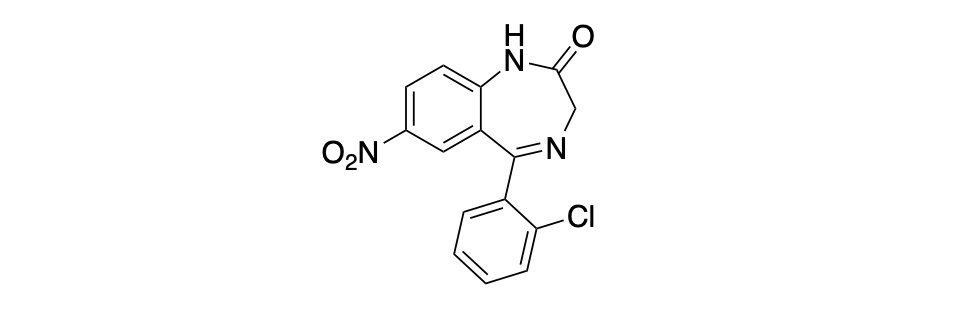
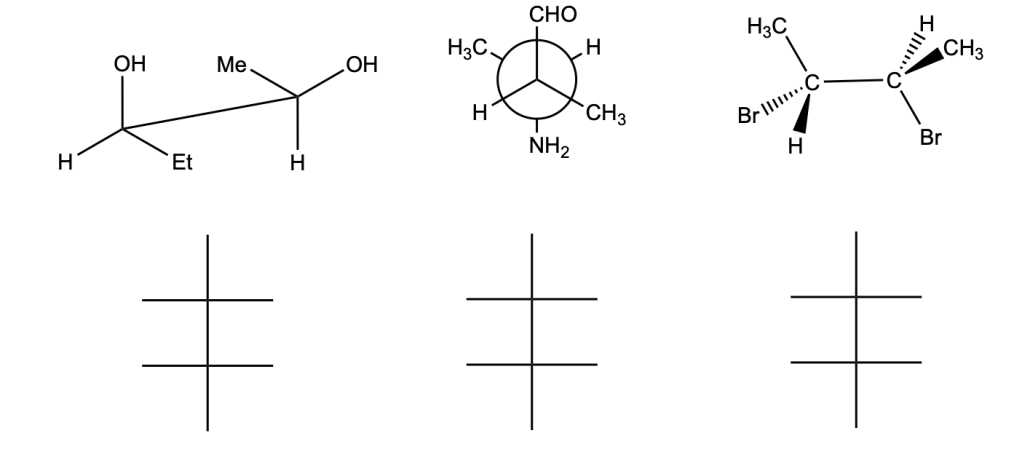
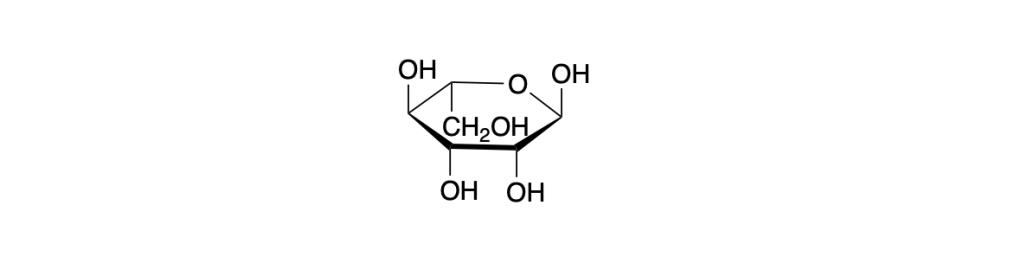
1. Trasformare le strutture in alto in proiezioni di Fischer ed assegnare la configurazione assoluta ai carboni chirali. (2 pt)

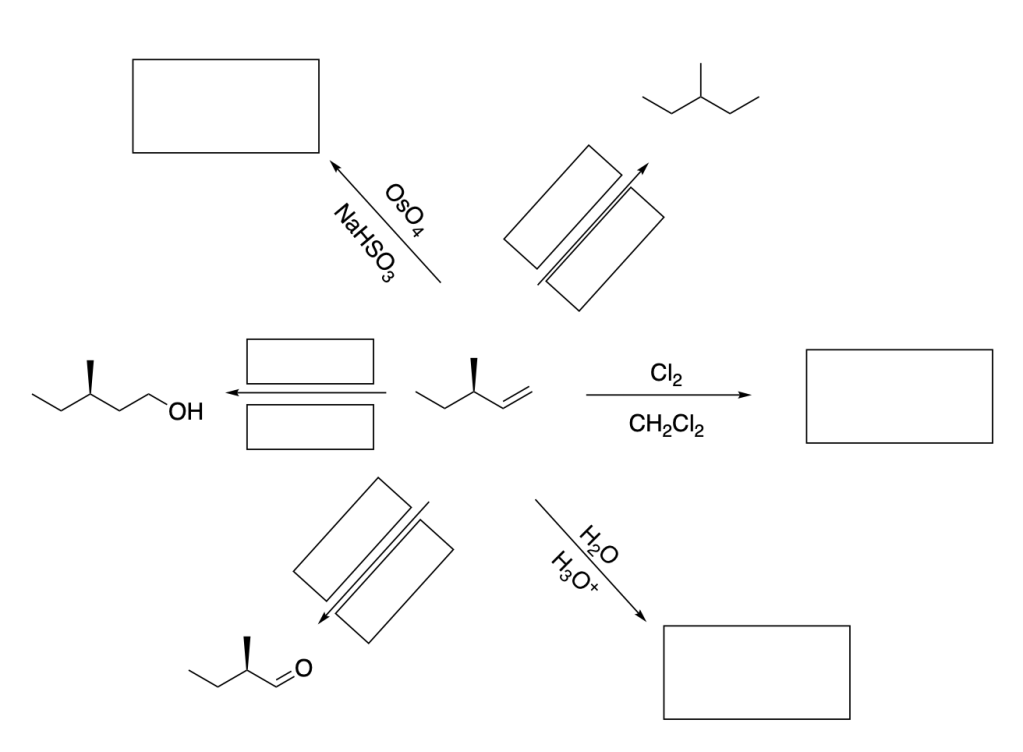
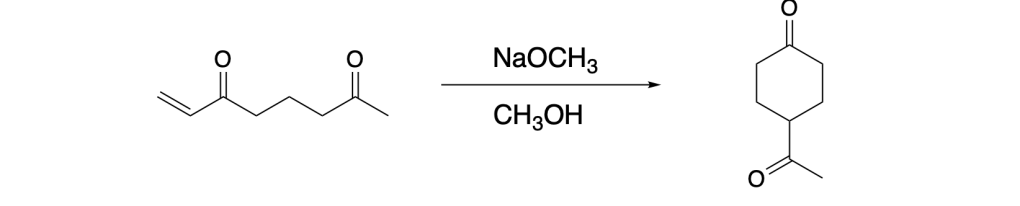
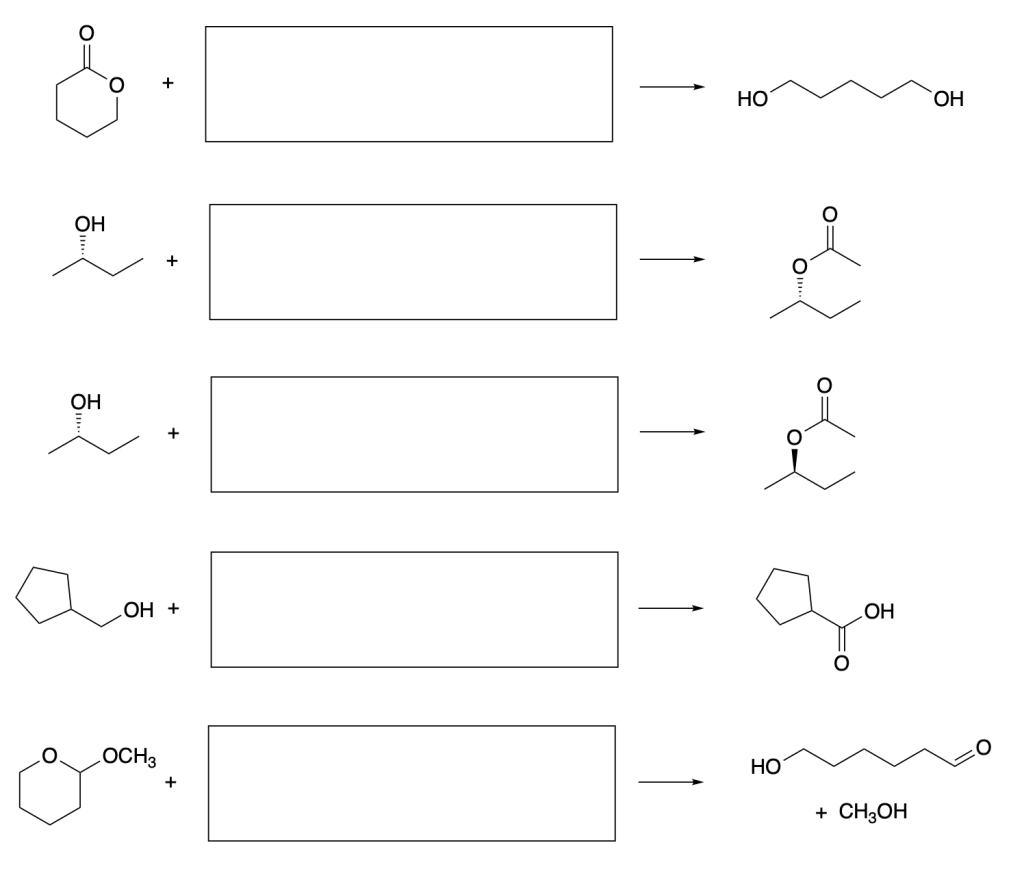
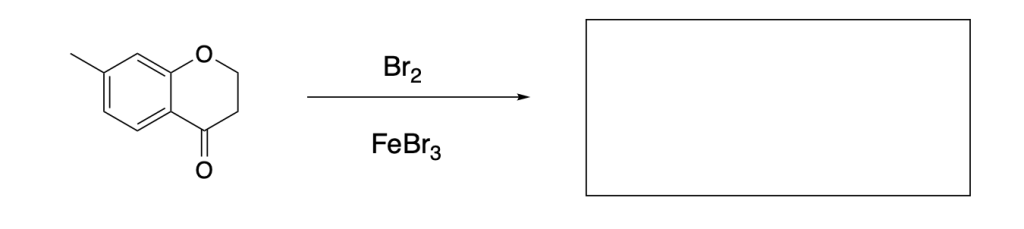
2. Scrivere il prodotto principale (o i prodotti principali) o i reagenti necessari per le seguenti trasformazioni. (6 pt)
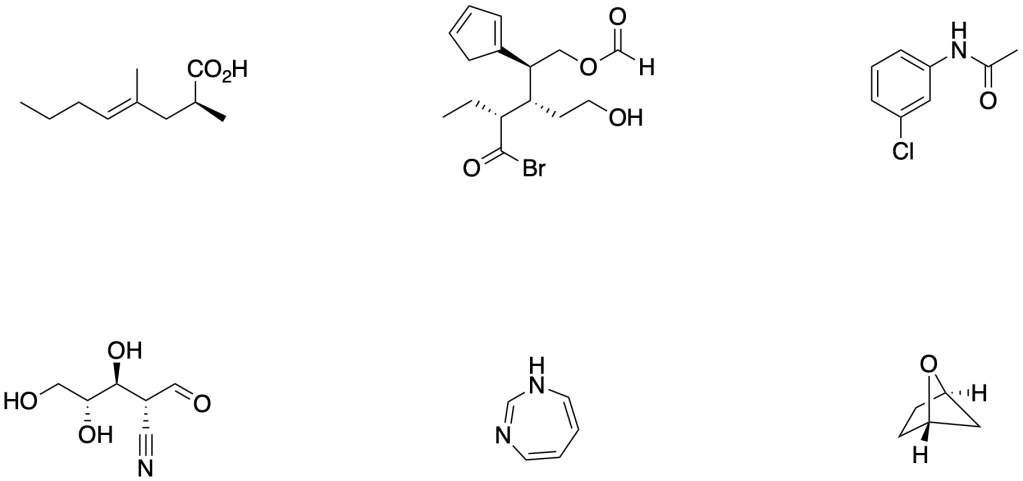
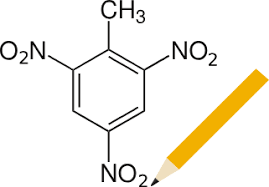
3. scrivi il nome IUPAC dei seguenti composti specificando la stereochimica (3 pt)

4. Disegna le proiezioni di Fischer dei prodotti formati per reazione del D-galattosio (epimero in 4 del glucosio) con (a) HNO3 e (b) AgNO3 in NH3, H2O (reazione di Tollens). Indicare se ciascun prodotto è otticamente attivo o inativo. (3 pt)
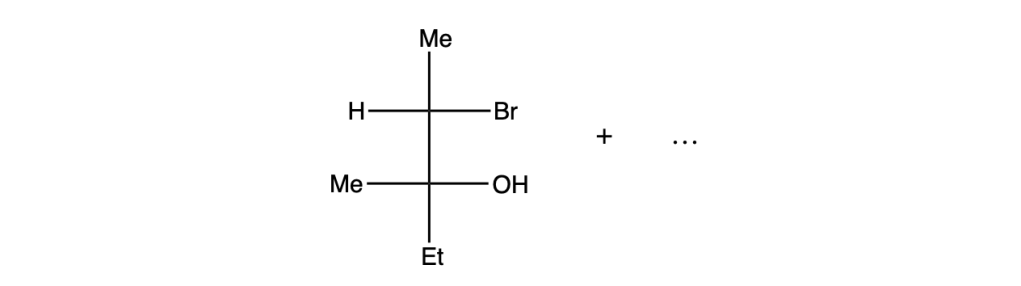
5. Scrivere le condizioni di reazione sulle frecce e illustrare i due diversi meccanismi di eliminazione dell’1-bromo 1,2-dimetilicloesanolo. (7 pt)

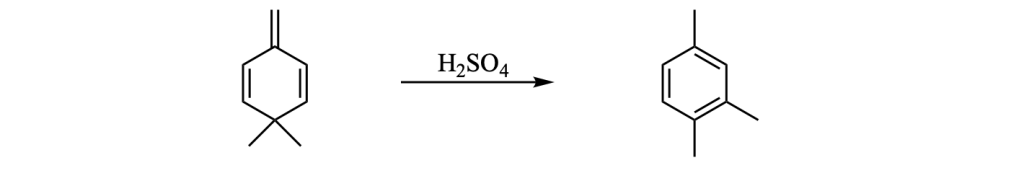
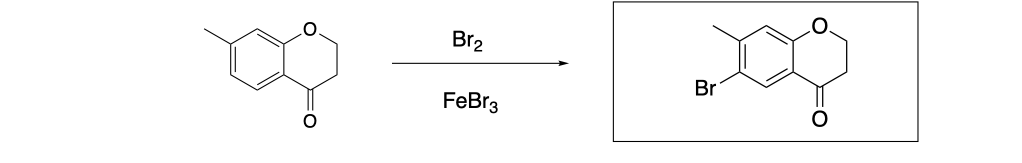
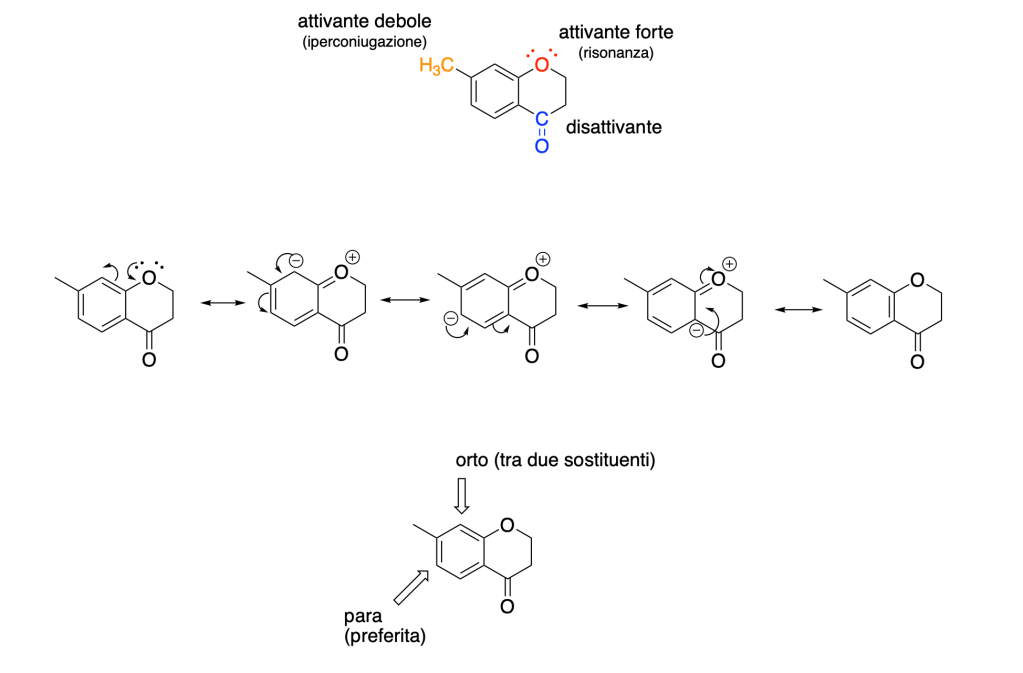
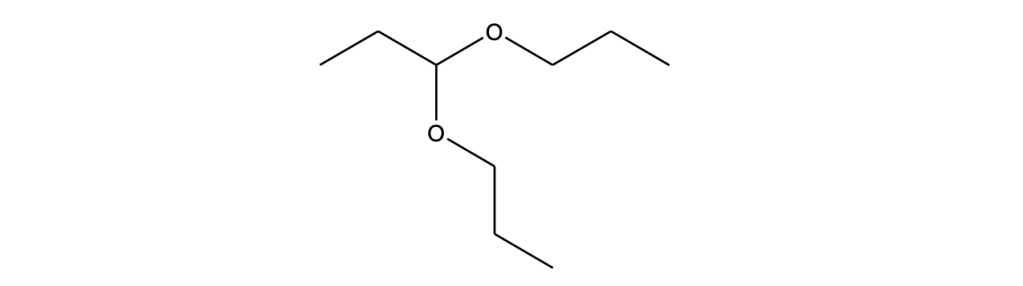
6. Proporre un meccanismo per la seguente reazione: (3 pt):
7. La meclizina è un antiemetico. Essa può essere prodotta attraverso la seguente serie di reazioni. (6 pt)

Proporre i reagenti degli stadi A-F, indicando il tipo di reazione che avviene in ogni stadio.






























You must be logged in to post a comment.