Esercitazione per la prova scritta (IV)

Suggerimento: per poter usare questi set di esercizi come test di autovalutazione, svolgerli senza l’ausilio di libro/appunti ed impiegando un tempo massimo di 2 ore per ciascun set.
PRIMO SET
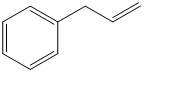
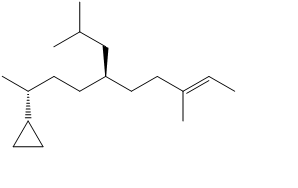
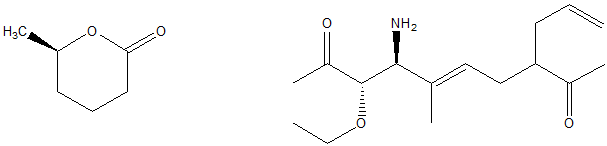
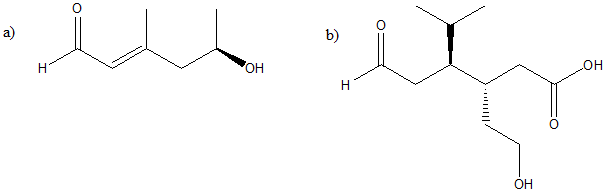
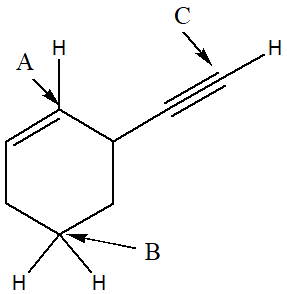
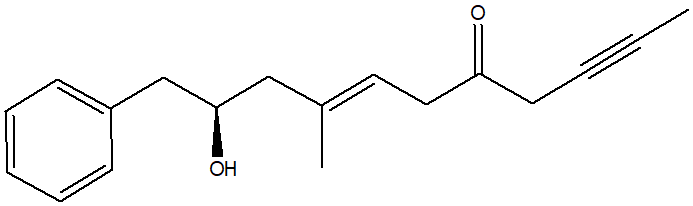
1. Attribuire il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
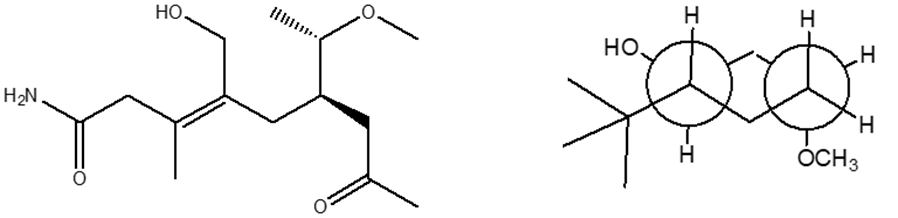
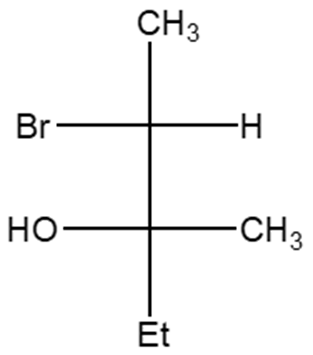
2) Scrivere, in proiezione di Fischer, il (2R,3R)-2-bromo-3-metil-2-esanolo
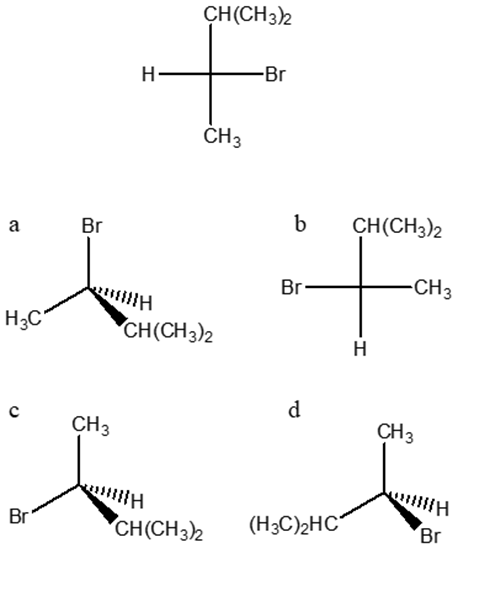
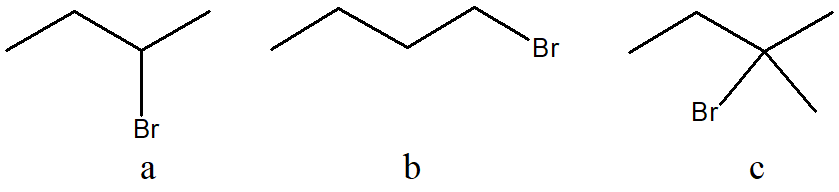
3) Stabilire le configurazioni assolute dei carboni chirali e dire qual è la relazione esistente tra i seguenti composti (enantiomeri/diastereoisomeri/stesso composto/isomeri costituzionali/altro).

a e b sono________________________________
a e c sono________________________________
b e c sono________________________________
4) Completare la seguente struttura di Lewis e calcolare la carica formale per gli atomi di carbonio, azoto e ossigeno. Attenzione: se è possibile avere più strutture di risonanza, scegliere una di quelle che contribuiscono di più all’ibrido di risonanza
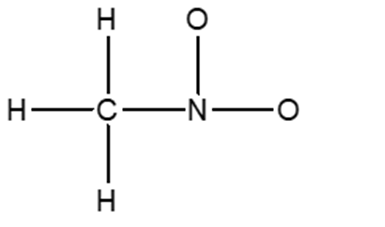
5) Cerchiare la/le molecola/e che ha/hanno momento dipolare nullo

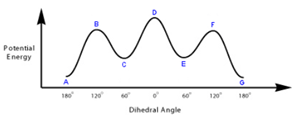
6) Quello riportato di seguito è il diagramma delle variazioni di energia potenziale rispetto all’angolo diedro per l’1,2-dibromoetano.
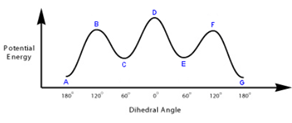
a) A cosa corrispondono B,D,F?
b) Disegnare le proiezioni di Newman di tutti i conformeri sfalsati, indicandoli con la lettera corrispondente sul grafico c) Discutere dei fattori che giustificano la minore energia potenziale dei conformeri più stabili.
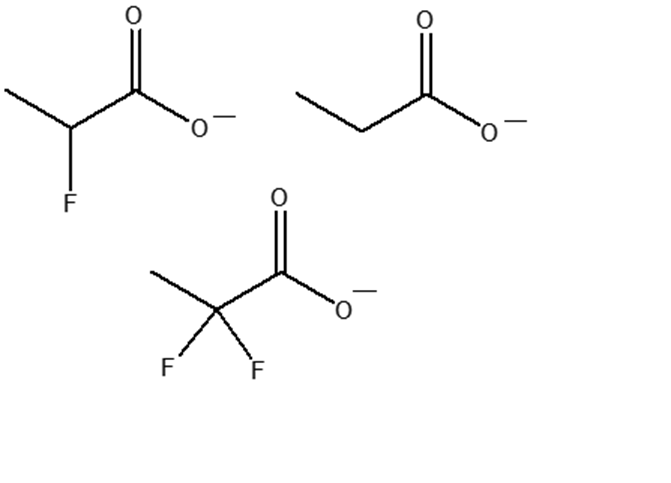
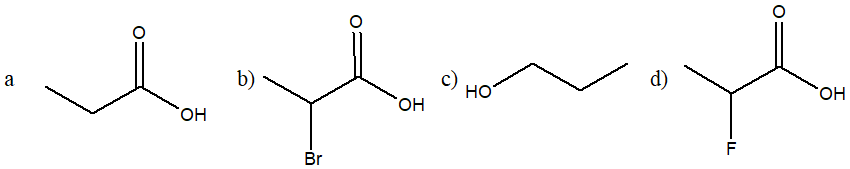
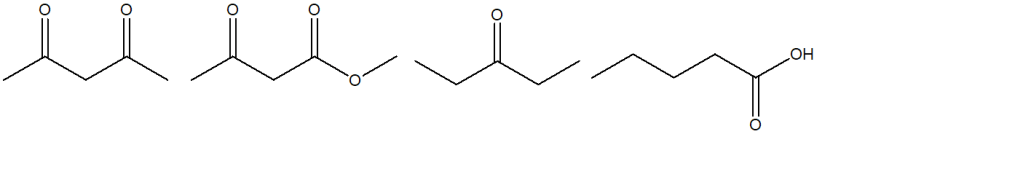
7) Disporre i seguenti composti in ordine di acidità decrescente (dal più acido al meno acido) e spiegare sinteticamente il perché:
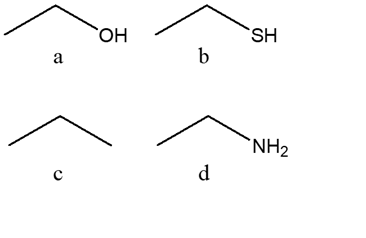
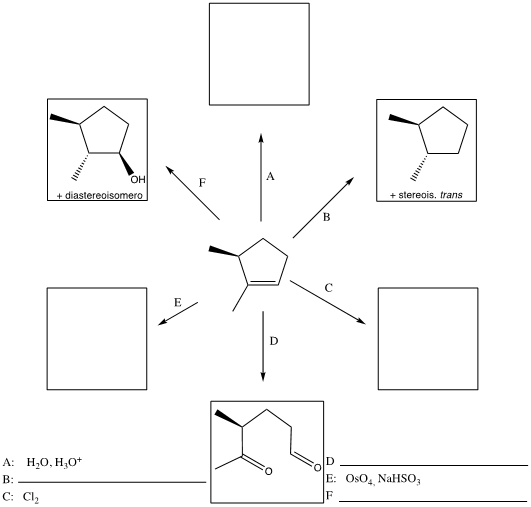
8) Indicare le condizioni ottimali per ottenere ciascuno dei seguenti composti a partire dal 2-metil-2-butene. Se quello ottenuto non è l’unico prodotto di reazione, indicare gli ulteriori altri prodotti formati, dire in che relazione sono col prodotto riportato e indicare se si formano o meno in quantità equimolari rispetto a quest’ultimo. NB: se non si formano ulteriori prodotti, scrivere “nessuno” nella casella dedicata.

9) Scrivere i prodotti delle seguenti reazioni
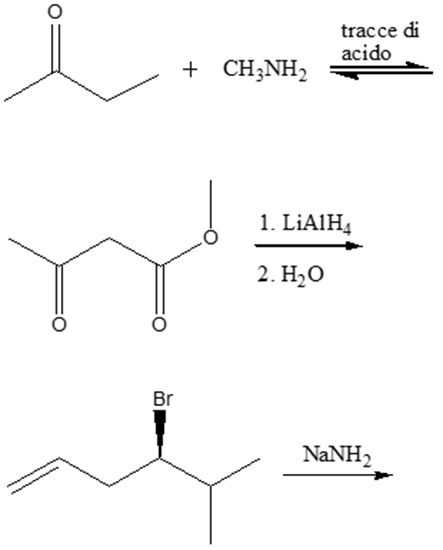
10) Mostrare il meccanismo della prima reazione dell’esercizio 9
SECONDO SET
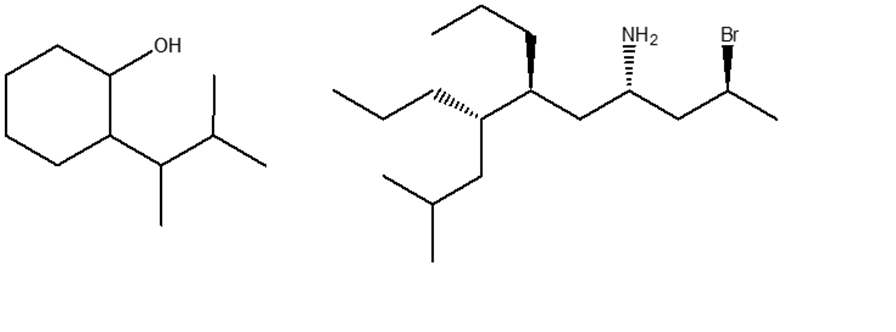
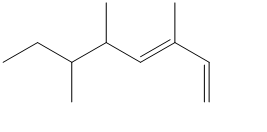
1. Attribuire il nome IUPAC, comprensivo di stereochimica (se esplicitata nella struttura), ai seguenti composti:
2. Scrivere la formula condensata di un isomero strutturale del 2,3-dimetilpentano
3. La struttura di seguito riportata è quella della chinina. Osservare gli atomi e i legami indicati da lettere e numeri e completare le seguenti frasi o rispondere alle seguenti domande

I) Le coppie solitarie dell’atomo di ossigeno a si trovano in orbitali_______; quella dell’atomo di azoto b si trova in un orbitale_______
II) Osservare il legame indicato dalla c e indicare il tipo di orbitale/i molecolare/i:
III) Quali orbitali atomici si sovrappongono per formare il legame c?
IV) Qual è il legame più corto tra quelli indicati dai numeri da 1 a 4?
4) Cerchiare la base più debole e motivare sinteticamente la scelta.
5) Quali dei seguenti composti è otticamente attivo? NB: è possibile scegliere più opzioni
a) (3R,4S)-3,4-dibromoesano
b) (2R,3S)-2,3-dibromopentano
c) (2R,3R)-2,3-dibromobutano
d) (1S,2R)-1,2-diclorociclopentano
6) Qual è il numero massimo di stereoisomeri per il seguente composto?

7) Partendo dall’opportuno alchene, illustrare il meccanismo di reazione della sintesi del seguente composto. Indicare eventuali altri prodotti fornendo per tutti il nome IUPAC completo di stereochimica.
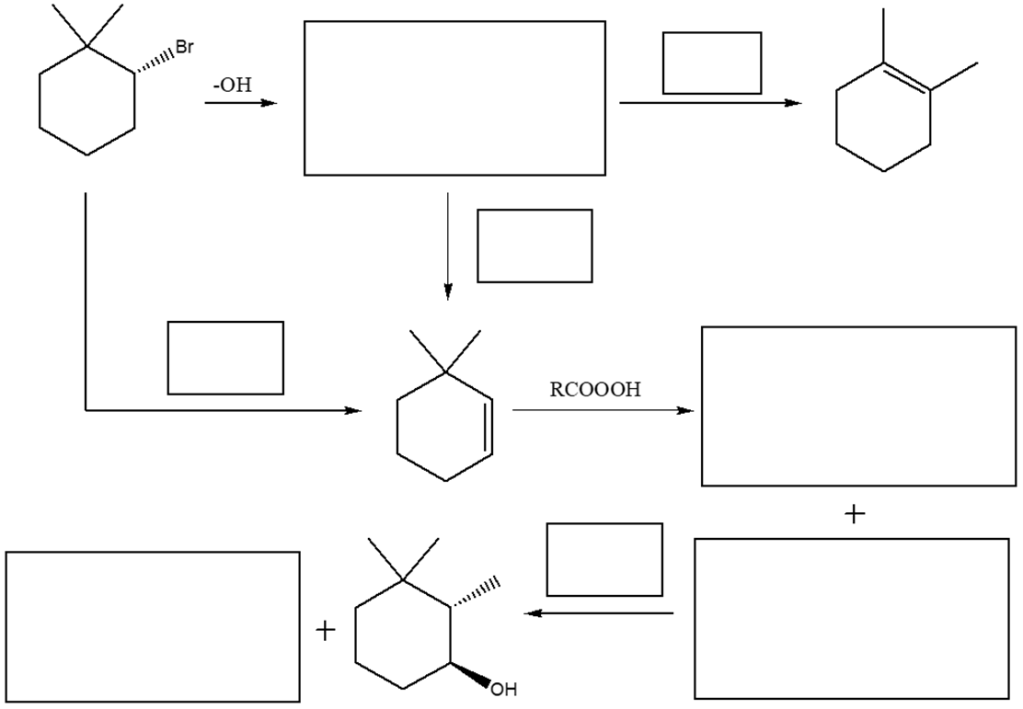
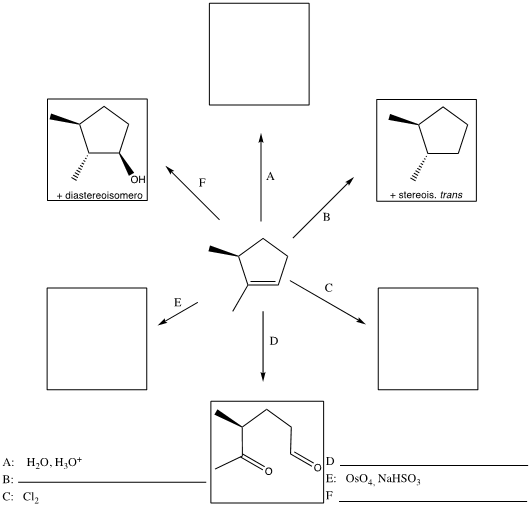
8) Completare il seguente schema inserendo le condizioni di reazione o i prodotti mancanti nei riquadri. Evidenziare la stereochimica quando opportuno.
9) Scrivere il D-glucopiranosio
TERZO SET
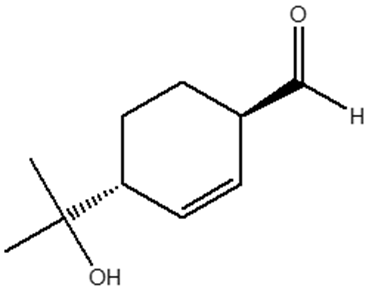
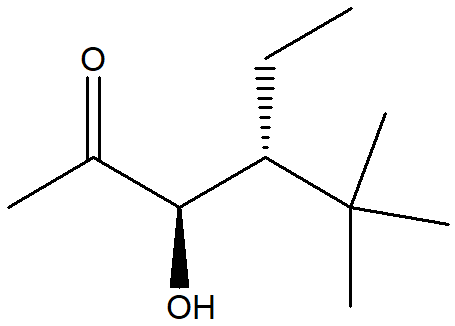
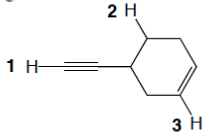
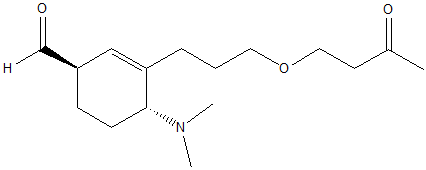
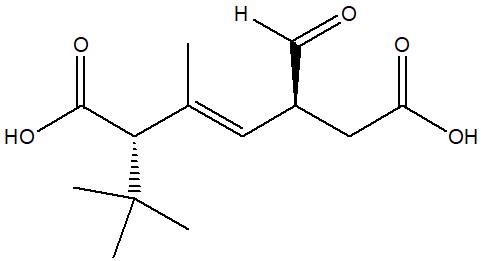
1. Assegnare il nome IUPAC, comprensivo di stereochimica, ai seguenti composti:
2. Disegnare il 2-terz-butil-4-etil-1-metilcicloesano. Qual è il numero massimo di stereoisomeri possibili con questa struttura? Disegnare il conformero più stabile dello stereoisomero più stabile.
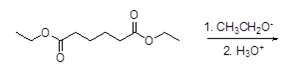
3. Completare la reazione e dire dove è spostato il seguente equilibrio
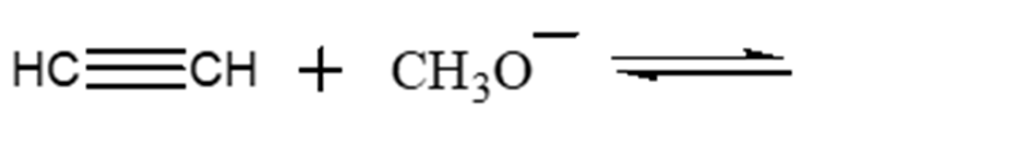
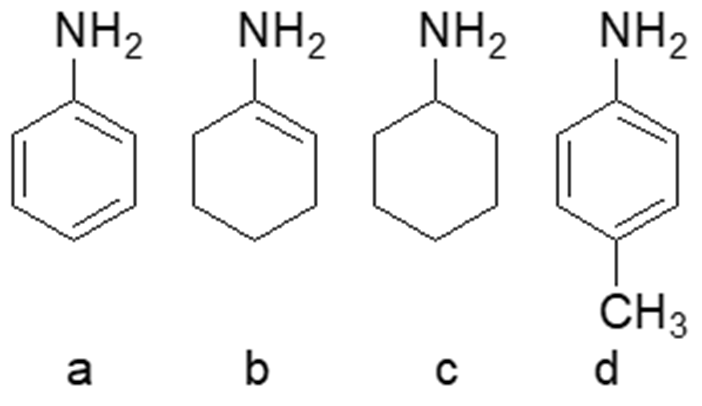
4) Disporre i seguenti composti in ordine di basicità crescente e motivare la risposta data
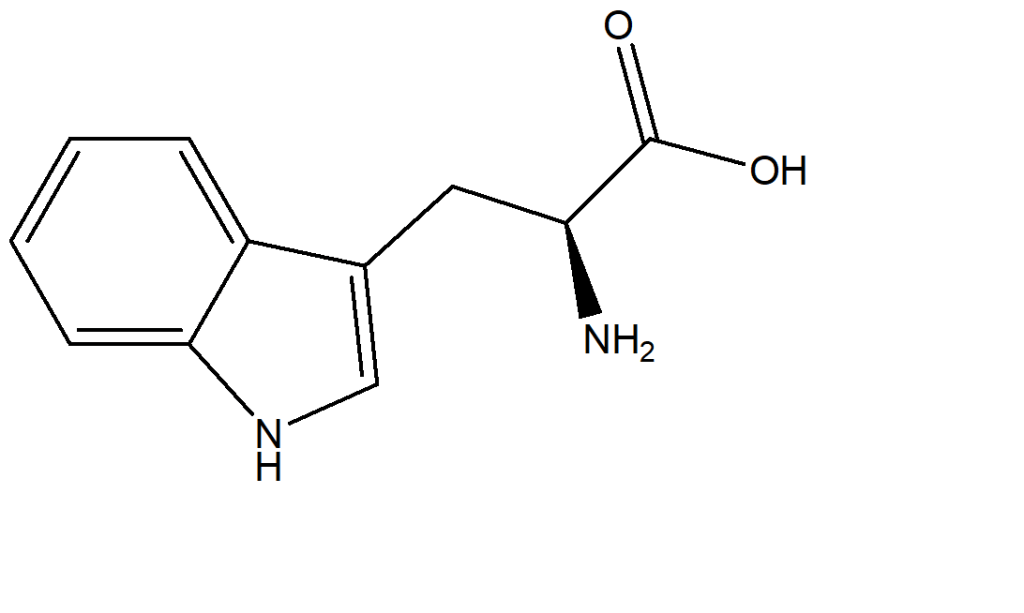
5) Quella di seguito riportata è la struttura dell’amminoacido triptofano. Dire come sono ibridati gli eteroatomi
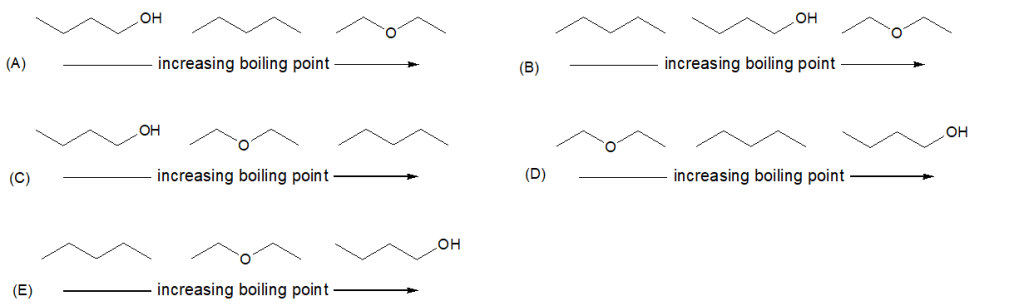
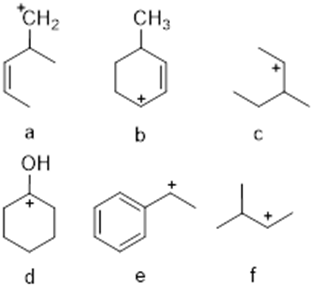
6) Dire quale tra le strutture a-d rappresenta l’enantiomero del seguente composto:

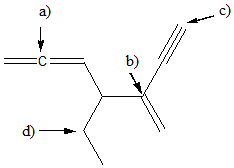
7) Scrivere tutte le strutture limite di risonanza del seguente carbocatione

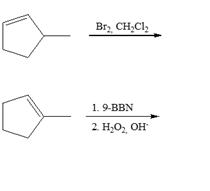
8) Scrivere i prodotti principali delle seguenti reazioni. Indicare la stereochimica, quando opportuno

9) Mostrare le condizioni di reazione e il meccanismo per ottenere il 2-metil-2-butanolo a partire dall’opportuno cloruro acilico
10) Di seguito è riportata la curva di titolazione per l’amminoacido arginina, insieme alla struttura dell’amminoacido a pH<2. Scrivere la forma zwitterionica e dire a quale valore di pH è presente. Quale sarà la struttura a pH>13?

Cosa fare se si riscontrano difficoltà o se si hanno dubbi:
-rivedere gli argomenti problematici (NB: non si possono risolvere gli esercizi senza aver studiato la teoria, per cui sarà necessario studiare e approfondire l’argomento ed eventualmente-successivamente-esercitarsi ulterioremente utilizzando sia gli esercizi del libro sia quelli presenti su questo blog).
-contattare il docente: è possibile sia chiedere spiegazioni, sia fare ricevimento (anche in gruppo) o organizzare esercitazioni dedicate



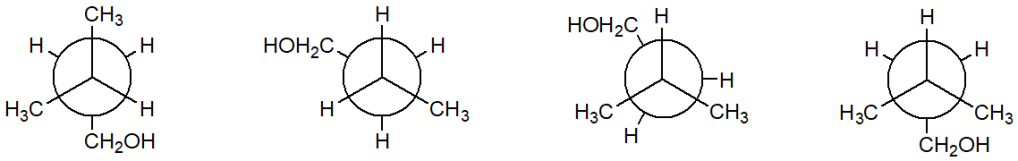









































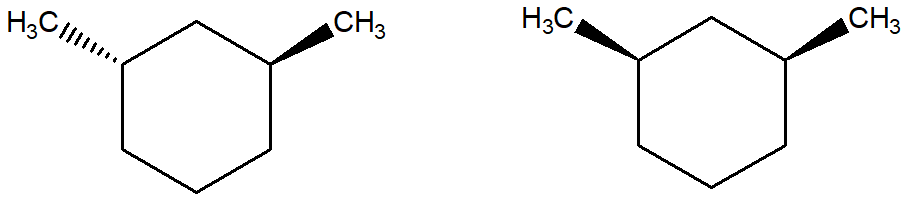

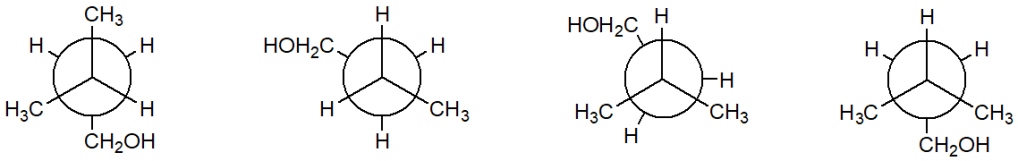



You must be logged in to post a comment.